新型冠状病毒肺炎患者IgM抗体与血细胞计数及C反应蛋白的相关性研究*
黄琼 徐云云 刘海燕 李宗光 吴萍 胡安群
2019年12月以来,一种β属的新型冠状病毒SARS-CoV-2引起的肺炎(COVID-19)在全球蔓延,对人民健康造成巨大威胁。目前,实时荧光RTPCR检测SARS-CoV-2核酸阳性是COVID-19确诊的主要病原学依据,但是核酸检测过程复杂,耗时较长,针对这一现状,本研究利用SARS-CoV-2的POCT快速检测试剂盒,即胶体金免疫层析技术对患者血清中的SARS-CoV-2特异性IgM抗体进行体外定性检测,旨在评价该方法在COVID-19诊断中的应用价值,为COVID-19的防治工作提供科学依据。同时,本研究对本院确诊患者的血细胞计数及C反应蛋白(CRP)进行统计分析,现报告如下。
资料与方法
1 临床资料 59例患者均为安庆市立医院北院区(新型冠状病毒定点收治医院)收治的确诊为COVID-1 9的住院病例,其中男3 5例,女2 4例,年龄为(20~75)岁,平均(46±13)岁。所有确诊患者均符合国家卫生健康委员会印发的《新型冠状病毒肺炎诊疗方案(试行第六版)》诊断标准,即通过对咽拭子或肛拭子进行实时荧光RT-PCR检测SARS-CoV-2核酸阳性,并均已排除血液病等因素所致的外周血细胞或生化指标的改变。同时将流行期内无SARSCoV-2接触史的30例健康体检者作为对照,男14例,女16例,年龄为(20~75)岁,平均(42±7)岁。本研究已通过安庆市立医院医学伦理委员会批准,批件号:医学伦理(2020)第4号。
2 试剂 新型冠状病毒(SARS-CoV-2)特异性IgM抗体检测试剂盒(胶体金免疫层析法),由军事医学研究院微生物流行病研究所和北京热景生物技术股份有限公司联合研制(产品批号:20200209)。
3 方法
3.1 血细胞计数及血清CRP检测:严格按照操作规程操作,用真空采血管采集患者疾病早期及对照组静脉血2 mL,EDTA-K2抗凝,进行外周血细胞计数。另用生化管采集静脉血(3~4)mL,分离血清,进行CRP检测。外周血细胞计数采用全自动血液细胞分析仪sysmex XN-550,CRP检测采用全自动生化分析仪cobas8000,操作详见说明书。
3.2 SARS-CoV-2特异性IgM抗体检测:分别于发病后(2~36)d采集患者血清样本,按试剂盒说明书进行SARS-CoV-2特异性IgM抗体检测,在室温放置15 min观察结果。同时采集健康体检者血清30份作为对照。
4 统计学处理 应用SPSS 16. 0软件,数据以“均数±标准差()”表示。两组间比较采用两独立样本的t检验,P<0. 05表示差异有统计学意义。
结 果
1 COVID-19患者外周血细胞及CRP的变化 59例COVID-19患者中,大多数患者白细胞正常或减低,占96.61%,其中白细胞降低占22.03%,升高者仅为2例(3.39%)。淋巴细胞计数正常者占66.1%,降低者占33.9%,无一例患者淋巴细胞升高。另外,发现有69.49%的患者C反应蛋白水平升高。见表1。

表1 59例COVID-19患者外周血细胞及C反应蛋白的变化[n(%)]
2 COVID-19患者与对照组外周血细胞计数及CRP水平的变化比较 疾病早期COVID-19患者外周血白细胞、淋巴细胞及C反应蛋白水平与对照组比较,差异均有统计学意义(P<0.05)。见表2。
3 COVID-19患者血清SARS-CoV-2特异性IgM抗体检测结果 59例COVID-19确诊患者中,52例患者SARS-CoV-2特异性IgM抗体检测为阳性,阳性率达88.14%,结果见表3。对照组30例同期健康体检者血清SARS-CoV-2特异性IgM抗体均为阴性。
4 COVID-19患者中IgM阳性组和IgM阴性组外周血细胞计数及CRP水平的变化比较 IgM阳性组的外周血白细胞、淋巴细胞及C反应蛋白水平与IgM阴性组比较,差异均无统计学意义(P>0.05)。见表4。

表2 疾病早期COCVRIDP-19患者与对照组外周血s细胞计数及水平的变化比较(±)
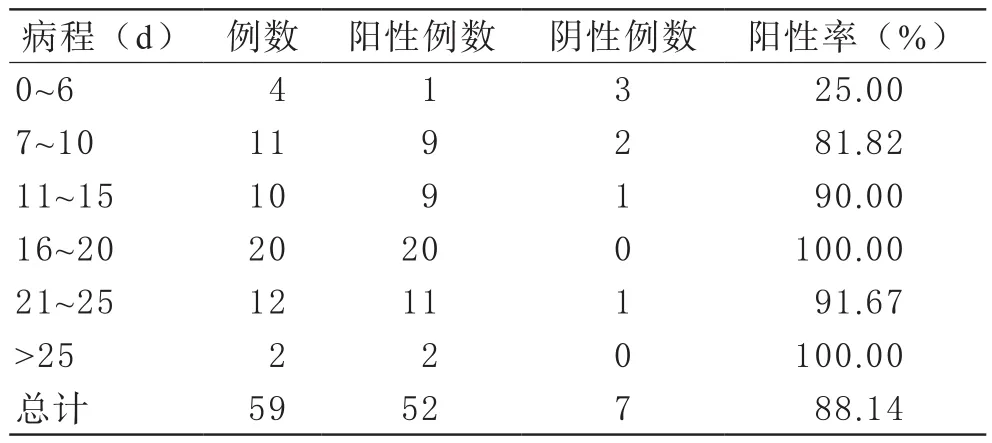
表3 COVID-19患者血清SARS-CoV-2特异性IgM抗体阳性率与病程的关系

表4 SARS-CoV-2 IgMC阳R性P组和SARS-CoV-2 IgMs阴性组外周血细胞计数及水平的变化比较(±)
讨 论
SARS-CoV-2是一种从未在人类中发现的新型冠状病毒,主要通过呼吸道飞沫和密切接触传播。基于现有的流行病学调查,潜伏期一般不超过14 d,多为(3~7)天[1]。该病毒引发的COVID-19传播迅速广泛,传染性强,人群普遍易感[2]。因此,对COVID-19患者的及时发现和快速诊断是控制疫情传播的重要环节。
在临床诊疗过程中,对疑似病例首先进行血细胞计数分析。发病早期白细胞计数正常或降低、淋巴细胞计数减少是目前作为临床诊断COVID-19或疑似COVID-19的重要依据之一。为探讨外周血白细胞、淋巴细胞及C反应蛋白在COVID-19诊断中的实际价值,我们对本院收治的59例确诊患者的检测结果进行统计分析。结果显示59例COVID-19患者中,44例(74.58%)白细胞计数正常,13例(22.03%)减少,升高者仅为2例(3.39%)。同时,在33.9%的患者中观察到淋巴细胞减少症,无一例患者淋巴细胞计数升高。据相关研究报道,在SARS-CoV和MERS-CoV感染的患者中同样存在该现象,即白细胞一般正常或减低,常伴有淋巴细胞计数减少[3,4]。另外,大部分患者血清C反应蛋白升高。通过对COVID-19组与对照组外周血白细胞、淋巴细胞及C反应蛋白的比较,我们发现COVID-19组白细胞、淋巴细胞均显著低于对照组,而C反应蛋白显著高于对照组。在研究中,我们还发现淋巴细胞计数与病情变化密切相关,尤其当外周血淋巴细胞计数过低或进行性下降时,多提示预后不良。因此,在COVID-19的诊断、病情观察及判断预后上均应高度重视淋巴细胞的变化。
SARS-CoV和MERS-CoV感染的患者病死率较高(11%和41%)[5,6],但轻症和无症状携带者很少,病毒进行人传人主要是重症期传播,传染性相对较弱。而SARS-CoV-2感染中80%是轻症,且轻症和无症状病毒携带者的潜伏期就有传染性[7],因而早期明确诊断采取隔离措施对控制疫情爆发很重要。目前实验室检测SARS-CoV-2的特异性方法主要有三种,即病毒分离培养、病毒核酸检测(RT-PCR和基因组测序)及病毒特异性抗体检测(免疫层析、酶联免疫吸附实验等方法)。在分子生物学诊断技术诞生之前,病毒分离培养是病毒检测的金标准。研究发现,体外分离培养时,SARS-CoV-2在96 h左右即可在人呼吸道上皮细胞内发现,而在VeroE6和Huh-7细胞系中分离培养约需6 d。由于病毒分离培养与鉴定的方法繁杂,需要提供活细胞,要求条件严格及培养周期长[8],在普通的临床实验室难以进行,因此不能广泛应用于临床诊断。目前,多家公司已成功研制出SARS-CoV-2核酸检测试剂盒,RT-PCR凭借高敏感性与特异性、耗时短、程序简便等特点,成为SARSCoV-2感染诊断的重要技术方法。据研究显示,已利用RT-PCR从COVID-19患者的痰液、鼻咽拭子、下呼吸道分泌物、血液、粪便等多种标本中检测出SARSCoV-2核酸阳性[9]。但是,在临床实践中SARSCoV-2核酸检测多次出现“假阴性”,可能与患者病情轻重、疾病不同阶段、样本类型及样本质量等多种因素有关[10]。因此,如果将SARS-CoV-2核酸检测作为唯一确诊COVID-19的病原学依据,可能出现漏检和治疗延误。
与核酸检测相比,利用胶体金免疫层析技术检测COVID-19患者血清特异性IgM抗体,具有以下优势:①操作方便、快捷,适用于早期轻症和无症状感染者的大规模筛查;②操作空间不受限制,对操作者的专业技能要求低,可大幅提高基层医院对病毒感染的筛查能力。本研究采用胶体金免疫层析技术分别于发病后第(2~36)d对59例确诊患者进行血清SARS-CoV-2特异性IgM抗体检测。结果显示在59例患者中,有52例患者IgM抗体检测为阳性,阳性率为88.14%。在病程第(0~6)d、(7~10)d、(11~15) d、(16~20)d,观察到分别有25%、81.82%、90%、100% 的患者出现IgM抗体阳性。其中,一患者最早于病程第3天出现IgM抗体阳性。另外,还发现在病程第(21~25)d检测的12例患者中,1例IgM抗体检测为阴性。仅有2例患者在发病第25天以后进行抗体检测,其中一患者最迟在病程的第36天还可检测到IgM抗体。由于第25天以后的的病例数较少,抗体水平的变化尚需要进一步观察。通常机体感染病原微生物后,IgM抗体的产生存在一定的窗口期。对于在发病早期未产生抗体的患者,阴性结果不能排除病毒的感染,可动态观察血清IgM抗体的变化。SARS-CoV-2特异性IgM抗体的产生及消失在时间上有较大的个体差异,在排除试剂盒因素的前提下,可能与以下因素有关:第一,病人发病的确切时间掌握不够准确,未能在最佳时间采集到标本,因此检测结果不能准确地反映病情;第二,不同患者被感染的病毒载量和潜伏期长短有个体差异;第三,严重的COVID-19患者T淋巴细胞及亚群严重受损,不能辅佐B细胞有效产生抗体。
另外,本研究根据SARS-CoV-2特异性IgM抗体的检测结果将COVID-19患者分为IgM阳性组和IgM阴性组,发现两组患者的白细胞、淋巴细胞计数及C反应蛋白水平差异无统计学意义,说明COVID-19患者的IgM抗体与血细胞计数及C反应蛋白水平不具有相关性。
基于以上研究,可以考虑将SARS-CoV-2核酸检测和血清抗SARS-CoV-2 IgM抗体检测共同用于COVID-19的诊断和疗效评价,IgM抗体检测能够为核酸检测提供有效补充。本研究仅为初步探索性分析,存在一些不足:由于SARS-CoV-2特异性IgM抗体检测试剂盒上市较晚,对于部分已发病的患者未能在病程早期及时进行检测,导致本研究的患者检测时间点不统一,缺乏对同一病例的连续追踪观察,尚不能完全反映COVID-19患者体内的特异性抗体产生及变化规律。在后期实验中,我们将进一步对SARSCoV-2血清特异性IgM和IgG抗体进行追踪观察和滴度试验,为疾病的防治与疫苗研发提供参考依据。
利益冲突 所有作者均声明不存在利益冲突

