奥希替尼固体分散体的制备及体外溶出度研究
王思哲,冯菊红*,王喻华,张恒宜,罗文涛,胡学雷
(1.武汉工程大学化工与制药学院,湖北 武汉 430074;2.绿色化工过程教育部重点实验室,湖北 武汉 430074)
奥希替尼(Osimertinib)商品名为Tagrisso,是由阿斯利康(AstraZeneca)公司研究生产的第3代突变体选择性表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TKI)[1],主要适用于带有特殊EGFR基因变异和接受过其它EGFR抑制剂治疗后病情步入非小细胞癌晚期的患者。目前,大部分东亚地区包括中国在内的非小细胞癌患者体内基因突变是由于EGFR的突变,其中绝大部分患者服用EGFR-TKI后疗效显著[2],而患有EGFR T790M突变阳性转移性的非小细胞癌患者只有通过奥希替尼的治疗,病情才能得到缓解。据报道[3],约30%的EGFR突变患者使用奥希替尼后病情得到缓解。鉴于奥希替尼Ⅰ期和Ⅱ期的临床研究结果,美国FDA在2015年11月13日批准奥希替尼上市[4]。
奥希替尼在水中的溶解度极低,溶出效果不好[5]。有研究者尝试将奥希替尼分散于亲水性高分子载体中形成固体分散体,来提高其溶解度和生物利用度[6]。文献报道的制备固体分散体的方法有很多,主要是物理混合法、溶剂法、熔融法和溶剂-熔融法[7]。其中溶剂法操作简单,适用于各种载体,制备的固体分散体分散效果好且能显著改善溶出效果。因此,作者选择泊洛沙姆188(F68)、聚乙烯吡咯烷酮(PVPK30)、共聚维酮(coPVP)等高分子载体,采用溶剂法制备奥希替尼固体分散体[8];以体外溶出度为评价指标,对制备条件进行优化,并通过扫描电镜(SEM)、X-射线衍射法(XRD)和差示扫描量热法(DSC)对最优条件下制备的固体分散体进行物相鉴定[9-10]。
1 实验
1.1 试剂与仪器
奥希替尼(多次重结晶),自制;共聚维酮(coPVP),上海昌为医药辅料技术有限公司;聚乙烯吡咯烷酮(PVPK30),上海哲研生物试剂有限公司;泊洛沙姆188(F68),武汉格奥化学技术有限公司;无水甲醇(分析纯)、十二烷基硫酸钠(SDS),国药集团化学试剂有限公司。
UV2450型紫外分光光度计,日本Shimadzu公司;RCZ-6B1型药物溶出度仪,上海黄海药检仪器厂;FA1604型电子天平,上海越平科学仪器有限公司;D/MAX-RB型X-射线衍射仪、JSM-5610LV型扫描电镜,日本理学公司;NETSCHE STA-449C型同步热分析仪,美国STA公司。
1.2 奥希替尼固体分散体的制备
采用溶剂法制备奥希替尼固体分散体。按合适比例分别准确称取奥希替尼和载体(F68、PVPK30和coPVP),过80目筛;将载体投入烧瓶底部并加入50 mL无水甲醇,搅拌加热;待载体完全溶解后投入奥希替尼,加热到60 ℃搅拌一定时间;反应结束后蒸除溶剂,减压干燥;将干燥后的产物在研钵中研碎并过80目筛,分别得到以F68、PVPK30和coPVP为载体的奥希替尼固体分散体,标记为SD1、SD2、SD3。
以奥希替尼与coPVP的物理混合物作为对照。制备步骤如下:按合适比例分别准确称取奥希替尼和载体coPVP,过80目筛,置于烧杯中,搅拌均匀,即得奥希替尼与coPVP的物理混合物,标记为PM。
1.3 奥希替尼固体分散体的制备条件优化
以体外溶出度为评价指标,分别考察奥希替尼与载体质量比(1∶1、1∶3、1∶5、1∶7、1∶9)、反应时间(15 min、30 min、45 min、60 min)、反应温度(55 ℃、60 ℃、64 ℃)对奥希替尼固体分散体制备的影响。
1.4 奥希替尼固体分散体的表征
通过SEM、XRD、DSC等对最优条件下制备的奥希替尼固体分散体进行表征,并与奥希替尼、coPVP、PM进行对比。
1.5 体外溶出度的测定
溶出介质的确定:分别配制0.4%的SDS水溶液、含0.4%SDS的磷酸盐缓冲液(pH值4.5)、含0.4%SDS的磷酸盐缓冲液(pH值6.8),作为溶出介质;按体外溶出度测定方法考察奥希替尼在3种溶出介质中的溶出效果。结果表明,奥希替尼在3种溶出介质中的体外溶出度没有明显差异。综合考虑,选择含0.4%SDS的磷酸盐缓冲液(pH值4.5)作为溶出介质。
体外溶出度的测定:按照《中华人民共和国药典》(四部)测定体外溶出度。准确称取奥希替尼10 mg并过80目筛,放入装有900 mL溶出介质的溶出杯中,搅拌桨转速为75 r·min-1、溶出杯内温度为(37±0.5) ℃,分别在10 min、15 min、20 min、30 min、45 min和60 min时用针筒吸取5 mL溶出液(同时补充相同体积和相同温度的新鲜溶出介质),迅速经0.45 μm微孔滤膜过滤,测定滤液在262 nm处吸光度,代入回归方程得到奥希替尼浓度,计算体外溶出度。
2 结果与讨论
2.1 检测波长的确定
分别配制奥希替尼、F68、PVPK30和coPVP的0.4%SDS水溶液,然后在200~400 nm波长范围内进行紫外吸收光谱测试。结果表明,在262 nm处,奥希替尼有最大吸收且F68、PVPK30、coPVP对奥希替尼的测定没有影响。因此,选择262 nm为检测波长。
2.2 溶剂的选择
精密称量100 mg奥希替尼6份,研磨均匀,过80目筛,分别加入水、二氯甲烷、无水甲醇、乙醇、丙酮、乙酸乙酯,在(25±2) ℃下每隔5 min用力摇晃溶液30 s,使之溶解,记录奥希替尼在30 min内的溶解情况。结果表明,奥希替尼略溶解于无水甲醇、乙醇、二氯甲烷、丙酮,不溶解于水和乙酸乙酯。综合考虑,选择无水甲醇为溶剂。
2.3 标准曲线的绘制
准确称取奥希替尼10 mg,用无水甲醇溶解,定容于50 mL容量瓶中,即得200 μg·mL-1奥希替尼标准溶液。用移液枪准确量取0.500 mL、0.625 mL、1.000 mL、1.250 mL、2.500 mL和5.000 mL的标准溶液置于50 mL容量瓶中,定容,得到一系列梯度浓度溶液,测定各溶液在262 nm处吸光度。以奥希替尼浓度(c)为横坐标、吸光度(A)为纵坐标绘制标准曲线,并进行拟合得到线性回归方程:A=0.0439c+0.0551(R2=0.9999)。
2.4 方法学考察
2.4.1 精密度
取10 μg·mL-1奥希替尼甲醇溶液,测定其在262 nm处吸光度,连续测定6次,吸光度的RSD为0.58%。表明,仪器和方法精密度好,测试结果稳定。
2.4.2 回收率
分别取5 μg·mL-1、10 μg·mL-1和20 μg·mL-1的固体分散体溶液,测定其在262 nm处吸光度,每个浓度测定3次,代入回归方程得到奥西替尼溶液浓度,计算回收率分别为98.19%、99.01%和99.24%,RSD分别为0.71%、0.65%和0.63%。表明,回收率较好,该方法稳定可行。
2.5 奥希替尼固体分散体的最优制备条件
2.5.1 奥希替尼与载体质量比
固定反应温度为60 ℃,分别以F68、PVPK30和coPVP为载体,在奥希替尼与载体质量比分别为1∶1、1∶3、1∶5、1∶7、1∶9时制备奥希替尼固体分散体SD1、SD2和SD3,考察奥希替尼与载体质量比对体外溶出度的影响,结果如图1所示。
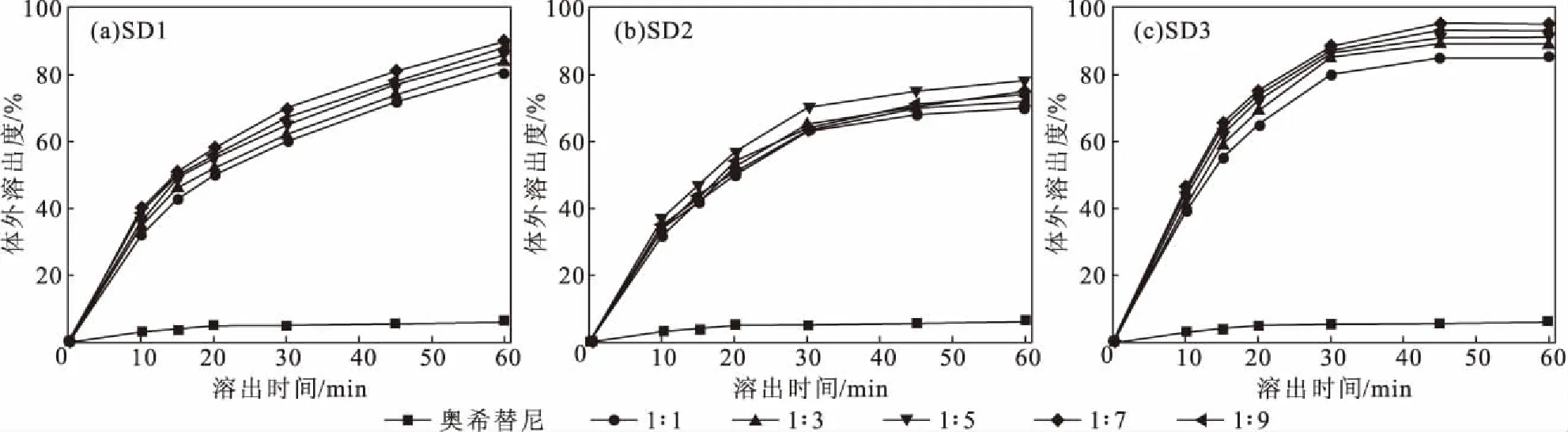
图1 奥希替尼与载体质量比对体外溶出度的影响Fig.1 Effect of mass ratio of Osimertinib to carrier on in vitro dissolution
从图1可知,奥希替尼原料药的体外溶出度很低;将奥希替尼分散在载体中形成固体分散体后,溶解度增大,溶出效果得到改善,体外溶出度明显提高,其中以coPVP为载体制备的固体分散体SD3的溶出效果最好(图1c)。因此,选择coPVP为载体。从图1还可以看出,随着载体用量的增加,体外溶出度先升高后降低;当奥希替尼与coPVP的质量比为1∶7时,所制备的固体分散体在45 min时达到溶解平衡,体外溶出度达到最高,为95.6%。因此,确定最佳奥希替尼与coPVP质量比为1∶7。
2.5.2 反应时间
固定奥希替尼与coPVP质量比为1∶7、反应温度为60 ℃,分别反应15 min、30 min、45 min、60 min制备固体分散体SD3,考察反应时间对体外溶出度的影响,结果如图2所示。
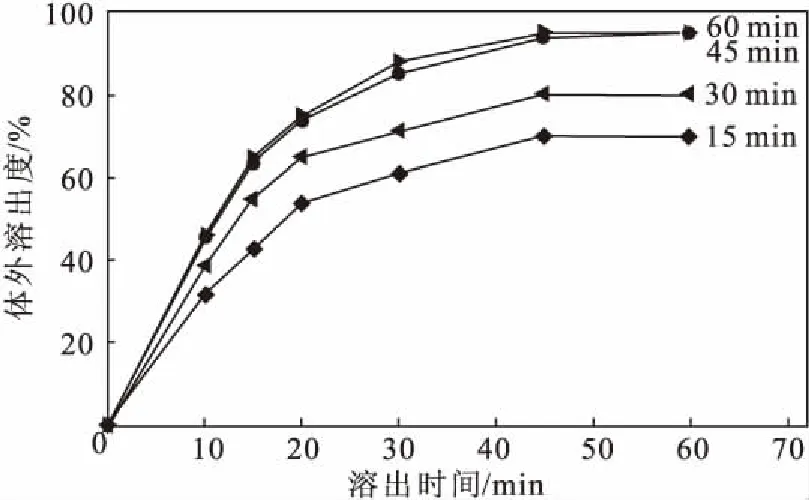
图2 反应时间对体外溶出度的影响Fig.2 Effect of reaction time on in vitro dissolution
从图2可知,延长反应时间可以提高奥希替尼固体分散体的体外溶出度,但当反应时间超过45 min后,体外溶出度变化不明显。 因此,确定最佳反应时间为45 min。
2.5.3 反应温度
固定奥希替尼与coPVP质量比为1∶7、反应时间为45 min,分别在55 ℃、60 ℃、64 ℃制备固体分散体SD3,考察反应温度对体外溶出度的影响,结果如图3所示。

图3 反应温度对体外溶出度的影响Fig.3 Effect of reaction temperature on in vitro dissolution
从图3可知,反应温度为60 ℃时所制备的奥希替尼固体分散体的溶出效果最好,体外溶出度最高,在含0.4%SDS的磷酸盐缓冲液(pH值4.5)中,45 min达到溶解平衡,体外溶出度达到95.6%。
2.6 奥希替尼固体分散体的表征
2.6.1 SEM分析
奥希替尼、coPVP、PM(1∶7)、固体分散体SD3(1∶7)的SEM照片如图4所示。
从图4可知,奥希替尼主要以交错的棍棒状晶体形态存在;coPVP是球状晶型形态;PM(1∶7)中coPVP的球状晶型表面附着有奥希替尼,并没有完全结合;而固体分散体SD3(1∶7)的外观和形态与前三者有显著差异,呈现出不规则形态,未见奥希替尼的棍棒状颗粒和coPVP的球状颗粒,清楚显示奥希替尼和coPVP完全融合,说明奥希替尼已高度分散于载体coPVP中,形成了固体分散体。
2.6.2 XRD分析
奥希替尼、coPVP、不同质量比的固体分散体SD3的XRD图谱如图5所示。
从图5可知,奥希替尼有大量的特征衍射峰,其中13.37°处的衍射峰强度最强,说明奥希替尼是一种高结晶度药物;coPVP是一种无定形白色粉末,只在17.56°处有一个宽峰;不同质量比的固体分散体SD3的XRD图谱中,奥希替尼的晶体特征峰消失,说明奥希替尼的晶型结构消失而转变为无定形态,奥希替尼已高度分散于coPVP中,与SEM结果一致。
2.6.3 DSC分析
奥希替尼、coPVP、PM(1∶7)、固体分散体SD3(1∶7)的DSC曲线如图6所示。

a~d:奥希替尼、coPVP、PM(1∶7)、SD3(1∶7)
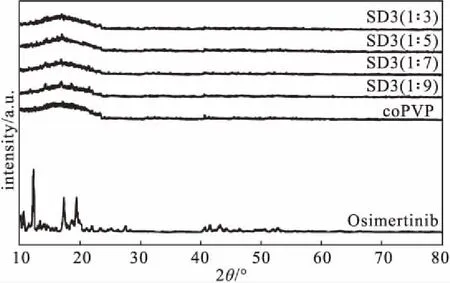
图5 奥希替尼、coPVP、不同质量比的固体分散体SD3的XRD图谱Fig.5 XRD patterns of Osimertinib,coPVP,and SD3 with different mass ratios
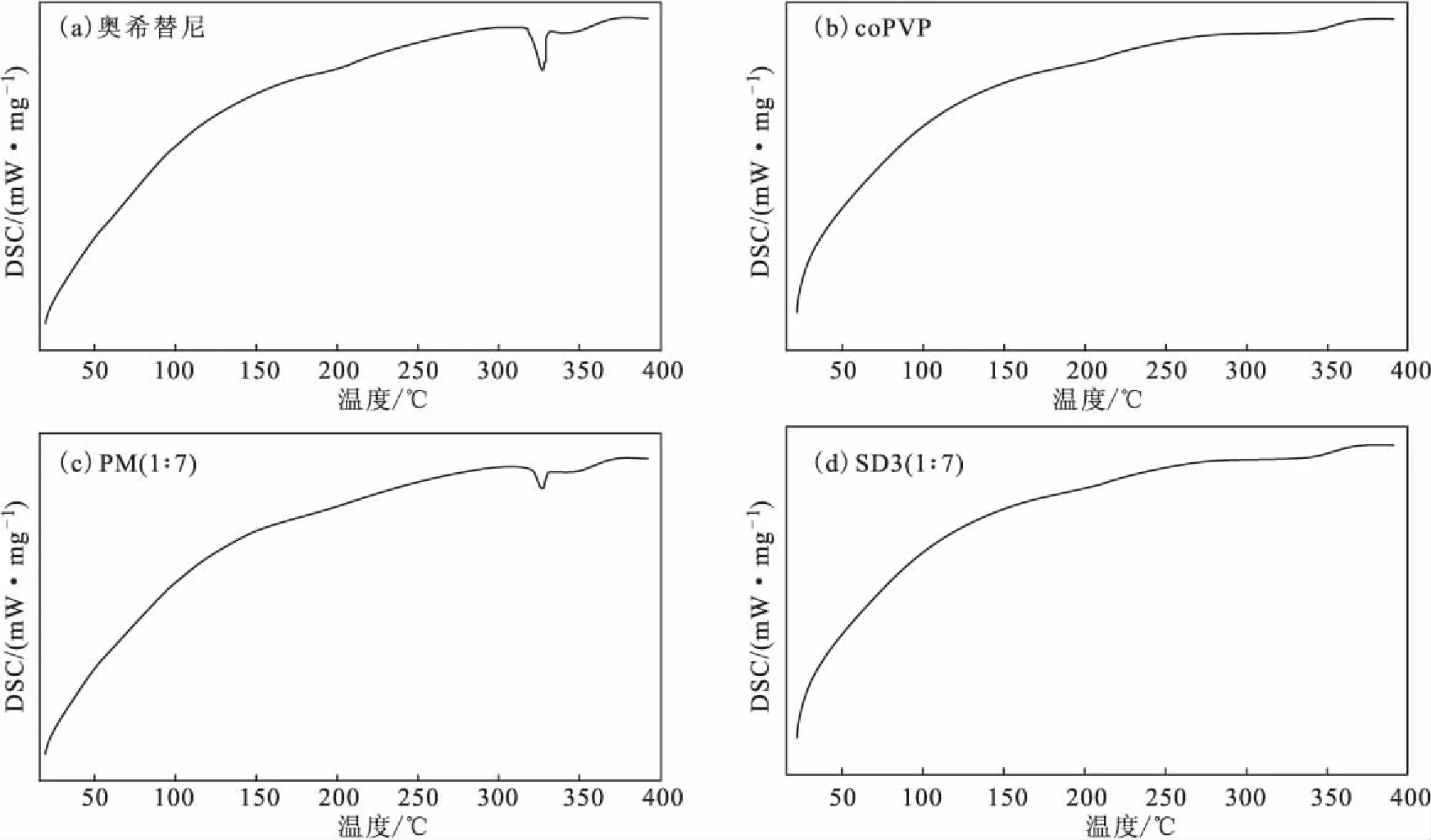
图6 奥希替尼、coPVP、PM(1∶7)、固体分散体SD3(1∶7)的DSC曲线Fig.6 DSC curves of Osimertinib,coPVP,PM(1∶7),and SD3(1∶7)
从图6可知,奥希替尼在326 ℃时出现了一个尖锐的吸热峰,是奥希替尼晶体熔化成无定形所致;PM(1∶7)在326 ℃左右也出现该吸热峰;而在固体分散体SD3(1∶7)中没有发现该吸热峰,说明奥希替尼在固体分散体中已经转化为无定形态且高度分散,与SEM与XRD结果一致。
3 结论
为了改善奥希替尼的溶出效果,采用溶剂法制备奥希替尼固体分散体,最优制备条件为:奥希替尼与coPVP质量比1∶7、反应温度60 ℃、反应时间45 min,在此条件下制备的固体分散体的溶出效果最佳,45 min时体外溶出度达到最高(95.6%)。

