水合肼还原法回收金刚石废料中铜的研究
冉敬文,李 沙,余 祎
( 黄冈师范学院 化学化工学院,湖北 黄冈 438000)
金刚石刀具以人造金刚石为切割材料, 碳化钨为刀具的胎体材料, 以金属铜等金属为粘合剂加工而成。随着科学技术的进步,金刚石刀具市场前景广泛,已经广泛应用于陶瓷工业、玻璃器皿、珠宝首饰、钢铁行业等材料的切割加工和民用、公用施工建设中[1-3]。但其价格昂贵,成本高,其使用也受到了一定限制。据统计,金刚石刀具在加工过程中,为了避免基体受到损坏,每张锯片大约有 10%~15%的磨料层被弃用,磨料层中除了含有昂贵的金刚石外,还含有大量有价金属[4-5],富含Cu、Zn、Co、Ni,造成金属铜铁等金属和稀有金刚石重大浪费, 使资源紧张形势更为严峻。采取合理手段对这些资源进行回收和再利用,既减少了资源浪费,一定程度上促进了国民经济的增长,同时还起到减少污染、保护环境的作用,因此有必要对金刚石等有价物质进行回收利用,既可以带来经济效益,也增加了社会效益。
目前市场上回收有价值铜的常用方法:一是利用强氧化剂(如硝酸、王水、氯气等)直接将金刚石刀头腐蚀溶解[6],对浸出的金刚石颗粒进行清洗、分选后直接用于再生产刀具;对富含金属离子的酸性溶解液进行化学提取,普遍采用的方法是直接加入铁屑置换Cu2+,经过沉降,洗涤,干燥得到铜粉。由于金刚石刀具的主成分是铁,其腐蚀溶解后在溶液中以Fe3+形式存在,当加入铁屑置换Cu2+时,要消耗更多铁屑使得Fe3+转化成Fe2+,最后需在处理废水时消耗更多的碱来沉淀,再者氢氧化铁难洗难滤,附加值有限,这样会过多增加回收成本。二是用浸出-隔膜电沉积法从废弃金刚石刀头中回收有价值成分[7-9],它以FeCl3为浸出剂,通过加热、隔膜电积处理得到铁合金。此法解决了环境污染问题,但能耗较高且不适合规模化应用。为回避这一问题,本文对此工艺进行改进,直接用酸性溶解液调节pH后加入强还原剂水合肼将Cu2+、Co2+和Ni2+还原成单质,使其形成金属混合物,再通过人为调节各金属单质比例直接用于金刚石刀具的再生产。实验中对水合肼还原金属离子的条件进行详细研究。
1 实验
1.1 主要的仪器设备和试剂
TAS-986原子吸收分光光度计(北京普析通用公司);等离子体光谱质谱仪(ICP-MS 2600,日本岛津);波长色散型X射线荧光光谱仪(XRF-1800,日本岛津);粉沫X-射线衍射仪(SHIMADZU XRD-6100,日本岛津)。
NaOH(AR),H2SO4(98%,AR),水合肼(80%),Cu/Co/Ni标准溶液。
1.2 实验原理与方法
实验原理:2Cu2+/Ni2+/Co2++N2H4+4OH-=2Cu/Ni/Co↓+N2↑+4H2O
副反应:4Cu2++N2H4+8OH-=2Cu2O↓+N2↑+6H2O
Cu2O+H2SO4=CuSO4+Cu+H2O
1.3 实验方法
利用废硝酸浸蚀金刚石废料,生成的氮氧化物引入碱液处理,过滤,所得金刚石颗粒回收,滤液分别稀释成不同浓度的溶液测其Cu2+、Co2+和Ni2+摩尔浓度;调节溶液pH至4左右,加入不同比例的还原剂水合肼,反应不同时间后过滤测其滤液中的Cu2+、Co2+和Ni2+摩尔浓度;所得固体粉沫洗涤,定量加入硫酸溶液浸泡半小时,过滤,测其滤液中的Cu2+、Co2+和Ni2+摩尔浓度,通过三次溶液中Cu2+、Co2+和Ni2+浓度计算回收率。
回收率公式为:

初步试验发现反应时间、还原剂的比例和温度是影响收率的主要因素,整个实验通过条件试验优化各因子,选出最优方案。
1.4 正交试验
初步实验结果表明,反应时间、还原剂的比例和温度是影响收率的主要因素。因此,根据正交设计法的基本原则,选取反应时间(t)、氧化剂Cu2+、Co2+和Ni2+总量:还原剂水合肼的比例(B)和温度(T)三个因素来进行条件优化,每个因素考察三个水平变量。各因素与水平的对应关系如表1。

表1 因素与水平的对应关系Tab. 1 The relationship between the factors and the levels
2 结果与讨论
2.1 正交结果分析
三因素三水平正交实验结果如表2所示,考察指标为铜、钴和镍的总回收率。从表2可以看出,以极差来判断,影响收率的三因素中氧化还原剂的比例最明显,其次是反应时间,反应温度则相对影响不明显。这主要是还原剂在与Cu2+/Co2+/Ni2+发生作用时,也缓慢与Fe3+作用,从而消耗更多还原剂肼,导致需要肼过量,当还原剂肼的量不足时,生成更多的是Cu2O,影响整个Cu的收率。整个氧化还原反应是放热反应且较剧烈,反应溶液自身温度很快就升高,自身反应放热可以维持反应所需能量,因而在温差不大的情况下,反应速度影响较小。

表2 正交试验分析Tab. 2 Analysis of orthogonal experiments
注:Ki/3为各自对应水平下的平均值
2.2 Cu2O含量的调整
使用水合肼做还原剂时,Cu2+难免有部分还原成了难溶于水的Cu2O,这样对金属粉带来了新的杂质,为消除其影响,采用歧化反应将其去除掉。实验中Cu2O的歧化反应速度采用同样质量、室温、同样反应时间(30 min)的条件下进行,考察不同浓度的硫酸(过量)对其收率的影响,此副反应收率以实际得到的铜质量/理论量,结果见图1。从图1中可看出,随着硫酸浓度的升高,氧化亚铜转化成铜的收率逐渐增加,当硫酸浓度达到3 mol·L-1以上时,转化率不再明显增加,说明反应已经完成。故条件优化中选取3 mol·L-1的硫酸浸泡滤渣。
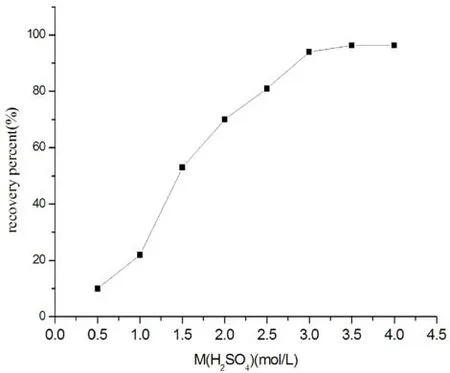
图1 硫酸浓度对收率的影响Fig. 1 Effect of sulfuric acid concentration on yield
实验结果表明,利用水合肼直接还原Cu2+/Co2+/Ni2+回收有价金属是可行的,在保证充足还原剂的情况下,有价金属回收率达到98.1%,此方法应用到金刚石废料的回收中,可以节省资源,节约成本,应用前景可观。

