山茱萸中具有抗氧化活性的环烯醚萜类成分
栾 娜 钟祥键 王 欣 冀麟麟 李金杰 尚小雅
(北京联合大学 生物活性物质与功能北京市重点实验室 北京100191)
山茱萸(Cornus officinalis)是山茱萸科山茱萸属植物,主产于我国安徽、河南和山西等地,其干燥成熟果肉被作为一种药食同源药材使用,具有补益肝肾、涩精固脱等功效,主要用于治疗眩晕耳鸣、腰膝酸软等症[1,2]。研究表明,山茱萸中的化学成分类型主要有环烯醚萜及其苷类、三萜类、黄酮类、鞣质类等[4-6]。多篇文献报道山茱萸具有降糖、抗炎、抗氧化、神经保护等功效[7-9]。
日本学者Arihi 早在1985年就报道山茱萸乙醇提取物具有抗氧化活性[10]。另有多篇文献报道了山茱萸醇提物、山茱萸总苷及山茱萸多糖等都具有抗氧化活性[11-13],并将其作为可食用天然抗氧化剂的一个潜在来源进行研究。截至目前,有学者发现山茱萸果中的高含量成分熊果酸、没食子酸和鞣花酸有抗氧化活性[14-15]。然而,山茱萸中的抗氧化活性成分究竟是什么尚无定论。为研究山茱萸中的抗氧化活性成分,采用大孔吸附树脂柱色谱将山茱萸乙醇提取物分离为不同洗脱部位,其中20%乙醇洗脱部位具有抗氧化活性。本文对20%乙醇洗脱部位中富含环烯醚萜的活性组分进行系统分离纯化,从中分离并鉴定4 个环烯醚萜类化合物,它们均表现出一定的抗氧化活性,其中2 个化合物为新的天然产物。
1 材料与方法
1.1 材料与仪器
山茱萸干燥果实,购于河南省西峡县,由宣武医院王文教授鉴定其为山茱萸(Cornus officinalis)的果实,标本保存在北京联合大学生物活性物质与功能食品北京市重点实验室标本室。
薄层色谱硅胶(GF254)和柱色谱硅胶(160~200 目),青岛海洋化工厂;Sephadex LH-20 凝胶,Pharmacia 公司。FRAP 抗氧化活性测试试剂盒,南京建成生物科技有限公司。氯仿、甲醇、乙醇及硫酸等试剂,均为分析纯级,北京化学试剂厂;色谱级甲醇,美国Thermo Fisher 公司;实验用超纯水,由Millipore 纯水仪生产。
Waters2545 高效液相色谱仪,配备Waters2998 紫外灯,色谱柱为Sunfire C18 制备柱(19 mm×250 mm×5μm),美国Waters 公司;Inova 500 核磁共振仪,美国Varian 公司;Combiflash Companion 快速分离仪,美国ISCO 公司;紫外灯(CREST C-650),美国CREST 公司。
1.2 试验方法
1.2.1 山茱萸的提取及粗分 山茱萸干燥果实共25 kg,以10 倍量的50%乙醇溶液超声提取,每次1 h,共3 次。合并3 次提取液,减压浓缩得到提取物浸膏(4.3 kg)。提取物浸膏经HP-20 大孔吸附树脂柱色谱分离,最终得到4 个部位,即:水、20%乙醇、60%乙醇、95%乙醇洗脱部位。
1.2.2 环烯醚萜的分离纯化 将大孔吸附树脂20%乙醇洗脱部位(1.25 kg)用甲醇超声溶解,用正相硅胶拌样,之后上正相硅胶色谱柱,以氯仿-甲醇混合溶液为流动相梯度洗脱,洗脱梯度为V(氯仿)∶V(甲醇)=91∶9,89∶11 和0∶100,根据薄层色谱,合并相同洗脱流分,得到3 个组分 (A1~A3)。选择A1 组分,用纯水溶解,上低压反相硅胶柱色谱,采用V(乙醇)∶V(水)=5 ∶95~100 ∶0 梯度洗脱,收集洗脱液后,根据薄层色谱进行合并,得到组分A1-1~A1-14。组分A1-4 采用Sephadex LH-20 凝胶柱色谱分离,流动相为V(氯仿)∶V(甲醇)=67∶33,收集洗脱液浓缩后采用薄层色谱检测,将具有相同紫色斑点的部分合并,合并后有白色固体析出,过滤,用甲醇反复淋洗,最终得到化合物1(178 mg)。组分A1-6 用正相硅胶拌样后,以V(氯仿)∶V(甲醇)=95∶5~0∶100 为流动相进行正相硅胶柱色谱分离,合并洗脱液后得到5 个亚组分A1-6-1~A1-6-5。组分A1-6-2 首先经过Sephadex LH-20 凝胶柱色谱分离,V(氯仿)∶V(甲醇)=67∶33 为流动相,收集相同流分后采用HPLC柱色谱纯化,流动相为V(甲醇)∶V(水)=45∶55,得到化合物2(56 mg)。组分A1-1 采用正相硅胶拌样后,通过正相硅胶柱色谱,以V(氯仿)∶V(甲醇)=97∶3~50∶50 分离,得到6 个亚组分A1-1-1~A1-1-6,亚组分A1-1-4 经过Sephadex LH-20 凝胶柱色谱,以V(石油醚)∶V(氯仿)∶V(甲醇)=45 ∶45:10 分离,收集相同流分后采用制备HPLC 柱色谱进行纯化,流动相为V(甲醇)∶V(水)=60∶40,得到化合物3 (11 mg)。亚组分A1-1-5 采用Sephadex LH-20 凝胶柱色谱分离,以V(石油醚)∶V(氯仿)∶V(甲醇)=45∶45∶10 分离,之后采用制备HPLC 柱色谱纯化,流动相为V(甲醇)∶V(水)=58∶42,得到化合物4(27mg)。
1.2.3 FRAP 抗氧化活性测定 FRAP 标准曲线的绘制:根据试剂盒方法,准确称取FeSO4·7H2O粉末27.8 mg,溶解并定容1 mL。取适量100 mmol/L FeSO4溶液分别稀释至0.15,0.3,0.6,0.9,1.2 mmol/L 和1.5 mmol/L,测定各浓度的OD 值,绘制标准曲线。
总抗氧化能力测定:在96 孔板中加入180 μL FARP 工作液,随后加入浓度为0.1 mmol/L 的单体化合物溶液,轻轻混匀,于37 ℃孵育3~5 min,在波长593 nm 处测定OD 值,根据标准曲线计算样品的总抗氧化能力[16]。
2 结果与分析
2.1 化合物结构鉴定结果
2.1.1 马钱子苷(loganin) 马钱子苷,白色无定型粉末,ESI 质谱显示m/z 435.14984[M+HCOOHH]-。1H NMR 谱显示:δH7.40 (1H,s)处有一个连氧烯氢信号,δH5.28 (1H,d,J=4.5 Hz)处有一个半缩醛氢信号,δH3.71 (3H,s)处有一个甲氧基氢信号,δH1.11 (3H,d,J=7.0 Hz)处为甲基信号。此外,在δH3.12~4.66 处为一组葡萄糖氢信号,其端基氢信号在δH4.66 (1H,d,J=7.9 Hz)处,耦合常数J=7.9 Hz,表明葡萄糖构型为β 构型。根据以上氢谱数据推测其可能为环烯醚萜苷类成分。对13C NMR 谱分析表明其有17 个碳信号,其中在δC169.5 为羰基碳信号,δC152.1 和 114.0为一组双键碳信号,δC97.7 为半缩醛碳信号,δC75.1 为连氧次甲基碳信号,δC51.6 处为甲氧基碳信号。此外,葡萄糖碳信号分别为δC62.7,71.6,75.0,78.0,78.4,100.1,其中δC100.1 为葡萄糖端基碳信号。将以上NMR 数据与文献[17]数据对比,鉴定该化合物为马钱子苷。
图1 马钱子苷的结构Fig.1 Chemical structure of loganin

图2 马钱子苷的质谱图Fig.2 ESI-MS of loganin

图3 马钱子苷的1H-NMR 图Fig.3 1H-NMR of loganin
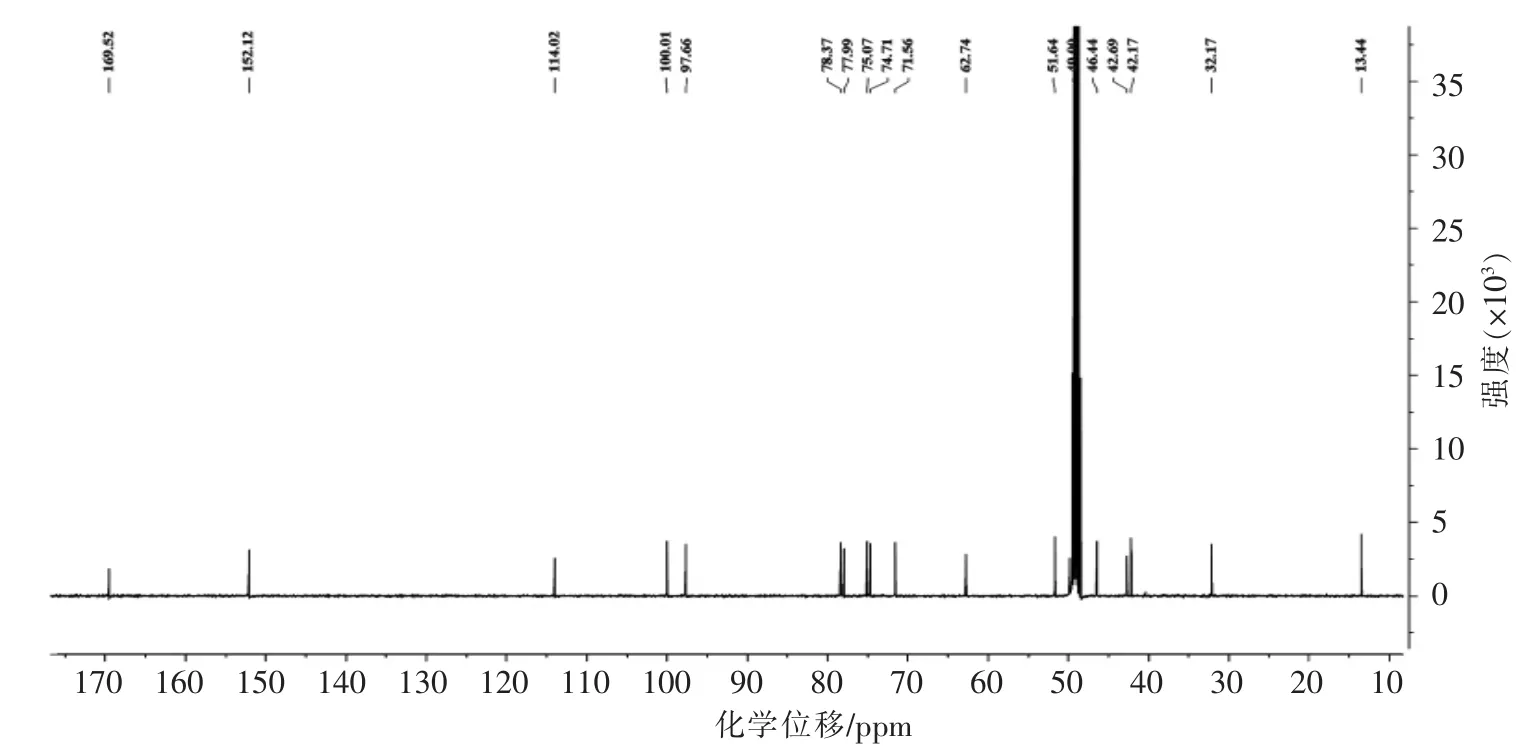
图4 马钱子苷的13C-NMR 图Fig.4 13C-NMR of loganin
2.1.2 马钱素-7-酮 (ketologanin) 马钱素-7-酮,白色无定型粉末,ESI 质谱显示m/z 433.13431[M+HCOOH-H]-。1H NMR 谱显示:δH7.46(1H,s)为烯氢信号,δH5.61 (1H,d,J=3.1 Hz)为半缩醛氢信号,甲氧基信号在δH3.67 (3H,s)处,一个甲基双峰信号在δH1.12 (3H,d,J=7.2 Hz),δH3.14~4.32 处有6 个葡萄糖氢信号,其端基氢信号在δH4.66(1H,d,J=7.9 Hz)。葡萄糖构型通过耦合常数确定为β 型构型。13C NMR 谱显示有17 个碳信号,δC13.6 处为甲基碳信号,δC51.7 处为甲氧基碳信号,δC95.2 处为半缩醛碳信号,δC111.0和153.3 处为一组双键碳信号,δC220.7 和168.8分别为酮羰基信号和酯羰基信号,δC62.7~100.1处为6 个葡萄糖碳信号,端基碳信号为δC100.1。综上所述,推测该化合物为环戊烷环烯醚萜苷类化合物,再与文献[18]数据对比,鉴定化合物为马钱素-7-酮(ketologanin)。

图5 马钱素-7-酮的结构Fig.5 Chemical structure of ketologanin

图6 马钱素-7-酮质谱图Fig.6 ESI-MS of ketologanin

图7 马钱素-7-酮的1H-NMR 图Fig.7 1H-NMR of ketologanin

图8 马钱素-7-酮的13C-NMR 图Fig.8 13C-NMR of ketologanin
2.1.3 1-β-甲氧基马钱子苷元 (1-β-O-methyl loganin aglucone) 1-β-甲氧基马钱子苷元,无色油状物,ESI 质谱显示m/z 243.12209[M+H]+。1HNMR 谱显示δH7.35 (1H,s)处为一个烯氢信号,4.93 (1H,d,J=3.3 Hz)处为半缩醛氢信号,3.40(3H,s)和3.65 (3H,s)为两个甲氧基信号,1.05(3H,d,J=7.2 Hz) 处有甲基信号,1H-NMR 谱数据表明其可能为环烯醚萜类成分。13C-NMR 谱显示有12 个碳信号,δC51.6 和57.1 处为两个甲氧基碳信号,δC169.5 处为一个酯羰基信号,其余9个碳信号为环烯醚萜结构信号,因此推测其为环烯醚萜类成分。将以上数据与文献[19]数据对比,鉴定该化合物为1-β-甲氧基马钱子苷元(1-β-Omethyl loganin aglucone)。
图9 1-β-甲氧基马钱子苷元的结构Fig.9 Chemical structure of 1-β-O-methyl loganin aglucon

图10 1-β-甲氧基马钱子苷元的质谱图Fig.10 ESI-MS of 1-β-O-methyl loganin aglucon

图11 1-β-甲氧基马钱子苷元的1H-NMR 图Fig.11 1H-NMR of1-β-O-methyl loganin aglucon

图12 1-β-甲氧基马钱子苷元的13C-NMR 图Fig.12 13C-NMR of 1-β-O-methyl loganin aglucon
2.1.4 1-去羟基马钱子苷元(1-deoxyloganin aglycone) 1-去羟基马钱子苷元,无色油状物,ESI 质谱显示m/z 213.11269[M+H]+。1H-NMR 谱显示一个烯氢信号δH7.55 (1H,s),一个甲基氢信号δH1.05 (3H,d,J=7.1 Hz)和一个甲氧基氢信号δH3.66 (3H,s)。13C-NMR 谱显示有11 个碳信号,其中δC112.9,156.8 和170.0 3 个信号为α,β 不饱和酮信号,两个连氧碳信号位于δC75.2 和67.9。根据NMR 数据推测该化合物为环烯醚萜类成分,未发现半缩醛信号,推测该化合物为C-1 位去羟基的环烯醚萜类成分。将以上数据与文献[20]数据对比,鉴定该化合物为1-去羟基马钱子苷元(1-deoxyloganin aglycone)。

图13 1-去羟基马钱子苷元的结构Fig.13 Chemical structure of 1-deoxyloganin aglycone

图14 1-去羟基马钱子苷元的质谱图Fig.14 ESI-MS of 1-deoxyloganin aglycone
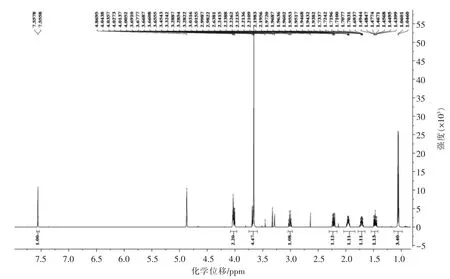
图15 1-去羟基马钱子苷元的1H-NMR 图Fig.15 1H-NMR of 1-deoxyloganin aglycone
2.2 化合物的波谱数据
2.2.1 马钱子苷的波谱数据 马钱子苷为白色粉末,ESI-MS m/z 435.14984[M+HCOOH-H]-。1HNMR (CD3OD,500MHz)δ:5.28 (1H,d,J=4.5 Hz,H-1),7.40 (1H,s,H-3),3.13 (1H,m,H-5),1.63 (1H,m,H-6α),2.24 (1H,m,H-6β),4.05 (1H,m,H-7),1.89 (1H,m,H-8),2.04(1H,m,H-9),1.11 (3H,d,J=7.0 Hz,H-10),3.70 (3H,s,11-OMe),4.66 (1H,d,J=7.9 Hz,H-1′),3.20 (1H,m,H-2′),3.35 (1H,o,H-3′),3.29 (1H,o,H-4′),3.38 (1H,m,H-5′),3.66 (1H,dd,J=5.7,11.9 Hz,H-6α′),3.91(1H,dd,J=2.1,11.9 Hz,H-6β′);13C-NMR(CD3OD,125MHz)δ:13.4 (C-10),31.6 (C-5),42.1 (C-8),42.7(C-6),46.5 (C-9),51.6 (11-OCH3),62.7 (C-6′),71.6 (C-4′),74.7 (C-7),75.0 (C-2′),78.0 (C-5′),78.4 (C-3′),97.7 (C-1),100.1 (C-1′),114.0 (C-4),152.1 (C-3),169.5(C-11)。
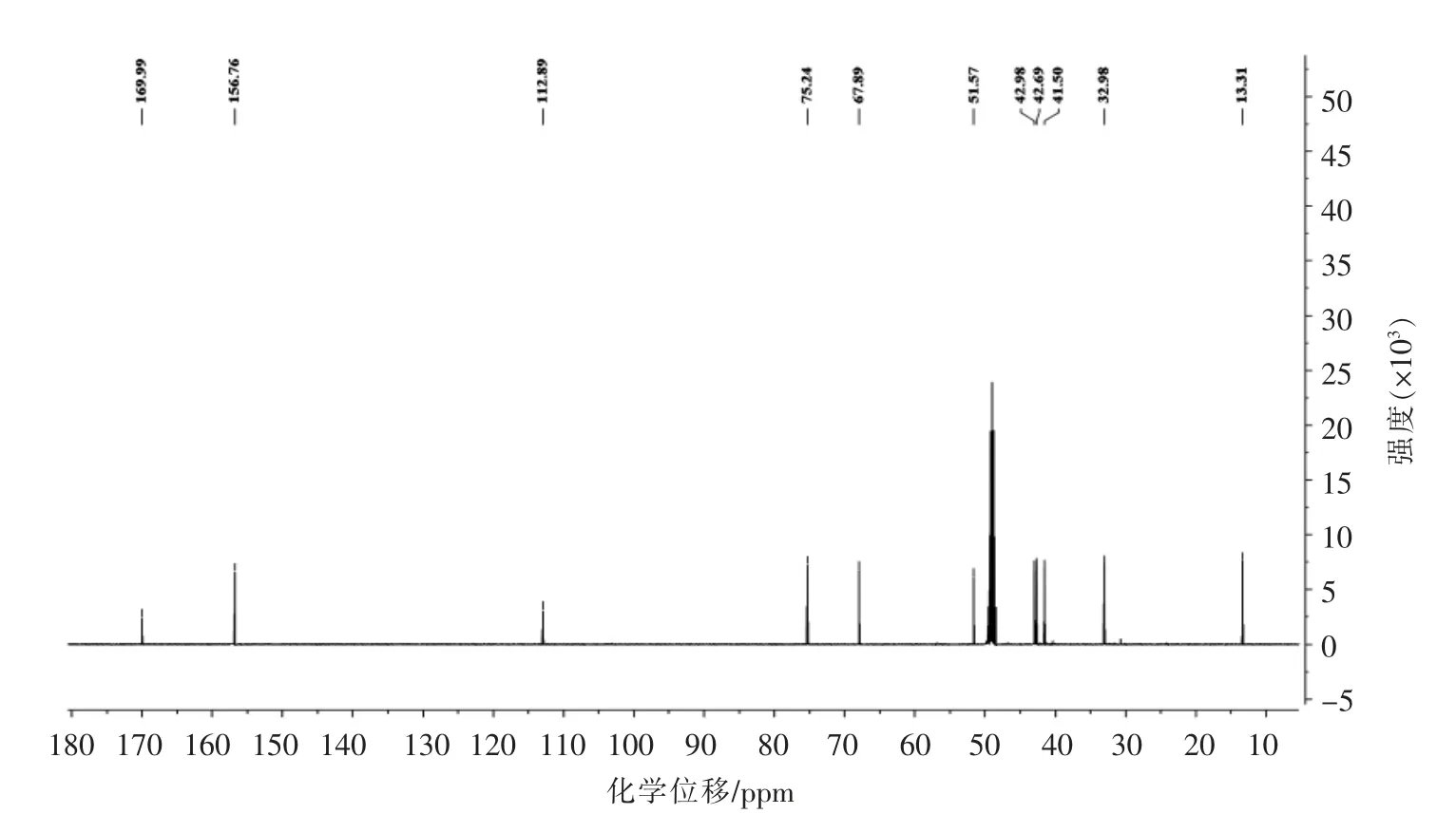
图16 1-去羟基马钱子苷元的13C-NMR 图Fig.16 13C-NMR of 1-deoxyloganin aglycone
2.2.2 马钱素-7-酮的波谱数据 马钱素-7-酮为白色粉末,ESI-MS m/z[M+HCOOH-H]-。1H-NMR(CD3OD,500MHz) δ:5.61 (1H,d,J=3.1 Hz,H-1),7.46 (1H,s,H-3),3.23 (1H,m,H-5),2.31 (1H,m,H-6α),2.58 (1H,dd,J=8.3,11.0 Hz,H-6β),2.06 (1H,m,H-8),2.51 (1H,m,H-9),1.12 (3H,d,J=7.2 Hz,H-10),3.67(3H,s,11-OMe),4.64 (1H,d,J=7.9 Hz,H-1′),3.16 (1H,dd,J=8.0,9.2 Hz,H-2′),3.35(1H,m,H-3′),3.21 (1H,m,H-4′),3.36 (1H,m,H-5′),3.62 (1H,dd,J=6.2,11.9 Hz,H-6α′),3.87 (1H,dd,J=2.2,11.9 Hz,H-6β?);13C-NMR (CD3OD,125MHz)δ:13.6 (C-10),28.3(C-5),43.4(C-6),44.6 (C-8),46.5 (C-9),51.7(-OCH3),62.7 (C-6′),71.5 (C-4′),74.6 (C-2′),77.9 (C-5′),78.4 (C-3′),95.2 (C-1),100.1(C-1′),111.0 (C-4),153.3 (C-3),168.8 (C-11),220.7(C-7)。
2.2.3 1-β-甲氧基马钱子苷元 1-β-甲氧基马钱子苷元为无色油状物,ESI-MS m/z 243.12209[M+H]+。1H-NMR (CD3OD,500MHz)δ:7.53 (1H,s,H-3),4.93 (1H,d,J=3.3 Hz,H-1),4.04 (1H,m,H-7),3.01 (1H,m,H-5),2.17 (1H,m,H-9),2.09 (1H,m,H-6α),1.65 (1H,m,H-6β),2.05 (1H,m,H-8),1.05 (3H,d,J=7.2 Hz,H-10),3.40 (3H,s,11-OMe),3.65 (3H,s,7-OMe)。13C-NMR (CD3OD,125MHz) δ:15.0 (C-10),33.5 (C-5),39.8 (C-6),40.2 (C-8),47.3(C-9),51.6 (11-OMe),57.1 (7-OMe),75.3 (C-7),103.3 (C-1),113.4 (C-4),152.6 (C-3),169.5(C-11).
2.2.4 1-去羟基马钱子苷元 1-去羟基马钱子苷元为无色油状物,ESI-MS m/z 213.11269 [M+H]+。1H-NMR (CD3OD,500MHz)δ:7.55 (1H,s,H-3),4.00 (1H,o,H-1α),3.67 (1H,o,H-1β),7.55 (1H,s,H-3),3.00 (1H,m,H-5),1.46(1H,m,H-6α),2.22 (1H,m,H-6β),4.01(1H,o,H-7),1.71 (1H,m,H-8),2.21 (1H,m,H-9),1.05 (3H,d,J=7.1 Hz,H-10),3.66(3H,s,-OCH3)。13C-NMR (CD3OD,125MHz)δ:13.3 (C-10),32.9 (C-5),41.5 (C-6),42.6(C-8),42.9 (C-9),51.6 (-OCH3),67.9 (C-1),75.2 (C-7),112.9 (C-4),156.8 (C-3),170.0(C-11)。
2.3 抗氧化活性
总抗氧化活性采用FRAP 总抗氧化能力检测试剂盒测定,结果显示:化合物1~4 均具有一定的抗氧化活性(表1),其中化合物1 和化合物2 的抗氧化活性强于化合物3 和4,推测环烯醚萜类成分连接单糖形成环烯醚萜苷后活性可能有所提升。
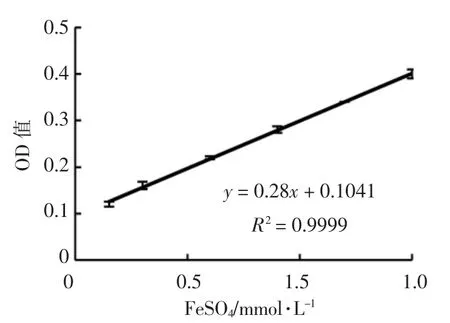
图17 FeSO4 标准曲线Fig.17 The standard curve of FeSO4

表1 环烯醚萜抗氧化活性Table 1 Antioxidant activities of iridoids from Cornus officinalis
3 结论
采用多种柱色谱相结合的方式(正相硅胶柱色谱、闪式低压正反相柱色谱、Sephadex LH-20凝胶柱色谱和反相高效液相色谱) 对山茱萸乙醇提取物中具有抗氧化活性的20%乙醇洗脱部位进行化学成分分离和纯化,共分离并鉴定了4 个环烯醚萜类化合物,分别为马钱子苷(1)、马钱素-7-酮(2)、1-β-甲氧基马钱子苷元(3)和1-去羟基马钱子苷元(4),其中化合物3 和4 为首次从山茱萸属中分离得到的新天然产物。
对分离得到的4 个环烯醚萜苷类化合物,采用铁离子还原力(FRAP)试验测定其总抗氧化能力,结果化合物1~4 均显示一定的抗氧化活性,其中马钱子苷和马钱素-7-酮的抗氧化能力最强。山茱萸中的其它环烯醚萜类成分也具有很好的抗氧化活性,说明山茱萸的抗氧化活性不是由单一成分引起,而是多成分共同作用的结果。

