人细小病毒B19核酸检测试剂国家参考品的建立
麻婷婷 许四宏 周海卫
人细小病毒B19(human parvovirus B19,B19V)属于细小病毒亚科,红病毒属[1]。成年后多达40%~60%的人被B19V 感染,老年约90%的人呈抗体阳性[2]。B19V 传播全年发生,但可能在冬季后期至夏季初见顶[3]。B19V 的唯一传染源为患者,主要通过呼吸道传播(飞沫、气溶胶)、血液制品污染和垂直传播[4]。B19V 在世界范围内有1 型、2 型和3 型,其中1 型可分为1a 和1b 型,3 型可以分为3a 和3b 型。1a型是目前在我国流行的主要型别,同时有少量1b 型和3 型存在[5]。目前国内B19V 核酸检测已有多家公司的产品研发成功,由于该类产品均无系统的质量评价和统一的质量标准,使得这些产品均未在我国获批上市。因此,建立人细小病毒B19 核酸检测试剂国家参考品,用于企业试剂研发的质量控制及评价已刻不容缓。为规范和提高国内此类产品的质量,本实验研制了人细小病毒B19 核酸检测试剂国家参考品,并制定了其质量标准。现报道如下。
1 材料与方法
1.1 试验材料
1.1.1 参考品原料来源
血浆样本由兰州生物制品研究所、武汉生物制品研究所、深圳市卫光生物制品股份有限公司及首都医科大学附属北京地坛医院提供。
1.1.2 国际标准品
世界卫生组织(world health organization,WHO)国际参考品(3rd WHO International Standard for Parvovirus B19 for Nucleic Acid Amplification Techniques,NIBSC code:12/208),标示浓度为1 410 000 IU/mL。WHO 国际参考品(Parvovirus B19 DNA Nucleic Acid Amplification Technology(NAT)based assays Genotype Panel,NIBSC code:09/110),该参考品包含B19 病毒1 型、2 型和3a 型,标示浓度分别为5.98 log10 IU/mL、5.94 log10 IU/mL和5.97 log10 IU/mL。
1.1.3 检测试剂
初筛使用上海科华生物工程股份有限公司的人细小病毒B19 核酸检测试剂盒(PCR-荧光探针法),确认使用In-house 巢式PCR 扩增及测序方法,引物序列见表1[6]。巢式PCR 第一轮反应条件为:第一步94℃热启动2 min;第二步94℃20 s,55℃30 s,72℃45 s,40 个 循 环;第 三 步72℃7 min。第二轮反应条件将循环过程中退火温度升至58℃。

表1 人细小病毒B19 核酸检测试剂国家参考品PCR 扩增及测序引物[6]Table 1 PCR amplification and sequencing primers of reference panel for Human Parvovirus B19 nucleic acid detection kits[6]
协作标定使用试剂包括苏州华益美生物科技有限公司、中山大学达安基因股份有限公司、上海之江生物科技股份有限公司和罗氏诊断产品上海有限公司共4 家企业的产品。稳定性研究使用试剂为上海科华生物工程股份有限公司的人细小病毒B19 核酸检测试剂盒(PCR-荧光探针法)。均匀性研究使用罗氏诊断产品上海有限公司的cobas TaqScreen DPX Test(甲肝和人细小病毒B19检测试剂盒)检测。
1.2 试验方法
1.2.1 参考品制备
筛选及确认后的原料样本经离心、过滤、稀释及分包装后组成参考品,分别编号为8 份阳性参考品PC01~PC08,10 份阴性参考品NC01~NC10,1 份高浓度样本经阴性稀释液稀释后得到精密度参考品(CV1、CV2)、以及1 份高浓度样本经稀释得到最低检出限参考品(L1、L2)。
1.2.2 溯源标定
将WHO 第三代人细小病毒B19 核酸国际标准品(NIBSC 编号12/208)进行梯度稀释后作为标准品,使用6 家企业的产品对精密度和最低检出限参考品进行溯源标定和赋值。
1.2.3 稳定性及均匀性考核
本参考品为定性使用。选择参考品中精密度以及浓度较低的阳性参考品PC04~PC08,分别经室温(25℃)放置24 h 及反复冻融3 次等处理后使用定性检测试剂盒进行检测,以考核其短期稳定性。
选择精密度参考品CV1 和CV2 进行均匀性研究。分别随机抽取10 支CV1 和CV2 样本,使用定性试剂盒进行检测,每支样本重复检测2 次。
1.2.4 统计分析
使用SPSS 16.0 软件进行统计分析。计量资料采用(±s)表示,组间采用t检验,多组间采用F检验,P<0.05 为差异有统计学意义。
2 结果
2.1 参考品的组成
收集的样本经PCR 扩增初筛、确认和定值后确定了参考品的组成。见表2。

表2 人细小病毒B19 核酸检测试剂国家参考品组成Table 2 Composition of reference panel for Human Parvovirus B19 nucleic acid detection kits
2.2 基因分型结果
对参考品中的阳性参考品进行基因分型,除PC01 属于1b 型以外,其余阳性均属于1a 型,见图1。
2.3 协作标定结果及质量标准
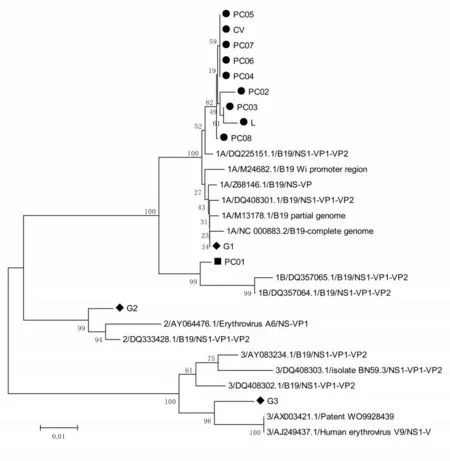
图1 人细小病毒B19 核酸检测试剂国家参考品原料样本基因进化分析结果Figure 1 Phylogenetic tree of reference panel for Human Parvovirus B19 nucleic acid detection kits
精密度参考品CV1 和CV2 的标定结果分别为中强阳性和弱阳性样本(Ct 值及定量值数据未展示)。4 种检测试剂对参考品进行标定。见表3。
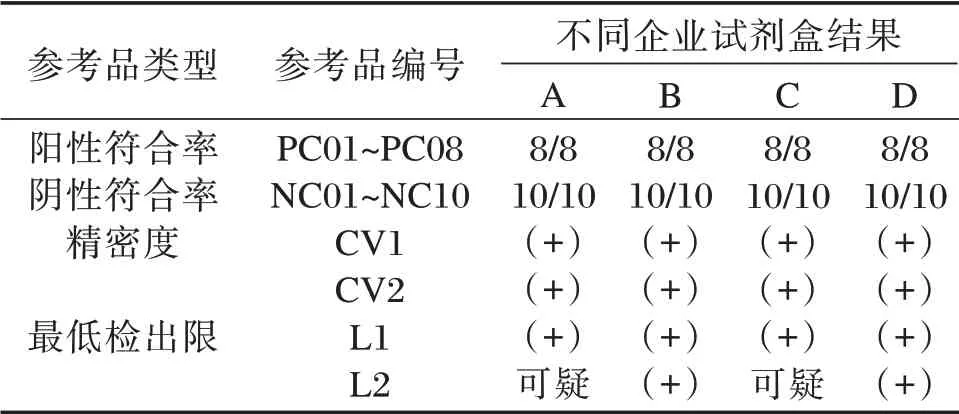
表3 人细小病毒B19 核酸检测试剂国家参考品协作标定Table 3 Cooperative calibration of reference panel for Human Parvovirus B19 nucleic acid detection kits
参考美国食品和药物管理局(food and drug administration,FDA)血液筛查标准(104IU/mL)及协作标定结果制定本参考品质量标准[7]:阳性参考品符合率8/8;阴性参考品符合率10/10;精密性变异系数≤5.0%;最低检出限参考品L1 应为阳性,L2可为阳性或阴性。
2.4 稳定性和均匀性
使用配对T 检验对不同处理后检测的Ct 值与-70℃保存条件下进行比较,室温25℃放置1 天处理的P值为0.175,反复冻融3 次处理的P值为0.174,表明2 种不同处理均不影响本参考品的稳定性。稳定性考察结果见表4。

表4 人细小病毒B19 核酸检测试剂国家参考品短期稳定性考察结果Table 4 Short-term stability test on reference panel for Human Parvovirus B19 nucleic acid detection kits
使用单因素方差分析对精密度参考品CV1 和CV2 的均匀性检测结果进行统计检验后显示,CV1 和CV2 的P值 分别 为0.574(F值=0.330)和0.867(F值=0.029),表明均匀性符合要求。
3 讨论
国际已有上市的B19V 核酸检测商用试剂盒(Qiagen 公司artus Parvo B19 LC PCR Kit 和Roche公司cobas TaqScreen DPX Test)[8]。FDA 对B19V核酸检测试剂要求必须涵盖目前已知的所有基因型,同时需要对检测方法进行方法学验证包含特异性、精密度、最低检出限等性能指标,欧洲药品管理局(european medicines agency,EMA)也有类似的标准[9]。WHO 已建立了第三代人细小病毒B19 核酸国际标准品和第一代人细小病毒B19 核酸分型国际参考品(NIBSC 编号分别为12/208 和09/110)[10]。目前我国还没有B19V 核酸诊断试剂的行业标准、审评指导原则和标准物质,还没有上市的B19V 核酸检测试剂。为对国内此类产品进行系统的质量评价并建立统一的质量标准,本研究研制了人细小病毒B19 核酸检测试剂定性用国家参考品(编号为370005-201601)。
本课题组对最低检出限和精密度参考品使用多家试剂进行定值,并已将其溯源至WHO 的第三代人细小病毒B19 核酸国际标准品(NIBSC编码12/208)。B19V 能明确引起输血者感染的最低病毒载量还没有明确,大多数实验结果显示,病毒滴度为105IU/mL 时一般不会发生感染[11-12]。因此美国FDA、欧洲药典和国际血浆蛋白治疗协会先后将混合血浆B19V DNA 含量不超过104IU/mL 作为核酸检测筛查的标准[7,13-14]。本研究将最低检出限参考品L1 和L2 浓度分别设定为2.4×103和2.4×102IU/mL,并要求L1 应为阳性,L2 可为阳性或阴性,该标准既满足上述各机构B19 核酸检测筛查标准又能对试剂进行灵敏度评估并体现试剂间性能差异。同时为保证样本在运输、保存和使用过程中的稳定性,对参考品的稳定性进行了考查,结果本研究中的冻融及室温处理方式不会影响本参考品的稳定性。其均匀性评估结果显示参考品的均匀性也能够满足使用需要。
另外,为满足国内企业研发试剂溯源需求,本课题组还研制了人细小病毒B19 核酸检测试剂国家标准品(编号为370023-201601),并同样将其量值溯源至WHO 的第三代人细小病毒B19 核酸国际标准品,企业可用于研发试剂及质量控制时的量值溯源、性能评估及质量控制等。本参考品及上述标准品的研制确定了我国B19V 核酸检测试剂的最低质量要求,能够为企业研发相关试剂建立统一的质量标准。