白酒中微量元素快速检测技术的探讨
◎ 武静文,赵 荻,蒲道俊,徐 洁,范能全
(1.重庆市食品药品检验检测研究院,重庆 401121;2.西南药业股份有限公司,重庆 400038)
中国白酒文化历史悠久,近年来越来越多的消费者追求饮酒口感及其健康属性,而白酒中的金属元素是高品质白酒的关键影响因素,如酒体中钙、镁、铁、铜、锌等元素,能够促进酒精的分解,使酒体更加醇厚、丰满圆润[1];白酒中的铅、锰、镉、铝等元素,长期摄入会严重影响人体健康[2]。近年来白酒质量问题屡见报端[3],建立白酒中多种元素快速检测技术,不仅是市场监管部门的监管需要,同时也是生产厂家保证白酒稳定性的技术支撑。
白酒元素检测前处理技术是元素检测的核心,相较于一般样品直接通过硝酸-微波消解进行前处理,白酒中乙醇与浓硝酸混合会发生剧烈反应,产生大量有刺激性气味,有毒的二氧化氮气体,密封的装置会发生爆炸。目前,国家标准未给出白酒元素检测前处理方法[4],其他文献资料所采用方法多为将白酒水浴浓缩赶醇后再进行消解处理[5],其缺点在于前处理复杂且耗时长,易造成元素损耗和污染,此法尤其不适用于批量大、检验快的监督监管。感耦合等离子体原子发射光谱法(ICP-OES法)相比于其他的元素定量分析方法如原子吸收法(包括石墨炉法和火焰法)、电感耦合等离子体质谱法(ICP-MS法),具有抗干扰性强、线性范围宽、能准确快速地同时测定多种元素等优点[6]。本研究拟采用微波消解法、稀释法(包含3种处理方式)对市面所售常见高浓度白酒(56%)进行前处理,并运用ICP-OES对白酒中23种元素进行测定比对,以期筛选出白酒元素快速测定的最佳前处理方法。
1 材料与方法
1.1 仪器与试剂
iCAP7400型电感耦合等离子体发射光谱仪(ICPOES),生产厂家为美国Thermo Fisher;MARS6型微波消解仪,生产厂家为美国CEM。
铝(Al)、砷(As)、硼(B)、钡(Ba)、镉(Cd)、钴(Co)、铬(Cr)、铜(Cu)、铁(Fe)、锂(Li)、镁(Mg)、锰(Mn)、镍(Ni)、铅(Pb)、锑(Sb)、锡(Sn)、锶(Sr)、钛(Ti)、铊(Tl)、钒(V)和锌(Zn)多元素混合标准液,浓度为100 μg·mL-1。
硅(Si)标准溶液:批号为18B044,购自国家有色金属及电子材料分析测试中心,浓度为1 000 μg·mL-1;钙(Ca)标准溶液:批号为19092,购自中国计量科学研究院,浓度为1 000 μg·mL-1;硝酸为优级纯,水为超纯水。研究所用样品为56%某二锅头白酒,批号为20181220,产品执行标准为GB/T 10781.2—2006(一级),提供单位为北京某白酒公司。
1.2 ICP-OES仪器参数
泵速:50 r·min-1;辅助气流量:0.5 L·min-1;RF功率:1 150 W;观测方式为水平;元素波长:B 249.773 nm;Al 396.152 nm;Si 212.412 nm;Li 670.784 nm;Mg 279.553 nm;Ca 317.933 nm;Ti 334.941 nm;Zn 213.856 nm;Cu 324.754 nm;Ni 221.647 nm;Co 228.616 nm;Fe 259.940 nm;Mn 259.373 nm;Cr 283.563 nm;As 189.042 nm;Sn 189.989 nm;Sb 206.833 nm;Sr 407.711 nm;Tl 190.856 nm;V 292.402 nm;Cd 228.802 nm;Ba 445.403 nm;Pb 220.353 nm。
1.3 溶液的制备
(1)标准溶液制备。取100 μg·mL-1多元素混标溶液5 mL、1 000 μg·mL-1硅标准溶液0.5 mL、1 000 μg·mL-1钙标准溶液0.5 mL,加入至50 mL容量瓶中,用5%硝酸定容至刻度,得到10 μg·mL-1混标溶液。分别取10μg·mL-1混标溶液0.25 mL、0.5 mL、1 mL、1.5 mL、2.5 mL、4 mL、5 mL和7.5 mL加入各自对应的50 mL容量瓶中,用5%硝酸定容至刻度,得到50 ng·mL-1、100 ng·mL-1、200 ng·mL-1、300 ng·mL-1、500 ng·mL-1、800 ng·mL-1、1 000 ng·mL-1和1 500 ng·mL-1混标系列溶液。
(2)微波消解法样品待测液制备。取白酒2 mL放入聚四氟乙烯消解罐中,在赶酸仪上100 ℃浓缩至0.5 mL,加入7 mL HNO3,加盖密封后放入微波消解仪,将温度5 min内升高到120 ℃,并维持10 min,再于5 min内将温度升高到185 ℃,维持20 min。然后在赶酸仪上80 ℃低温赶酸3小时,经多次冲洗至50 mL容量瓶中,定容到刻度。同时进行空白试验。
(3)A稀释法样品制备。取白酒20 mL置于50 mL聚四氟乙烯消解罐中,在赶酸仪上100 ℃浓缩至10 mL,经1% HNO3多次冲洗至50 mL容量瓶中,定容到刻度。同时进行空白试验。
(4)B稀释法样品制备。取白酒2 mL置于50 mL容量瓶中,加1% HNO3定容至刻度。
(5)C稀释法样品制备。取白酒0.5 mL置于50 mL容量瓶中,加1% HNO3定容至刻度。
1.4 供试品加标溶液制备
(1)微波消解法加标溶液制备。取白酒2 mL放入聚四氟乙烯消解罐中,在赶酸仪上100 ℃浓缩至0.5 mL,加入7 mL HNO3、1mL 10 μg·mL-1混标溶液,按照上述样品待测液制备方法定容至50 mL,得200 ng·mL-1加 标 溶 液。同 法 制 得500 ng·mL-1、800 ng·mL-1的加标溶液。
(2)A稀释法样品加标液制备。取白酒20 mL放入50 mL聚四氟乙烯消解罐中,在赶酸仪上100 ℃浓缩至10 mL,经1% HNO3多次冲洗至50 mL容量瓶中,加入1 mL 10 μg·mL-1混标溶液,定容到刻度。同法制得500 ng·mL-1、800 ng·mL-1的加标溶液。
(3)B稀释法样品加标液制备。取白酒2 mL放入50 mL容量瓶中,加入1 mL 10 μg·mL-1混标溶液,用1% HNO3定容至刻度。同法制得500 ng·mL-1、800 ng·mL-1的加标溶液。
(4)C稀释法样品加标液制备。取白酒0.5 mL放入50 mL容量瓶中,加入1 mL 10 μg·mL-1混标溶液,用1% HNO3定容至刻度。同法制得500 ng·mL-1、800 ng·mL-1的加标溶液。
1.5 线性关系、检出限及定量限
在确定的仪器测量条件下,将标准曲线溶液引入光谱仪,以溶液浓度为横坐标,以发射的谱线强度为纵坐标绘制标准曲线,取样品空白,连续测定11次,由11次浓度读数的标准偏差(SD)计算检出限(3SD)和定量限(10SD)[7-8]。
1.6 精密度与稳定性测定
精密度考察指标包括重复性和中间精密度。取500 ng·mL-1标准溶液连续测定6次,将各元素浓度得到相对标准偏差(RSD)作为精密度[9]。由分析员M对500 ng·mL-1标准溶液重复进样3次,1 d后由分析员N新配制500 ng·mL-1标准溶液并重复进样3次,统计6次结果的相对标准偏差作为中间精密度[10]。
取500 ng·mL-1标准溶液,分别取两个时间点各测定1次,根据各元素两次浓度值按式(1)计算变化率。

式中,A-第一时间点的测定值,B-不同时间的测定值,C-变化率[11]。
1.7 特异性与系统适用性
取标准空白、100 ng·mL-1标准溶液、500 ng·mL-1标准溶液及样品溶液按顺序进行测定[12]。考察100 ng·mL-1标准溶液、500 ng·mL-1标准溶液所测浓度是否存在5倍关系来确定元素所选波长是否具有专属性。对比所测元素在100 ng·mL-1前后两次的变化率以验证白酒溶液是否对检测系统带来实质性干扰[13]。
2 结果与分析
2.1 线性关系、检出限及定量限的考察
由表1可知,23种元素线性在0~1 500 ng·mL-1范围内均表现良好,Ni、Mn、Cr、Ti、Al和Sr相关系数在0.997~0.999,其余16种元素均在0.999以上,表明元素所选波长的线性性能良好。
Li、Ni、Co、Cd、Mn、Mg、Cr、V、Ca、Ti、Ba和Zn等11种元素检出限在1 ng·mL-1以内,定量限在3 ng·mL-1以下,检测性能良好,其余元素检出限均在6 ng·mL-1以内,定量限在20 ng·mL-1以下,满足检测需求。
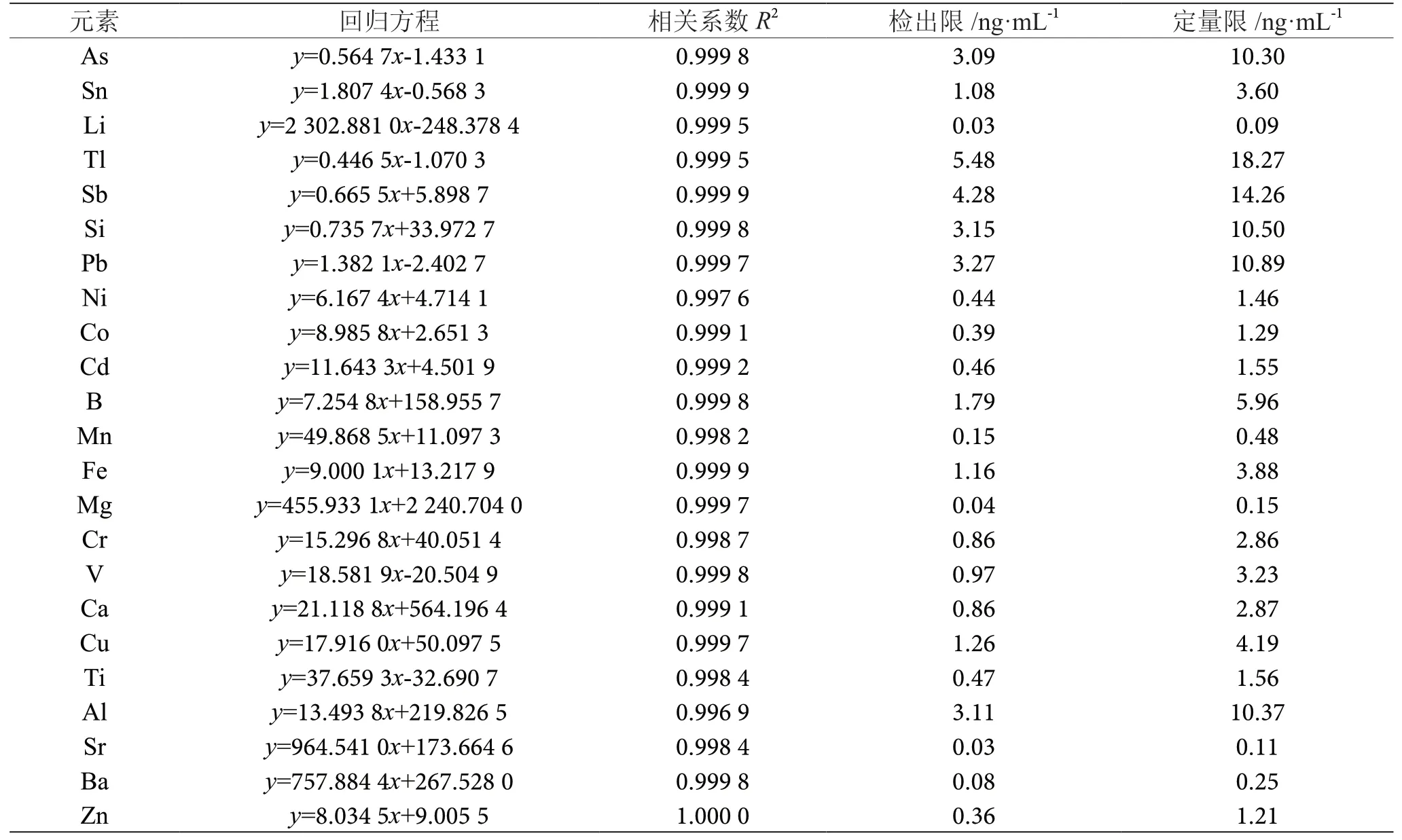
表1 各元素线性关系、检出限及定量限表
2.2 精密度与稳定性
由表2可知,23种元素的重复性均在1%以内;Cd、Mn、Ti三种元素的中间精密度在3%~6%,其余元素的中间精密度均小于3%;所有元素在2 h变化率在10%以内,表明ICP-OES分析性能良好,受到检测人员、测定时间等干扰因素的影响较小,能够满足方法学要求。
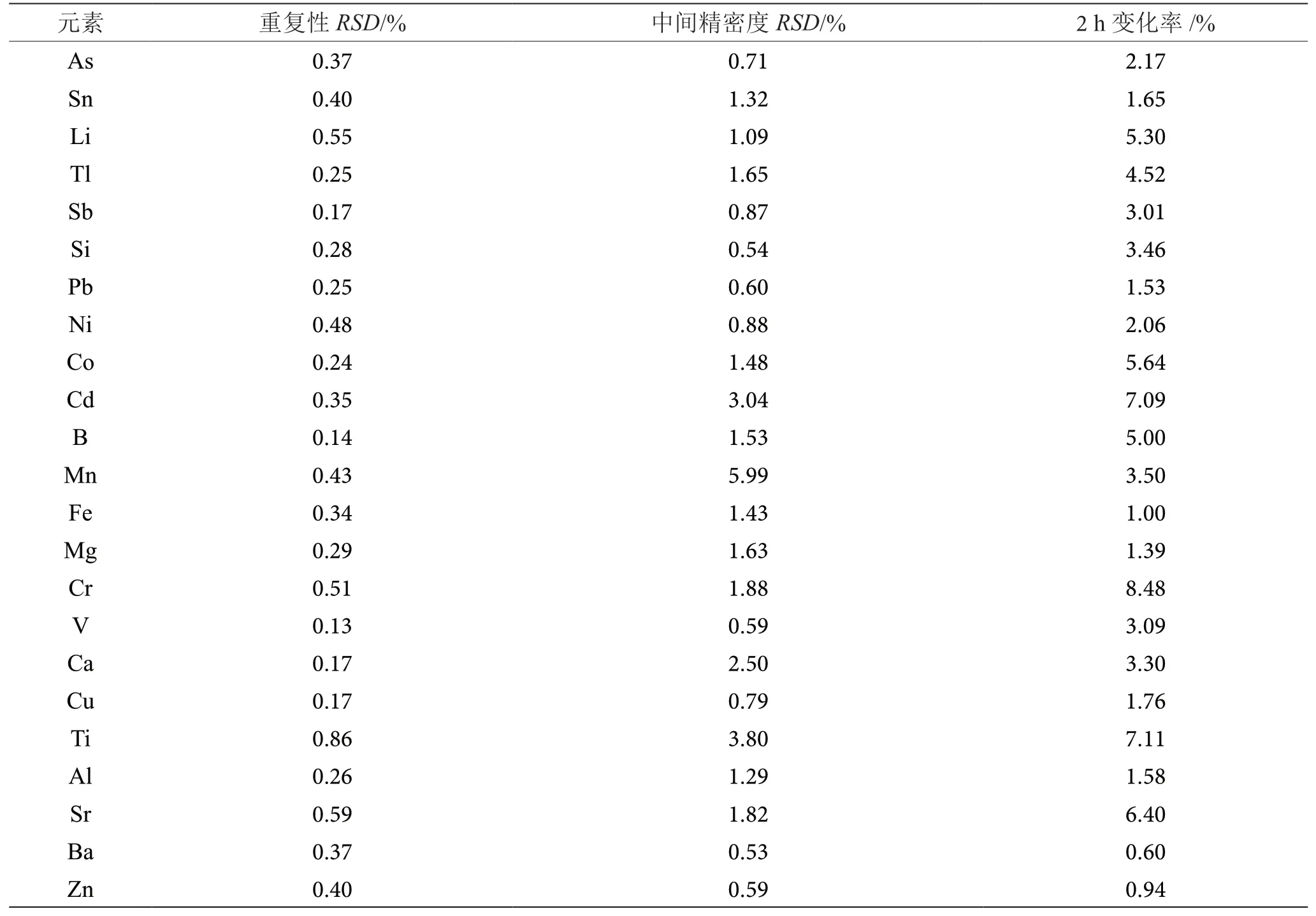
表2 精密度与稳定性实验结果表
2.3 特异性与系统适用性
由表3可知,500 ng·mL-1标准溶液所测浓度约为100 ng·mL-1标准溶液的5倍,而标准空白基本均未检出,显示元素所选波长具有特异性。23种元素在100 ng·mL-1标准溶液的变化率均为5%以内,表明白酒溶液并未对检测系统带来实质性干扰,系统适用性结果良好。
2.4 加标回收试验
由表4可知,除A稀释法、B稀释法As的加标回收率在130%以上,其余方法的元素加标回收率在70%~130%,均符合方法学要求。加标回收率偏高的原因可能为,甲醇、乙醇等有机物质使溶液的表面张力和粘性降低,同时溶液的可燃性使仪器尾焰温度提高,从而影响谱线强度,使测量值偏高[14-15]。
2.5 样品含量试验结果
用4种处理方式对同一样品进行处理,含量测定结果见表5。由表5可知,随着稀释倍数的增加(2.5倍、25倍、100倍),稀释法所测样品含量逐渐升高,到100倍测量结果已无法呈现线性关系,严重偏离真值;表明稀释法虽然能有效降低样品待测液中有机物质的干扰,但稀释倍数是影响结果的关键因素。微波消解法可有效减少有机物质干扰,常用作测定食品、药品中元素含量的方法,结果可靠。依据微波消解法结果,A、B稀释法结果接近,C稀释法不符合测定要求。
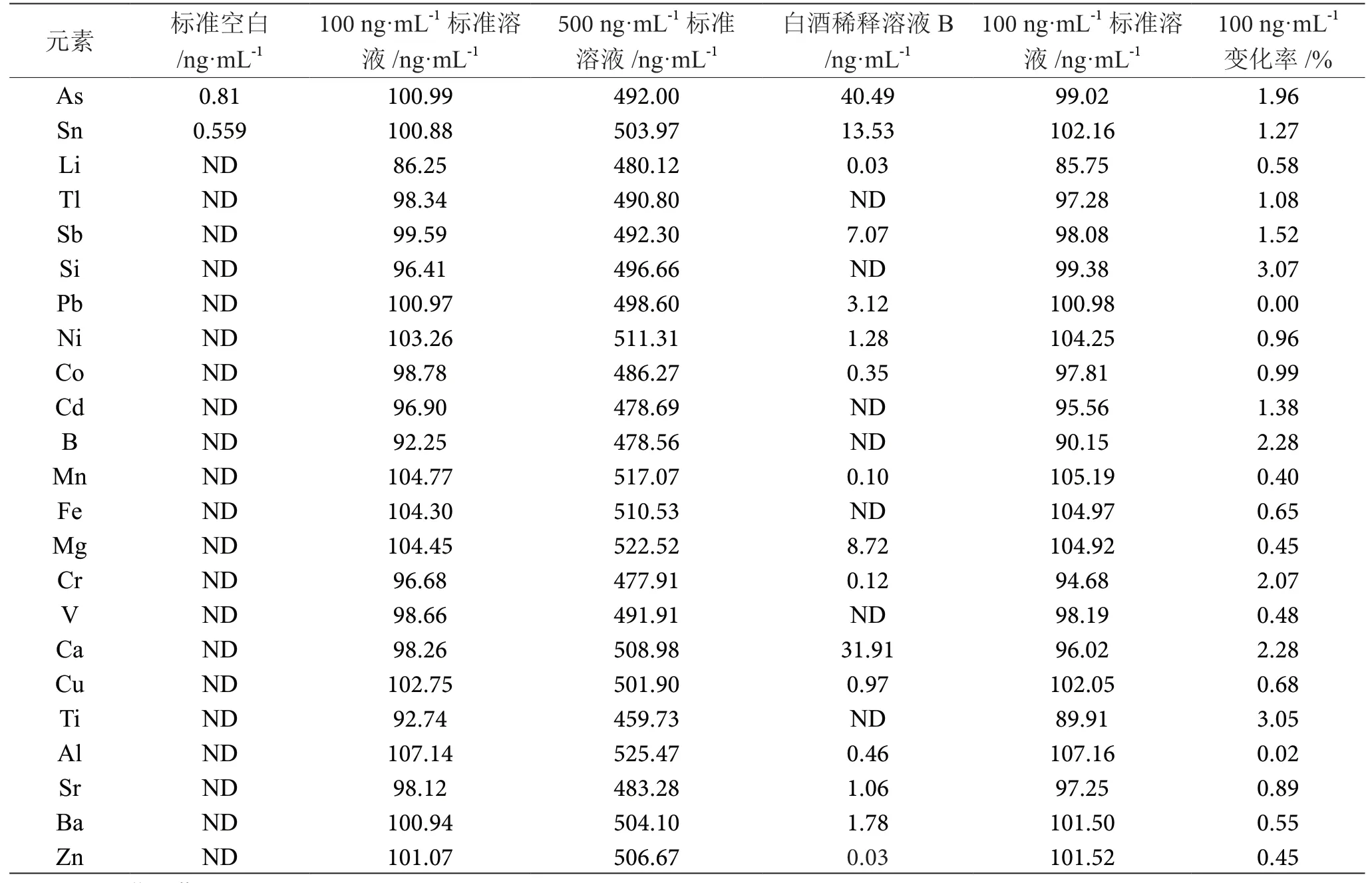
表3 特异性与系统适用性实验结果表
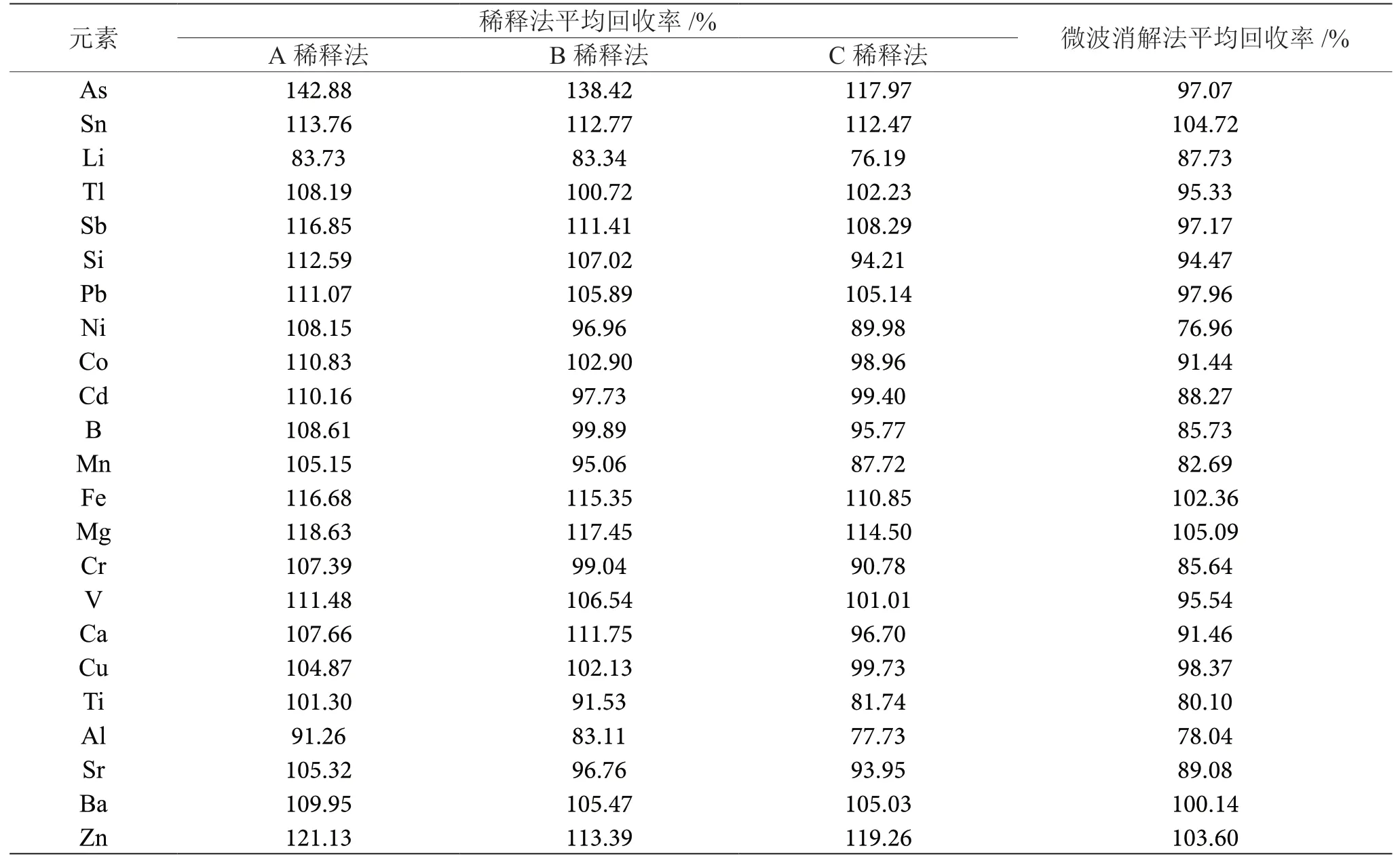
表4 加标回收率试验结果表

表5 样品含量试验结果表
2.6 方法学比对与评价
由于稀释法、消解法的系统适用性良好,样品处理液均不会对检测系统带来明显影响,为体现方法的精密性,以加标回收率作为方法比对与评价的指标:加标回收率100%±10%划为优秀,80%~90%或110%~120%为良好,70%~80%或120%~145%为合格。由图1可知,4种方法回收率的效果优劣顺序为B稀释法>微波消解法>C稀释法>A稀释法。
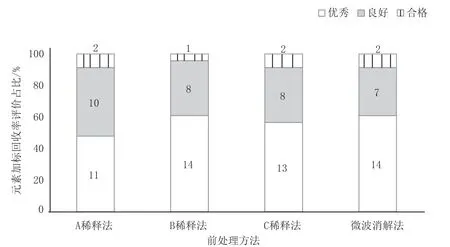
图1 方法类型-加标回收率评价图
3 结论
(1)23种元素的检出限均低于6 ng·mL-1,能够满足检测需要,白酒稀释溶液未对ICP-OES检测系统形成有效干扰。常用快速分析多种元素的仪器主要有电感耦合等离子体质谱仪(ICP-MS)和ICP-OES,相比于ICP-MS,ICP-OES虽然具有较高的检出限(ICP-OES法的检出限为10-10,ICP-MS法的检出限为10-15~10-12),但灵敏度与稳定性一般成反比关系,因此ICP-OES抗干扰性较好[16],更适合稀释法这种简单、快捷的前处理方法。
(2)微波消解结合微波加热和高压消解两方面的性能,有效减少消解过程中造成的挥发损失和环境污染、降低试剂用量,但此法缺点为消解完毕后冷却时间较长且由于受到微波消解仪的限制,一般不能同时处理大批样品[17]。通过以微波消解法样品测定结果为参考值,稀释A法和B法与参考法较为接近;通过以加标回收率作为方法比对与评价的指标,优劣顺序为B稀释法>微波消解法>A稀释法;前处理耗时长短顺序为B稀释法>A稀释法>微波消解法;综合上述,白酒中23种元素的快速检测前处理方法选用B稀释法。

