阿帕替尼联合化疗作为二线及以上方案治疗晚期胃癌或胃食管结合部腺癌的疗效观察
何昌霞,丁德权,曹齐生,陈 磊,杜成荣,黄志荣
(马鞍山市人民医院肿瘤介入科,安徽省马鞍山市 243000)
胃癌(gastric carcinoma,GC)在中国的恶性肿瘤中发病率居第2位,死亡率居第3位。患者经常在临床诊断时已达局部晚期或全身多处转移,无手术指征,通常采用以化疗为主的综合治疗[1-2]。尽管已有多种化疗药物用于晚期GC一线或二线治疗,但是在二线治疗失败后缺乏公认的标准治疗方案[3]。近年来,GC的靶向治疗中抗血管生成药物是一个研究热点。血管生成是肿瘤恶性生长的关键环节之一,持续的血管生成和肿瘤的发生、发展、转移有关,抗血管生成是肿瘤治疗的有效途径和重要方法[4]。阿帕替尼是新一代小分子血管内皮生长因子受体-2(vascular endothelial growth factor receptor-2,VEGFR-2)酪氨酸激酶抑制剂,其主要作用机制是竞争性结合该受体胞内酪氨酸ATP结合位点,高度选择性地抑制VEGFR-2酪氨酸激酶活性,阻断血管内皮生长因子(vascular endothelial growth factor,VEGF)结合后的信号传导,从而强效抑制肿瘤血管生成,发挥抗肿瘤作用[5]。多中心、随机、双盲临床试验证实,相较于安慰剂,阿帕替尼可延长全身化疗失败的晚期GC或胃食管交界癌(adenocarcinoma of the gastroesophageal junction,AGEJ)患者中位生存期(median overall survival,mOS)和中位无进展生存期(median progression free survival,mPFS),且不良反应可控[6]。阿帕替尼目前已经用于临床治疗晚期胃癌或胃-食管结合部腺癌。然而,抗血管生成药物联合化疗治疗晚期胃癌的临床疗效仍不清楚,两者是否具有协同抗肿瘤作用需进一步研究。本研究旨在晚期GC或AGEJ患者中比较阿帕替尼联合化疗与单独化疗作为二线及以上治疗方案的疗效。
1 资料和方法
1.1 一般资料
选择2015年2月—2018年1月在本院肿瘤介入科治疗的晚期GC或AGEJ患者129例。按照治疗方法不同分别纳入单独化疗组(77例,接受单独化疗)和联合化疗组(52例,接受阿帕替尼联合化疗)。本研究经本院伦理委员会批准。
纳入标准:①年龄18~75岁;②东部肿瘤协作组(ECOG)体能状态评分0~1分;③经胃镜检查及病理学确诊的晚期GC或AGEJ(局部晚期、复发胃或胃食管结合部腺癌且患者无手术完全切除适应证;或存在转移性病灶);④既往至少一线化疗失败;⑤有至少1个可用影像学CT或MRI测量的靶病灶。
排除标准:①患有高血压且经降压药物治疗无法降至正常范围者(收缩压>140 mmHg,舒张压>90 mmHg);②具有出血倾向的患者,凝血功能异常的患者,或服用止血剂、抗凝剂的患者;③存在心、脑、肝、肾等重要器官功能障碍,或血液学检查不符合化疗基本要求;④具有影响口服药物的多种因素,例如无法吞咽、恶心、呕吐、慢性腹泻和肠梗阻等;⑤具有明确的胃肠道出血倾向的患者,例如有局部活动性溃疡病灶,且大便潜血(++);2个月内有黑便、呕血病史者;⑥存在其他化疗相关禁忌证。
1.2 治疗方案
联合化疗组患者在化疗基础上同时接受口服阿帕替尼治疗(商品名艾坦,购自江苏恒瑞医药股份有限公司),剂量为500 mg/天,每日1次,口服,28天为1个治疗周期。当治疗过程中出现与阿帕替尼相关的3级或以上不良反应时,可减阿帕替尼剂量为250 mg/天。两组患者均接受以紫杉类或伊立替康类或奥沙利铂为基础的单药或者联合化疗方案[7]。所有方案持续21~28天为1个周期,均完成2~6个周期治疗。稳定和有效的患者继续行原化疗方案(不允许剂量增加),直至进展或出现不能耐受的毒性,或患者拒绝接受化疗。出现3、4级毒性的患者减少化疗药物的剂量25%~50%,或停止化疗,并给予支持治疗。
1.3 疗效及不良反应评价标准
参照RECIST 1.1实体瘤疗效评价标准[8]进行近期疗效评价,分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD),以CR+PR为客观缓解;以CR+PR+SD为疾病控制。完全缓解(CR):所有靶病灶消失,全部病理淋巴结(包括靶结节和非靶结节)短直径必须减少至<10 mm。部分缓解(PR):靶病灶直径之和比基线水平减少至少30%。疾病进展(PD):以整个研究期间所有测量的靶病灶直径之和的最小值为参照,直径增加至少20%(如果基线测量值最小就以基线值为参照),同时直径和的绝对值增加至少5 mm(出现一个或多个新病灶也视为疾病进展)。疾病稳定(SD):靶病灶减小的程度没达到PR,增加的程度也没达到PD水平,介于两者之间,以直径之和的最小值作为参考。每两个周期化疗后进行CT和/或MRI等相关影像学检查以评价疗效直至疾病进展。无进展生存期(PFS)指患者阿帕替尼联合化疗或单独化疗作为二线及以上治疗至出现疾病进展或末次随访时间。所有不良反应评价按照美国国立癌症研究所制订的通用药物毒性反应标准(NCI-CTC 3.0)版分级标准来进行[7]。
1.4 随访
治疗期间的前12个月内,每2个周期进行1次肿瘤影像学评估;之后每3个周期进行1次肿瘤影像学评估。患者在停止治疗时也应完成安全性检查和影像学评估。安全性随访期从末次治疗后开始,每30天随访1次,直至末次给药后90天。生存随访期至患者死亡、失访。在此期间,每1个月通过电话随访等有效方式进行1次访视,收集患者生存信息。
1.5 统计方法
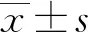
2 结 果
2.1 临床病理特征
两组患者基线资料包括性别、年龄、ECOG体能状态评分、化疗方案、病理分级、原发病灶部位、既往是否行胃切除术、转移情况、转移灶个数、既往化疗和是否接受放疗,差异均无显著性,具有可比性(P>0.05;表1)。
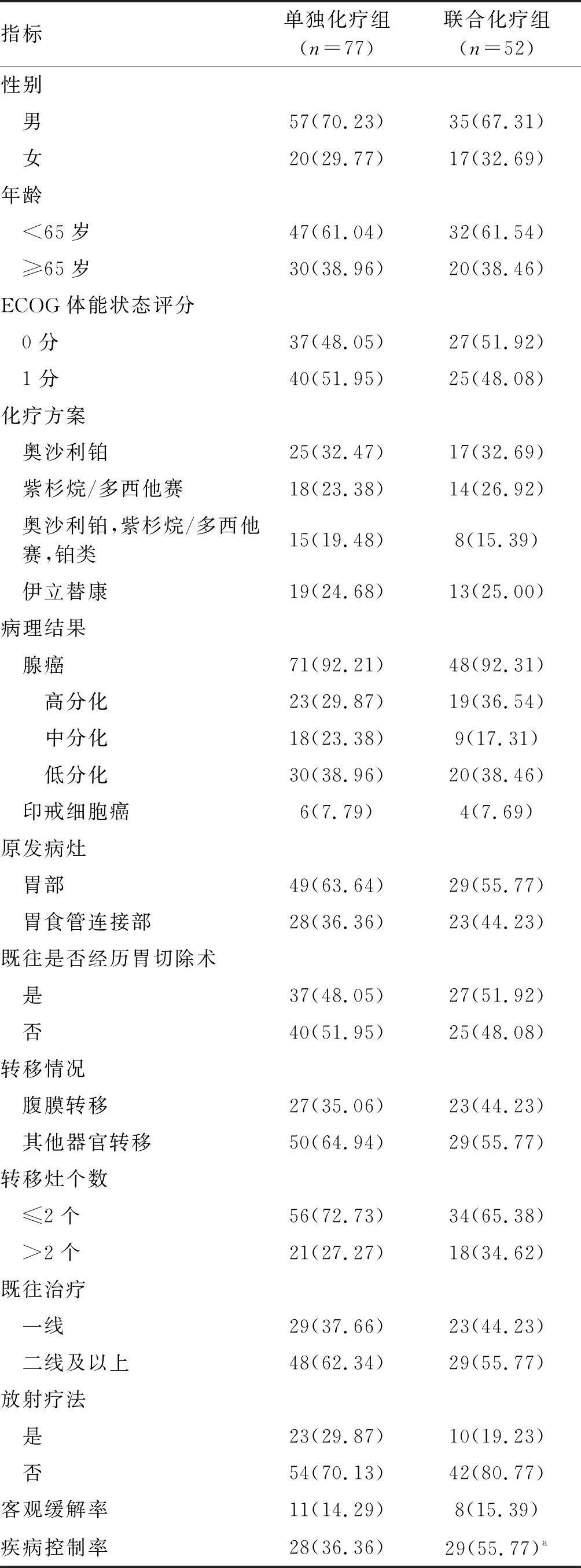
表1 联合化疗组和单独化疗组患者病理特征比较 单位:例(%)
2.2 短期疗效和生存分析
联合化疗组中客观缓解率为15.39%,单独化疗组中客观缓解率为14.29%,两组比较差异无统计学意义(P>0.05)。联合化疗组患者疾病控制率高于单独化疗组(55.77%比36.36%,P<0.05;表1)。Kaplan-Meier生存曲线结果显示,联合化疗组患者的中位PFS显著长于单独化疗组患者(P<0.05;图1A),且转移灶个数≤2个患者的中位PFS显著长于转移灶个数>2个(P<0.05;图1B)。
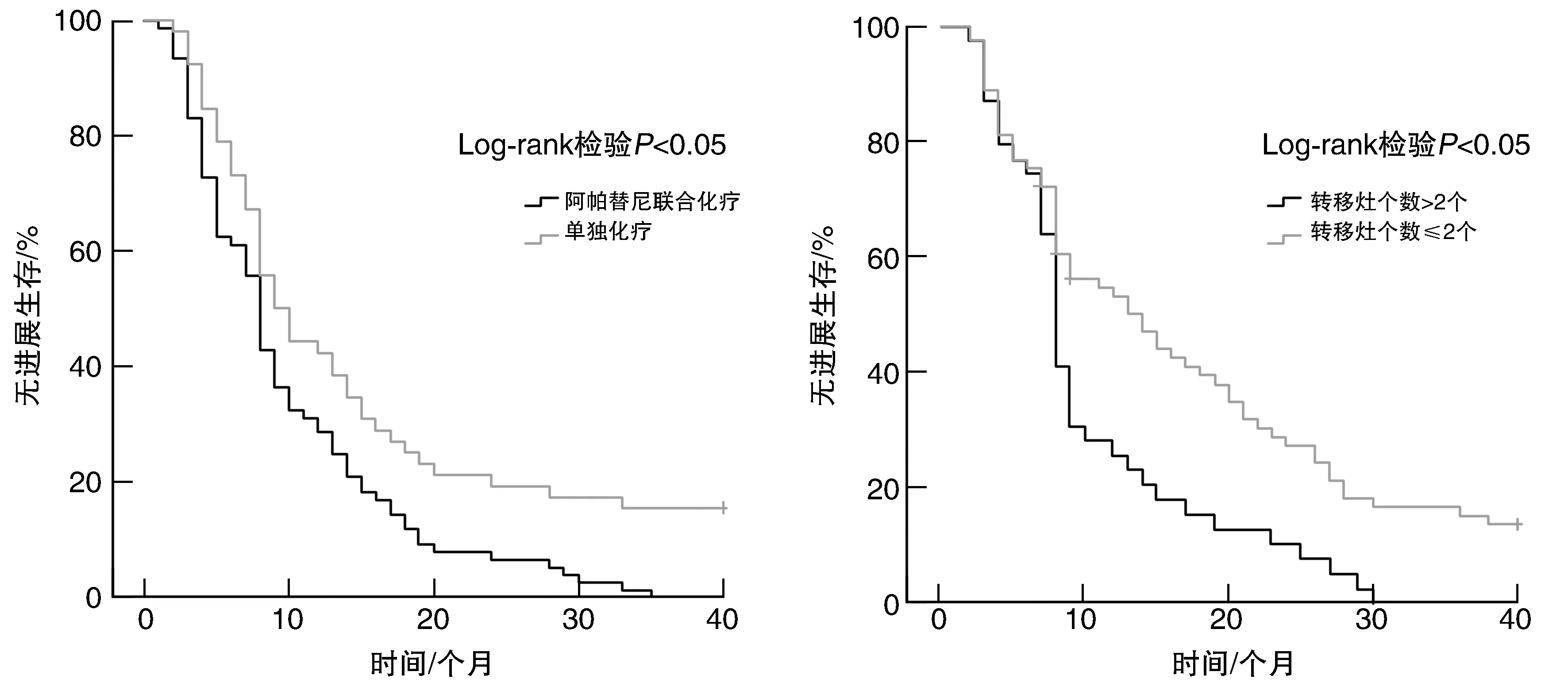
图1 Kaplan-Meier生存曲线评估晚期GC或AGEJ患者PFS
2.3 晚期GC或AGEJ PFS影响因素分析
多因素Cox回归分析结果显示,经过校正其他混杂因素,转移灶个数>2个(P<0.05)和治疗方法(P<0.05)均是晚期GC或AGEJ患者PFS的独立影响因素(表2)。
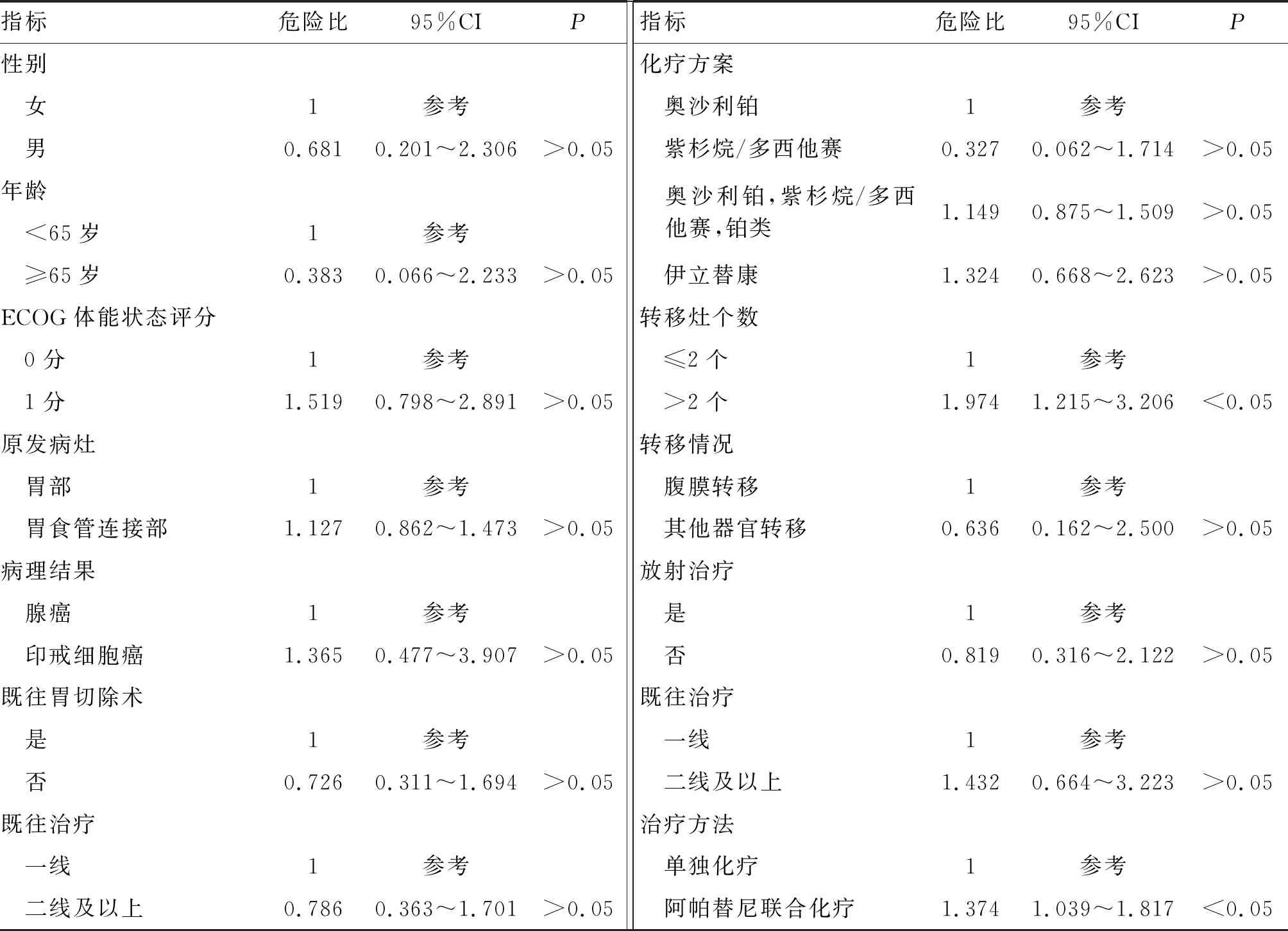
表2 影响晚期GC或AGEJ患者PFS的多因素Cox回归分析
2.4 安全性分析
129例患者均至少接受了2个治疗周期,患者平均完成了(4.5±2.3)个治疗周期,患者常见的不良反应有白细胞减少症、中性粒细胞减少症、贫血、血小板减少症、蛋白尿、高血压、手足综合征、转氨酶升高、高胆红素血症、出血、感觉神经病变、腹部疼痛、呕吐或食欲降低、低蛋白血症和腹泻。与单独化疗组比较,联合化疗组患者发生手足皮肤反应、蛋白尿、高血压等的比例较高,差异均有统计学意义(P<0.05)。所有的上述毒性反应在经药物减量、停药及对症治疗后均在患者可耐受范围内,没有患者出现5级不良反应(表3)。
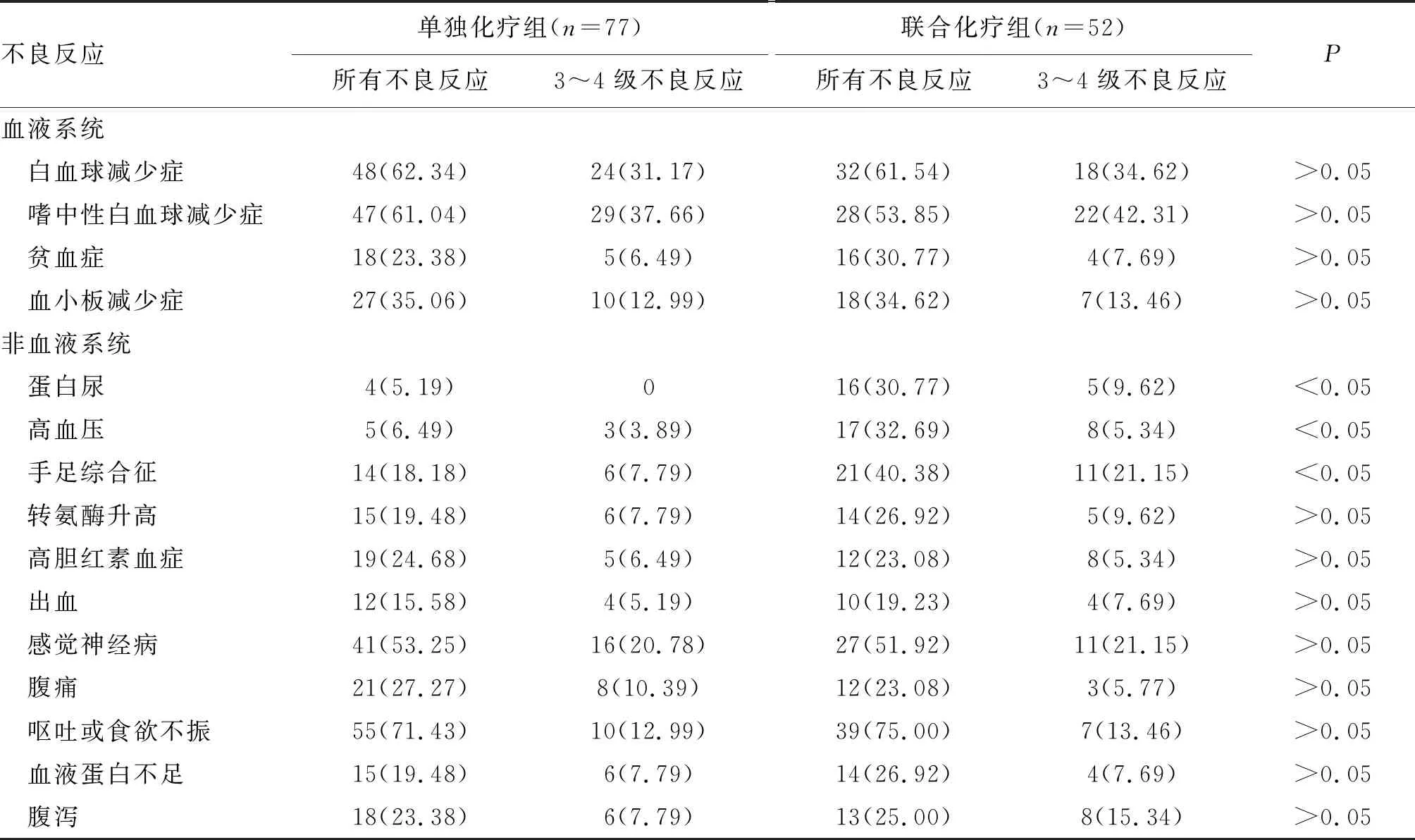
表3 联合化疗组和单独化疗组不良反应的比较 单位:例(%)
3 讨 论
GC或AGEJ复发和转移风险较高,在东亚地区的发病率和死亡率一直居高不下[9]。与单纯支持疗法比较,晚期GC姑息性化疗的疗效已经得到广泛认可。晚期GC的二线治疗具有一定程度的生存获益,标准治疗方案尚未确立。中国近年来使用紫杉类、奥沙利铂以及伊立替康为主方案解救一线治疗失败的晚期GC,但由于化疗药物的毒副作用和肿瘤细胞的耐药性等因素,化疗的结果仍不尽如意[10]。血管生成在实体肿瘤发生发展过程中扮演着不可或缺的角色,因此,靶向肿瘤血管生成可作为研究及治疗的热点,一些小分子靶向药物联合化疗治疗晚期GC显示出独特的优势,为晚期GC一线治疗失败的患者带来希望,其中VEGFR-2被认为是其家族中与血管生成关系比较密切的受体[11]。REGARD及RAINBOW临床试验均显示雷莫芦单抗作为二线药物可改善GC患者生存结局[12]。与雷莫芦单抗比较,阿帕替尼口服给药更方便,患者依从性更好。阿帕替尼作用靶点主要为VEGFR-2,抑制VEGF与之结合及自体磷酸化,从而抑制血管形成,降低肿瘤微血管密度,有效抑制肿瘤血管生长[4]。
阿帕替尼用于三线治疗晚期GC的大型临床实验已经结束,已在临床上用于治疗三线及三线以上的晚期GC或AGEJ患者。Guo等[13]将阿帕替尼用于二线方案对晚期GC进行治疗发现,阿帕替尼治疗二线及二线以上治疗失败的晚期GC仍有较好的疾病控制及生存获益,不良反应可控制。本文研究结果表明,与单纯化疗组比较,联合化疗组晚期GC或AGEJ既往至少一线化疗失败患者PFS呈现延长趋势,且患者耐受性好,阿帕替尼相关不良反应可控。与既往阿帕替尼联合多西他赛作为二线化疗治疗进展性GC的临床试验结果相一致[14]。
作为特异性靶向VEGFR2靶点的小分子酪氨酸激酶抑制剂,阿帕替尼目前在胃癌、结直肠癌、肺癌等领域均取得了不错的治疗效果[5]。在安全性方面,2期和3期阿帕替尼临床研究中,不良反应的类型和发生率基本一致,亦与已上市的其他同类药物相类似。常见的不良反应包括白细胞减少、中性粒细胞减少、血小板下降、高血压、蛋白尿、手足皮肤反应、乏力、食欲减退和腹泻等,未出现非预期的不良反应。多数不良反应均可通过暂停给药、剂量下调及对症处理实现控制和逆转[15]。目前对阿帕替尼生物标志物的研究还比较少,主要集中在阿帕替尼治疗引起的不良反应及对疗效的预测方面,比如服用阿帕替尼早期出现高血压、磷酸化VEGFR-2高表达、蛋白尿和手足综合征等表现对抗血管生成治疗效果可能有潜在预测价值[16]。本研究结果显示阿帕替尼和化疗联合治疗以及转移灶个数<2个是进展性GC预后的独立影响因素,这与既往阿帕替尼单药治疗的临床试验结果一致[17]。
综上所述,本文研究结果表明,与单独化疗比较,阿帕替尼联合化疗方案可以显著提高晚期GC或AGEJ既往至少一线化疗失败患者的疾病控制率,延长患者的无进展生存期,耐受性好,带来临床获益,值得推广应用。阿帕替尼联合哪种化疗方案会有更好的临床疗效和安全性,以及是否可以把阿帕替尼提前用于一线治疗可能会带来更大的临床获益等问题,仍然需要临床长期随访的大样本多中心随机对照试验来验证。

