“益生菌1号”治疗肠易激综合征的临床疗效研究
刘 宣,刘露路,王 珏,郑 艳,曾 懿,古 赛
(重庆医科大学附属第一医院消化内科,重庆 400016)
肠易激综合征(IBS)是十分常见的慢性功能性胃肠病,主要表现为反复腹痛伴大便习惯、性状改变,根据粪便性状其分为腹泻型IBS(IBS-D)、便秘型IBS(IBS-C)、混合型IBS(IBS-M)和不定型IBS(IBS-U),其全球发病率高达10%~20%,且以IBS-D亚型为主,造成较大的医疗负担。IBS发病机制尚未完全明了,已有证据表明,胃肠道微生物失调和IBS有关[1-6],补充益生菌可能对IBS患者产生一定疗效。人体肠道微生态十分复杂,有益菌种类繁多,针对IBS给予单一或混合益生菌治疗的研究近年来也十分活跃,本研究旨在观察由婴儿双歧杆菌B145、嗜酸乳杆菌LA85、干酪乳杆菌LC89及乳酸片球菌4种益生菌组合而成的一种新型复合益生菌制剂(“益生菌1号”)治疗IBS患者中2个亚型即IBS-D、IBS-C的临床疗效,为治疗IBS提供更多的选择。
1 资料与方法
1.1资料
1.1.1研究对象 选取2020年7-12月本院收治的300例IBS患者。
1.1.2纳入标准 (1)年龄18~65岁;(2)男女不限;(3)根据罗马Ⅳ诊断标准诊断为IBS-D、IBS-C;(4)1年内行肠镜检查未见异常;(5)大便隐血阴性;(6)自愿接受并遵守本研究方案,按时接受复查及随访;(7)签署知情同意书。
1.1.3排除标准 (1)妊娠及哺乳妇女,或者研究期间有生育计划的女性患者;(2)伴有精神性疾病患者;(3)研究前1个月服用过抗生素者(服用抗生素者停用抗生素1个月后可入组);(4)近2周服用过益生菌、做过肠道清洁或肠镜的患者(服用益生菌者停药2周后及做肠道清洁或肠镜者2周后可入组);(5)对本研究所用药物过敏患者;(6)有消化系统肿瘤及胃肠道手术史、肠梗阻、消化道出血患者;(7)严重心肺疾病、糖尿病患者,或其他慢性疾病需要长期服药的患者;(8)不愿意加入本试验,拒绝签署知情同意书或综合判断依从性较差的患者。
1.1.4剔除标准和终止标准(不纳入研究结果分析) (1)出现难以忍受的不良反应,患者要求停药,但纳入不良反应的结果分析;(2)患者或家属要求退出本研究;(3)患者用药期间不能按本研究要求服药,漏服药或自行服用可能影响本研究结果的药物(如抗生素、止泻药、泻药、其他益生菌制剂或抗精神病类药物等);(4)未能按本研究流程完成随访的患者或失访者。
1.2方法
1.2.1药物 (1)“益生菌1号”由婴儿双歧杆菌B145、嗜酸乳杆菌LA85、干酪乳杆菌LC89及乳酸片球菌4种益生菌组成,每毫升含益生菌CFU大于100×108个。(2)安慰剂中则不含上述益生菌。2种药物为饮品,均由北京百思乐乳业有限公司统一生产,外观包装一致,均为淡橙色液体,呈微酸甜、微醇香口味,低温(15 ℃以下)储存。
1.2.2研究方法 (1)信息采集:包括患者姓名、性别、年龄、身高、体重、联系方式等,以及纳入、排除标准中涉及的信息。(2)随机分组:采用随机数字表法,按照服药药物不同将患者分为试验组(服用“益生菌1号”)和对照组(服用安慰剂),并根据IBS类型不同将试验组和对照组分为IBS-D试验亚组、IBS-C试验亚组、IBS-D对照亚组、IBS-C对照亚组。(3)双盲:研究过程中研究者及患者均不知情所服用的药物为试验用药还是安慰剂,直至整个临床试验完成,从而保证双盲。(4)实施:口服“益生菌1号”或安慰剂,每天2次,每次25 mL,连续2周。
1.2.3观察指标 于服药0、1、2周,停药1周评估各组患者IBS病情严重程度调查表(IBS-SSS)评分、布里斯托大便分类法(Bristol)分型评分;于服药0、2周评估各组患者IBS生活质量量表(IBS-QOL)评分,并记录服药期间不良反应发生情况。(1)IBS-SSS: 即腹痛程度及频率、腹胀程度、大便满意度及肠道症状对生活的困扰5个问题,患者在100分的视觉模拟尺度上回答每个问题,总分0~500分[7]。IBS-SSS应答率是以服药2周后IBS-SSS总分下降50分作为应答,有应答的患者占该研究组所有患者的比例即为总体应答率。(2)大便Bristol分型评分:总分1~7分[8]。(3)IBS-QOL:包含34个条目和8个维度[9],得分越高表明生活质量越差。(4)用药期间不良反应:便秘、腹泻加重发生情况。
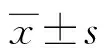
2 结 果
2.1一般情况 将300例符合纳入、排除标准的IBS患者(其中IBS-C 76例,IBS-D 224例)随机分为试验组154例(IBS-C试验亚组 40例,IBS-D试验亚组114例)与对照组146例(IBS-C对照亚组 36例,IBS-D对照亚组110例)。各组患者在性别、年龄、体重指数(BMI),IBS-SSS、IBS-QOL评分方面比较,差异均无统计学意义(P>0.05)。见表1。共计264例患者完成本研究,其中试验组134例(IBS-C试验亚组 37例,IBS-D试验亚组 97例),对照组130例(IBS-C对照亚组 35例,IBS-D对照亚组 95例)。
2.2IBS症状评估 服药前,试验、对照组患者间IBS-SSS评分比较,差异无统计学意义(P>0.05)。服药1、2周后,试验、对照组患者IBS-SSS评分较服药前均有显著下降,且试验组下降程度较对照组更明显,差异均有统计学意义(P<0.05),而试验、对照组患者服药2周与服药1周的IBS-SSS评分比较,差异均无统计学意义(P>0.05)。见表2。试验组患者IBS-SSS应答率[43.51%(67/154)]显著高于对照组[26.71%(39/146)],差异有统计学意义(P<0.05)。
亚组分析结果显示,服药1、2周后,IBS-D试验、对照亚组患者IBS-SSS评分较服药前均有显著下降,且试验亚组下降程度较对照组明显,差异均有统计学意义(P<0.05);而试验、对照亚组患者服药2周与服药1周的IBS-SSS评分比较,差异均无统计学意义(P>0.05)。IBS-C试验亚组患者IBS-SSS评分仅在服药2周后较服药前显著降低,差异有统计学意义(P<0.05);而IBS-C对照亚组服药前后无明显改变,差异无统计学意义(P>0.05)。见表2。

表1 患者基线资料情况
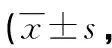
表2 服药前后各组患者IBS-SSS评分比较分)
停药1周后,对照组患者IBS-SSS评分较服药2周时显著回升,差异有统计学意义(P<0.05),而试验组较服药2周时无明显改变,差异无统计学意义(P>0.05)。见表3。
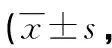
表3 试验、对照组患者停药1周与服药2周时IBS-SSS评分比较分)
2.3大便Bristol分型评分 服药前,IBS-D试验、对照亚组患者大便Bristol分型评分比较,差异均无统计学意义(P>0.05)。服药1、2周后,试验、对照亚组患者大便Bristol分型评分均较服药前显著降低,且试验亚组降低程度较对照亚组明显,差异均有统计学意义(P<0.05);而试验、对照亚组患者服药2周与服药1周的大便Bristol分型评分比较,差异均无统计学意义(P>0.05)。IBS-C试验、对照亚组患者治疗前后大便Bristol分型评分无明显变化,差异均无统计学意义(P>0.05)。见表4。
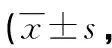
表4 服药前后各亚组患者大便Bristol分型评分比较分)
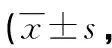
续表4 服药前后各亚组患者大便Bristol分型评分比较分)
与服药2周时比较,IBS-D对照亚组患者停药1周后大便Bristol分型评分显著回升,IBS-C对照亚组患者此评分显著下降,差异均有统计学意义(P<0.05);而IBS-D、IBS-C试验亚组较服药2周时前无明显改变,差异均无统计学意义(P>0.05)。见表5。
2.4IBS-QOL评分 服药前,试验组与对照组、IBS-D试验亚组与IBS-D对照亚组、IBS-C试验亚组与IBS-C对照亚组患者IBS-QOL评分比较,差异均无统计学意义(P>0.05)。服药2周后,试验、对照组及IBS-D试验、对照亚组患者IBS-QOL评分均较服药前显著下降,且试验组及IBS-D试验亚组下降程度较对照组及IBS-D对照亚组更明显,差异均有统计学意义(P<0.05)。IBS-C试验、对照亚组患者服药前后的IBS-QOL评分比较,差异均有统计学意义(P<0.05),未见其改变的组间差异。见表6。
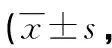
表5 各亚组患者停药1周与服药2周时大便Bristol分型评分比较分)
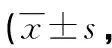
表6 服药前后各组患者IBS-QOL评分比较分)
2.5不良反应 本研究共发生5例不良反应,均发生在试验组中,见表7。其中IBS-D试验亚组患者中发生1例腹泻加重而中途退出研究,1例便秘加重;IBS-C试验亚组患者中发生3例便秘加重,其中1例中途退出研究。所有的不良反应在研究结束时均得到了解决。

表7 试验、对照组患者不良反应发生情况[n(%)]
3 讨 论
IBS病因及机制尚不十分清楚,大多认为是多因素相互作用的结果,而肠道微生态失衡可能是其机制之一。肠道菌群失衡主要体现在细菌种类、数量及分布异常上。有研究表明,IBS患者肠道菌群多样性减少,尤其是乳杆菌种群和双歧杆菌种群的减少[10],肠道微生态失衡可能通过增加肠道通透性、改变肠道动力、增加肠道敏感性和造成免疫系统活性失调而成为IBS的潜在触发因素[11]。近年来的研究还进一步证实微生物区系紊乱可能与IBS伴随的认知变化、焦虑和抑郁状态相关[12]。因此,补充益生菌制剂,维持肠道微生态平衡可能使IBS患者获益。
本研究为随机、双盲、安慰剂对照临床试验。部分关于IBS流行病学调查表明,IBS患者大多数为IBS-D和IBS-C[13-15],故本研究未纳入IBS-U和IBS-M病例。本研究结果发现,IBS-D试验亚组IBS-SSS评分、大便Bristol分型评分在服药1、2周后显著下降,IBS-QOL评分在服药2周后显著下降。IBS-C试验亚组IBS-SSS评分及IBS-QOL评分在服药2周后显著下降,而大便Bristol分型评分无明显改变,表明服用“益生菌1号”均能改善IBS-D和IBS-C患者临床症状,尤其对于IBS-D患者,还能改善其大便性状,提高生活质量。针对IBS-D患者,“益生菌1号”在服药1周时即起效,而对于IBS-C患者,起效稍慢,需服药2周方能见效。本研究中还观察到,停药1周内,试验组大多数患者症状无反复,表明“益生菌1号”在停药1周内能继续维持良好效应,其作用可能通过改变IBS患者肠道微生态,从而持续改善患者临床症状。
本研究观察到,“益生菌1号”针对IBS-C患者改善大便性状,提升生活质量方面尚不甚满意,可能与本次研究纳入IBS-C样本量相对较少,研究干预时间尚短,且是否在治疗IBS-C患者中存在延迟效应等有关。有研究表明,益生菌治疗IBS干预8周或更长时间,疗效较为显著[16]。一项关于益生菌治疗IBS-C的meta分析结果显示,试验干预期为2~16周,大多为4周以上,且提到干预2、4周间存在显著差异[17]。本研究中,IBS-C亚组服药2周后IBS-SSS评分才有显著降低,但短期内对大便性状和生活质量提升尚无明显效果,表明本研究中IBS-C亚组可能需要设置更长的干预期。
IBS患者常伴有或轻或重的焦虑和(或)抑郁情绪,往往这种情绪可能通过脑肠轴再次加重IBS患者症状[18]。IBS-QOL涉及焦虑不安、行为障碍、躯体意念、健康担忧、饮食限制、社会功能、性行为及人际关系8个维度,其评分下降可反映IBS患者焦虑、抑郁情绪也得到改善。IBS-D试验亚组患者IBS-QOL评分下降程度较IBS-D对照亚组有显著差异,说明“益生菌1号”在缓解患者IBS临床症状的同时,也显著改善了生活质量,减轻了焦虑和抑郁等负面情绪。
综上所述,服用“益生菌1号”2周可显著改善IBS-D、IBS-C患者临床症状,改善IBS-D患者的大便性状及生活质量,且服药1周开始起效,停药1周效果仍持续存在。IBS-C患者益生菌起效时间相对需要更长,考虑在IBS-C亚组中可能存在效应延迟情况。“益生菌1号”对IBS-D患者起效更快、效果更好。服药2周时,各组均未出现严重不良反应,说明“益生菌1号”是一种安全、有效的新型复合益生菌制剂,在IBS的治疗中值得推广,尤其在IBS-D患者中疗效显著。

