田蓟苷固体分散体的制备及体内药动学研究
于宁 谭梅娥 郑瑞芳 曾晓红
【摘 要】 目的:制备田蓟苷固体分散体(Til-SD),并考察其体内药动学行为。方法:以体外Til累积溶出度为考察指标,采用单因素试验对制备方法、载体的种类、载体与原料比例、制备温度、制备时间分别考察,在单因素试验基础上,采用正交试验设计优化制备工艺。通过差示扫描量热法(DSC)对Til-SD物相进行表征。大鼠灌胃给药后,HPLC法测定Til血药浓度,计算主要药动学参数。结果:采用溶剂-熔融法,载体为Plasdone S-630,Til与载体的比例为1∶7,制备温度为80℃、制备时间为60min时,制备的Til-SD的累积溶出度较原料药增加最为明显,在溶出30min时,累积溶出度可达91.1%,较原料药提高了7.4倍多。Til以非晶型状态均匀分散于载体Plasdone S-630中。与Til原料药比较,固体分散体相对生物利用度提高到218.5%。结论:固体分散体可促进Til口服吸收,提高其生物利用度。
【关键词】 田蓟苷;固体分散体;体内药动学;差示扫描量热法;生物利用度
【中图分类号】R285.5 【文献标志码】 A【文章编号】1007-8517(2021)04-0019-06
Abstract:Objective To prepare tilianin solid dispersions, and to investigate its in vivo pharmacokinetic behaviors.Methods Taking the cumulative percentage of dissolution in vitro as the index of investigation, taking the preparation technology, type of carrier, the ratio of carrier to raw material, mixing temperature and mixing time were the investigation factors. Based on the single factor experiment, orthogonal experiment design was used to optimize the experiment. Differential Scanning Calorimetry (DSC) was used to characterize the optimal solid dispersion. Rats were given intragastrical administrtaion, after which HPLC was adopted in the plasma concentration determination of tilianin, and main pharmacokinetic parameters were calculated.Results The optimum prepartion process of tilianin solid dispersion prepared is melting-solvent method, when the carrier was Plasdone S-630, the ratio of raw materials to carriers was 1∶7, mixing temperature was 80℃ and the mixing time was 60min, the cumulative dissolution percentage of tilianin solid dispersion can reach 91.1% in 30min, which is more than 7.4 times higher than tilianin. Tilianin mostly existed in solid dispersion in amorphous form. Compared to tilianin, the bioavailability of tilianin solid dispersions was enhanced to 218.5%,repectively.Conclusion Solid dispersion technology can obviously promote the in vivo absorption of tilianin and enhance its bioavailability.
Keywords:Tilianin; Solid dispersion; In vivo pharmacokinetics; Differential Scanning Calorimetry; Bioavailability
田薊苷(Tilianin,Til)是从新疆维吾尔族习用药材香青兰中,提取分离得到的天然黄酮类活性单体。香青兰主要用于治疗冠心病和高血压,始载于维吾尔古典医籍《阿里卡农》,已经有数百年的药用历史。课题组前期研究证明,Til是香青兰抗心肌缺血再灌注损伤的主要活性物质,与普萘洛尔疗效相比,较小剂量的Til即具有同等作用[1-5]。但Til水溶性差,在37℃纯水中的平衡溶解度为1.57mg/L,导致其体内吸收受到极大限制,严重影响药效发挥[6-8]。
固体分散体(Solid Dispersion,SD)是将难溶性药物在一定条件下高度分散到水溶性高分子材料中形成的一种给药制剂,其制备工艺相对简单,能够将药物高度分散,可大大改善药物的溶出与吸收,从而提高药物生物利用度,近年来,它已成为改善中药难溶性药物溶解性的常用技术[9-16]。因此,本实验将Til制成固体分散体(Til-SD),测定累积溶出度,采用DSC技术研究晶型变化,考察体内药动学,以期为Til相关口服制剂研究提供参考。
1 仪器与材料
Agilent1200高效液相色谱仪(美国Agilent公司);DRT TW型调温电热套(巩义市予华仪器有限责任公司);AB135-S梅特勒-托利多电子天平(瑞士);ZRS-8GD智能溶出仪(天津市天大天发科技有限公司);101-1型电热恒温鼓风干燥箱(上海跃进医疗器械厂);DZF-150型数显恒温真空干燥箱(河南省大康县教材仪器厂);EYELASB-2000型旋转蒸发仪(上海爱朗仪器有限公司);Vortex-5涡旋混合器(海门市其林贝尔仪器制造有限公司);KQ-100 DE型数控超声波清洗器(昆山市超声仪器有限公司);200F-3型差示扫描量热仪(德国耐士科技有限公司)。
田蓟苷原料药(批号:20171012,纯度≥98%,新疆维吾尔自治区药物研究所);PVPK30(批号:93811436W0,德固赛中国投资有限公司);Eudragit EPO100(批号:B060362009, 德固赛中国投资有限公司);Plasdone S-630(批号:15100265044,德国BASF公司);乙腈(色谱纯,美国Fisher公司);其他试剂均为分析纯;清洁级SD大鼠,体质量230~270g,购自新疆医科大学动物中心,许可证号:SCXK(新)2011-0004。
2 方法与结果
2.1 Til含量测定
2.1.1 色谱条件 Hypersil BDS C18 色谱柱(250mm×4.6mm,5μm);流动相为乙腈-0.5%甲酸水溶液(27∶73);体积流量1.0mL/min;波长为330nm;柱温为35℃。
2.1.2 线性关系考察 精密称取Til对照品适量,加入适量乙腈超声溶解,配制成每1mL含Til 180μg的对照品储备液,采用乙腈逐步稀释成1.80、3.24、9.00、12.60、18.00、27.00μg/mL的系列Til对照品溶液,在“2.1.1”项下色谱条件下进样测定,以峰面积(Y)对溶液质量浓度(X)进行回归,得方程为Y=29.311X+2.3420,r= 0.9993,表明在1.80~27.00μg/mL范围内线性关系良好。
2.1.3 方法学考察 取浓度为18.00μg/mL的Til对照品溶液,在上述色谱条件下,连续进样6次,测得峰面积的RSD为1.22%,表明仪器精密度良好;取Til-SD适量置于50mL量瓶中,45mL乙腈超声处理后定容至50mL,于0、2、4、6、8、12h在上述色谱条件下进样测定,测得峰面积RSD为1.37%,表明供试品溶液室温放置12h内稳定;精密称取已知含有量的Til-SD适量,加入一定质量浓度的对照品溶液,置于50mL量瓶中,45mL乙腈超声处理后定容至50mL,在上述色谱条件下进样测定,测得加样回收率为98.89~101.01%,RSD为1.13%。
2.2 体外溶出度试验 取待测样品适量,相当于原料药20mg,加入适量蒸馏水制成混悬液后置于活化后的透析袋中。用含0.2% SDS水溶液900mL作为溶出介质,温度为37℃,转速为100r/min,分别于10、15、30、45、60、90min时取样2mL,补加同体积等温空白溶出介质,取样溶液用0.45μm微孔滤膜过滤,取续滤液在“2.1.1”项下色谱条件进样测定,计算不同时间点的累积溶出度。
2.3 Til-SD制备工艺研究
2.3.1 制备方法载体材料及的比较 筛选亲水性高分子载体材料PVPK30、Eudragit EPO100、Plasdone S-630,分别通过溶剂法、溶剂-熔融法和熔融法制备固体分散体,确定Til-SD的制备方法及载体材料。
2.3.1.1 溶剂法 称取Til 20mg、载体材料PVPK30、Eudragit EPO100、Plasdone S-630分别称取140mg(原料与载体比例为1∶7),置于圆底烧瓶中,加入100mL无水乙醇,搅拌直至Til和载体均溶解成澄明液体,减压旋蒸除去有机溶剂,迅速置于-20℃冰箱中冷冻固化24h后,将干燥物取出,研碎,过80目筛,置干燥器避光保存。
2.3.1.2 溶剂-熔融法 称取Til 20mg置于烧杯中,加入100mL无水乙醇,备用;载体材料PVPK30、Eudragit EPO100、Plasdone S-630分別称取140mg,置于圆底烧瓶中,在80℃水浴加热使其熔融,将Til无水乙醇溶液加入熔融载体中继续搅拌均匀后,继续搅拌至60min,水浴蒸发除去有机溶剂,迅速置于-20℃冰箱中冷冻固化24h后,其他操作同上溶剂法。
2.3.1.3 熔融法 载体材料PVPK30、Eudragit EPO100、Plasdone S-630分别称取140mg,置于烧杯中,在80℃水浴加热其熔融,加入Til 20mg,边加边搅拌,使Til完全融于载体中,迅速置于-20℃冰箱中冷冻固化24h后,其他操作同上溶剂法。
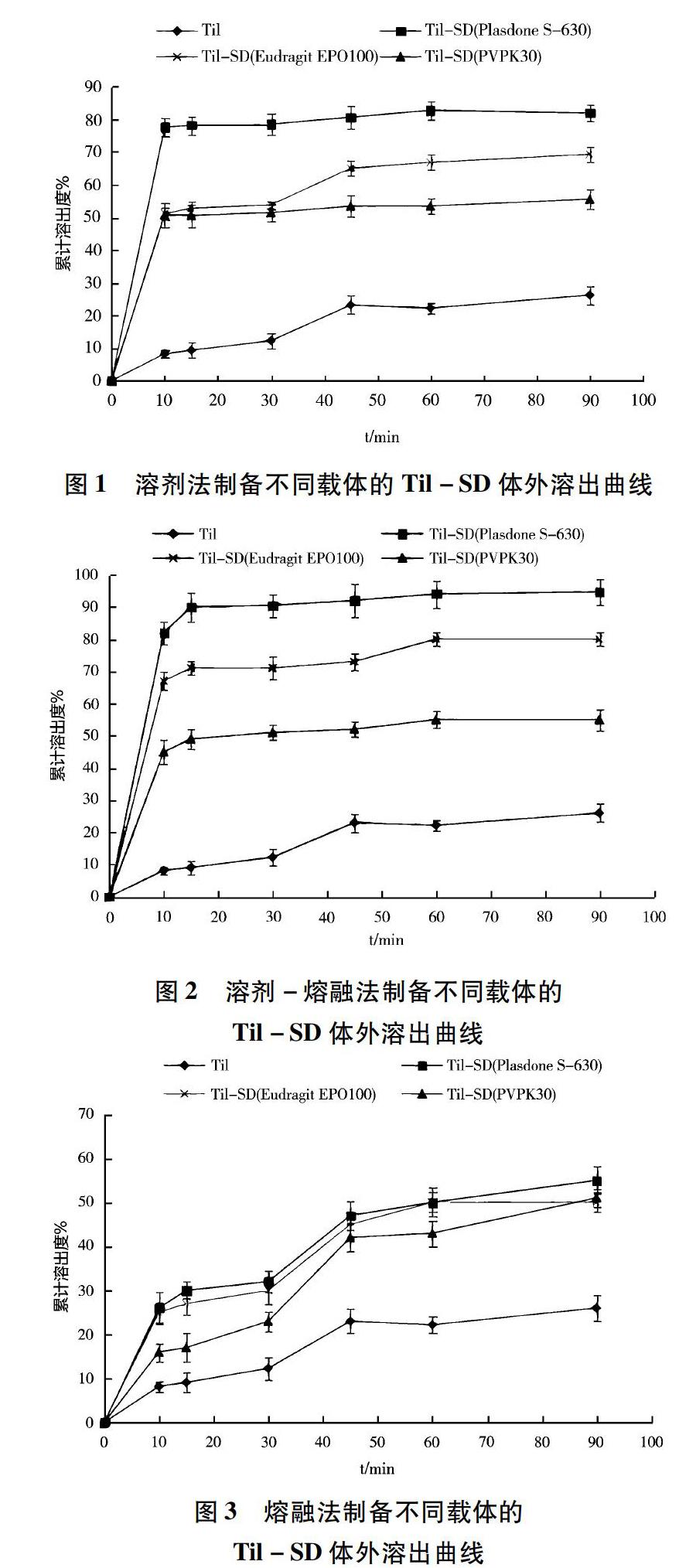
测定上述方法制备的Til-SD累积溶出度,结果如图1~3所示。表明,采用溶剂-熔融法、载体为Plasdone S-630制备Til-SD,Til的累计溶出度在60min时,可达到90%以上,因此,确定采用溶剂-熔融法,载体为Plasdone S-630制备Til-SD。
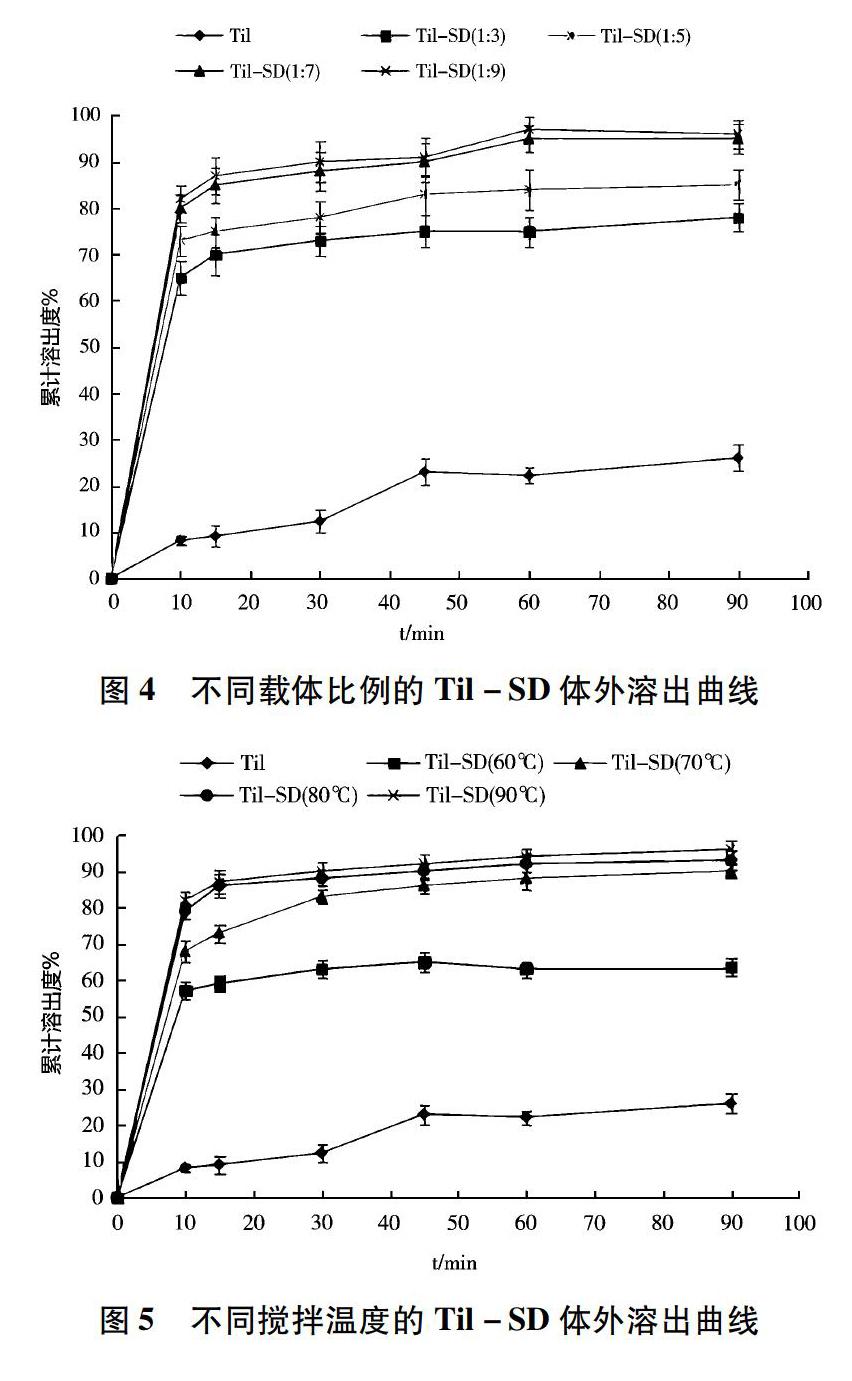
2.3.2 原料与载体材料比例的筛选 以Plasdone S-630为载体材料,Til原料用量为20 mg、分别选择原料与载体比例为1∶3、1∶5、1∶7、1∶9,照上述溶剂-熔融法制备固体分散体。测定并计算Til累积溶出度,结果如图4所示,表明,原料与载体比例为1∶7和1∶9时,Til的累积溶出度接近且均高于1∶3和1∶5,因此,选择原料与载体比例为1∶5、1∶7、1∶9进行正交试验。
2.3.3 制备温度的确定 以 Plasdone S-630为载体,称取原料用量20mg、原料与载体比例为1∶7、制备温度分别为 60、70、80、90℃,照上述溶剂-熔融法制备Til-SD,测定并计算其Til累积溶出度。结果如图5所示。可知,随着制备温度的增加,Til累积溶出度逐渐增加且均高于原料药,且制备温度分别为70、80、90℃时,Til累积溶出度明显高于60℃时制备的Til-SD,故选择制备温度为70、80、90℃进行正交试验。
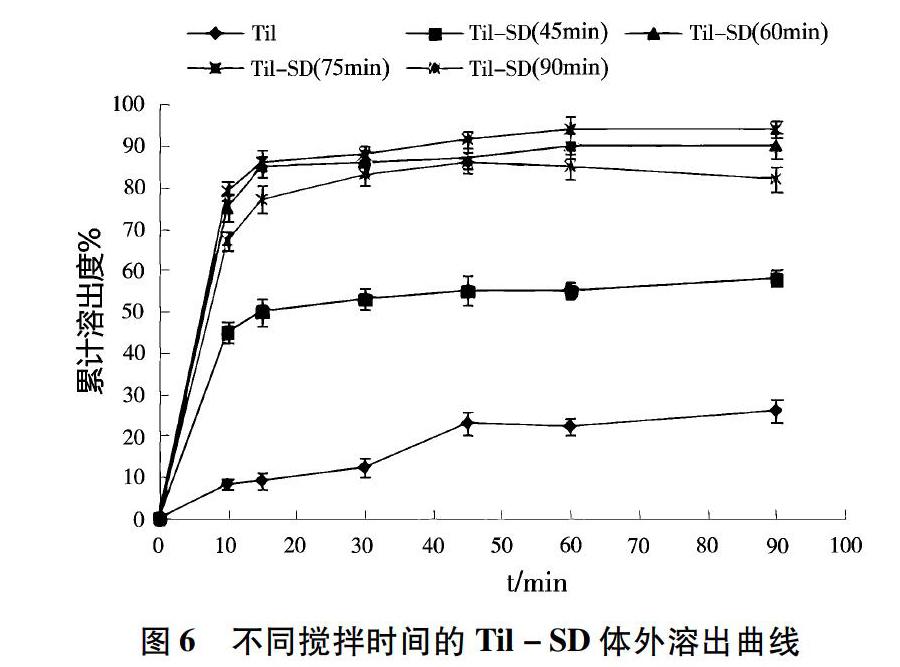
2.3.4 搅拌时间的筛选 以Plasdone S-630为载体材料,称取原料用量20mg,原料与载体比例为1∶7,搅拌时间分别45、60、75、90min,照上述溶剂-熔融法制备Til-SD。测定并计算累积溶出度,结果如图6所示。可知,搅拌时间为 60、75、90min时,Til累积溶出度明显高于45min,且均高于原料药,但搅拌时间为90min时,Til累积溶出度低于60、75min,故选择搅拌时间60、75、90min进行正交试验。
2.3.5 正交试验优化制备工艺 结合前期Til-SD单因素试验考察情况,采用L9(34)正交实验进一步优化Til-SD制备工艺。称取Til原料20mg,Plasdone S-630为载体材料适量,采用溶剂-熔融法,以Til累积溶出度为考察指标,选择原料与载体材料比例(A),制备温度(B) ,搅拌时间(C) 3个主要因素,每个因素设置3个考察水平,因素水平、试验设计与结果和方差分析分别见表1~3。
直观分析知,影响累积溶出效果的因素为:A(原料与载体材料比例)>B(制备温度)>C(搅拌时间)。经方差分析可知:原料与载体材料比例和制备温度对累积溶出度有显著影响,鉴于搅拌时间对累积溶出度无显著性影响。因此,为降低成本、节省工时,最终组合为A2B2C1即原料与载体材料比例为1∶7,制备温度为80℃,搅拌时间为60min。按照优化后的处方工艺制备3批Til-SD,结果显示,在溶出30min时,累积溶出度均达到90%。
2.4 体外溶出度测定 按“2.2”项下方法测定Til、Til-SD体外溶出度,结果如图7所示。由此可知,在溶出30min时,Til-SD累积溶出度为91.1%,而田蓟苷仅为 12.3%。
2.5 Til-SD的差示扫描量热法分析 取Til原料药、Plasdone S-630、物理混合物以及Til-SD进行DSC分析。精密称取约10mg待测样品置于DSC坩埚中,空白坩埚作对照,N2为保护气,升温范围为20~300℃,升温速率为10℃/min。结果如图8所示。载体Plasdone S-630有一处吸热峰,在69℃附近,为其熔点。原料药Til在250℃附近有一处吸热峰。物理混合物可看到田蓟苷和Plasdone S-630的吸热峰都存在。Til-SD中无Til的吸热峰,只剩下Plasdone S-630的吸热峰。说明此Til-SD中Til以非晶型均匀分散在载体Plasdone S-630中。
2.6 大鼠体内药动学研究
2.6.1 灌胃液配置 取Til原料药、Til-SD适量,置于含0.5%羧甲基纤维素钠的蒸馏水中,振摇使分散,配制成2mg/mL(以Til计)混悬液,即得。
2.6.2 给药方案与血样采集 取大鼠12只,随机分为2组,每组6只,实验前12h禁食不禁水,按50mg/kg剂量(以Til计)分别给予上述2种灌胃液,于0.083、0.167、0. 25、0.5、1、2、3、4、5、6、7、8、10、12h玻璃毛细管眼眶取血约0.3mL,置于含有10μL肝素钠的1.5mL的EP管中,混匀后迅速离心5min (4000r/min),转移上层血浆至另一空白离心管中,冷冻保存。
2.6.3 血浆样品处理方法 取血浆样品在室温下解冻,精密吸取100μL置1.5mL离心管中,加入乙腈100μL,涡旋混合5min,高速离心10min (10000r/min),取上清液置离心管中,氮气吹干,残渣加入100μL流动相复溶。
2.6.4 对照品溶液的配制 取“2.1.2”项下对照品储备液,进一步用乙腈稀释配制成540、252、180、64.8、36ng/mL的系列对照品溶液。
2.6.5 线性及专属性考察 精密量取100μL的Til质量浓度为540、252、180、64.8、36ng/mL的系列对照品溶液,氮气吹去有机溶剂,加入100μL大鼠空白血浆,按照“2.6.3”项下方法操作,记录HPLC色谱峰面积,以Til质量浓度为横坐标(X),Til峰面积为纵坐标(Y), 绘制标准曲线,回归方程为Y=1.0243X+0.6763,r=0.9900,在36~540ng/mL呈现良好的线性关系。专属性试验结果如图9所示,表明该方法专属性较高,样品处理过程中未引入干扰性杂质,内源性物质不干扰Til的测定。
2.6.6 方法学考察 取低、中、高质量浓度(36、180、540ng/mL)的含药血浆,日内精密度结果表明,低、中、高质量浓度血浆样品的RSD分别为6.89%、6.78%和7.21% (n=3);日間精密度RSD分别为8.56%、9.21%和7.34% (n=3),表明该方法精密度良好。将测定质量浓度与实际配制质量浓度比较,计算回收率,在86.83%~94.01%之间。血浆样品保存于-20℃冰箱中,于 0、1、2、3、4、5d测定Til峰面积,得RSD为7.11%,表明样品在放置过程中稳定性良好。
2.6.7 数据处理 按“2.6.2”项下给药方法,按照“2.6.3”处理,“2.1.1”项色谱条件进行含量检测,通过3P97程序统计矩模型计算主要药动学参数,结果见表4,再绘制血药浓度-时间曲线,结果如图10所示。由此可知,Til-SD的Tmax显著缩短 (P<0.05) ,Cmax、AUC0-t、AUC0-∞显著升高 (P<0.05),相对生物利用度增加到218.5%。
3 讨论
固体分散体技术能改善难溶性药物水溶性、溶出度。Til难溶于水,生物利用度较低,而将其制备成固体分散体可在一定程度上改善这些问题。本实验首次将Til制备成Til-SD,以Til体外累积溶出度为考察指标,采用单因素试验对制备方法、载体的种类、载体与原料比例、制备温度、制备时间进行考察,在单因素试验基础上,采用正交试验设计优化制备工艺,研究结果表明,当采用溶剂-熔融法,载体为Plasdone S-630,田蓟苷与Plasdone S-630比例为1∶7,制备温度为80℃,搅拌时间为60min时,制备的Til-SD,在溶出30min时,Til累积溶出度可达到90%,约为原料药的7.4倍,解决了Til水溶性低的问题。在一定范围内,Til-SD累积溶出度随载体比例的增大而升高,可能是因为Til在载体Plasdone S-630中为非晶型分散状态,分散度得到提高,故在很大程度上提高了累积溶出度;随着制备温度的升高,Til-SD的累积溶出度随之增大,温度过低不利于Til-SD的制备;随着搅拌时间的延长,Til均匀分散在载体中累积溶出度增加,但是搅拌一定时间后趋于过饱和状态,Til累积释放百分率降低。
大鼠灌胃给药Til原料药及Til-SD,药动学结果表明,与原料药日服同剂量给药相比较,Til-SD的T max、C max、AUC 0-t均有一定的差异,T max减小,说明Til-SD加快Til的吸收。C max增加,与体外溶出行为相吻合,说明体内外相关性较好。Til-SD的AUC 0-t是原料Til的约2.185倍,说明Til研制成Til-SD后,相对生物利用度提高到218.5%,进而表明增加了Til的吸收。Til原料药与Til-SD体外溶出结果与体内药动学结果呈现了体内外一致性。
目前多数研究仍以单一方法为主,缺乏对不同制备工艺制备固体分散体的比较。本实验采用3种常用方法(溶剂法、溶剂-熔融法和熔融法)分别制备Til-SD,比较研究利用不同工艺制备Til-SD的累积溶出度差异。本实验成功制备了Til-SD,其工艺简单,材料安全,促进药物吸收结果明显,今后将对其药效学进行评价,以期为相关制剂研发提供更全面可靠的依据, 为天然产物Til的研究、开发及应用提供更多的参考。
参考文献
[1]田友清, 尚靖, 阿布卡德. 香青兰及其含药血清对H9c2心肌细胞三种缺氧/复氧损伤模型的影响[J]. 中国新药杂志, 2012, 21(15):1736-1748.
[2]郭新红, 曹文疆, 樊鑫梅, 等. 田蓟苷对大鼠心肌缺血再灌注损伤的保护作用[J]. 中国实验方剂学杂志, 2013, 19(5):168-172.
[3]ZENG C, JIANG W, ZHENG R F, et al. Cardioprotection of Tilianin ameliorates myocardial ischemia-reperfusion injury: Role of the apoptotic signaling pathway[J]. Plos One, 2017, 12(4):3253-3265.
[4]馬丽月, 曾诚, 郑瑞芳, 等. 田蓟苷对脑缺血再灌注损伤模型大鼠脑组织的保护作用研[J]. 中国药房, 2018, 29(20):2805-2810.
[5]曹文疆, 彭克军, 袁勇, 等. 田蓟苷对大鼠血脂水平和炎症因子的影响[J]. 中国实验方剂学杂志, 2013, 19(11):164-167.
[6]曾诚, 马丽月, 于宁, 等. 香青兰提取物基本理化性质研究[J]. 中草药, 2016, 47(21): 3817-3823.
[7]曾诚, 杨晓艺, 帕伊曼·亥米提, 等. 田蓟苷在不同介质中的平衡溶解度及油水分配系数 [J]. 中国医院药学杂志, 2017, 37(1): 84-87.
[8]黄志巧, 邢建国, 王新春, 等. 田蓟苷在Caco-2细胞模型中的吸收特性研究[J]. 中国中药杂志, 2012, 37(9): 1315-1318.
[9]陈娇婷, 林乐迎, 黄浩, 等. 聚乙二醇1000维生素E琥珀酸酯在蛇床子素固体分散体制备中的应用[J]. 医药导报, 2016, 35(3):299-301.
[10]李韶静, 廖应芬, 杨慧慧, 等. 槲皮素固体分散体的制备及大鼠体内生物利用度研究[J]. 中草药, 2017, 48(20): 4229-4234.
[11]刘蒸生, 郝海军, 马进安, 等.高乌甲素磷脂复合物及其固体分散体在大鼠体内的药动学[J]. 医药导报, 2018, 37(4):449-452.
[12]俞迪佳,刘扬,朱缨,等. 蛇床子素固体分散体的制备与分析[J]. 中国民族民间医药, 2011,7 (14): 40-41.
[13]张铁山, 尚曙玉, 王聪颖, 等. 2种斯皮诺素固体分散体的制备及其体内药动学行为[J]. 中成药, 2019, 41(9): 2025-2029.
[14]时念秋, 张勇, 冯波, 等. 不同制备工艺制得姜黄素固体分散体的性质比较研究[J]. 中国药学杂志, 2016, 51(10): 821-826.
[15]陈晓丹. 川芎嗪自微乳化缓释固体分散体的研制[D]. 广州: 广州中医药大学, 2013.
[16]文君. 格列美脲固体分散体及其分散片的制备工艺研究[D]. 济南: 山东大学, 2013.
(收稿日期:2020-08-28 编辑:刘斌)

