基于UPLC-Q-TOF/MS的复方鱼腥草合剂大鼠血清药物化学研究
金汉台,刘建庭,王建方,张洪兵,刘芯亦,何厚洪,许 浚*,张铁军*
1.浙江康恩贝中药有限公司,浙江 丽水 323400
2.天津药物研究院 释药技术与药代动力学国家重点实验室,天津 300462
3.天津药物研究院 天津市中药质量标志物重点实验室,天津 300193
4.浙江康恩贝制药股份有限公司,浙江 杭州 310052
5.浙江省中药制药技术重点实验室,浙江 杭州 310052
6.天津中医药大学,天津 301617
复方鱼腥草合剂由鱼腥草、黄芩、板蓝根、连翘和金银花5味中药组成,具有清热解毒之功效,临床上常用于外感风热引起的咽喉肿痛、急性咽炎、扁桃腺炎有风热证候者[1]。由于复方鱼腥草合剂为临床疗效确切的中药复方制剂,其化学成分组成复杂,药效物质基础尚不清楚,严重制约了其临床推广应用。
中药血清药物化学依据中药经口给药的特点,通过分析口服给药后能进入血液的化学成分及其代谢产物,从入血成分的角度,研究中药的药效物质基础[2-3]。同时,超高效液相色谱-质谱联用技术(UPLC-Q-TOF/MS)具有快速、灵敏、高效的特点,也为中药吸收入血成分的快速发现和辨识提供了技术方法。近年来,质量标志物(quality marker,Q-Marker)作为中药质量的核心,是与药效密切相关的标志性活性化学成分,更重要的是,Q-Marker贯穿质量传递体系,是质量过程控制的基础[4-5]。因此,对于Q-Marker的发现,研究从药材到复方制剂再到血液的化学转移过程非常重要。
本研究采用UPLC-Q-TOF/MS技术,在口服给予复方鱼腥草合剂的大鼠血浆中共鉴定出24个化学成分,其中包括15个原型成分和9个代谢产物,为其药效物质基础和Q-Marker的确定奠定了基础。
1 仪器与材料
1.1 仪器
Acquity UPLC超高效液相色谱仪(美国Waters公司);Xevo G2 Q-TOF高分辨质谱(美国Waters公司);AB204-N电子天平(德国Meteler公司);BT25S电子天平(德国 Sartorius 公司);超声波清洗仪(宁波新芝生物科技公司);VORTEX-5旋涡混合器(海门市其林贝尔仪器制造公司);TG20-WS台式高速离心机(长沙维尔康湘鹰离心机有限公司)。
1.2 材料
咖啡酸(批号110885-200102)、黄芩苷(批号110715-201821)、汉黄芩苷(批号112002-201702)、黄芩素(批号111595-201808)、汉黄芩素(批号111514-201605)购自中国食品药品检定研究院,连翘苷(批号PS006-0025MG)购自成都普思生物科技股份有限公司,对照品质量分数均大于95%;甲醇(色谱纯)、乙腈(色谱纯)、甲酸(色谱纯),购自天津康科德科技有限公司;纯净水购自杭州娃哈哈饮用水有限公司;复方鱼腥草合剂来自浙江康恩贝中药有限公司。
雄性SD大鼠,SPF级,体质量170~190 g,购自斯贝福(北京)生物技术有限公司,动物许可证号SCXK(京)2019-0010。置于室温25 ℃、湿度50%,12 h昼夜交替,自由采食、饮水饲养适应1周。实验前禁食(不禁水)12 h。动物实验经天津天诚新药评价有限公司批准,伦理批准号2019110103。
2 方法
2.1 动物实验
取10支(10 mL/支)复方鱼腥草合剂,采用旋转蒸发仪减压浓缩至20 mL,作为复方鱼腥草合剂大鼠ig溶液。
雄性SD大鼠,随机分为2组并称定体质量,对照组按10 mL/kg ig给予纯净水,鱼腥草合剂给药组按10 mL/kg的剂量ig给予复方鱼腥草合剂大鼠ig溶液。给药1 h后以1%戊巴比妥钠麻醉,腹主动脉取血置肝素化试管中,于4 ℃条件下3500 r/min离心10 min分离血浆,置−20 ℃冰箱中保存备用。
2.2 溶液及血浆样品的制备
2.2.1 对照品溶液的制备 取黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、咖啡酸、连翘苷对照品适量,加甲醇配制成质量浓度为1 mg/mL的混合对照品溶液,经0.22 μm微孔滤膜滤过,供UPLC-Q-TOF/MS检测分析。
2.2.2 供试品溶液的制备 取复方鱼腥草合剂适量,经0.22 μm微孔滤膜滤过至进样小瓶中,作为复方鱼腥草合剂体外供试品溶液,供UPLC-QTOF/MS检测分析。
2.2.3 血浆样品的制备 取大鼠给药血浆样品500µL置于EP管中,加入2 mL甲醇,涡旋1 min混匀,于4 ℃条件下9000×g离心10 min沉淀蛋白,上清液4 ℃下N2吹干,残渣以200 µL甲醇涡旋1 min复溶,经0.22 μm微孔滤膜滤过,续滤液供UPLC-Q/TOF-MS检测分析。空白血浆进行同样操作。
2.3 UPLC-MS分析条件
2.3.1 色谱条件 Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm)色谱柱;流动相:0.1%甲酸水溶液(A)-乙腈(B),梯度洗脱:0~2 min,95% A;2~9 min,95%~80% A;9~20 min,80%~70% A;20~24 min,70%~62% A;24~27 min,62% A;27~30 min,62%~35% A;30~31 min,35%~5%A;31~33 min,5% A;柱温35 ℃;体积流量0.2 mL/min;进样量5 μL。
2.3.2 质谱条件 Xevo G2 Q-TOF高分辨质谱仪,配备电喷雾离子源(ESI),负离子模式下进行监测,负离子模式毛细管电压2 kV。离子源温度110 ℃,样品锥孔电压30 V,锥孔气体积流量50 L/h,氮气脱气温度350 ℃,脱气体积流量800 L/h,扫描范围m/z50~2000,内参校准液亮氨酸脑啡肽用于相对分子质量实时校正。
2.4 数据处理
使用MasslynxTM4.1软件进行数据处理,分析色谱图信息以及各色谱峰的质谱信息,对给药组和对照组大鼠血浆样品进行原型成分和代谢物的检测和分析。
3 结果
采用“2.3”项下所述优化的UPLC-Q-TOF/MS条件,对复方鱼腥草合剂、大鼠空白血浆及给药血浆样品进行检测分析,在负离子模式下,复方鱼腥草合剂、大鼠空白血浆和给药血浆样品的色谱图如图1所示。
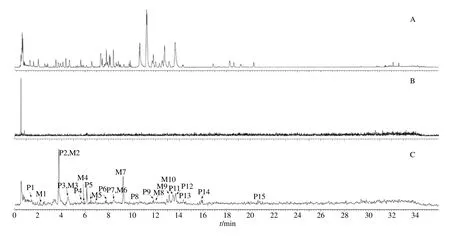
图1 负离子模式色谱图Fig.1 Negative ion mode chromatogram
通过比对分析复方鱼腥草合剂制剂和给药血浆样品的色谱图,同时存在于复方鱼腥草合剂与给药血浆样品中的离子被认为是潜在的以原型形式吸收的药物成分。通过查阅Massbank、Chemspider等公共数据库,并结合复方鱼腥草合剂所含化学成分的相关文献报道[6],分析质谱裂解规律,在给予复方鱼腥草合剂的大鼠血浆中共鉴定得到24个移行成分,包括15个吸收原型成分和9个代谢产物,其UPLC-Q-TOF/MS数据见表1、2。TOF/MS的实测值与理论值比较,精确质量数的误差均小于1×10−5。代谢产物的主要代谢途径见图2、3。
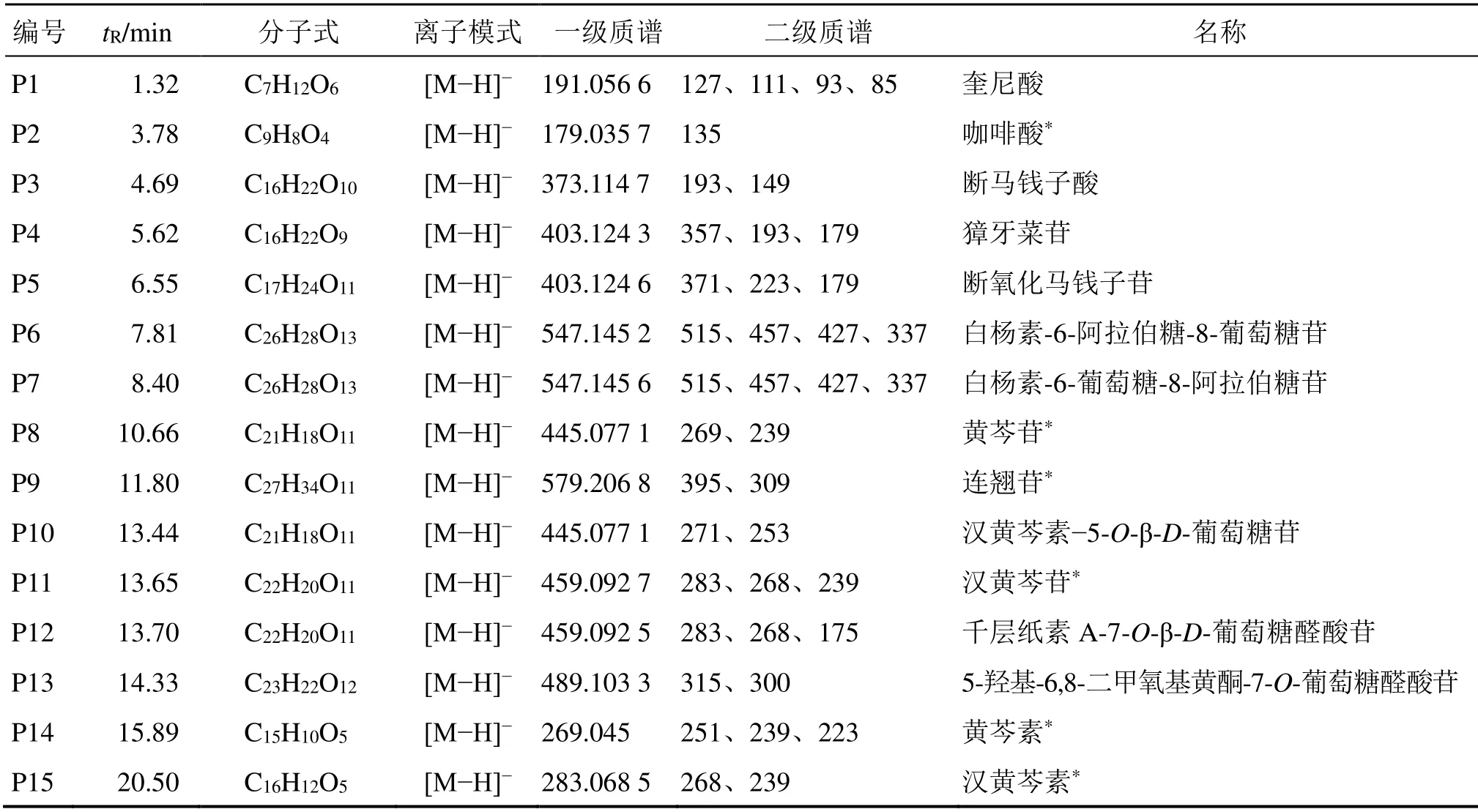
表1 鱼腥草合剂吸收入血原型成分LC-MS数据Table 1 LC-MS data of plasma prototype components of Yuxingcao Mixture
3.1 原型成分的鉴定
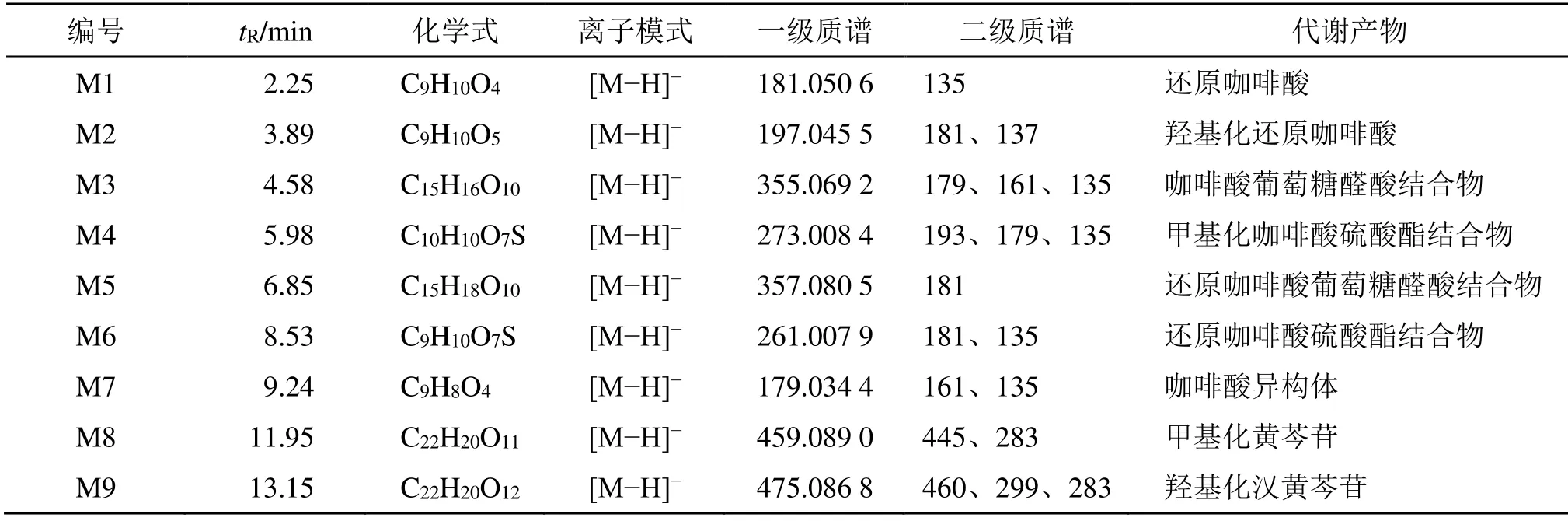
表2 复方鱼腥草合剂血浆代谢成分LC-MS数据Table 2 LC-MS data of plasma metabolic components of Yuxingcao Mixture
在给予复方鱼腥草合剂的大鼠血浆中鉴定出15个原型成分,包括9个黄酮醇及黄酮苷类成分,3个环烯醚萜类、2个有机酸类和1个木脂素类成分。
P2的准分子离子为 [M-H]−m/z179.035 7,确定分子式为C9H8O4,发生中性丢失形成碎片离子[M-CO2-H]−m/z135,通过与对照品比对,鉴定P2为咖啡酸。
P4的准分子离子为 [M+HCOOH-H]−m/z403.124 3,确定分子式为C16H22O9,碎片离子m/z357 为 [M-H]−,m/z195为 [M-C6H10O5-H]−,结构中可能存在1分子六碳糖,通过查阅Massbank等数据库,推测P4为獐牙菜苷。
P5的准分子离子为 [M-H]−m/z403.124 6,确定分子式为C17H24O11,碎片离子m/z371为 [MCH3OH-H]−,m/z223为 [M-C6H10O5-H2OH]−,通过查阅Massbank等数据库,推测P5为断氧化马钱子苷。
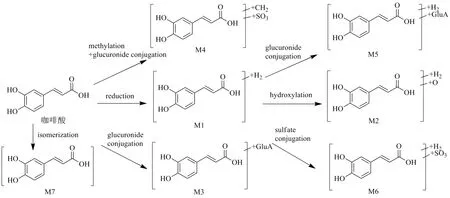
图2 咖啡酸可能的代谢途径Fig.2 Metabolic pathways of caffic acid
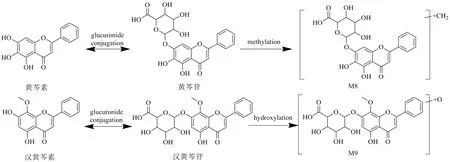
图3 汉黄芩苷和黄芩苷可能的代谢途径Fig.3 Metabolic pathways of wogonin and baicalin
P11的准分子离子为 [M-H]−m/z459.092 7,确定分子式为C22H20O11,脱去葡萄糖醛酸形成碎片离子[M-GluA-H]−m/z283.06,再脱去CH2形成[M-GluA-CH3-H]−m/z268.03,再脱去CO和CO2分别形成碎片离子m/z239和m/z224,通过与对照品比对并结合文献报道[7-9],P11被鉴定为汉黄芩苷。通过相似的分析手段,与对照品比对,P8、P9、P14和P15被鉴定为黄芩苷、连翘苷、汉黄芩苷和汉黄芩素。
3.2 代谢产物的鉴定
在给予复方鱼腥草合剂的大鼠血浆中初步鉴定出9个代谢产物,代谢途径包括甲基化、葡萄糖醛酸结合和硫酸酯结合等,如图2、3所示。
M1的准分子离子为 [M-H]−m/z181.050 6,确定分子式为C9H10O4,m/z181比咖啡酸的准分子离子(m/z179)多2(H2),并且表现出相同的碎片离子m/z135 [M-CH2O2-H]−,推测M1为咖啡酸的还原产物。
M3的准分子离子为 [M-H]−m/z355.069 2,其碎片离子m/z179为m/z355脱去葡萄糖醛酸(176)形成,与咖啡酸准分子离子相同,此外,m/z179再脱去CO2(44)形成碎片离子m/z135,这与咖啡酸裂解方式一致,推测M3为咖啡酸的葡萄糖醛酸结合物。
M4的准分子离子为 [M-H]−m/z273.006 0,确定分子式为C10H10O7S,脱去1分子硫酸酯基(80)形成 [M-SO3-H]−m/z193的碎片离子,提示经过硫酸酯结合代谢途径,又脱去CH2形成与咖啡酸的准分子离子相同的碎片离子,提示可能是经过甲基化代谢途径,推测M4为甲基化咖啡酸的硫酸酯结合物。以相似的方式,通过与原型成分的裂解规律进行对比,推测出M1~M7为咖啡酸代谢产物,代谢途径包括了还原、甲基化、葡萄糖醛酸结合和硫酸酯结合等。
M8的准分子离子为[M-H]−m/z459.089 0,确定分子式为C22H20O11,与汉黄芩苷的分子式相同,比黄芩苷的准分子离子多14(CH2),脱去CH2形成[M-CH2-H]−m/z445的碎片离子,或脱去葡萄糖醛酸,形成 [M-C6H8O6-H]−m/z283的碎片离子,推测M8为黄芩苷的甲基化代谢产物。
M9的准分子离子为 [M-H]−m/z475.086 8,确定分子式为C22H20O10,碎片离子m/z460为母离子丢失CH3(15)而形成,说明结构里含有甲基,碎片离子m/z299为m/z475脱去葡萄糖醛酸(176)形成,m/z283为m/z299脱去O(16)形成,且与汉黄芩素准分子离子相同,提示可能是经过羟基化代谢途径,推测M9为汉黄芩苷的羟基化代谢产物。
4 讨论
本实验在正、负离子模式下对样品均进行了检测分析,体外样品在正、负离子模式下均显示出峰,但负离子响应更高,血浆样品在负离子模式下的基质响应更低,而峰数量未有明显变化,故选用负离子模式。考察了大鼠取血时间,分别在0.5、1、2 h进行了血浆采集,发现在1 h的血浆样品中获得的原型成分和代谢物较多,因此选用1 h的血浆样品进行分析。在血浆样品处理过程中考察了甲醇沉淀蛋白法和乙腈沉淀蛋白法,使用甲醇沉淀蛋白可降低基质的干扰,提高仪器灵敏度,故使用甲醇沉淀蛋白法。对流动相的选择,比较了甲醇-水、乙腈-水、乙腈-0.1%甲酸水,使用乙腈可以缩短保留时间,提高分离度,优化峰形,使用0.1%甲酸水可使黄酮类成分响应变高,更易被检测出,故选用乙腈-0.1%甲酸水作为流动相。
以咖啡酸和绿原酸为代表的有机酸类成分是复方鱼腥草合剂中的重要成分,绿原酸可以在肠道菌群的作用下被水解为咖啡酸[10-11],咖啡酸具有广泛药理活性,研究表明咖啡酸及其衍生物具有抗氧化、抗炎、镇痛、免疫调节、抗菌和抗病毒等多种重要的药理作用[12-13],这可能是复方鱼腥草发挥清热解毒功效的原因之一,并且咖啡酸入血迅速,并在体内发生广泛的代谢[14-15],产生多种类型的代谢产物,如甲基化、硫酸结合和葡萄糖醛酸结合等,本实验中检测到了7个咖啡酸相关代谢物,代谢途径与文献报道基本一致,其中M7可能是其它原型成分经过相关代谢而形成,但由于仅靠质谱数据无法确定其结构,而M7的分子式与咖啡酸相同,碎片也大致相似,因此M7被推测成咖啡酸的异构化产物。复方鱼腥草合剂中含量最多的成分是以黄芩素和黄芩苷为代表的黄酮醇和黄酮苷类成分[16-17],雷奇林等[18]用网络药理学的方法探究黄芩抗炎的作用机制,结果表明黄芩苷、黄芩素、汉黄芩苷、汉黄芩素等黄酮类成分通过MAPK14、EGFR、TNFRSF1A、SELE等靶点抑制炎症因子的产生、抑制炎症因子与相应受体结合、阻断炎症反应的启动等,最终发挥抗炎效应。这可能是复方鱼腥草合计发挥抗炎作用的原因之一。此外,黄芩苷等黄酮类成分的代谢被广泛报道[19-22],黄芩苷和黄芩素等成分经结肠吸收入血[23],在肠道菌群作用下可以发生多种代谢途径,黄芩苷和汉黄芩苷均可以发生脱糖化,形成相应苷元被吸收入血,而在血中黄芩素可以发生葡萄糖醛酸化、双葡萄糖醛酸化和甲基化,汉黄芩素可以发生去甲基化和葡萄糖醛酸化。本实验中,黄芩苷和汉黄芩苷的相关代谢物被少量检测出,这可能是由于复方鱼腥草合剂作为1个复方制剂,药味多,所含化学成分复杂,各个成分在吸收入血过程中可能形成竞争或协调作用,黄芩苷等成分在在肠道和血浆代谢的过程中受到其他成分影响,而未表现出与单味药或单个成分相的多种代谢途径。
在口服给予复方鱼腥草合剂后的大鼠血浆中初步鉴定出24个化学成分,包括15个原型吸收成分和9个代谢产物,来自于鱼腥草、黄芩和金银花等药材,主要为黄酮类和有机酸类成分,代谢途径主要为Ⅱ相代谢,包括甲基化、葡萄糖醛酸结合和硫酸酯结合等。这些原型成分和代谢产物,可能是复方鱼腥草合剂潜在的活性成分,为其Q-Marker的确定奠定了基础。
利益冲突所有作者均声明不存在利益冲突

