芩连润肺汤的HPLC指纹图谱建立、含量测定及多元统计分析
闫凯莉 尹程程 刘梦瑶 崔长升 汪莹 孙晓舟 孙丽平 齐滨 刘莉


中圖分类号 R284.1 文献标志码 A 文章编号 1001-0408(2021)16-1956-08
DOI 10.6039/j.issn.1001-0408.2021.16.07
摘 要 目的:建立芩连润肺汤的指纹图谱,测定其中11种成分的含量,并进行聚类分析、正交偏最小二乘判别法(OPLS -DA)分析。方法:采用高效液相色谱法(HPLC)。色谱柱为ZORBAX Eclipse Plus C18,流动相为乙腈-0.05%磷酸溶液(梯度洗脱),检测波长为260 nm,柱温为30 ℃,流速为1.0 mL/min,进样量为10 μL。以汉黄芩苷为参照,采用《中药色谱指纹图谱相似度评价系统(2012版)》绘制10批芩连润肺汤的HPLC指纹图谱并进行相似度评价,确定共有峰;同法测定芩连润肺汤中11种成分的含量;采用SPSS 21.0软件进行聚类分析,采用SIMCA 14.0软件进行有监督模式的OPLS-DA分析,并筛选影响其质量的标志物。结果:10批芩连润肺汤共有21个共有峰,与对照指纹图谱的相似度均大于0.98;共指认了11个共有峰,分别为芦丁、连翘酯苷A、连翘酯苷B、鸢尾苷、野鸢尾苷、黄芩苷、连翘苷、汉黄芩苷、黄芩素、次野鸢尾黄素、汉黄芩素。上述11种成分检测进样量的线性范围分别为9.960 0~49.800 0、1.974 0~9.870 0、0.672 0~3.360 0、0.960 0~4.800 0、0.549 0~2.745 0、5.040 0~25.200 0、1.374 0~6.870 0、0.615 0~3.075 0、0.759 9~3.795 0、0.162 0~0.810 0、0.042 0~0.210 0 μg(r均大于0.999);精密度、稳定性(48 h)、重复性试验的RSD均小于2%;平均加样回收率为95.81%~100.29%(RSD为0.43%~1.73%,n=6);含量分别为8.924 4~12.820 8、0.352 2~0.868 7、0.435 6~0.711 2、0.389 8~1.309 0、0.335 8~0.530 1、1.680 5~4.542 3、0.701 8~1.584 2、2.240 2~5.442 5、2.351 0~5.558 9、0.106 0~0.182 2、0.076 8~0.128 9 mg/g。聚类分析结果显示,当类间距为10时,10批样品可聚为两类,S1~S3聚为一类、S4~S10聚为一类;当类间距为5时,第2类又可聚为两类,S6、S7、S9聚为一类,S4、S5、S8、S10聚为一类。OPLS-DA分析结果显示,S6、S7、S9位于得分图的上方,S4、S5、S8、S10位于得分图的左下侧,S1~S3位于得分图的右下侧,与聚类分析结果一致;黄芩苷、鸢尾苷、连翘酯苷A、黄芩素、汉黄芩苷的变量重要性投影值均大于1。结论:所建指纹图谱、含量测定方法的精密度较高、稳定性较好,结合多元统计分析 可用于芩连润肺汤的质量控制。黄芩苷等5种成分为影响芩连润肺汤的质量标志物。
关键词 芩连润肺汤;高效液相色谱法;指纹图谱;含量测定;聚类分析;正交偏最小二乘判别法
HPLC Fingerprint Establishment, Content Determination and Multivariate Statistical Analysis of Qinlian Runfei Decoction
YAN Kaili1,YIN Chengcheng2,LIU Mengyao1,CUI Changsheng1,WANG Ying1,SUN Xiaozhou3,SUN Liping3, QI Bin1,LIU Li1(1. School of Pharmacy, Changchun University of TCM, Changchun 130117, China; 2. Jilin Ginseng Academy, Changchun University of TCM, Changchun 130117, China; 3. Childrens Diagnosis and Treatment Center, the Affiliated Hospital of Changchun University of TCM, Changchun 130117, China)
ABSTRACT OBJECTIVE: To establish the fingerprint of Qinlian runfei decoction, determine the contents of 11 components, and conduct cluster analysis and orthogonal partial least squares discriminant analysis (OPLS-DA). METHODS: HPLC method was used. The determination was performed on ZORBAX Eclipse Plus C18 column with mobile phase consisted of acetonitrile- 0.05% phosphoric acid solution (gradient elution) at the flow rate of 1.0 mL/min. The detection wavelength was set at 260 nm, and column temperature was 30 ℃. The sample size was 10 μL. Using wogonoside as reference, HPLC fingerprints of 10 batches of Qinlian runfei decoction were drawn and the similarity evaluation was conducted with Similarity Evaluation System of TCM Chromatographic Fingerprint (2012 edition), the common peaks were also confirmed; the contents of 11 components in Qinlian runfei decoction were determined by the same method. SPSS 21.0 software was used for cluster analysis, and SIMCA 14.0 software was used for OPLS-DA to screen marker components affecting quality. RESULTS: There were 21 common peaks in 10 batches of Qinlian runfei decoction, and the similarity with control fingerprint was greater than 0.98. A total of 11 common peaks were identified, which were rutin, forsythiaside A, forsythiaside B, iris, irigenin, baicalin, forsythiaside, wogonoside, baicalein, irisflorentin and wogonin. The linear ranges of 11 components were 9.960 0-49.800 0, 1.974 0-9.870 0, 0.672 0-3.360 0, 0.960 0-4.800 0, 0.549 0- 2.745 0, 5.040 0-25.200 0, 1.374 0-6.870 0, 0.615 0-3.075 0, 0.759 9-3.795 0, 0.162 0-0.810 0, 0.042 0-0.210 0 μg (all r>0.999); RSDs of precision, stability (48 h) and repeatability tests were less than 2%; the average recoveries were 95.81%-100.29% with RSDs of 0.43%-1.73% (n=6); the contents were 8.924 4-12.820 8, 0.352 2-0.868 7, 0.435 6-0.711 2, 0.389 8-1.309 0, 0.335 8-0.530 1, 1.680 5-4.542 3, 0.701 8-1.584 2, 2.240 2-5.442 5, 2.351 0-5.558 9, 0.106 0-0.182 2, 0.076 8- 0.128 9 mg/g, respectively. The results of cluster analysis showed that when class spacing was 10, it could be divided into two groups, S1-S3 and S4-S10; when the class spacing was 5, the second class could be divided into two categories, S6, S7, S9 were clustered into one category, and S4, S5, S8, S10 were clustered into one category. The results of OPLS-DA analysis showed that S6, S7 and S9 were at the top of the figure, S4, S5, S8 and S10 were at the lower left side of the figure, and S1-S3 were at the lower right side of the figure, which was consistent with the cluster analysis results; VIP values of baicalin, iris, forsythiaside A, baicalein and wogonoside were all greater than 1. CONCLUSIONS: Established fingerprint and content determination methods have high precision and good stability. Combined with multivariate statistical analysis, it can be used for the quality control of Qinlian runfei decoction. Five components as baicalin are the marker components affecting the quality of Qinlian runfei decoction.
KEYWORDS Qinlian runfei decoction; HPLC; Fingerprint; Content determination; Cluster analysis; Orthogonal partial least square discriminat analysis
芩连润肺汤是国医大师王烈教授基于“热毒理论”提出的临床验方[1]。该方由黄芩、连翘、射干、石膏组成,其中黄芩为君药,擅清肺热、泻肺火;连翘为臣药,可疏散风热、清热解毒;射干,石膏均为佐使药,射干清肺火、消痰利咽,石膏清热泻火;整方以清肺热、泻火毒为主,临床常用于治疗细菌、病毒等引起的小儿肺炎,且效果显著[2-6]。芩连润肺汤作为复方制剂,具有多成分、多靶点的作用优势,其中黄芩中含有黄芩苷、汉黄芩苷、黄芩素、汉黄芩素,具有抗炎、抗病毒、保护心血管、缓解肺损伤等药理作用[7-9];连翘中含有连翘苷、连翘酯苷A、连翘酯苷B、芦丁,具有解热抗炎、改善急性肺损伤、保护神经、抗感染等活性[10-11];射干中含有鸢尾苷、野鸢尾苷、次野鸢尾黄素,具有清热解毒、利咽消痰等作用[12]。目前,关于芩连润肺汤的研究较少,其质量控制也仅以方中单一药材所含成分的含量为指标[13]。由于该方所含成分较多,因此以单一药材所含成分为指标进行质量控制具有一定的局限性。
中药质量标志物是由刘昌孝院士根据中药生物属性、炮制过程及配伍理论等特点提出的新概念。中药复方化学成分复杂,单一指标不能全面衡量其质量,化学成分与药效作用密不可分,中药药效是多种成分综合贡献的结果,与中医整体观相吻合,质量标志物为中药复方质量控制研究提供新思路[14-15]。中药指纹图谱是一种综合、可量化的鉴定手段,操作简便、专属性好、分析速度快,已被广泛应用于中药复方的质量控制[16]。聚类分析、正交偏最小二乘判别法(OPLS-DA)可以有效评价不同产地药材之间化学成分的差异性,筛选共有的特征成分[16]。基于此,本研究建立了芩连润肺汤的高效液相色谱(HPLC)指纹图谱,并同法测定了其中芦丁、连翘酯苷A、连翘酯苷B、鸢尾苷、野鸢尾苷、黄芩苷、连翘苷、汉黄芩苷、黄芩素、次野鸢尾黄素、汉黄芩素等11种活性成分的含量,同时采用聚类分析、OPLS-DA法进行多元统计分析,以筛选影响芩连润肺汤的质量标志物,旨在为其质量控制提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器有LC-10AT VP型HPLC仪及配备的SPD-10AVP型紫外检测器(日本Shimadzu公司),KQ5200型台式超声波清洗器(昆山美美超声仪器有限公司),ST-40R型高速冷冻离心机[赛默飞世尔科技(中国)有限公司],DV215CD型十万分之一电子天平(美国OHAUS公司)等。
1.2 药品与试剂
汉黄芩素(批号DST190212-025,纯度≥98%)、汉黄芩苷(批号DST190709-026,纯度≥98%)、黄芩苷(批号DST190518-023,纯度≥98%)、黄芩素(批号DST191012- 024,纯度≥98%) 、连翘苷(批号DST190213-048,纯度≥99%)、连翘酯苷B(批号DST191020-050,纯度≥98%)、芦丁(批号DST181101-017,纯度≥98%)、 野鸢尾苷(批号DST191011-247,纯度≥98%)、次野鸢尾黄素(批号DST190619-055,纯度≥99%)、鸢尾苷(批号DST190801-073,纯度≥98%)对照品均购自成都德思特生物技术有限公司;连翘酯苷A对照品(批号Z10N9L71605,纯度≥98%)购自上海源叶生物科技有限公司;乙腈(美国Tedia公司)为色谱纯,磷酸(长沙市汇虹化玻仪器设备有限公司)为分析纯,水为纯净水。
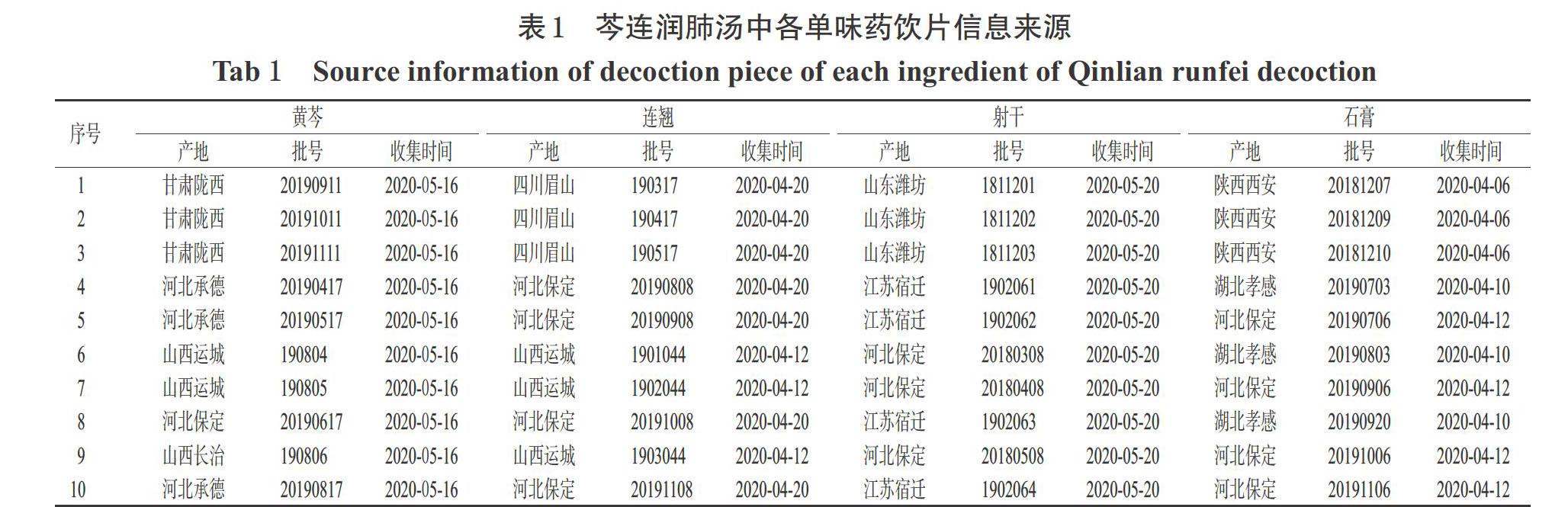
各单味药饮片均购自安徽援康中药饮片股份有限公司,由长春中医药大学药学院肖井雷副教授鉴定,分别为唇形科植物黄芩Scutellaria baicalensis Georgi的干燥根,木樨科植物连翘Forsythia suspensa(Thunb.)Vahl的干燥果实,鸢尾科植物射干Belamcanda chinensis(L.)DC.的干燥根茎以及硫酸盐类矿物硬石膏族石膏。芩连润肺汤中各单味药饮片来源信息见表1。
2 方法与结果
2.1 HPLC指纹图谱的建立
2.1.1 色谱条件 以ZORBAX Eclipse Plus C18(250 mm×4.6 mm,5 μm)为色谱柱,以乙腈(B)-0.05%磷酸溶液(A)为流动相进行梯度洗脱(0~13 min,1%B→5%B;13~22 min,5%B→10%B;22~30 min,10%B→18%B;30~45 min,18%B→20%B;45~55min,20%B→33%B;55~75 min,33%B→40%B;75~90 min,40%B→53%B;90~95 min,53%B);檢测波长为260 nm;柱温为30 ℃;流速为1.0 mL/min;进样量为10 μL。
2.1.2 混合对照品溶液的制备 精密称取芦丁、连翘酯苷A、连翘酯苷B、鸢尾苷、野鸢尾苷、黄芩苷、连翘苷、汉黄芩苷、黄芩素、次野鸢尾黄素、汉黄芩素对照品适量,加70%乙醇溶解并定容,混匀,制成上述成分质量浓度分别为3.320、0.658、0.224、0.320、0.183、1.680、0.458、0.205、0.253、0.054、0.014 mg/mL的混合对照品溶液。
2.1.3 供试品溶液的制备 精密称取各单味药饮片适量,粉碎(过二号筛),按芩连润肺汤处方比例(射干、连翘、黄芩、石膏质量比为3、3、2、1)精密称取各饮片粉末,加入8倍量水(mL/g),回流提取两次,每次3 h,合并滤液,减压浓缩干燥,即得芩连润肺汤提取物浸膏(以下简称“芩连润肺汤”),得率为21.4%(每克浸膏相当于饮片总量5 g),共制备10批(表1中各序号对应药材饮片所制为1批,依次编号S1~S10)。精密称取上述芩连润肺汤1.0 g,置于具塞锥形瓶中,精密加入70%乙醇10 mL,称定质量,超声(功率250 W,频率50 kHz)提取40 min,放冷至室温,再次称定质量,用70%乙醇补足减失的质量,摇匀,以4 000 r/min离心5 min,取上清液,经0.22 μm滤膜滤过,取续滤液,即得。
2.1.4 各单味药饮片溶液的制备 分别称取各单味药饮片(质量与“2.1.3”项下对应药材相同),按“2.1.3”项下方法制备各单味药提取物浸膏。取上述各提取物浸膏约0.5 g,再按“2.1.3”项下方法制备各单味药饮片溶液。
2.1.5 精密度试验 取“2.1.3”项下供试品溶液(编号S1)适量,按“2.1.1”项下色谱条件进样测定6 次,以汉黄芩苷为参照(S),计算各共有峰的相对保留时间和相对峰面积。结果,21个共有峰相对保留时间的RSD为0.01%~0.21%(n=6),相对峰面积的RSD为0.15%~2.29%(n=6),表明方法精密度良好。
2.1.6 稳定性试验 取“2.1.3”项下供试品溶液(编号S1)适量,分别于室温下放置0、2、8、12、18、24 h时按“2.1.1”项下色谱条件进样测定,以汉黄芩苷为参照(S),计算各共有峰的相对保留时间和相对峰面积。结果,21个共有峰相对保留时间的RSD为0.37%~0.45%(n=6),相对峰面积的RSD为1.09%~2.58%(n=6),表明供试品溶液于室温下放置24 h内稳定性良好。
2.1.7 重复性试验 取同一批芩连润肺汤样品(编号S1),共6 份,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,以汉黄芩苷为参照(S),计算各共有峰的相对保留时间和相对峰面积。结果,21个共有峰相对保留时间的RSD为0.19%~0.28%(n=6),相对峰面积的RSD为1.03%~2.61%(n=6),表明方法重复性良好。
2.1.8 指纹图谱的建立 取10批芩连润肺汤样品,按“2.1.3”项下方法制备供试品溶液,采用《中药色谱指纹图谱相似度评价系统(2012版)》,以S1为对照(因S1批样品显示的色谱信息较多),时间窗设置0.1 min,以中位数法,经过多点校正后自动匹配生成HPLC叠加指纹图谱和对照指纹图谱,详见图1、图2。结果,10批芩连润肺汤样品共有21个共有峰。其中,与单味药饮片(取“2.1.4”项下各单味药饮片溶液同法进样所得色谱图,图略)比对,结果,峰13、16、17、19、21为黄芩专属峰;峰1、2、3、4、5、6、7、8、10、14、15为连翘专属峰;峰9、11、12、18、20为射干专属峰。
2.1.9 相似度评价 采用《中药色谱指纹图谱相似度评价系统(2012版)》对10批芩连润肺汤样品进行相似度评价。结果,10批样品图谱与对照指纹图谱的相似度为0.988~0.995,表明不同批次样品相似度较高,详见表2。
2.1.10 共有峰的指认 通过与混合对照品色谱图(图3A,测定方法见“2.2”项)比对,指认共有峰11个,分别为芦丁(峰5)、连翘酯苷A(峰6)、连翘酯苷B(峰8)、鸢尾苷(峰9)、野鸢尾苷(峰12)、黄芩苷(峰13)、连翘苷(峰15)、汉黄芩苷(峰17)、黄芩素(峰19)、次野鸢尾黄素(峰20)、汉黄芩素(21峰)。由于黄芩为方中君药,其所含成分汉黄芩苷(峰17)的分离度较好、出峰时间稳定,峰面积适中,对照品易得,故以汉黄芩苷为参照(S)计算各共有峰的相对保留时间和相对峰面积,结果见表3、表4。
2.2 芩连润肺汤中11种活性成分的含量测定
2.2.1 色谱条件 同“2.1.1”项。
2.2.2 混合对照品溶液的制备 同“2.1.2”项。
2.2.3 供试品溶液的制备 同“2.1.3”项。
2.2.4 阴性对照溶液的制备 按芩连润肺汤处方比例,分别制备缺黄芩、连翘、射干的阴性样品,再按“2.2.3”项下方法分别制备各阴性对照溶液。
2.2.5 系统适用性试验 取上述混合对照品溶液、供试品溶液、阴性对照溶液适量,按“2.2.1”项下色谱条件进样测定,记录色谱图。结果,各成分分离度均大于1.5,理论板数均不低于10 000,阴性对照溶液对各成分的测定均无干扰,详见图3。
2.2.6 线性关系考察 精密吸取“2.2.2”项下混合对照溶液3、5、7、10、12、15 μL,按“2.2.1”项下色谱条件进样测定,记录峰面积。以各待测成分的进样量(X,μg)为横坐标、峰面积(Y)为纵坐标进行线性回归,结果见表5。
2.2.7 精密度试验 取“2.2.2”项下混合对照品溶液,按“2.2.1”项下色谱条件连续进样测定6次,记录峰面積。结果,11种成分峰面积的RSD分别为1.07%、0.38%、0.27%、0.43%、1.55%、0.19%、0.33%、0.88%、0.39%、0.62%、0.52%(n=6),表明仪器精密度良好。
2.2.8 重复性试验 取同一批芩连润肺汤样品(编号S1)1 g,共6份,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并按标准曲线法计算含量。结果,11种成分含量的RSD分别为1.26%、1.08%、1.32%、1.51%、1.30%、1.24%、1.31%、1.42%、1.30%、1.33%、1.45%(n= 6),表明方法重复性良好。
2.2.9 稳定性试验 取“2.2.3”项下供试品溶液(编号S1),分别于室温下放置0、2、8、12、18、24、48 h时按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,11种成分峰面积的RSD分别为1.32%、1.25%、1.28%、1.47%、1.01%、1.22%、1.05%、1.29%、1.15%、1.24%、1.20%(n=7),表明供试品溶液在室温下放置48 h内稳定性良好。
2.2.10 加样回收率试验 取已知含量的芩连润肺汤样品(编号S1),每份约0.5 g,共6份,精密称定,分别加入适量的“2.2.2”项下混合对照品溶液,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表6。
2.2.11 样品含量测定 取10批芩连润肺汤样品,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定,记录峰面积并按标准曲线法计算样品中11种成分的含量。每样品平行测定3次,取平均值,结果见表7。
2.3 聚类分析
聚类分析是目前常用的数据挖掘分析方法之一[17]。以10批芩连润肺汤中11种成分的峰面积为变量,借助SPSS 21.0统计软件,采用离差平方和法以欧式距离为区间进行聚类分析,结果见图4。由图4可见,当类间距为10时,10批样品可聚为两类,S1~S3聚为一类、S4~S10聚为一类;当类间距为5时,第2类又可聚为两类,S6、S7、S9聚为一类,S4、S5、S8、S10聚为一类。这提示不同产地黄芩、连翘、射干药材质量存在差异。
2.4 OPLS-DA分析
采用SIMCA 14.0软件选择有监督模式的OPLS-DA分析10批芩连润肺汤样品中11个成分的峰面积差异,其OPLS-DA得分图见图5。由图5 可见,代表模型预测性的累积预测率(Q 2)=0.826>0.5,表明模型具有好的预测准确性;代表样本分离趋势的X轴方向模型的累积解释率(R 2)=0.967>0.5,表明模型稳定性及预测力较好(R 2、Q 2数值越接近1说明模型稳定性及预测力越好)[18-19]。10批样品中,S6、S7、S9在得分图的上方,S4、S5、S8、S10在得分图的左下侧,S1~S3在得分图的右下侧,与聚类分析结果一致。
变量重要性投影(VIP)值能准确反映引起差异的主要物质,且VIP>1可作为筛选具有显著贡献变量的标准[20]。本研究采用SIMCA 14.0软件进行OPLS-DA分析,并提取11个活性成分的VIP值,结果见图6。由图6可见,黄芩苷(峰13)、鸢尾苷(峰9)、连翘酯苷A(峰6)、黄芩素(峰19)、汉黄芩苷(峰17)的VIP值均大于1,表明这5个成分在整个模型中的贡献度高于平均水平,是影响芩连润肺汤质量的差异标志物。
3 讨论
本课题组前期采用紫外检测器在190~400 nm波长范围内对待测成分进行扫描。结果发现,在260 nm波长处所得色谱峰数量较多、峰形较好,故选择260 nm為检测波长。由于芩连润肺汤中化学成分复杂,采用等度洗脱难以实现分离,故采用梯度洗脱。同时,本课题组考察了甲醇-水、乙腈-水、乙腈-磷酸溶液等不同流动相系统的分离效果,结果发现,乙腈-磷酸溶液的分离效果相对较好;又对流动相中磷酸的浓度(0.05%、0.1%、0.2%)进行了考察,结果发现,磷酸浓度对分离效果影响不大,故选择乙腈-0.05%磷酸溶液为流动相。
本研究采用HPLC法建立了芩连润肺汤的指纹图谱,共确定了21个共有峰,指认出了其中的11个化学成分,分别为芦丁、连翘酯苷A、连翘酯苷B、鸢尾苷、野鸢尾苷、黄芩苷、连翘苷、汉黄芩苷、黄芩素、次野鸢尾黄素、汉黄芩素;10批样品共有峰的相对保留时间差异较小,而相对峰面积差异较大,提示各批样品成分相似但含量各异;各批样品图谱与对照指纹图谱的相似度结果均大于0.98,表明样品质量差异不大[21]。含量测定结果显示,10批样品中芦丁、黄芩素、汉黄芩苷、黄芩苷含量较高,其他成分含量相对较低;10批样品中各成分含量存在差异,这可能与单味药材饮片的产地、生长环境、生长年限和气候条件有关[22-23],但具体原因有待进一步研究。
聚类分析结果显示,当类间距为10时,可聚为两类,S1~S3聚为一类、S4~S10聚为一类;当类间距为5时,第2类又可聚为两类,S6、S7、S9聚为一类,S4、S5、S8、S10聚为一类,表明不同产地样品间质量存在差异。OPLS-DA分析结果显示,黄芩苷(峰13)、鸢尾苷(峰9)、连翘酯苷A(峰6)、黄芩素(峰19)、汉黄芩苷(峰17)可能是影响芩连润肺汤质量的差异标志物。
综上所述,所建指纹图谱、含量测定方法的精密度较高、稳定性较好,结合多元统计分析可用于芩连润肺汤的质量控制。黄芩苷等5种成分为影响芩连润肺汤质量的差异标志物。
参考文献
[ 1 ] 孔一卜,郭婷婷,郭磊,等.国医大师王烈热毒理论治疗小儿风热感冒经验[J].中华中医药杂志,2020,35(1):173-175.
[ 2 ] 万巧凤,顾立刚,殷胜骏,等.黄芩苷对FM1肺炎小鼠肺损伤的作用机制研究[J].中国药理学通报,2012,28(2):208-212.
[ 3 ] 游本铿.基于数据挖掘的《伤寒论》肺热证研究[D].北京:北京中医药大学,2015.
[ 4 ] 周婧媛.基于中医传承辅助平台系统研究中药治疗肺炎喘嗽的用药规律[D].南京:南京中医药大学,2019.
[ 5 ] 李冰,孙丽平,郭磊,等.清肺饮加减治疗风热郁肺型小儿肺炎喘嗽的效果[J].长春中医药大学学报,2020,36(2):286-288.
[ 6 ] 赵蓓,冯杨.清肺饮治疗小儿毛细支气管炎的临床分析[J].现代医院,2019,19(8):1222-1224.
[ 7 ] 张笛,罗雅菲,徐凌云.黄芩苷和黄芩素抗肿瘤作用研究新进展[J].中南药学,2020,18(4):613-620.
[ 8 ] 王家伟,易登良,王涛,等.黄芩素对大鼠心肌缺血-再灌注损伤的保护作用及对Janus激酶-信号转导与转录激活分子信号通路的影响[J].中国老年学杂志,2020,40(11):2410-2414.
[ 9 ] 刘嘉,严宝飞,曾明月,等.黄芩-金银花药对治疗新型冠状病毒肺炎潜在作用机制的网络药理学研究[J].世界中医药,2020,15(4):502-511.
[10] 曲欢欢.连翘化学成分和生物活性研究[D].西安:西北大学,2008.
[11] 韩彦琪,曹勇,董亚楠,等.基于神经网络分析的疏风解毒胶囊抗炎作用谱效关系研究[J].中草药,2019,50(15):3526-3533.
[12] 张琳,张妮.川射干的化学及药理研究进展[J].陕西中医学院学报,2014,37(5):91-93.
[13] 王晓月,邸子真,王光函,等.黄芩射干汤中黄酮类成分指纹图谱的相关性[J].沈阳药科大学学报,2017,34(6):473-476.
[14] 刘昌孝.发展中药质量标志物(Q-marker)理论方法和策略,研究提升中药科学技术水平[J].药学学报,2019,54(2):185-186.
[15] 刘昌孝.中药质量标志物(Q-marker):提高中药质量标准及质量控制理论和促进中药产业科学发展[J].中草药,2019,50(19):4517-4518.
[16] 周欣,张琳,毛婵,等.基于化学计量学方法结合正交偏最小二乘判别分析的陈皮饮片HPLC指纹图谱研究[J].中草药,2019,50(9):2194-2200.
[17] 刘杰,刘广学,尚明英,等.華细辛和北细辛HPLC特征图谱识别与抗炎靶点及抗炎成分分析[J].中国中药杂志,2020,45(6):1374-1383.
[18] LIANG J,WU W Y,SUN G X,et al. A dynamic multiple reaction monitoring method for the multiple components quantification of complex traditional Chinese medicine preparations:Niuhuang shangqing pill as an example[J]. J Chromatogr A,2013,1294:58-69.
[19] 陶晓赛,龚海燕,谢彩侠,等.基于UPLC指纹图谱结合化学计量学评价不同产地盾叶薯蓣药材质量[J].中草药,2021,52(1):227-233.
[20] 田双双,赵晓梅,刘珊珊,等.基于UPLC特征图谱及萜类成分含量测定的泽泻产地差异研究[J].中国中药杂志,2020,45(7):1545-1557.
[21] 李先端,顾雪竹,程立平,等.黄芩饮片规格分级市场情况调查及有关古今文献论述[J].中药材,2014,37(1):150-152.
[22] 杨洋,王志强,任丽丽,等.不同产地黄芩药材中主要药效成分含量变化规律研究[J].天津中医药大学学报,2020,39(3):324-329.
[23] 胡金婉,原江锋,王大红,等.不同产地连翘中主要活性成分含量的比较[J].河南科技大学学报(自然科学版),2021,42(1):81-86.
(收稿日期:2021-03-09 修回日期:2021-07-14)
(编辑:陈 宏)

