水化学性质对纳米银颗粒在含藻水环境中归趋的影响

摘要:水化学性质和微藻的存在都能显著影响金属纳米颗粒在水环境中的迁移和毒性。本研究以莱茵衣藻为模式生物,研究了pH,HPO42-,Ca2+和富里酸(SRFA)对含藻环境中纳米银颗粒(Ag-NPs)的归趋和毒性的影响。结果表明,高pH和HPO42-浓度会抑制Ag-NPs的溶解,减弱藻细胞对Ag的胞外吸附和胞内吸收,降低生物可利用Ag含量,从而降低Ag-NPs对微藻的毒性。增加Ca2+ 浓度可促进Ag-NPs的溶解,但会减少藻细对Ag的吸附和吸收,降低生物可利用Ag含量,同样会降低Ag-NPs对微藻的毒性。然而,较高的SRFA浓度会促进Ag-NPs的溶解,增强藻细胞对Ag的胞外吸附和胞内吸收,提高生物可利用Ag含量,从而增强Ag-NPs对微藻的毒性。
关键词:Ag-NPs;莱茵衣藻;水化学性质;归趋;毒性
随着社会对纳米产品的需求不断增长,纳米金属材料的生产和使用量与日俱增。然而,纳米金属材料在给人们带来便利的同时,也通过生产、使用、消耗和回收利用等过程进入水环境[1],对水环境造成污染。金属纳米颗粒化学性质活泼,进入水环境后易被氧化溶解,释放出相应的金属离子,溶解过程会受水环境理化性质(离子强度、pH等)及本身特性(粒径、形态、涂层等)的影响。
微藻是水生生态系统中最重要的初级生产者,在自然水生环境中普遍存在。微藻由于细胞结构简单、繁殖快、比表面积大以及对污染物高度敏感等特点,已成为研究污染物在水体中迁移转化规律及其水生态毒性评价的模式水生生物。目前相关研究主要集中在金属纳米颗粒对水生环境中各种藻类的毒性作用[2, 3],而对水环境中金属纳米颗粒与微藻的交互作用以及水化学性质对金属纳米颗粒在含藻水环境中归趋的影响研究不够深入。因此,本研究旨在探讨水化学性质(pH、HPO42-、Ca2+、SRFA)对含藻水环境中Ag-NPs归趋的影响,以及水化学性质对Ag-NPs胁迫下莱茵衣藻毒性的影响。
1实验方法
实验取用对数生长期(106 cells/L)的莱茵衣藻,向藻液中添加Ag-NPs储备液使其浓度为10 mg/L,設置水化学条件及浓度分别为:pH(5-9)、磷酸氢根离子(HPO42-,0-10 mM)、钙离子(Ca2+,0-5 mM)、富里酸(SRFA,0-50 mgC/L),每组实验设置3个平行样,于96 h测定莱茵衣藻的生物量及溶解态、胞外、胞内的Ag含量。
2结果与讨论
2.1水化学性质对Ag-NPs在含藻水环境中溶解特性的影响
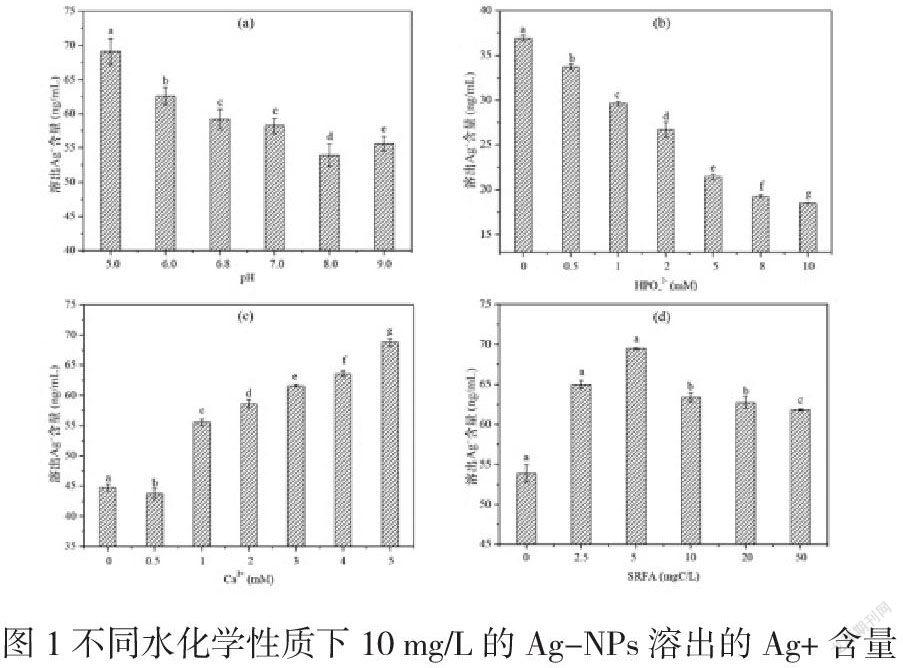
对于金属纳米颗粒来说,溶解性是评定其生态毒性必须考虑的因素。图1为Ag-NPs浓度为10 mg/L时,pH、HPO42-、Ca2+、SRFA对含藻水环境中Ag-NPs溶解特性的影响。当pH从5.0升高到8.0,溶出Ag+的含量逐渐下降,表明弱碱性条件下可抑制Ag-NPs的溶解(图1 a)。原因可能是pH增加导致水环境中的H+减少,溶解作用的必要条件无法被满足,Ag+ 溶出量减小;也可能是高pH时,Ag-NPs表面形成氢氧化层,导致碱性条件下金属纳米颗粒的溶解作用减弱[4]。
从图1(b)可以看出,随着HPO42-浓度从0 mM增加到10 mM时,溶出Ag+的含量下降了约50%,表明HPO42-可抑制Ag-NPs的溶解。分析原因可能是磷酸盐在颗粒表面的吸附抑制Ag-NPs的溶解[5];S2-、Cl-和PO43-等电解质则能够与Ag+结合形成相对稳定的物质,从而影响Ag+的溶出[6]。
由图1(c)所示,随着Ca2+浓度的增加,溶出Ag+的含量大幅上升,当Ca2+浓度为5 mM时,溶出Ag+的含量较对照组升高了35%。表明Ca2+能够促进Ag-NPs的溶解。
当SRFA浓度为2.5和5 mgC/L时,溶出Ag+的含量逐渐增加;然而,随着SRFA浓度进一步增加,溶出Ag+的含量逐渐降低,但仍高于对照组(图1 d),表明SRFA可促进Ag-NPs的溶解。由于SRFA能与Ag+络合,为了达到溶液中离子析出-络合的动态平衡,Ag-NPs则会析出更多的Ag+,所以SRFA可促进Ag-NPs的溶解。
2.2水化学性质对莱茵衣藻吸附/吸收Ag的影响
如图2所示,pH从5.0增加到9.0,胞内吸收的Ag含量逐渐下降(图2 a)。结果表明,较高的pH会抑制藻细胞对Ag的吸附和吸收,可能是由于pH的增加促进Ag+ 转化为Ag-NPs[7]。
由图2(b)可知, HPO42-浓度从2 mM增加至10mM时,胞外吸附Ag含量显著降低(P < 0.05),较对照组下降了51%。另一方面,随着HPO42-浓度增加,胞内吸收Ag含量逐渐降低。结果表明,HPO42-的增加可有效降低含藻水环境中Ag-NPs的生物利用度。
从图2(c)可以看出,Ca2+浓度从0 mM增加至1 mM,胞外吸附Ag含量显著降低(P < 0.05),较对照组下降了60.75%。对于胞内吸收Ag含量而言,随着Ca2+浓度增加,胞内吸收Ag含量逐渐下降,最终降至对照组的61.76%。虽然添加Ca2+能够促进Ag-NPs的溶解,但根据BLM的假设,水中的阳离子可以与有毒的金属离子竞争在生物体上结合位点,从而导致胞内吸收Ag和胞外吸附Ag含量下降。
随着SRFA浓度升高,胞外吸附Ag含量和胞内吸收Ag含量显著升高(P < 0.05),当SRFA浓度为50 mgC/L时,胞外吸附Ag含量和胞内吸收Ag含量分别较对照组升高了89.72%和126%(图2 d)。
2.3水化学性质对Ag-NPs胁迫下莱茵衣藻毒性的影响
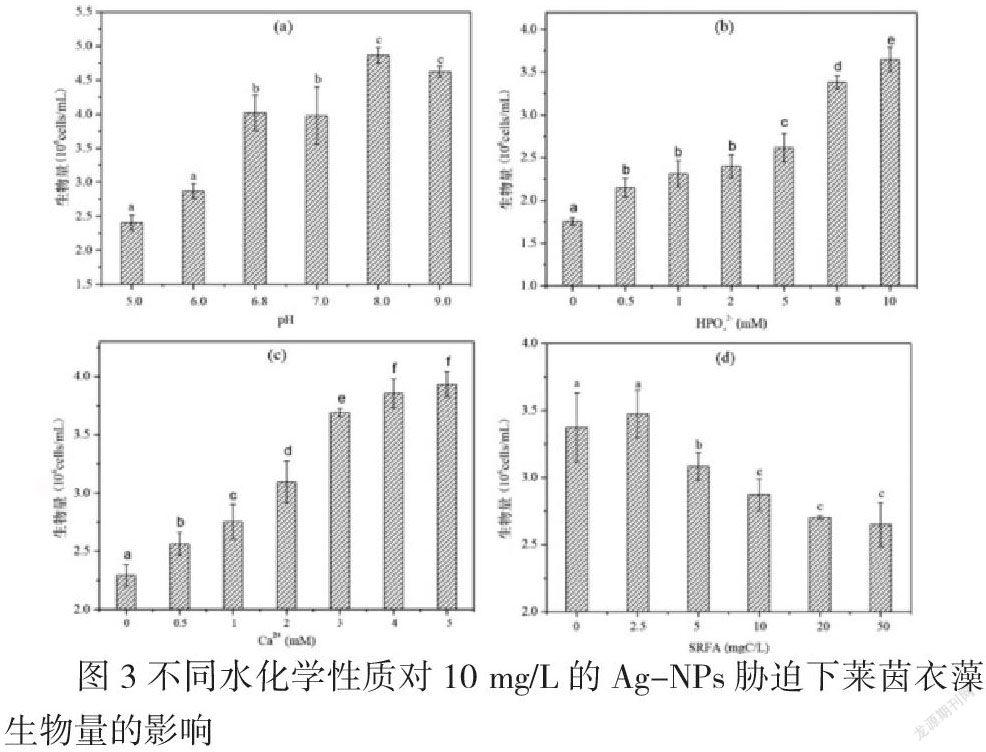
如图3所示,投加10 mg/L Ag-NPs后的藻液pH为6.8;pH减小至5.0时,莱茵衣藻生物量下降40.14%;pH增加到8.0时,生物量升高了21.08%,pH增加到9.0生物量有所下降,但仍较pH为6.8时的生物量升高了15.03%(图3 a)。结果表明,Ag-NPs对莱茵衣藻的生长受pH的影响较为显著,当受到Ag-NPs胁迫时,弱碱性条件更利于莱茵衣藻的生长。
从图3(b)可以看出,随着HPO42-浓度逐渐增加,莱茵衣藻生物量逐渐升高,当HPO42-浓度为10 mM时,生物量与对照组相比升高51.88%。由图3(c)所示,随着Ca2+浓度逐渐增加,莱茵衣藻生物量逐渐升高。水中的阳离子能够与金属离子竞争结合位点,从而降低Ag的生物利用量,减弱Ag-NPs毒害作用,有利于莱茵衣藻生长。
当SRFA浓度为2.5 mgC/L时,莱茵衣藻生物量较对照组稍有上升,随着SRFA浓度继续增加,生物量逐渐下降。不同的金属纳米颗粒与不同的溶解性有机物相互作用时,产生的影响不同,高浓度SRFA会增加金属离子在莱茵衣藻细胞壁和细胞内的积累,增强细胞毒性,从而抑制莱茵衣藻生长。
3结论
水化学性质对Ag-NPs的Ag+释放行为有显著影响。较高的pH和HPO42-浓度会显著抑制Ag+的释放,而Ca2+和SRFA的存在则会促进Ag+的释放。藻类细胞对Ag的胞外吸附和胞内吸收也受到水化学性质的影响。较高的pH,HPO42-浓度和Ca2+浓度会显著减少藻细胞对Ag的吸附/吸收,而SRFA会增强藻细胞对Ag的吸附/吸收。此外,水化学性质能够影响Ag-NPs对莱茵衣藻的毒性效应。较高的pH,HPO42-浓度和Ca2+浓度会减弱Ag-NPs对莱茵衣藻的生长抑制作用,而当SRFA浓度超过2.5 mgC/L时,会增强Ag-NPs对莱茵衣藻的毒性。
4参考文献:
[1] Gottschalk F and Nowack B. The release of engineered nanomaterials to the environment[J]. Journal of Environmental Monitoring, 2011, 13(5): 1145-1155.
[2] Sendra M, Yeste M P, Gatica J M, et al. Direct and indirect effects of silver nanoparticles on freshwater and marine microalgae (Chlamydomonas reinhardtii and Phaeodactylum tricornutum). Chemosphere, 2017, 179: 279-289.
[3] Suman T Y, Radhika Rajasree S R, Kirubagaran R. Evaluation of zinc oxide nanoparticles toxicity on marine algae chlorella vulgaris through flow cytometric, cytotoxicity and oxidative stress analysis. Ecotoxicology and Environmental Safety, 2015, 113: 23-30.
[4] Li M, Lin D, Zhu L. Effects of water chemistry on the dissolution of ZnO nanoparticles and their toxicity to Escherichia coli[J]. Environmental Pollution, 2013, 173: 97-102.
[5] Li M, Zhu L, Lin D. Toxicity of ZnO nanoparticles to Escherichia coli: mechanism and the influence of medium components[J]. Environmental Science & Technology, 2011, 45(5): 1977-1983.
[6] Li M, Pokhrel S, Jin X, et al. Stability, bioavailability, and bacterial toxicity of ZnO and iron-doped ZnO nanoparticles in aquatic media[J]. Environmental Science & Technology, 2011, 45(2): 755-761.
[7] Adegboyega N F, Sharma V K, Siskova K M, et al. Enhanced formation of silver nanoparticles in Ag+-NOM-iron (II, III) systems and antibacterial activity studies[J]. Environmental Science & Technology, 2014, 48(6).
作者簡介:江丹丹1988年5月 中级工程师 硕士研究生 研究方向:水环境污染及修复
水发规划设计有限公司 山东 济南 250000

