磁共振弥散加权成像和磁共振波谱成像鉴别诊断脑胶质瘤的临床价值
郑晓昀,常莎,黄正旺,苏仕炜
广东同江医院 (广东佛山 538300)
脑胶质瘤按照恶性程度可分为低级别、高级别脑胶质瘤。临床认为,明确脑胶质瘤的恶性程度是制定及实施后期治疗方案的基础。因此,选取有效的检查方式明确患者的脑胶质瘤恶性程度十分必要。磁共振弥散加权成像(magnetic resonance imaging diffusion weighted imaging,MRI-DWI)能显示不同恶性程度脑胶质瘤病灶特异的信号强度改变,是鉴别诊断脑胶质瘤的常用方法,但在临床诊断过程中仍会出现漏诊及误诊[1]。目前,磁共振波谱成像(magnetic resonance spectroscopy,MRS)是唯一一种能无创性地观察活体组织代谢及生化变化的技术,可通过测定脑内感兴趣区的N-乙酰基天门冬氨酸(N-acetyl aspartate,NAA)、胆碱化合物(Choline,Cho)以及肌酸(Creatine,Cr)等代谢产物的浓度来获取不同肿瘤病灶组织的生理及病理信息,并辅助鉴别诊断脑胶质瘤[2]。但业界对MRI-DWI、MRS鉴别诊断脑胶瘤的价值尚存争议。基于此,本研究旨在进一步分析MRI-DWI、MRS鉴别诊断脑胶质瘤的临床价值,现报道如下。
1 资料与方法
1.1 一般资料

1.2 方法
MRI-DWI检查:患者取仰卧位,选用Achieva 3.0T型磁共振扫描仪(荷兰飞利浦公司),正交头颅线圈,并将头部置于线圈内;先实施常规扫描,设置T1WI(TR/TE为440 ms/ll ms)及T2WI(TR/TE为3 600 ms/85 ms),视野250 mm×250 mm、层厚5 mm、层间距1 mm、矩阵320×224;再于肘前静脉使用高压注射器以2 ml/s的速度注入0.2 mmol/kg钆喷酸葡胺造影剂(上海旭东海普药业有限公司,国药准字H19991368,规格 20 ml︰9.38 g)行增强扫描,T1WI(TR/TE为620 ms/12 ms),视野270 mm×270 mm、层厚4 mm、层间距0.8 mm、矩阵300×432;再行MRI-DWI扫描,采用序列回波平面成像序列,TR/TE为500 ms/108 ms、视野37.3 mm×18.1 mm、层厚6 mm、层间距0.8 mm,矩阵128×128,弥散梯度因子b为02、800 s/m2,一次激励成像;弥散敏感梯度分别施加在频率编码、相位编码及选层方向上得到3组DWI图像,然后将DWI原始数据传入后台系统生成表观弥散系数(Apparent diffusion coefficient,ADC)分布图,选取肿瘤实质部分、坏死部分、瘤周水肿带及对侧相应部分正常脑白质内避开血管及脑脊液划定3个上感兴趣区(Region of interest,ROI),获取ADC值。
MRS扫描:患者取仰卧位,采用点分辨表面线圈波谱分析技术,TR/TE=1 500 ms/144 ms,于平轴位T2WI或增强后轴位T1WI定位肿瘤最大实性层面,范围包括肿瘤实性及边缘区、健侧脑组织,然后传入后台工作站进行处理,获得MRS代谢分布图,代谢物比率图,体素划定区域为肿瘤实性部分及相对应健侧部分,测定代谢物NAA、Cho、Cr浓度并计算Cho/NAA,Cho/Cr、NAA/Cr水平,由2名经验丰富的影像学医师共同阅片得出诊断结果。
手术病理分析:患者均在完成以上检查后1周内实施手术,以手术病理结果判定脑胶质瘤恶性程度。
1.3 评价指标
(1)诊断价值:以手术病理结果为金标准,对比分析MRI-DWI、MRS鉴别诊断脑胶质瘤的准确度、灵敏度、特异度。(2)一致性分析:采用Kappa进行一致性检验,分析MRI-DWI、MRS鉴别诊断脑胶质瘤结果与手术病理结果的一致性。
1.4 统计学处理
2 结果
2.1 手术病理结果
经手术病理结果确诊,60例脑胶质瘤患者中35例为低级别,25例为高级别。
2.2 MRI-DWI、MRS鉴别诊断脑胶质瘤结果
MRS鉴别诊断脑胶质瘤的准确度、灵敏度、特异度均高于MRI-DWI,差异有统计学意义(P<0.05)。经Kappa一致性检验,MRI-DWI鉴别诊断脑胶质瘤与手术病理结果的一致性一般(Kappa=0.414,P<0.05);MRS鉴别诊断脑胶质瘤与手术病理结果的一致性较好(Kappa=0.898,P<0.05),见表1~3。
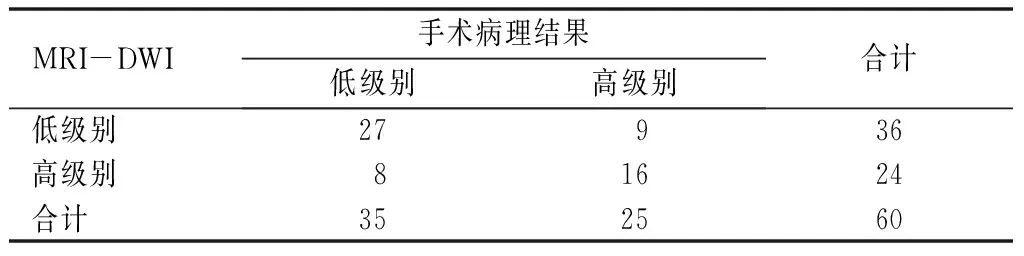
表1 MRI-DWI鉴别诊断脑胶质瘤结果与手术病理结果分析(例)

表2 MRS鉴别诊断脑胶质瘤结果与手术病理结果分析(例)

表3 MRI-DWI、MRS鉴别诊断脑胶质瘤结果(%)
3 讨论
外科手术是治疗脑胶质瘤患者的常用方法,能有效清除病灶,延长患者的生存期。但因为脑胶质瘤恶性程度不同其手术策略也不同,因此,术前采用科学、高效的影像学手段明确病灶恶性程度至关重要。
目前,MRI在脑肿瘤诊断中应用广泛,但常规MRI扫描在反映脑胶质瘤功能信息方面的作用有限。有研究表明,脑胶质瘤发生后,肿瘤组织的细胞间隙会影响间质水分子的弥散程度;并且病变程度越高的脑胶质瘤内的肿瘤细胞成分越多、间质成分越少,组织中水分子的面上运动越弱[4]。因此,采取相应措施明确患者肿瘤组织细胞水分子弥散程度可有效地鉴别诊断脑胶质瘤的恶性程度。MRI-DWI是唯一一种能在活体中评价分子弥散运动的无创诊断手段,其软组织分辨能力及多平面成像和多参数分析能力较强,在扫描后可准确测定ADC值,而ADC值可直接反映组织内水分子弥散快慢程度,组织中水分子弥散运动越快,ADC值高。因此,利用MRI-DWI可鉴别诊断脑胶质瘤恶性程度。但是有研究发现,肿瘤的ADC值和细胞构成的相关程度并非十分密切,细胞间质中的亲水物质-透明质酸可影响ADC值表达,造成漏诊及误诊,需寻求更为高效的诊断方案[5]。除MRI-DWI外,MRS是以化学位移、MRI耦合现象为核心的检查技术,近年来在脑胶质瘤鉴别诊断中应用广泛。本研究结果显示,MRI-DWI和MRS在脑胶质瘤鉴别诊断中均有一定价值,但MRS的诊断价值更好。其原因为,脑胶质瘤是由胶质细胞异常增生形成,在肿瘤生长的过程中,胶质细胞会浸润正常神经元,引起神经元代谢物质的改变。CHo、NAA、Cr均是神经元代谢物质,其中CHo参与生物膜的构成及细胞生物膜的转运,其水平可反映肿瘤增殖情况及细胞膜转运情况;NAA是正常神经元标志物,神经元被破坏可引起NAA水平降低;Cr能反映能量代谢情况,代谢增加可导致Cr降低[6]。一般而言,脑胶质瘤恶性程度越高,肿瘤的增殖能力越强,神经元受破坏程度越高,能量代谢就越强。利用MRS可准确获取代谢物NAA、Cho、Cr浓度并计算出Cho/NAA,Cho/Cr、NAA/Cr水平,通过代谢物比值能准确鉴别诊断脑胶质瘤恶性程度[7];且MRS一次扫描可获取肿瘤全部代谢信息,并不受病变部位、病变内成分等的影响,可有效提升诊断价值。
综上所述,MRS鉴别诊断脑胶质瘤的准确度、灵敏度、特异度均高于MRI-DWI,且MRS鉴别诊断脑胶质瘤的结果和手术病理结果的一致性更好。

