基于证据的化学项目式学习
李奕霖 吴晓红
摘要:基于证据的项目式学习是在项目进行的各个环节要有证据支撑,学生根据证据提出问题猜想、设计探究方案,并产生新证据支撑最终成果的得出。以初識人体缓冲机制为例,提供信息证据等引导学生从认识人体血液pH稳定原因到深入认识缓冲机制,熟练运用水溶液中离子平衡知识解决实际问题,体会生命中的化学,同时培养证据意识。
关键词:项目式学习;证据意识;缓冲溶液;离子平衡
文章编号:1008-0546(2021)03-0037-03 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2021.03.008
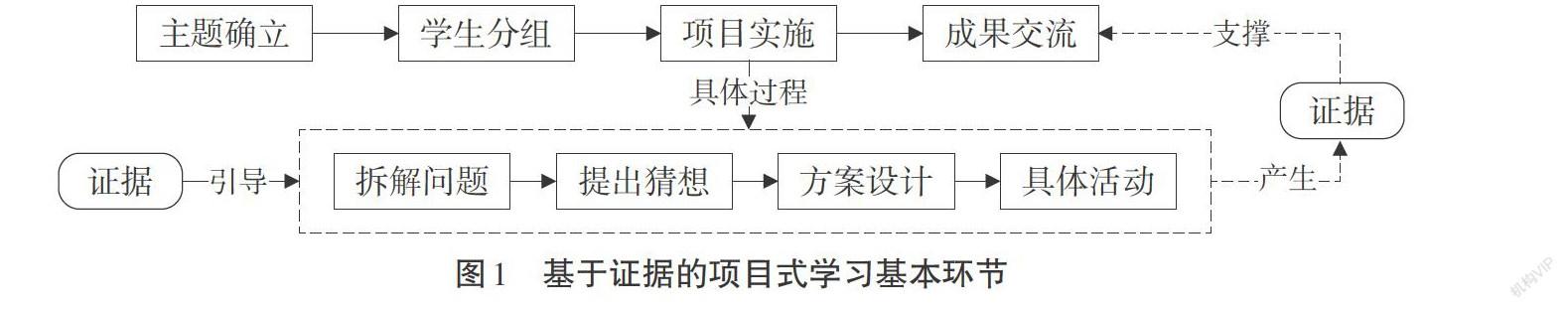
基于证据的化学项目式学习是指在项目式学习实施过程中通过证据引导学生完成系列环节并最终得到一定成果[1]。其进程分为主题确立、学生分组、项目实施、成果交流四步。在项目实施过程中,学生首先将主题问题拆解成一个个小问题并依据证据提出合理的猜想;其次,进一步收集证据设计探究方案并进行有理有据的探究;在实施的过程中产生证据为最终项目成果的得出作支撑,如图1所示。将证据贯穿项目实施始终,让学生在学习知识的同时形成证据意识,培养证据推理与模型认知等化学学科核心素养。
一、项目简介
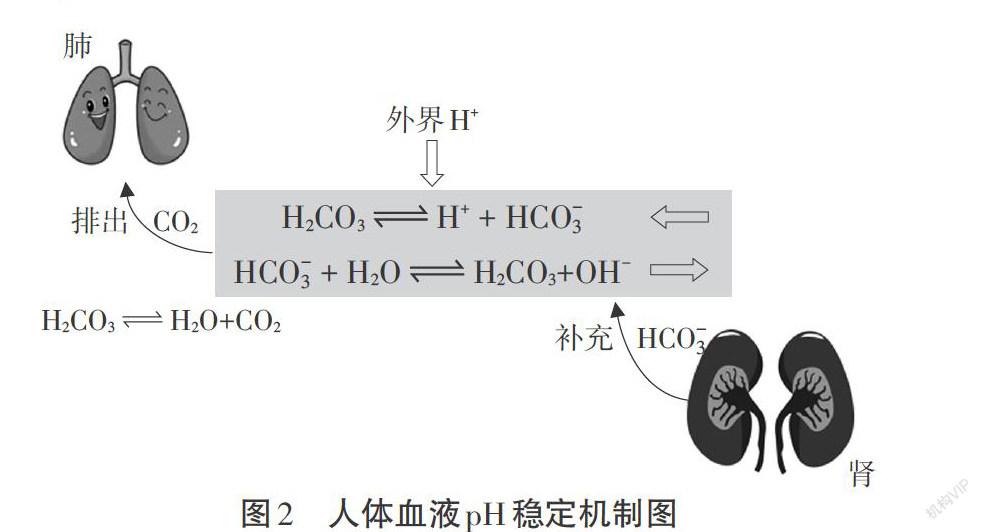
正常人的血液pH相对恒定,维持在7.34~7.45。然而,在正常情况下人体代谢会不断产生酸或碱,它们进入血液中并未引起pH明显的变化。究其原因,是由于血液中存在以HZCO3~HCO3-为主的缓冲体系。定性分析,以H2CO3~HCO3-为例,缓冲溶液作用的机制是水溶液中离子平衡(H2CO3H++HCO3-,HCO3-+H2OH2CO3+OH-)无论H+还是OH-的介入都会引起两个平衡移动来抵抗外界酸碱的作用[2]。定量分析,根据三段式进行缓冲体系pH计算公式推导,发现pH与缓冲体系共轭酸碱的浓度比有关,而与H+或OH-浓度无关。缓冲机制对于学生而言是一个较新的概念,但所用知识却是旧知,有利于提高学生对复习课的兴趣。同时该主题内容既帮助学生复习并应用离子平衡的原理,又涉及运用三段式、平衡常数相关知识进行数学推导,对该章节重点内容涵盖较全面,因此具有较好的教学价值。
在本项目中,教师以伪科学“酸碱体质”理论为导入引导学生根据日常生活中的证据推翻它,并继而提出主题问题“为什么人体血液pH能维持相对稳定”?然后将该问题拆解成三个小问题并形成子项目,分别是寻我维持血液pH稳定的因素、验证这些因素发挥作用的原理、理论上深度探析该原理。在子项目1中教师提供人体血气分析部分指标供学生形成证据,推理出血液pH稳定的因素与CO2和HCO3-有关。在子项目2中,学生设计实验证实保持pH不变的机制与溶液中离子平衡有关,并分析教师提供的人体代谢性酸碱中毒一般治疗方案,形成又一证据支撑相关结论。最后,在子项目3中教师根据学生前面的探究提出缓冲体系的概念,引导学生利用三段式进行缓冲体系pH计算公式的推导。以公式为证据分析得出缓冲体系pH与H+或OH-浓度无关,并将公式应用到血液pH计算中,结果与事实相符,首尾呼应。每一子项目中学生以已有知识为证据对问题进行合理的猜想,教师为学生探究与推理提供一定的信息,供学生分析并形成证据。
二、项目目标
(1)学会从已有的知识经验中搜集并利用证据,能利用证据解决问题,形成证据意识,落实证据推理核心素养;
(2)掌握科学探究的一般过程和规律,学会根据证据进行问题的猜想、科学的探究、结论的获得;
(3)能结合微粒观、平衡观解释人体血液维持稳定的原因,并认识缓冲作用,体会化学知识在生命健康中的重要性。
三、项目实施
1.项目背景
【背景情境】“酸碱体质”理论(通过食用苏打水等碱性食物、药品使血液越来越偏碱性,成为碱性体质从而利于健康)被不少养生达人奉为真理,大量的保健品也基于此诞生。就在近期,这套理论终于被“官宣”伪科学。美国圣地亚哥法庭判一个叫做罗伯特·欧·阳的人赔偿一名癌症患者1.05亿美元。而这位罗伯特·欧·阳就是“酸碱体质”理论的创始人。如果你们是癌症患者的律师,会如何反驳这套伪科学理论?
【学生】该理论是不成立的。(反驳的证据:①根据已学生物知识可知人体八大平衡之一是酸碱平衡,会自动调节酸碱平衡,使血液pH正常维持在7.34~7.45。②根据生活经验,正常人日常摄人食物既有酸性的、也有碱性的,并未影响到人体血液酸碱性改变。)
【提出问题】为什么人体血液pH能够维持稳定?
2.项目拆解
(1)子项目1:解读人体血气分析表
【拆解问题1]从血液环境中探寻影响血液酸碱性的因素。
【学生猜想】血液中含有一定的粒子造成血液偏碱性并保持pH稳定(猜想的证据:根据已有生物和化学知识,人体内液体由水及其溶解在水中的无机盐、有机物一起构成,统称为体液。血浆属于体液之一,类似于水溶液,pH是其重要的理化参数。溶液酸碱性取决于H+和OH-的浓度,电解质的电离,一些阴阳离子的水解都会产生H+或OH-。)。
【解决方案】参考资料了解血液环境中与pH相关的因素以及酸碱平衡紊乱后相关影响因素的变化。
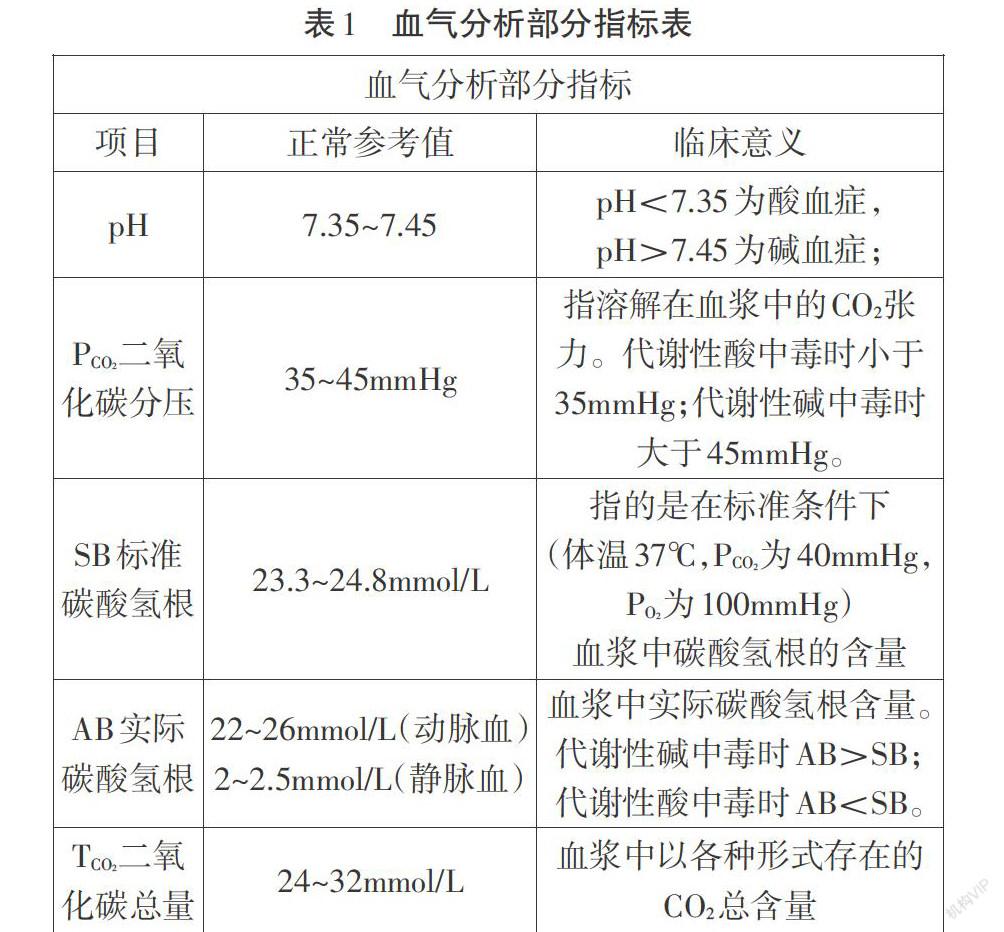
【具体探究】教师提供相关资料,人体血气分析部分指标说明,如表1。学生小组分析讨论,归纳由表格可发现的信息并作为证据继而得出初步结论[3]。
【结论展示】(1)血液呈现弱碱性是由于碳酸氢根的存在。(支撑的证据:通过血气分析表知,血液中含有一定量的HCO3-;根据已有的水溶液中离子平衡知识知HCO3-水解(HCO3+H2O=H2CO3+OH-)会产生少量OH-。)(2)血液pH是CO2与HCO3-洪同影响的结果。(支撑的证据:根据血气分析表可知代谢性酸(碱)中毒会打破血液pH稳定,除了体现在pH不在正常参考范围内,同时也伴随PCO2,AB发生变化。)
(2)子项目2:探析血液pH稳定原因
【拆解问题2】CO2与HCO3-是如何具体影响血液pH稳定。
【猜想】CO2与HCO3-之间存在的平衡关系维持血液pH稳定(猜想的证据:根据已有的离子平衡知识,CO2溶于水生成HZCO3,H2CO3电离会产生HCO3-,HCO3-水解也会生成H2CO3。这对平衡中产生H+和OH-影响着pH)。
【验证方案】思路1:营造体外含有H2CO3与HCO3-的溶液环境,添加少量外界酸碱,以及稀释,验证溶液pH不变。(设计的证据:较可能真实地模拟体内血液要探究的环境)
思路2:用其他弱酸及对应的盐代替H2CO3与HCO3-,如HAc与NaAc,营造溶液环境,添加少量外界酸碱,以及稀释,验证溶液pH不变。(替代的证据:根据已有知识,HAc与NaAc同样存在着电离与水解的平衡关系且HAc易保存。本探究验证的是H2CO3与HCO3-的作用机制对维持溶液pH有效而非粒子本身,因而找具有相同作用机制的粒子进行替代。)
【具体探究】教师提供实验药品和仪器,药品有0.9%的NaCl溶液、HAc、NaAc、稀盐酸、NaOH溶液、NaHCO3溶液、甲基橙、酚酞、紫色石蕊溶液等;仪器有锥形瓶、小烧杯、玻璃棒、量筒,pH试纸、pH计等。学生进行实验,验证实验组和对照组中有外界酸碱加入后酸碱性的变化。
【资料卡片】对于一般代谢性酸中毒,常用的治疗方法是补充NaHCO3碱性药物。对于代谢性碱中毒,有循环血容量不足的病人,先快速输人右旋糖酐70盐水注射液,恢复有效循环血容量,然后输生理盐水补足细胞外液容量,以减少远端肾曲小管的以H+换Na+,发挥肾脏排出HCO3-的功能;对于心力衰竭、肝硬化的病人可服抑制碳酸配酶利尿剂,减少H+排出,增加K+与Na+交换,减少HCO3-回收,增加HCO3-排出。(教师为学生认识人体中H2CO3~HCO3-通过平衡移动维持血液pH稳定提供事实证据)
【结论展示】在血液中CO2溶解生成H2CO3,H2CO3的电离与其对应的盐中微粒 HCO3-的水解维持着平衡状态,外界酸碱介入时会促进平衡移动消耗多余的H+或OH-,从而保持血液pH稳定。(支撑的证据:在探究实验中,实验组pH在外界酸碱的少量干预下维持稳定。通过教师提供的资料卡片可知在医学中,一般治疗代谢性酸(碱)中毒,原理都是补充(排出)HCO3-,促进平衡的移动。)
(3)子项目3:认识缓冲溶液
【拆解问题3】理论深入认识作用机制。
【教师】讲解缓冲作用以及缓冲溶液定义。
【学生】按照教师讲解思路分析加少量碱后,缓冲溶液起作用的原理。认识到H2CO3与HCO3在血液中实际上形成了缓冲体系。
【小组活动】理论计算推导缓冲溶液pH。
设体系中原有的浓度H2CO3为a,HCO3-为b,加入少量外界酸时,增加的H+浓度为x根据三段式算得pH=-lgk1-lga/b[4]。
【结论】缓冲溶液的pH与缓冲对中弱酸电离常数以及缓冲对共扼酸碱浓度比有关,故当有少量外界的酸碱介入或者稀释时,共扼酸碱浓度比基本不变从而保持溶液PH不变。(支撑的证据:推导的缓冲溶液pH计算公式)
【教师】提供信息37℃下,H2CO3电离常数是7.9×10-7;人体血浆中HCO3-是H2CO3含量的20倍;计算该温度、配比下HCO3-~H2CO3溶液的pH。
【学生】根据推导公式计算pH=7.4,与血液pH在7.35~7.45相吻合。
【小组活动】讨论配制缓冲溶液的注意事项及缓冲溶液的应用。
绘制H2CO3~HCO3-在人体中维持血液酸碱平衡的调节图示。
【最终成果】展示人体血液维持稳定的作用机制图,如图2。
四、项目反思
本项目通过“人体血液pH为什么会维持稳定”这一核心问题驱动学生探究其原因,按照“寻找与问题相关的因素——验证该因素的影响并分析因素作用的機制——上升高度认识原因背后的科学理论”的规律逐步认识缓冲机制,并将离子平衡相关知识得以回顾与运用。在知识层面,学生对缓冲机制的认识主要是通过自主探究的方式得到,更多的是内在动机驱动着学生,在项目探究中综合离子平衡的相关知识包括弱电解质电离平衡、离子水解平衡、平衡常数的计算等,有利于学生对知识整合并综合运用,提高理解与复习效果。在能力方面,该学习锻炼学生人际交往、动手实践等适应现代化社会生活的种种能力。同时项目活动各个环节基于证据进行,引导学生在解决问题中根据已有的经验知识作为证据提出对问题的猜想,针对猜想搜集相关信息结合已有知识经验作为证据进行合理的探究方案设计,在探究过程中产生的各种实验现象、计算的理论结果等等筛选出有效的,形成证据支撑最终结论,让整个过程有理有据,具有说服力。在这样的一步步引导下,有利于学生证据意识的培养,在信息化时代中,养成搜集信息、获取证据并科学推理的科学态度,打下终身学习的基础。
参考文献
[1]马宁,赵若辰,张舒然.项目式学习:背景、类型与核心环节[J].中小学数字化教学,2018(5):24-27
[2]兰婷,冀楠,王海波,秦向阳,何炜.化学教育医用基础化学缓冲溶液及其作用机制的教学设计与思考[J].化学教育(中英文),2020,41(10):67-70
[3]牛彩霞,邹映波.基于项目式学习的“水溶液中的离子平衡”专题复习——以“人体代谢性酸中毒治疗方案的设计”为例[J].化学教学,2020(6):53-58
[4]北京师范大学,华中师范大学,南京师范大学.无机化学(第四版)[M].北京:高等教育出版社,2003:310-312,323-329
*本文系国家自然科学基金地区科学基金项目“西北民族地区科学探究教育绩效评价及影响因素研究”(项目批准号71663042)阶段性研究成果。
**通讯联系人,E-mail:wxhnxuedu@163.com

