TiO2-WO3-ATP复合吸附剂对Pb(Ⅱ)的吸附性能研究
李静萍,薛田田,苏可心,郑 瑶
(兰州交通大学 化学化工学院,兰州 730070)
金属铅广泛的应用于蓄电池、机械制造业和轻工等行业,由此造成了日益严重的铅污染.铅可通过污染的空气、水、泥土和食品摄入人体,对人体的骨骼、肝脏和大脑等造成危害.因此寻求高效、低耗减少水体中铅污染的水处理方法尤为重要.
国内外处理重金属离子的方法主要有化学沉淀法、吸附法、微生物法以及膜分离技术[1].吸附法因具有操作简单,能耗低,所需工艺条件简单而被广泛应用.
近年来,无机硅酸盐矿物在功能复合吸附剂中的应用越来越多,其中凹凸棒石黏土由于其独特的孔道结构、大的比表面积、优异的吸附性能而成为研究热点之一,但天然凹凸棒石黏土中含有石英、碳酸盐等杂质[2],吸附能力不够高,吸附效果并不理想.加之我国凹凸棒石黏土矿发现的比较晚,未能高效率的利用,造成了资源的浪费.
本文采用的原料凹凸棒石黏土产自甘肃白银市靖远县,从本土资源的高值化利用出发,对凹凸棒石黏土进行柱撑改性.选用TiO2-WO3复合吸附剂作为柱撑剂,合成一种新型的TiO2-WO3-ATP复合吸附剂,并和ATP、HCl-ATP对Pb(Ⅱ)的吸附性能进行对比分析.通过单因素实验对吸附影响因素进行探究,并对TiO2-WO3-ATP复合吸附剂进行循环再生性能研究.在此基础上,通过吸附动力学实验,确定TiO2-WO3-ATP复合吸附剂对Pb(Ⅱ)的吸附动力学模型.本研究为凹凸棒石复合吸附剂去除Pb(Ⅱ)提供了理论支持.
1 实验部分
1.1 实验试剂及仪器
凹凸棒石黏土;盐酸;氢氧化钠;六偏磷酸钠;钛酸四丁酯(TBT);冰乙酸;钨酸钠;草酸;邻菲啰啉;二甲酚橙;六次甲基四胺;硝酸铅;以上试剂均为分析纯.
SHA-B型恒温振荡器;DF-101S型恒温磁力搅拌器;DHG-9247A型电热鼓风干燥箱;电热恒温水浴锅;721型可见光分光光度计;TGL-16C型高速旋转离心机;马弗炉;FE28型pH计;Gemini 500型扫描电镜仪;VERTEX 70型红外-拉曼光谱仪;DMAX U1TIMAIX型射线衍射仪;ASAP2460-4型比表面积及孔隙度分析仪.
1.2 HCl-ATP的制备
1.2.1 ATP的提纯
称取18.367 g凹凸棒石黏土于烧杯中,向其中加入900 mL蒸馏水,搅拌30 min后加入0.5%的六偏磷酸钠溶液160 mL,继续搅拌2 h后静置30 min,此时溶液会出现分层,抽出上层胶体液,加入5 mol/L的HCl溶液破乳,充分搅拌后离心,用蒸馏水清洗直到pH值不变,将洗涤后的凹凸棒石黏土于80 ℃烘干研磨过筛.提纯后的凹凸棒石黏土记为ATP.
1.2.2 ATP的酸活化
称取10 g提纯后的ATP于具塞锥形瓶中,加入5 mol/L的盐酸100 mL,放入恒温振荡器中,酸活化温度为70 ℃、酸活化时间为60 min.将酸活化后的ATP抽滤、洗涤至pH不变,80 ℃烘干,研细过160目筛备用,记为HCl-ATP.
1.3 TiO2-WO3-ATP复合吸附剂的制备
量取一定体积的无水乙醇,搅拌,滴加钛酸四丁酯和冰乙酸,搅拌30 min后形成A液.量取一定体积的蒸馏水和无水乙醇均匀混合配成B液,用HCl调节溶液的pH为4.在搅拌条件下,控制B液以1滴/秒的速度滴入A液,出现黄色透明溶胶后,立即加入1 mol/L的NaOH溶液改变酸碱比[3],继续搅拌30 min,静置3 h,得到TiO2溶胶.
称取一定质量的钨酸钠溶解于一定体积的蒸馏水中,搅拌10 min,缓慢滴入浓盐酸使溶液酸化,之后有白色絮状沉淀生成,继续搅拌,直到沉淀消失且不再有新的沉淀生成为止,向溶液中加入提前配置好的草酸溶液,搅拌30 min后即得到无色透明的WO3溶胶.
在搅拌条件下,将一定质量的WO3溶胶用分液漏斗,逐滴滴入TiO2溶胶中,使TiO2和WO3的摩尔比分别为5∶0,4∶1,3∶2,1∶1,2∶3,1∶4,0∶5.持续搅拌6 h,得到TiO2-WO3复合溶胶,制得TiO2-WO3柱撑剂.
将制得的TiO2-WO3柱撑剂缓慢滴入1%的HCl-ATP悬浊液中,在常温下搅拌20 h,静置24 h,反复抽滤洗涤十次,于烘箱中80 ℃烘6 h,烘干后研磨过160目筛,再于马弗炉中煅烧2 h.长时间陈化,TiO2、WO3胶粒间缓慢聚合,形成三维空间网络结构的凝胶[4],在干燥、煅烧固化后,得到不同TiO2-WO3摩尔比的TiO2-WO3-ATP(柱撑)复合吸附剂(灰白色),记为TiO2-WO3-ATP.根据不同TiO2-WO3摩尔比可分别表示为TiO2-WO3-ATP5∶0、TiO2-WO3-ATP4∶1、TiO2-WO3-ATP3∶2、TiO2-WO3-ATP1∶1、TiO2-WO3-ATP2∶3、TiO2-WO3-ATP1∶4和TiO2-WO3-ATP0∶5复合吸附剂.
1.4 单因素实验探究吸附Pb(Ⅱ)的影响因素
称取一定质量的吸附剂于具塞锥形瓶中,加入一定浓度的Pb(Ⅱ)溶液,于恒温振荡器中震荡吸附.改变吸附时间、温度、溶液pH和Pb(Ⅱ)初始浓度条件之一,进行不同吸附剂对Pb(Ⅱ)的吸附性能实验.按照公式(1)、(2)计算吸附率,吸附量.
吸附率:
(1)
吸附量:
(2)
其中:C0是吸附质的初始浓度,mg/L;Ce是吸附平衡时吸附质浓度,mg/L;V是吸附质溶液的体积,mL;m是吸附剂投加量,mg.
1.4.1 吸附时间
准确称取0.3 g的ATP、HCl-ATP和7种不同TiO2-WO3摩尔比的TiO2-WO3-ATP吸附剂,各取7份,置于100 mL具塞锥形瓶中,分别加入150 mg/L的Pb(Ⅱ)溶液50 mL,溶液pH为6,温度为35 ℃,恒温振荡吸附20,40,60,80,100,120,150 min后,讨论吸附时间对7种吸附剂对Pb(Ⅱ)吸附率的影响.
1.4.2 吸附温度
选ATP、HCl-ATP和TiO2-WO3-ATP4∶1为吸附剂,研究温度对TiO2-WO3-ATP复合吸附剂对Pb(Ⅱ)吸附率的影响.
准确称取0.3 g的ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂,各取6份,置于100 mL具塞锥形瓶中,分别加入150 mg/L的Pb(Ⅱ)溶液50 mL,溶液pH为6,温度为25,30,35,40,45,50 ℃,恒温振荡吸附100 min.讨论吸附温度对3种吸附剂吸附Pb(Ⅱ)吸附率的影响.
1.4.3 吸附pH
准确称取0.3 g的ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂,各取5份,置于100 mL具塞锥形瓶中,分别加入150 mg/L的Pb(Ⅱ)溶液50 mL,温度为35 ℃,溶液pH为2、3、4、5、6,恒温振荡吸附100 min.讨论溶液pH对3种吸附剂吸附Pb(Ⅱ)吸附率的影响.
1.4.4 Pb(Ⅱ)初始浓度
准确称取0.3 g的ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂,各取7份,置于100 mL具塞锥形瓶中,溶液pH为6,温度为35 ℃,Pb(Ⅱ)的初始浓度分别为150,200,250,300,350,400,450 mg/L,恒温振荡吸附100 min.讨论Pb(Ⅱ)的初始浓度对3种吸附剂吸附Pb(Ⅱ)吸附率的影响.
1.5 吸附剂的解吸再生实验
采用酸处理法进行吸附剂的解吸再生实验,将200 mL 0.2 mol/L的HCl溶液加入到3 g饱和吸附Pb(Ⅱ)的TiO2-WO3-ATP4∶1复合吸附剂中,25 ℃下解吸5 h,经洗涤、干燥.在相同条件下,进行TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附,重复解吸再生实验多次.
1.6 吸附Pb(Ⅱ)的动力学实验
准确称取0.3 g的ATP、HCl-ATP、TiO2-WO3-ATP4∶1的吸附剂,各取7份,置于100 mL具塞锥形瓶中,分别加入150 mg/L的Pb(Ⅱ)溶液50 mL,温度为35 ℃,恒温振荡吸附20,40,60,80,100,120,150 min.按下模型对数据进行动力学模型拟合分析.
1) 准一级动力学模型
众多因子中只存在一种因子决定反应速率称为准一级动力学,其应用于液相的模型方程式直线形式为[5]
ln(qe-qt)=lnqe-k1t,
(3)
其中:qe为吸附平衡时的吸附量,mg/g;qt为t时刻的吸附量,mg/g;k1为一级吸附速率常数,L/min;以ln(qe-qt对t作图,进行线性拟合.
2) 准二级动力学模型
准二级动力学模型假设吸附过程是以化学吸附为主,其直线形式为
(4)
其中:k2为二级速率常数,g/(mg·min).以t/qt对t作图,进行线性拟合.根据线性拟合参数R2判断是否符合准二级动力学模型.
2 讨论与分析
2.1 样品表征测试方法
2.1.1 SEM分析
图1为酸活化ATP前后的SEM图,其中图1(a)为ATP原土,图1(b)和图1(c)分别为HCl-ATP的低倍、高倍镜图.从图中可以看出,ATP原土表面结构致密,凹凸棒石的棒晶杂乱堆积在一起,呈板状结构,分散性较差.HCl-ATP的低倍镜图里,酸活化后的凹凸棒石黏土,由于八面体的溶解,出现了清晰的孔结构,呈团状堆积.HCl-ATP的高倍镜图里,酸活化后的凹凸棒石黏土,表面结构还是较紧密,虽出现孔结构,但孔结构数目较少,且表面还有一定的非棒晶形貌结构.主要原因为甘肃白银市靖远县的ATP纯度较低,凹凸棒石黏土中凹凸棒石含量<50%[6],因而推测出凹凸棒石黏土中凹凸棒石含量较低,含有较多其它伴生矿物等杂质所致.

图1 酸活化前后ATP的SEM图
图2是TiO2-WO3-ATP4∶1的SEM图.图2(a)和图2(b)分别是优选出的TiO2-WO3-ATP4∶1复合吸附剂的低倍、高倍镜图.可以看出,经柱撑改性后凹凸棒石黏土中凹凸棒石的棒晶分散性有所增加,棒晶结构更加明显,棒晶长短不一且较粗,跟原土和HCl-ATP相比,表面变的更加粗糙,孔洞和孔隙结构更加明显,且孔径较大,形状不均匀.

图2 TiO2-WO3-ATP4∶1的SEM图
2.1.2 FT-IR分析

图3 ATP和TiO2-WO3-ATP的FT-IR图
2.1.3 XRD分析
图4为ATP吸附剂和3种不同TiO2-WO3摩尔比(TiO2-WO3-ATP4∶1、TiO2-WO3-ATP2∶3、TiO2-WO3-ATP1∶4)复合吸附剂的XRD图.图中2θ=8.42°、19.68°、20.82°、34.78°黑色方框标记处是ATP特征衍射峰,其中2θ=8.42°处为凹凸棒石(110)晶面的特征衍射[8].2θ=26.56°时的衍射峰为石英相的特征衍射[9],该衍射峰十分尖锐且峰强度较高,说明ATP中有大量的石英杂质相.酸活化后ATP中石英相的衍射峰强度增强,说明酸活化使得ATP中八面体阳离子发生溶解,但大部分硅氧四面体的晶体结构仍然存在[10].2θ=27.82°、36.48°、54.8°处对应TiO2的特征衍射峰[11-12].2θ=24.12°处对应WO3的特征衍射峰.柱撑改性后2θ=8.42°处对应的凹凸棒石(110)晶面特征衍射峰发生了偏移,表明TiO2-WO3柱撑剂成功柱撑进入ATP的层间域[13].

图4 ATP和TiO2-WO3-ATP的XRD图
2.1.4 BET分析
图5为ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂的N2等温吸附、脱附曲线和孔径分布图.其中图5(a)为ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂的N2等温吸附、脱附曲线.从图5(a)中可以看出,随着相对压力的增加,ATP、HCl-ATP和TiO2-WO3-ATP4∶1对N2的吸附量均呈现增大趋势,在相对压力大约0.8之后,吸附量数值迅速上升,这说明脱附等温线在吸附等温线上方,产生吸附滞后环,属于典型的Ⅳ型等温线,表明三种吸附剂均有明显的介孔结构[14-15].
图5(b)为ATP、HCl-ATP和TiO2-WO3-ATP4∶1的孔径分布图.可以看出,3种吸附剂的内孔径数值在20~40 nm范围内,说明吸附剂的结构主要为介孔,与N2等温吸附、脱附曲线结果相一致.ATP在经过酸活化改性后,由于八面体片的溶解,介孔数量明显增多.柱撑改性后TiO2-WO3-ATP4∶1复合吸附剂中介孔、大孔数量均有所增加,进一步证实了TiO2-WO3成功柱撑进入凹凸棒石黏土片层间.
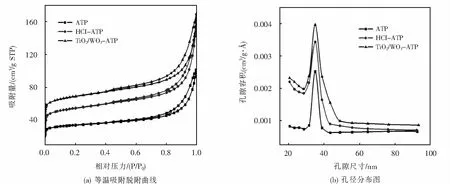
图5 ATP、HCl-ATP和TiO2-WO3-ATP吸附剂的N2等温吸附脱附曲线和孔径分布图
2.2 实验结果与讨论
2.2.1 单因素实验探究吸附Pb(Ⅱ)的影响因素
1) 吸附时间
时间对Pb(Ⅱ)吸附率的影响如图6所示.图6表明,ATP、HCl-ATP和7种不同TiO2-WO3摩尔比的TiO2-WO3-ATP复合吸附剂对Pb(Ⅱ)的吸附率,在初始阶段30~60 min阶段吸附率增加较快,60~90 min吸附率增加缓慢,100 min后吸附率基本不变,达到吸附平衡.在达到吸附平衡后,可以看出,7种不同TiO2-WO3摩尔比的TiO2-WO3-ATP复合吸附剂对Pb(Ⅱ)的的吸附率整体高于ATP以及HCl-ATP,这是因为经过酸化以后的ATP结构中八面体的溶解,孔径变大,表面变得更加粗糙,再经过TiO2-WO3柱撑后,进一步增大了比表面积,吸附能力明显提高.其中TiO2-WO3-ATP4∶1复合吸附率最大,为98.41%.

图6 时间对Pb(Ⅱ)吸附率的影响
2) 吸附温度
温度对Pb(Ⅱ)吸附率的影响如图7所示.图7表明,ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂对Pb(Ⅱ)的吸附率,随着温度的变化,3种吸附剂对Pb(Ⅱ)的吸附率变化趋势相似,在25 ℃~35 ℃范围内,吸附率均呈现增大趋势,35 ℃时,吸附率数值最大,分别为89.17%、93.93%、98.41%.35 ℃之后,随着温度的升高,吸附率呈现下降趋势.这是因为随着温度的升高(25 ℃~35 ℃范围内),Pb(Ⅱ)的热运动加快,使其更容易接触到吸附剂的部分活性位点[16],Pb(Ⅱ)的吸附速率大于解吸速率,吸附率增大,继续升高温度,Pb(Ⅱ)的解吸速率大于吸附速率,Pb(Ⅱ)从吸附剂表明脱落,导致吸附率减小.
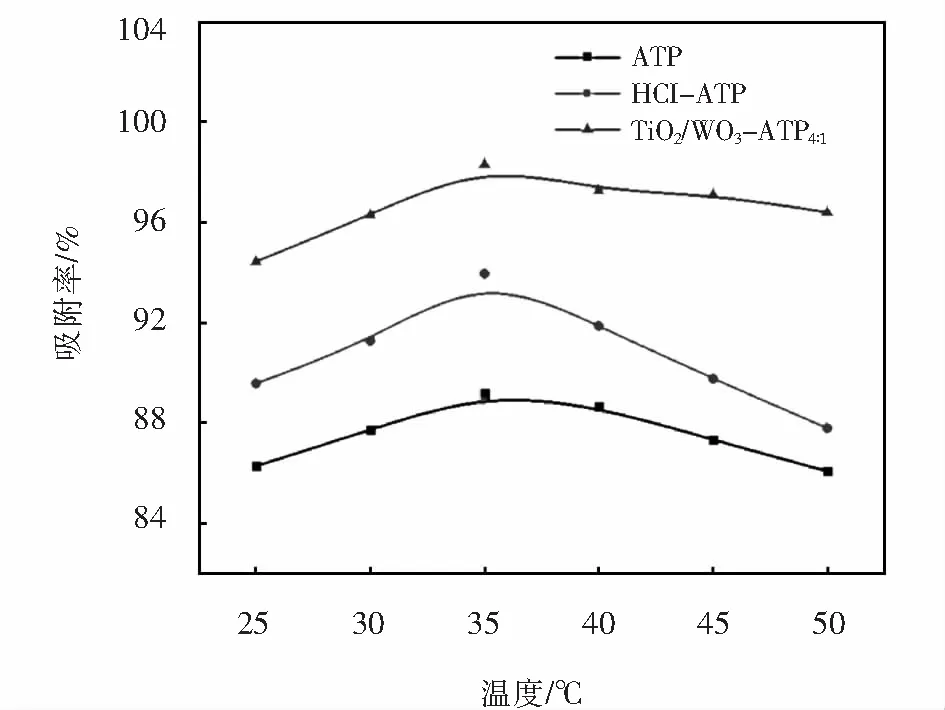
图7 温度对Pb(Ⅱ)吸附率的影响
3) 吸附pH值
pH对Pb(Ⅱ)吸附率的影响如图8所示.图8表明,ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂对Pb(Ⅱ)的吸附率,在pH值在2~6范围内,随着pH值增大,3种吸附剂对Pb(Ⅱ)的吸附率增大.在酸性条件下,溶液中H+与Pb(Ⅱ)竞争吸附位点,pH值越大,溶液中H+离子浓度越小,三种吸附剂对Pb(Ⅱ)的吸附率越大.在pH≥7.04(20 ℃,Pb(Ⅱ)浓度为0.1 mol/L)时,溶液中Pb(Ⅱ)会发生水解生成沉淀,2OH-+Pb2+=Pb(OH)2↓[17].所以,本实验不涉及碱性条件下,3种吸附剂对Pb(Ⅱ)吸附率的影响.

图8 pH对Pb(Ⅱ)吸附率的影响
4) 吸附质Pb(Ⅱ)的初始浓度
初始浓度对Pb(Ⅱ)吸附率的影响如图9所示.图9表明,ATP、HCl-ATP和TiO2-WO3-ATP4∶1吸附剂对Pb(Ⅱ)的吸附率,随着Pb(Ⅱ)起始浓度的增大,3种吸附剂对Pb(Ⅱ)的吸附率逐渐减小.Pb(Ⅱ)起始浓度在150 mg/L~300 mg/L范围内,ATP、HCl-ATP和TiO2-WO3-ATP4∶1对Pb(Ⅱ)的吸附率分别下降了2.29%、1.98%、0.78%,而Pb(Ⅱ)起始浓度在300 mg/L~450 mg/L范围内,ATP、HCl-ATP和TiO2-WO3-ATP4∶1对Pb(Ⅱ)的吸附率分别下降了11.49%、11.11%、11.54%.这是因为随着Pb(Ⅱ)起始浓度的增大,溶液中Pb(Ⅱ)浓度增大,而一定质量的吸附剂,吸附活性位点不变,因此,吸附剂对Pb(Ⅱ)的吸附率数值减小.
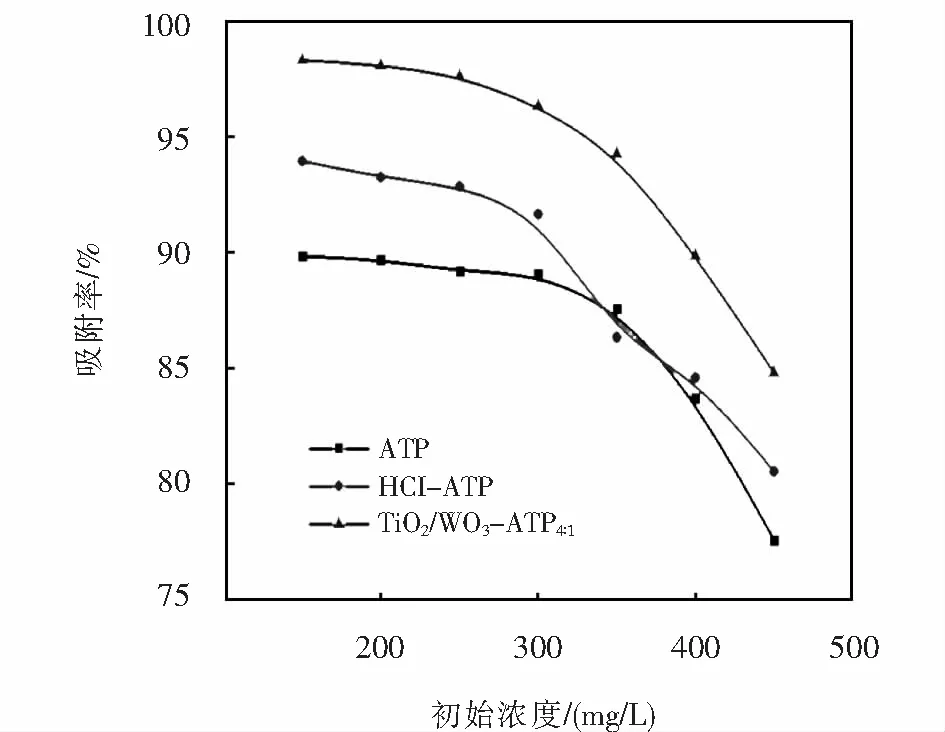
图9 初始浓度对Pb(Ⅱ)吸附率的影响
柱撑改性后的TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附率整体高于ATP和HCl-ATP,表明TiO2-WO3-ATP4∶1复合吸附剂在柱撑改性后吸附位点增多.投加量为0.3 g的TiO2-WO3-ATP4∶1复合吸附剂初始浓度在150~300 mg/L范围内,对Pb(Ⅱ)的吸附率均在95%以上.
2.2.2 吸附剂的解吸再生实验
1) 循环次数对Pb(Ⅱ)吸附率的影响如图10所示.图10表明,采用酸处理法进行TiO2-WO3-ATP4∶1复合吸附剂的解吸再生实验,循环4次后,再生后复合吸附剂吸附Pb(Ⅱ)的吸附率下降到39.17%,说明3次解吸再生后的TiO2-WO3-ATP4∶1复合吸附剂的吸附性能变差,TiO2-WO3-ATP4∶1复合吸附剂可循环吸附Pb(Ⅱ)3次.第3次解吸再生的TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附率可达58.64%.
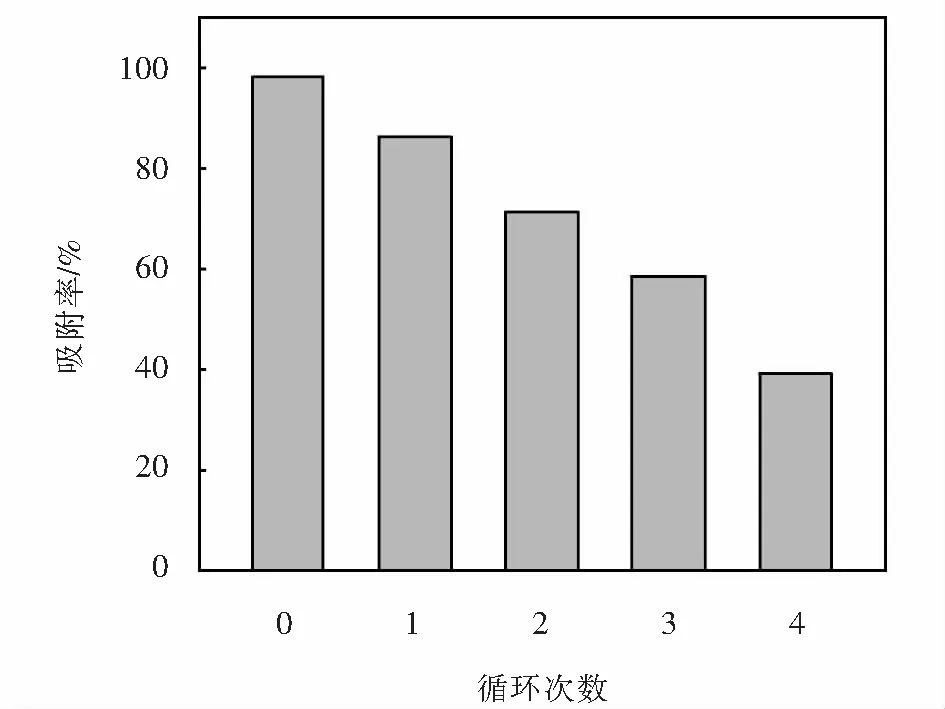
图10 循环次数对Pb(Ⅱ)吸附率的影响
2.3 吸附Pb(Ⅱ)的动力学
吸附时间与Pb(Ⅱ)吸附量关系如图11所示.图11表明,TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)吸附的初始阶段,随着时间的变化,吸附率数值明显增大,吸附100 min后,吸附率基本保持不变,达到吸附平衡状态.其中TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附率最大,HCl-ATP吸附剂次之,ATP吸附剂最小.

图11 吸附时间与Pb(Ⅱ)吸附量关系图
将上述数据用公式(3)和(4)进行线性回归,结果见图12,所求出的回归参数见表1.
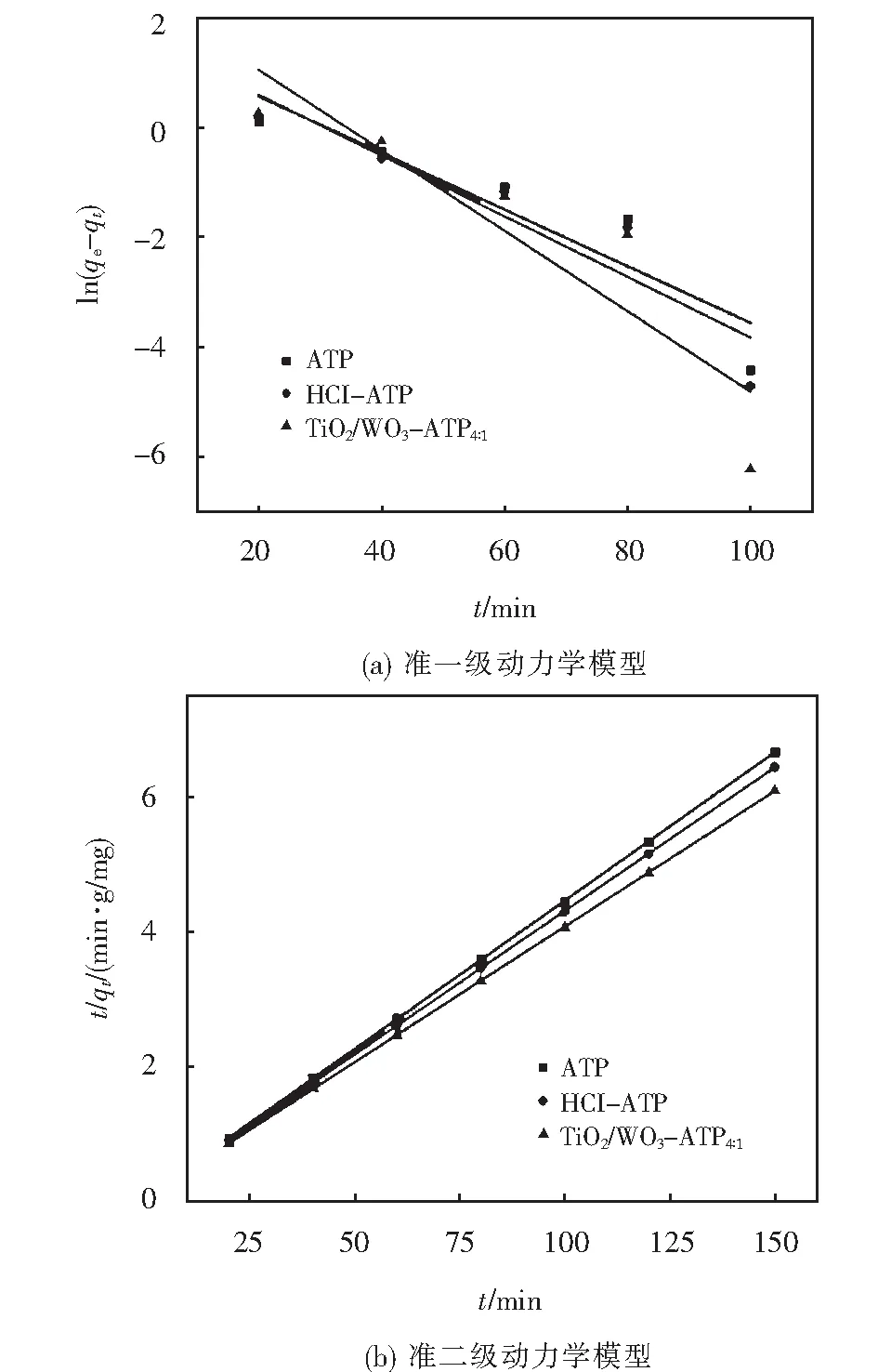
图12 吸附Pb(Ⅱ)的动力学方程回归图
对表1中吸附Pb(Ⅱ)的准一级和准二级动力学方程回归参数进行分析,发现ATP、HCl-ATP、TiO2-WO3-ATP4∶1吸附剂吸附Pb(Ⅱ)的准二级吸附速率方程的R2均大于0.999,高于准一级动力学方程的R2,说明吸附过程符合准二级动力学模型.准二级动力学模型认为化学吸附控制着整个吸附过程,表明三种吸附剂对Pb(Ⅱ)的吸附过程为化学吸附[18-19].
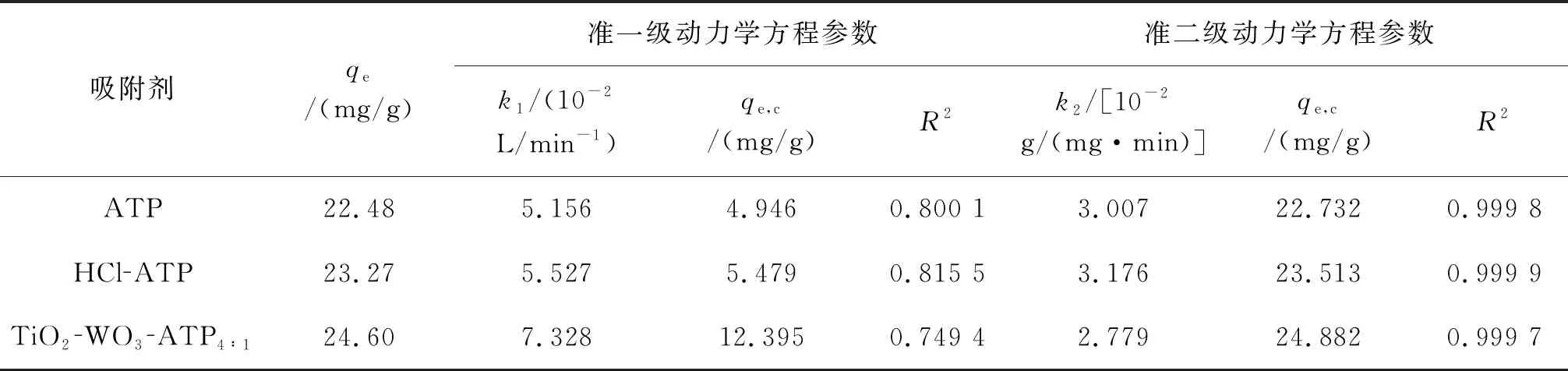
表1 吸附Pb(Ⅱ)的动力学方程回归参数表
2.4 吸附Pb(Ⅱ)机理分析
综合单因素实验、吸附动力学、吸附剂的解吸再生实验结果,TiO2-WO3-ATP4∶1的结构表征分析,推测TiO2-WO3-ATP4∶1对Pb(Ⅱ)的吸附机理为
1) 物理吸附:TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)吸附过程中,常温下的吸附率数值较大,表明TiO2-WO3-ATP4∶1复合吸附剂和Pb(Ⅱ)之间存在范德华力.
2) 化学吸附:TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)吸附过程中,其准二级吸附速率方程的R2为0.999 7,表明TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附为化学吸附.
因此,推断TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)吸附过程中既有物理吸附又有化学吸附.
3 结论
1) 通过ATP、HCl-ATP和3种不同TiO2-WO3摩尔比的TiO2-WO3-ATP吸附剂的SEM、FT-IR、XRD、BET的结构表征分析,TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)吸附性能最好.
2) TiO2-WO3-ATP4∶1复合吸附剂为0.3 g,Pb(Ⅱ)初始浓度为150 mg/L,溶液pH为6,温度为35 ℃,吸附时间100 min,TiO2-WO3-ATP4∶1对Pb(Ⅱ)的吸附率可达98.41%.
3) TiO2-WO3-ATP4∶1可循环吸附Pb(Ⅱ)3次,第3次解吸再生的TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附率可达58.64%
4) TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附过程可以用准二级动力学模型描述.
5) TiO2-WO3-ATP4∶1复合吸附剂对Pb(Ⅱ)的吸附过程既有物理吸附又有化学吸附.

