在线衍生-双三元高效液相色谱同时检测水产品中的甲醛及双乙酸钠含量
牛灿杰,徐腾洋,张水锋,赵淑娟,朱 帅,郑仕剑,黄润韬,盛华栋,*
(1.浙江方圆检测集团股份有限公司,浙江 杭州 310018;2.浙江省食品安全重点实验室,浙江 杭州 310018;3.浙江经贸职业技术学院,浙江 杭州 310012)
水产品味道鲜美,营养价值高,是消费者喜爱的食品之一,然而由于水产品富含水分,在流通过程中,易发生污菌腐败[1],抑菌防腐剂的添加时有发生。水产品中常用抑菌防腐剂有壳聚糖[2-5]、山梨酸钾[6-7]、乳酸链球菌素[8-9]、双乙酸钠[7,10]。关于水产品中双乙酸钠的防腐保鲜效果研究较多[7,10-12],研究表明双乙酸钠在水产品防腐方面具有广阔的应用前景及发展潜力[13-15]。甲醛因其具有防腐、定型、改善外观的效果,有可能被非法添加在水产品中,该问题越来越受到人们重视[16]。目前,我国针对水产品中双乙酸钠及甲醛的限量标准及检测方法仍比较匮乏。GB 2760—2014《食品添加剂使用标准》只规定了熟制水产品中双乙酸钠的限量,禁止使用甲醛作为水产品添加剂。我国针对水产品中双乙酸钠及甲醛的检测方法分别为GB 5009.277—2016《食品中双乙酸钠的测定》、SC/T 3025—2006《水产品中甲醛的测定》,均经酸化后采用传统水蒸气蒸馏提取,甲醛还需经过复杂耗时的衍生化反应及反萃取过程进行检测,采用分光光度法时灵敏度、准确度较低,且易受干扰造成假阳性结果[16],不利于大批量样品的快速定性定量检测。食品中双乙酸钠的检测方法有高效液相色谱法[17-18]和离子色谱法[19],前处理方法主要有直接浸提法[18]、水蒸气蒸馏法[17]、固相萃取法[20];采用直接浸提法,由于双乙酸钠酸化后产物乙酸吸收波长短,在反相色谱柱(如C18色谱柱)上吸附能力弱,基质复杂时干扰较严重,不适用于水产品中双乙酸钠的检测;采用固相萃取方法,步骤繁琐且在一定程度上增加了检测成本;采用传统水蒸气蒸馏提取,耗时、操作复杂,稳定性差且回收率低。针对水产品中甲醛检测方法的研究报道较多,主要有直接浸提柱前衍生法[21]及水蒸气蒸馏提取柱前衍生法[22];采用直接浸提法,主要提取水产品中的游离态甲醛,不能提取结合态甲醛,由于水产品富含蛋白质,易形成可逆结合态蛋白质-甲醛复合物,所以采用直接浸提法提取时甲醛的添加回收率不佳[23];水蒸气蒸馏能提取游离态甲醛和可逆结合态甲醛,适用于水产品中甲醛的提取,但传统的水蒸气蒸馏回收率不高。
目前,针对水产品中游离态及可逆结合态甲醛同时提取并在线衍生的方法鲜见报道,水产品中甲醛和双乙酸钠同时检测的方法也鲜见报道,但水产品中添加这两种防腐剂的可能性较大,而相关检测方法比较匮乏,因此开发快速、简便、高效,适用于水产品基质且可大通量检测的方法具有十分重要的意义。本实验探究采用凯氏定氮仪,同时进行水产品中双乙酸钠及甲醛的水蒸气蒸馏提取的前处理方法,并对水产品中甲醛在线衍生方法进行优化,减少有机溶剂反萃取步骤,建立采用双三元高效液相色谱同时快速检测水产品中甲醛和双乙酸钠的方法,旨在为保障消费者食品安全,满足水产品风险监测需要提供技术支持。
1 材料与方法
1.1 材料与试剂
66 批次水产品:带鱼5 批次,黄姑鱼5 批次、大黄鱼4 批次、梅鱼2 批次、鲳鱼3 批次、章跳鱼2 批次、龙头鱼7 批次、白果鱼3 批次、小黄鱼4 批次、多宝鱼2 批次,均为冷冻状态;鲫鱼8 批次,大闸蟹4 批次、石蟹3 批次、明虾3 批次、沼虾6 批次、梭子蟹2 批次,均为鲜活状态;三文鱼3 批次,为冰鲜状态;以上主要购自流通环节。
甲醛标准溶液(100 μg/mL) 环境保护部标准样品研究所;双乙酸钠(纯度98.0%) 日本TCI公司;2,4-二硝基苯肼(分析纯) 中国医药集团上海化学试剂有限公司;磷酸(纯度≥85%,分析纯) 杭州双林化工试剂厂;甲醇、乙腈(均为色谱纯) 美国天地有限公司;实验所用的水均为超纯水。
1.2 仪器与设备
UltiMate 3000 DGLC双三元高效液相色谱仪(配有两台二极管阵列检测器及变色龙Chromeleon7色谱数据处理系统) 美国Thermo Fisher公司;KN680凯氏定氮仪 济南阿尔瓦有限公司;AH-30全自动均质器 福建睿科集团股份有限公司;SK6200LHC超声仪 上海科导超声仪器有限公司。
1.3 方法
1.3.1 溶液的配制
2,4-二硝基苯肼溶液(衍生液):称取100 mg 2,4-二硝基苯肼溶解于50 mL乙腈-乙酸(4∶1,V/V)混合溶液。
4 mol/L磷酸溶液:在500 mL水中加入246 mL磷酸,混合后加水定容至1 000 mL,混匀。
1.3.2 标准溶液配制
分别取适量甲醛标准溶液,置于10 mL容量瓶中,用水定容至刻度,配制成质量浓度0.5、1.0、2.0、5.0、10.0、20.0 mg/L系列标准工作液;称取适量双乙酸钠标准品,配制成10 mg/mL标准储备液,分别取适量双乙酸钠标准溶液于凯氏定氮仪配套的消解管中,按实验方法和凯氏定氮仪设定程序进行水蒸气蒸馏,制得质量浓度为10、20、50、100、150、200 mg/L系列标准溶液。
1.3.3 样品前处理
准确称取10 g样品(取肌肉等可食部分)于具塞离心管中,加入20 mL超纯水,经均质机均质均匀,于超声仪中超声提取10 min,用约10 mL水少量多次转移至凯氏定氮仪配套的消解管中,加入5 mL 4 mol/L磷酸溶液,进行水蒸气蒸馏,接收冷凝后的蒸馏液,过膜,上机。
1.3.4 色谱条件
左泵系统:色谱柱:菲罗门Uranus C18(250 mm×4.6 mm,5 μm);柱温35 ℃;流动相:100% 1.5 g/L磷酸二氢铵溶液(用1 mol/L磷酸溶液调节pH值至3.0);流速1 mL/min;进样量10 μL;检测波长214 nm。
右泵系统:色谱柱:Agilent Eclipse XDB-C18(250 mm×4.6 mm,5 μm);柱温35 ℃;流动相:甲醇-水(60∶40,V/V);流速1 mL/min;在线衍生程序:取衍生液10 μL,样品溶液10 μL,充分混匀,反应4 min;检测波长355 nm。
1.4 图谱处理及数据分析
采用UltiMate 3000 DGLC双三元高效液相色谱仪的变色龙Chromeleon7色谱数据处理系统及Excel软件进行图谱分析及数据处理。
2 结果与分析
2.1 在线衍生条件选择
参考文献[24-27],在已有研究基础上,结合实际检测样品及仪器条件,对衍生液体积、衍生时间进行优化。
2.1.1 衍生液体积选择
分别取10 μL 10 mg/L甲醛标准溶液与5、10、20、30、40、50 μL衍生液进行在线衍生4 min,色谱图如图1所示,当衍生液的取样量为30、40、50 μL时,所得目标峰峰形逐渐变差,不利于准确定量,可能是由于衍生液过量造成色谱柱超载。衍生液体积为5、10、20 μL时,所得目标峰峰形良好。由于衍生液体积越大对色谱柱损伤越严重,因此,兼顾灵敏度及保护色谱柱的原则,选择衍生液的体积为10 μL。
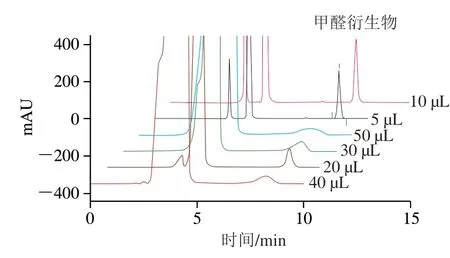
图1 不同衍生液体积所得甲醛衍生物色谱图Fig. 1 Chromatograms of formaldehyde derivatives with different volumes of derivatization agent
2.1.2 衍生反应时间的选择
设定衍生程序为:样液10 μL,衍生液10 μL,改变在线衍生时间1、2、3、4、5、6 min,连续进1 mg/L甲醛标准溶液6 针,测得相应峰面积值的平均值及相对标准偏差(relative standard deviation,RSD),结果如图2所示,就峰面积平均值而言,衍生时间由1 min增长时至2 min时,峰面积有所增加,2~5 min时,峰面积值基本稳定,这与吕春华等[26]的研究相符合;由峰面积的RSD可得,1~4 min时,随衍生时间的延长,峰面积的RSD逐渐减小,4、5、6 min峰面积的RSD改变不大,可能是随着衍生时间延长,反应趋于更加完全稳定,因此兼顾节约时间及保证稳定性的原则,衍生时间选择为4 min。
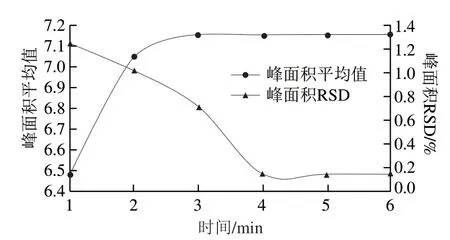
图2 不同衍生时间对应峰面积平均值及峰面积RSD(n=6)Fig. 2 Average peak area and RSD of peak area as a function of derivatization time (n = 6)
2.2 目标物馏出液体积确定
取空白鲫鱼试样10 g、双乙酸钠添加量1.0 g/kg、甲醛添加量0.05 g/kg,样品经磷酸酸化后经过水蒸气蒸馏,冷凝管冷却后,接收馏出液,每个馏出体积平行6 组实验,对不同馏出液体积对应的回收率进行考察,由图3可知,甲醛及双乙酸钠的回收率随馏出体积的增加而增大,馏出液体积为25 mL时,双乙酸钠及甲醛的平均回收率分别为20.6%(RSD=3.43%,n=6)和34.5%(RSD=4.14%,n=6);馏出液体积为50 mL时,双乙酸钠及甲醛的平均回收率分别为44.5%(RSD=3.21%,n=6)和54.3%(RSD=3.28%,n=6);馏出液体积为100 mL时,双乙酸钠及甲醛的平均回收率分别为75.5%(RSD=3.36%,n=6)和74.1%(RSD=2.44%,n=6);馏出液体积为200 mL时,双乙酸钠及甲醛的平均回收率分别为92.1%(RSD=2.16%,n=6)和82.8%(RSD=1.95%,n=6);馏出液体积为250 mL时,双乙酸钠及甲醛的平均回收率分别为99.0%(RSD=3.11%,n=6)和83.5%(RSD=1.91%,n=6);其中,馏出液体积由200 mL增加至250 mL时,甲醛回收率基本一致,双乙酸钠回收率由92.1%增加至99.0%,馏出时间延长约为1 min,兼顾双乙酸钠及甲醛的回收率,本实验馏出液体积为250 mL。

图3 不同馏出液体积对回收率的影响(n=6)Fig. 3 Effect of different distillate volumes on recoveries of formaldehyde and sodium diacetate (n = 6)
2.3 波长选择及色谱行为
分别取100 mg/L双乙酸钠标准溶液及10 mg/L甲醛标准溶液按1.3.4节色谱条件进样,所得色谱图如 图4所示。在190~400 nm波长处进行扫描,所得光谱见图5、6。由图5可得,双乙酸钠在200 nm左右有最大吸收,但200 nm左右的杂质吸收峰较多,而在214 nm处目标物也有较大吸收峰,同时杂质吸收峰较小,所以实验选择214 nm作为检测波长;甲醛在线衍生所得衍生物的光谱图(图6)表明甲醛衍生物在355 nm具有最大吸收,因此检测波长选定为355 nm。这与 GB/T 2116—2007《小麦粉与大米粉及其制品中甲醛次硫酸氢钠含量的测定》中,甲醛与2,4-二硝基苯肼衍生物的光谱图一致。
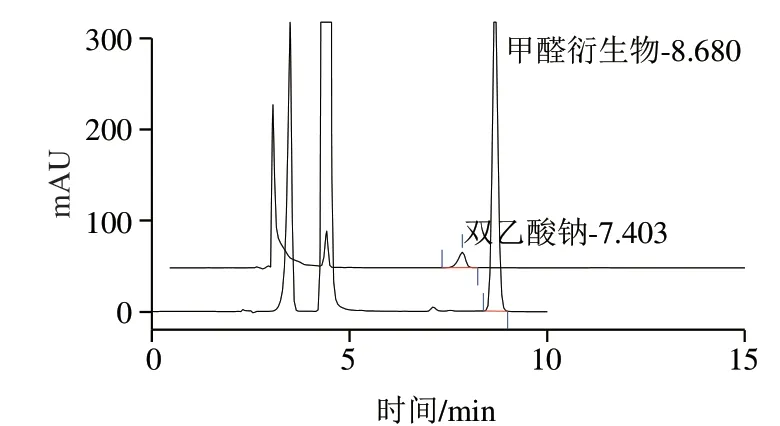
图4 双乙酸钠和甲醛标准溶液色谱图Fig. 4 Chromatograms of sodium diacetate and formaldehyde standard solutions
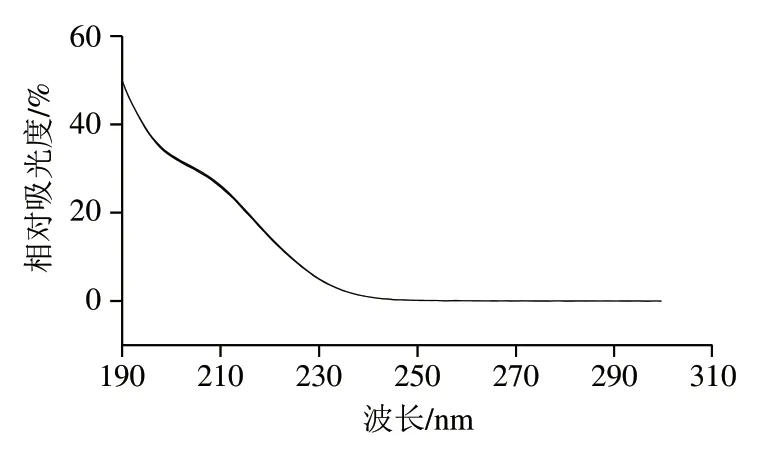
图5 双乙酸钠标准溶液光谱图Fig. 5 Ultraviolet absorption spectrum of sodium diacetate standard solution
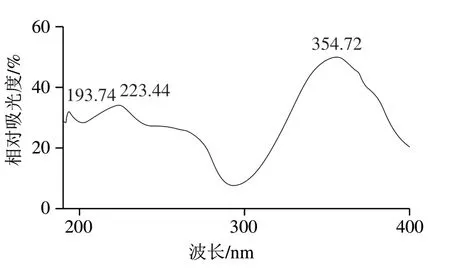
图6 甲醛标准溶液衍生后光谱图Fig. 6 Ultraviolet absorption spectrum of formaldehyde standard solution
2.4 标准曲线及检出限、定量限实验结果
按照1.3.2节配制的系列标准溶液,以待测组分的质量浓度为横坐标,以色谱峰面积为纵坐标, 绘制标准工作曲线,计算得到甲醛衍生物、双乙酸钠线性回归方程及相关系数分别为Y=5.660 3X+1.217 5(R2=0.999 9)、Y=0.180 9X+0.146 9(R2=0.999 7),甲醛在0.5~20.0 mg/L范围内线性关系良好,双乙酸钠在10~200 mg/L范围内线性关系良好。以3 倍性噪比对应的目标物质量浓度为检出限,折合到样品中,得甲醛及双乙酸钠的检出限分别为0.5、10 mg/kg。以10 倍性噪比对应的目标物质量浓度为定量限,折合到样品中,得甲醛及双乙酸钠的定量限分别为1.5、30 mg/kg。
2.5 方法回收率实验结果
按优化好的实验条件分别向鲫鱼及多宝鱼空白样品中加入低、中、高3个水平的甲醛及双乙酸钠标准溶液,根据董靓靓等[23]对40种水产样品中甲醛含量的调查结果,选定甲醛的添加量为10、20、50 mg/kg;由于目前GB 2760—2014中仅对熟制水产品中双乙酸钠的限量为1 000 mg/kg,暂根据此,选定双乙酸钠的添加量为200、500、1 000 mg/kg。每个质量浓度重复6 次平行,进行批内精密度实验及批间精密度实验,结果见表1、2。批内精密度实验中,甲醛回收率为81.4%~88.3%,RSD为1.73%~2.68%,双乙酸钠回收率为91.4%~102.9%,RSD为3.08%~4.16%;批间精密度实验中,甲醛回收率为80.6%~87.9%,RSD为2.07%~2.72%,双乙酸钠回收率为90.8%~105.1%,RSD为3.44%~4.64%,该方法回收率高、精密度好,可满足水产品中双乙酸钠及甲醛同时检测的要求。
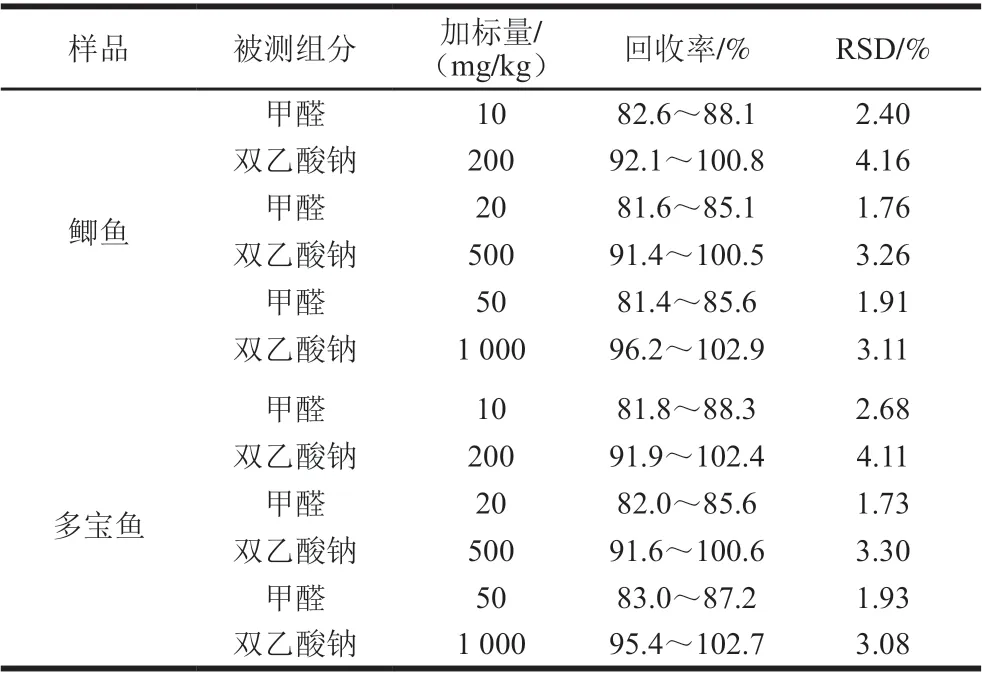
表1 甲醛、双乙酸钠回收率及RSD(n=6)(批内)Table 1 Recoveries and RSDs of formaldehyde and sodium diacetate for intrabatch repeability (n = 6)
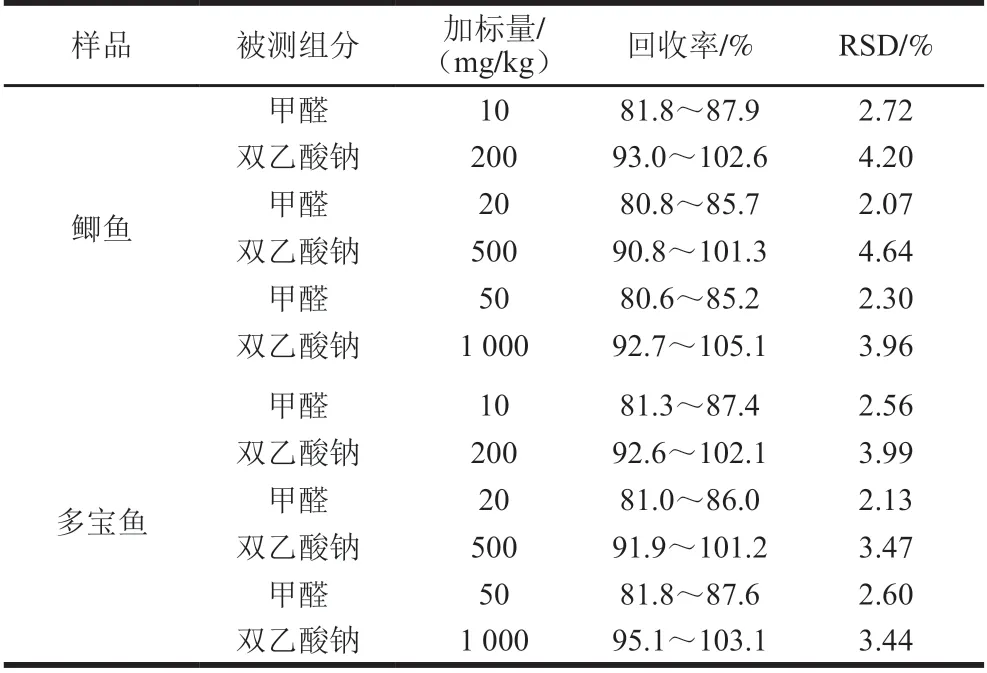
表2 甲醛、双乙酸钠回收率及RSD(n=6)(批间)Table 2 Recoveries and RSDs of formaldehyde and sodium diacetate for interbatch repeability (n = 6)
2.6 本方法与现有方法的比较
取2.5节中鲫鱼加标样品,其中甲醛添加量为 20 mg/kg,双乙酸钠添加量为500 mg/kg,分别依据本实验建立方法、SC/T 3025—2006、GB 5009.277—2016进行检测,重复6 次平行实验,所得数据见表3,由表3发现,就检测项目而言,本方法可同时检测水产品中甲醛及双乙酸钠含量,其余两方法只能完成一个项目的检测;就测得值而言,本方法中甲醛及双乙酸钠的回收率均高于另外两方法,更接近于理论值,可能是由于本方法采用凯氏定氮仪,空间更加密闭,空间体积更小,提高了蒸馏回收率,且本方法采用在线衍生程序,蒸馏提取后直接进高效液相色谱仪检测,减少了有机溶剂反萃取步骤,降低了过程损失;就检测时间而言,采用本方法25 min可以同时完成甲醛及双乙酸钠的检测,快速高效。分别采用SC/T 3025—2006、GB 5009.277—2016测定水产品中的甲醛及双乙酸钠时,仅单独检测一个样品中的双乙酸钠及甲醛需要150 min,且实验初需要搭建蒸馏装置,双乙酸钠的标准溶液也需经过蒸馏,平均到每个样品的时间远超150 min,不利于大批量样品检测,不能满足风险监测快速抽检的需要。

表3 本实验建立方法与现有方法对比Table 3 Comparison between DGLC and other methods
2.7 实际样品检测结果
结合本研究方法对66 批次水产品进行检测,结果发现,有5 批次水产品仅检测出双乙酸钠,分别为大黄鱼、带鱼、白果鱼、沼虾,检出结果范围为0.189~2.30 g/kg; 有7 批次水产品仅检测出甲醛,分别为石蟹、龙头鱼、带鱼、梅鱼,检出结果范围为3.24~78.4 mg/kg;有2 批次水产品同时检测出双乙酸钠和甲醛,结果见表4。 结合实际样品检测结果发现:1)水产品中双乙酸钠及甲醛的检出率分别为10.6%、13.6%,检出率较高;2)结合魏建华[28]、张璇[29]等的研究,龙头鱼中检出的甲醛含量低于报道中其平均天然本底含量,推测检出的甲醛可能是龙头鱼天然含有,还有可能是在贮存过程中自身产生,这就需要建立快速检测方法积累大量研究数据以判定是否为人为添加;3)水产品中双乙酸钠的检测以测定乙酸含量进行计算,水产品中乙酸本底值的调查研究目前鲜见报道,仍需要大量研究数据以建立及完善相关判定标准。大量研究数据的积累需要快速、稳定、可用于大通量检测的分析方法。
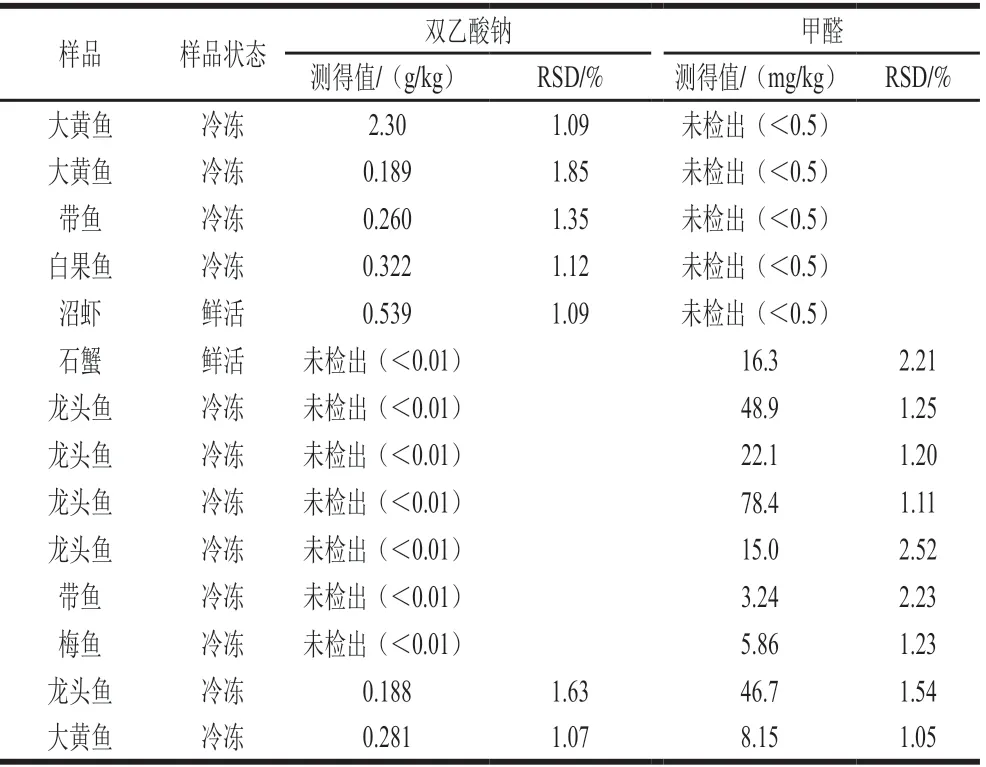
表4 阳性样品检出信息(n=3)Table 4 Results of detection of positive samples (n = 3)
3 结 论
本实验研究采用凯氏定氮蒸馏装置同时提取水产品中双乙酸钠、游离态及结合态甲醛的前处理方法,并对甲醛在线衍生方法进行优化,建立了采用双三元高效液相色谱同时检测水产品中甲醛及双乙酸钠的方法,缩短了检测时间,简化了操作步骤,减少了有机试剂的使用,自动化程度高,方法回收率较现有方法高,检出限较现有方法低,利于大批量水产品中甲醛及双乙酸钠的快速检测,为国家建立食品安全风险评估制度提供了基础技术参考。对66 批次水产品进行检测,发现了有检出样品,但仍旧无法进行判定,因此,建立可行的检测方法是基础,采用检测方法建立并逐步完善水产品中甲醛本底、乙酸本底含量数据库,为相关判定标准的建立积累基础数据,以利于监管部门监管,从而保障食品安全。

