超声波辅助龙虾壳制备谷氨酸螯合钙的工艺优化
朱继国,廖涛,熊光权,王炬光,白婵*,张庆芳*
(1.兰州理工大学 石油化工学院,兰州 730050;2.湖北省农业科学院农产品加工与核农技术研究所,武汉 430064)
近几年,随着小龙虾消费市场不断扩大,小龙虾养殖产量持续快速增长。2018年小龙虾总产量达163.87万吨[1],2019年小龙虾总产量高达190.6万吨。在工业中,加工后的整个虾中约有45%~60%变成副产品(头部和硬壳)[2],虾壳中主要含有甲壳质(15%~40%)、蛋白质(20%~40%)和碳酸钙(20%~40%)[3]。钙是人体不可或缺的营养素之一,涉及了大量的重要功能[4],钙的摄入量不足导致钙缺乏,会引起多种疾病。目前钙补充剂的种类繁多,其中氨基酸螯合钙因性质稳定,钙吸收率高于无机钙,易吸收,副作用小,同时还可以补充氨基酸,具有双重作用,被认为是较理想的钙补充剂。谷氨酸螯合钙是新型食品添加剂,安全性高,可以代替部分食盐,减少食盐摄入量,增加钙质摄入[5],增强食品口感,且钙的吸收效率是无机钙(CaCl2)的1.64倍。目前谷氨酸的制备主要是谷氨酸与贝壳、鸡蛋壳中和反应制备,而目前关于利用龙虾壳制备谷氨酸螯合钙的文章鲜有报道。因此,文章以虾壳中的钙为钙源,在超声波的辅助下,以钙螯合率为指标制备谷氨酸螯合钙,并用响应面法优化制备工艺,从而确定最佳的工艺条件,为废弃虾壳资源的再利用提供了新的思路。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
小龙虾:购于武汉悦活里超市;L-谷氨酸:北京鼎国昌盛生物技术有限责任公司;钙羧酸、乙二胺四乙酸二钠、柠檬酸钠、硫化钠、氢氧化钾、氢氧化钠、盐酸、硫酸、无水硫酸铜、硫酸镁、无水乙醇、石油醚、氯化镧、碘化钾、酒石酸钾钠等:国药集团化学试剂有限公司;硝酸和高氯酸:均为优级纯。
1.1.2 仪器与设备
ME303E电子分析天平 梅特勒-托利多国际贸易有限公司;消化炉、电热恒温干燥箱 上海一恒科学仪器有限公司;集热式恒温磁力搅拌器 郑州长城科工贸有限公司;SZF-06C脂肪测定仪 上海洪纪仪器设备有限公司;离心机;液晶超声波清洗器 昆山洁力美超声仪器有限公司;K9860全自动凯氏定氮仪 徐州淮博仪器设备有限公司。
1.2 方法
1.2.1 工艺流程
小龙虾→虾壳粉→加谷氨酸→超声处理→抽滤上清液→无水乙醇→离心→抽滤→干燥→成品。
1.2.2 虾壳粉的制备
将小龙虾除去全部肉质,虾壳用自来水反复清洗去除泥土及粘附的杂质,置于105 ℃鼓风干燥箱中烘干 24 h。将干燥好的虾壳先用破碎机粉碎30 s,再将粉碎后的虾壳粉用超微粉碎机粉碎20 min,然后收集分装密封备用。
1.2.3 虾壳营养成分分析
水分含量的测定:采用直接干燥法(GB 5009.3—2016)[6];灰分含量的测定:采用灼烧称重法(GB 5009.4—2016)[7];粗蛋白含量的测定:采用凯氏定氮法(GB 5009.5—2016)[8];粗脂肪含量的测定:采用索氏抽提法(GB 5009.6—2016)[9];钙含量的测定:采用原子吸收分光光度法(GB 5009.92—2016)[10]。
1.2.4 制备谷氨酸螯合钙的工艺流程
取1 g虾壳粉加入到50 mL的锥形瓶中,再加入一定量的蒸馏水,在搅拌下直接加入称量好的谷氨酸,然后将锥形瓶放入超声波清洗仪中,超声波处理一段时间后,取出锥形瓶放置水浴锅中水浴一段时间。
待反应结束后趁热抽滤收集滤液,由于谷氨酸螯合钙不溶于无水乙醇,将滤液与其等体积的无水乙醇混合进行沉淀,静置2 h后,通过高速离心过滤收集滤渣,并用无水乙醇多次洗涤滤渣,除去残余的谷氨酸及其他附着在其表面的残留物,将经过多次洗涤的滤渣置于 60 ℃的干燥箱内干燥6 h达到恒重即可得到谷氨酸螯合钙成品,然后测定谷氨酸螯合钙的螯合率。
1.2.5 钙含量的测定
利用原子吸收分光光度法测定谷氨酸螯合钙产品中的含钙量,谷氨酸螯合钙产品的螯合产率(X)计算公式如下:
式中:X为赖氨酸螯合钙产品的螯合产率(%);m0为虾壳粉中钙元素的总质量(mg);m1为螯合态钙元素的质量(mg) 。
1.3 单因素试验设计
1.3.1 摩尔比对螯合率的影响
虾壳粉1.0 g,摩尔比1∶1、2∶1、3∶1、4∶1、5∶1,料液比1∶20 (g/mL),超声时间20 min,反应温度55 ℃,超声功率100 W,螯合时间60 min,然后经乙醇沉淀、离心抽滤、洗脱干燥后制得谷氨酸螯合钙,测钙的螯合率。
1.3.2 料液比对螯合率的影响
虾壳粉1.0 g,摩尔比3∶1,料液比1∶15、1∶20、1∶25、1∶30、1∶35(g/mL),超声时间20 min,反应温度55 ℃,超声功率100 W,螯合时间60 min,然后经乙醇沉淀、离心抽滤、洗脱干燥后制得谷氨酸螯合钙,测钙的螯合率。
1.3.3 超声时间对螯合率的影响
虾壳粉1.0 g,摩尔比3∶1,料液比1∶30(g/mL),超声时间10,15,20,25,30 min,反应温度55 ℃,反应功率100 W,螯合时间60 min,然后经乙醇沉淀、离心抽滤、洗脱干燥后制得谷氨酸螯合钙,测钙的螯合率。
学生是教学活动的主人公,因此,混合式学习要重视学生的主体地位,采用多种方式调动学生学习积极性。学生是多元化的,潜能也是无限的,为了最大化地锻炼学生,激发学生的潜能,作为教师,可以在课堂上创新教学方法,可以经常在班会上创设英语诵读大赛、书写大赛、情景模拟等等,进行实际应用的比拼,激发学生的潜能,培养高职院校学生的兴趣爱好。“通过搭建各种各样的平台,学生学习成果得到展示,可以提升学生的自信心。此外可以利用多媒体作为学生成功的展示台,学生可以在平台中一次次展现着自己的特长,一次次提升着自我的能力。不断完善学生管理工作。最后,把混合式教学与实践教学进行结合,通过设置学分促使混合式教学不断完善。
1.3.4 反应温度对螯合率的影响
虾壳粉1.0 g,摩尔比3∶1,料液比1∶30(g/mL),超声时间25 min,反应温度35,45,55,65,75 ℃,超声功率100 W,螯合时间60 min,然后经乙醇沉淀、离心抽滤、洗脱干燥后制得谷氨酸螯合钙,测钙的螯合率。
1.3.5 超声功率对螯合率的影响
虾壳粉1.0 g,摩尔比3∶1,料液比1∶30(g/mL),超声时间25 min,反应温度65 ℃,超声功率60,70,80,90,100 W,螯合时间60 min,然后经乙醇沉淀、离心抽滤、洗脱干燥后制得谷氨酸螯合钙,测钙的螯合率。
1.4 响应面试验设计
在单因素试验结果的基础上,筛选出较合适的反应条件,为验证各反应条件的准确性,选择摩尔比(A)、料液比(B)、超声时间(C)、反应温度(D)为响应因素,以谷氨酸螯合钙的螯合率为响应值,得出最佳工艺参数。设计四因素三水平试验,见表1。
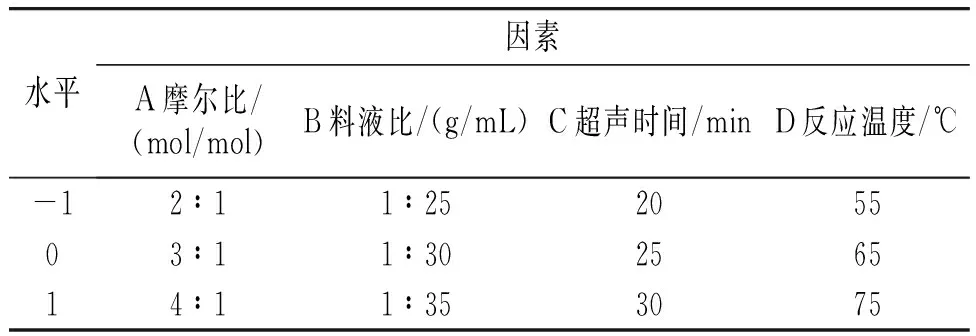
表1 谷氨酸螯合钙响应面试验因素与水平Table 1 Response surface test factors and levels of glutamate calcium chelate
1.5 数据统计分析
试验数据采用 SPSS 25.0软件进行方差分析,采用Origin 2018软件绘图,采用Design-Expert V8.0.6软件进行响应面分析。
2 结果与分析
2.1 虾壳的基本成分
小龙虾虾壳的基本成分见表2。

表2 小龙虾壳的基本组成成分(以干重计)Table 2 The basic components of lobster shells (calculated by dry weight)
由表2可知,虾壳中粗甲壳素的含量最高,为28%,其次为钙元素含量19.304%,粗蛋白的含量为14.48%,水分的含量为7.69%,粗脂肪的含量为0.2%。虾壳中的钙主要以碳酸钙的形式存在,是天然的优质钙源,目前虾壳中钙的提取方法主要有高温煅烧法、直接中和法和发酵法,将虾壳中的无机钙转化成有机钙,魏颖等[11]采用乳酸提取法从克氏原螯虾虾壳中提取乳酸钙,从10 g虾壳粉中提取钙762.48 mg。
2.2 谷氨酸螯合钙制备工艺条件的单因素试验
2.2.1 谷氨酸与虾壳粉中钙的不同摩尔比对钙螯合率的影响
由图1可知,谷氨酸螯合钙的螯合率随着谷氨酸与虾壳中碳酸钙的摩尔比的增加而升高,摩尔比在1∶1~3∶1的过程中,螯合率显著增加,当继续增加摩尔比时,螯合率有所增加,但是变化不明显。这是因为谷氨酸与碳酸钙反应生成谷氨酸螯合钙的理论摩尔比为2∶1[12],当反应体系中的摩尔比比理论摩尔比高时,将有利于促进钙离子的螯合,但当谷氨酸螯合钙已经达到了一种平衡状态后,继续增加摩尔比,对促进钙离子的螯合率的影响并不大,而且谷氨酸的利用率降低,造成资源浪费。所以,当谷氨酸与碳酸钙的摩尔比为3∶1时较为合理,可以获得理想的螯合率。
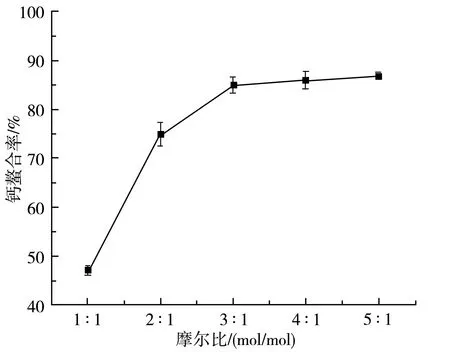
图1 摩尔比对钙的螯合率的影响Fig.1 Effect of molar ratios on the chelation rates of calcium
2.2.2 料液比对钙螯合率的影响
由图2可知,钙的螯合率随着料液比的变化先升高后降低,当料液比为1∶30时,钙的螯合率最高,为87.25%,可能是当料液比较小时,会导致产物谷氨酸螯合钙的浓度太大,使反应体系溶液易达到饱和,不利于反应向生成谷氨酸螯合钙的方向进行[13],因此随着料液比增大,钙的螯合率升高;但当料液比太大时,即反应物稀释过大,分子间的有效碰撞减小,阻碍了螯合反应的进行,所以钙的螯合率降低。因此,最佳的料液比为1∶30,可以获得理想的螯合率。
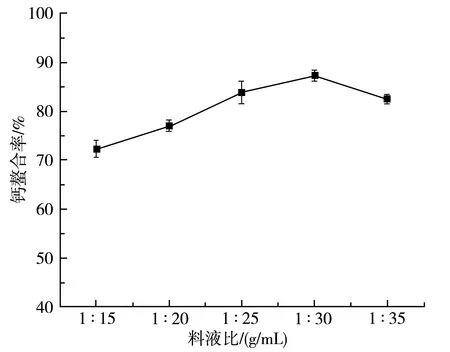
图2 料液比对钙的螯合率的影响Fig.2 Effect of the solid-liquid ratios on the chelation rate of calcium
2.2.3 超声时间对钙螯合率的影响
由图3可知,当超声时间少于25 min时,钙的螯合率随着超声时间的增加而升高,当超声时间超过25 min后,螯合率降低,在超声时间为25 min时螯合率最高,为89.78%。超声时间对谷氨酸螯合钙的影响具有两面性,超声处理可促进物料与溶剂间的接触,提高反应体系中分子的碰撞频率,从而加速反应过程,但超声处理时间过长会破坏产物晶体的生成,或改变产品的物理性质[14]。因此,最佳的超声时间为25 min。
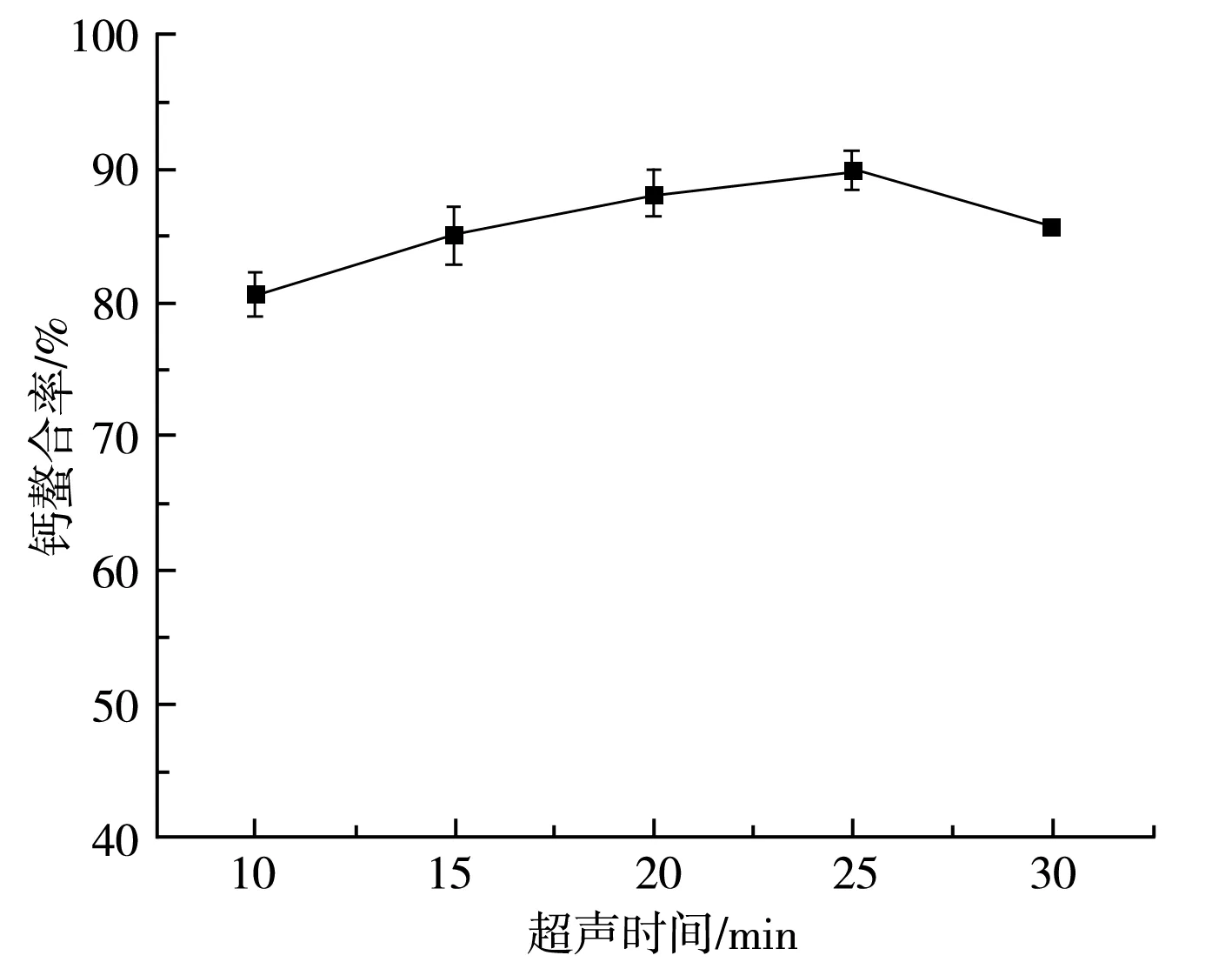
图3 超声时间对钙的螯合率的影响Fig.3 Effect of ultrasonic time on the chelation rate of calcium
2.2.4 温度对钙螯合率的影响
由图4可知,随着温度的增高,螯合率逐渐升高,当温度为65 ℃时螯合率最高,为90.58%。当温度继续增高时,螯合率降低,当温度为75 ℃,螯合率为81.58%,比温度为65 ℃时的螯合率减少了9%。随着温度的上升,分子运动加剧,加大了分子间的碰撞几率,加快了反应速率,产品的螯合产率自然会随之升高[15]。在温度较高时,螯合物在高温条件下会发生一定程度的分解,导致螯合率下降。因此,最佳的反应温度为65 ℃。
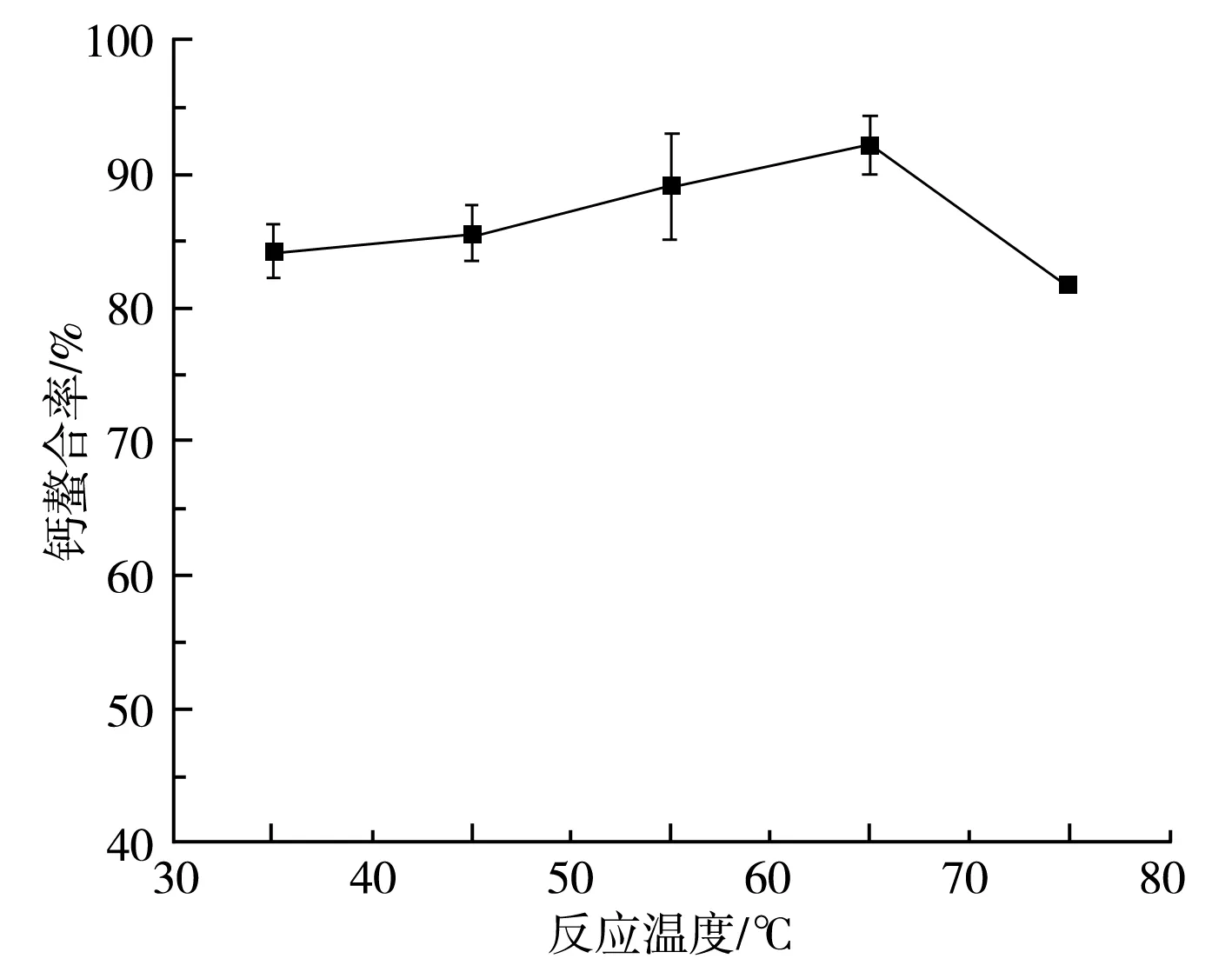
图4 反应温度对钙的螯合率的影响Fig.4 Effect of reaction temperature on the chelation rate of calcium
2.2.5 超声功率对钙螯合率的影响
超声波的空穴作用有助于晶核的形成,加快晶体的生长速率,提高反应速率,缩短反应时间[16]。由图5可知,随着超声功率的增加,钙的螯合率逐渐升高,当超声功率为100 W时钙的螯合率最高,为90.90%。梁春娜等[17]在采用超声波法从鸡蛋壳中制备醋酸钙工艺研究中,所得最佳工艺中超声波功率为100 W。超声功率过大,强烈空化作用产生的能量会破坏晶体的生成和增大,只有功率达到一定范围时,才有强化成核或强化结晶作用。因此,最佳的超声功率为100 W。
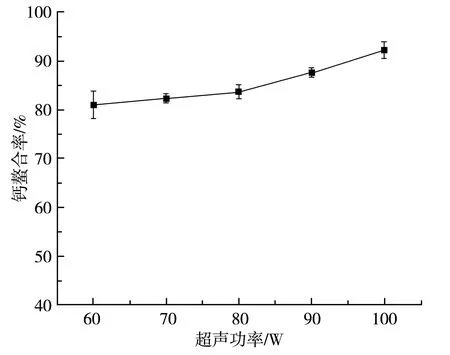
图5 超声功率对钙的螯合率的影响Fig.5 Effect of ultrasonic power on the chelation rate of calcium
2.3 谷氨酸螯合钙制备的响应面试验
根据单因素试验结果,固定超声功率为100 W,反应时间为60 min,以摩尔比(A)、料液比(B)、超声时间(C)、反应温度(D)为试验因素,以谷氨酸螯合钙的螯合率为响应值,由Design-Expert V8.0.6软件设计出的试验方案及结果见表3。
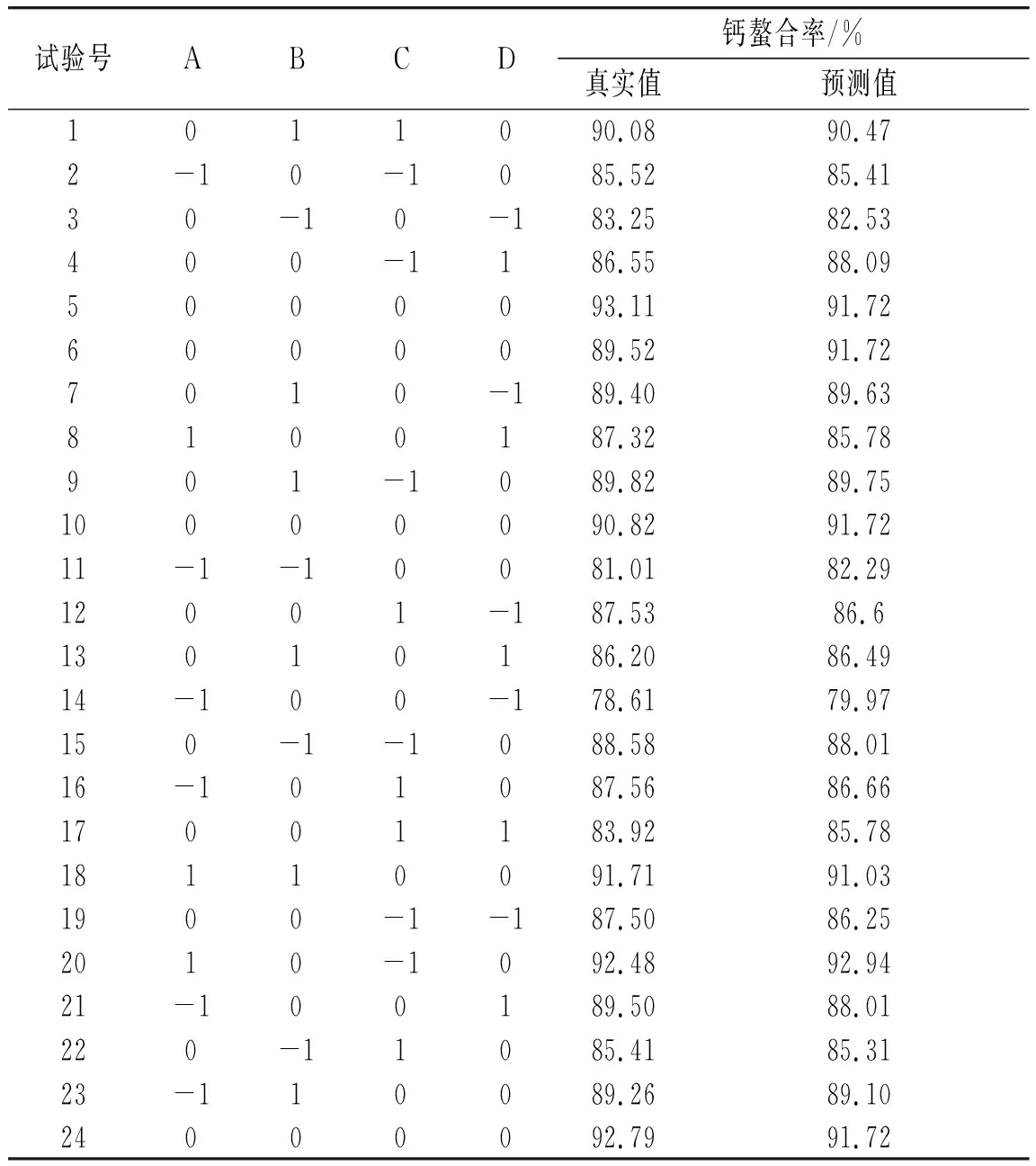
表3 响应面设计试验及结果Table 3 Response surface design test and results
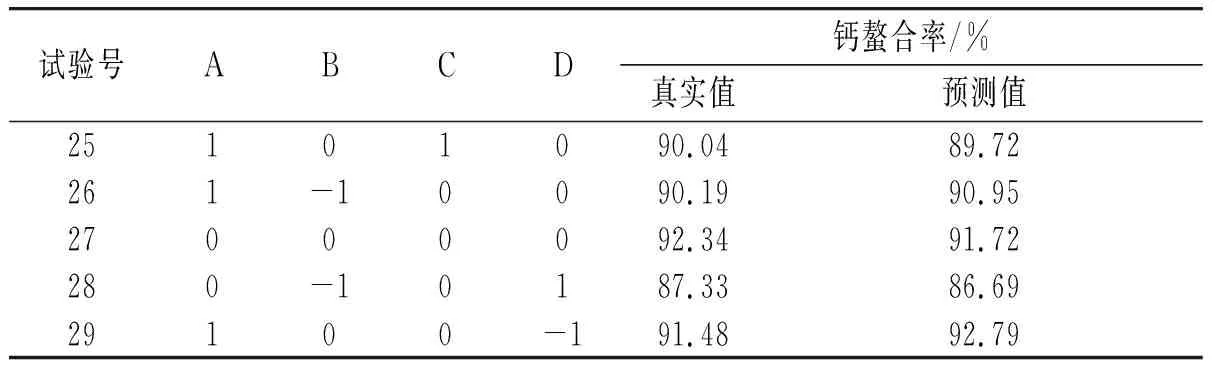
续 表
通过表3的试验数据,采用 Design-Expert V8.0.6软件进行拟合,得谷氨酸螯合钙的螯合率对摩尔比(A)、料液比(B)、超声时间(C)、反应温度(D)的二次多项回归模型方程:钙螯合率=91.72+2.65A+1.73B-0.49C+0.25D-1.68AB-1.12AC-3.76AD+0.85BC-1.82BD-0.66CD-1.53A2-1.84B2-1.49C2-3.54D2。
由表4可知,模型的F=10.03,P<0.0001,表明回归模型极显著;本试验失拟误差 P=0.5687>0.05,失拟检验是一种用来判断回归模型是否可以接受的检验,说明该模型与试验拟合误差不显著,拟合度较好,数据较准确,该模型可以使用;本试验相关系数R2=0.9093,说明有90.93%的数据可以用此方程解释;变异系数C.V.=1.68%,C.V.表示试验的精确度,值越小,试验的可靠性越高,模型越精确,重现性很好[18]。综上所述,该模型的拟合度较好,能充分反映出各试验因素与螯合率之间的关系,可以用该模型对钙的螯合率进行分析和预测。
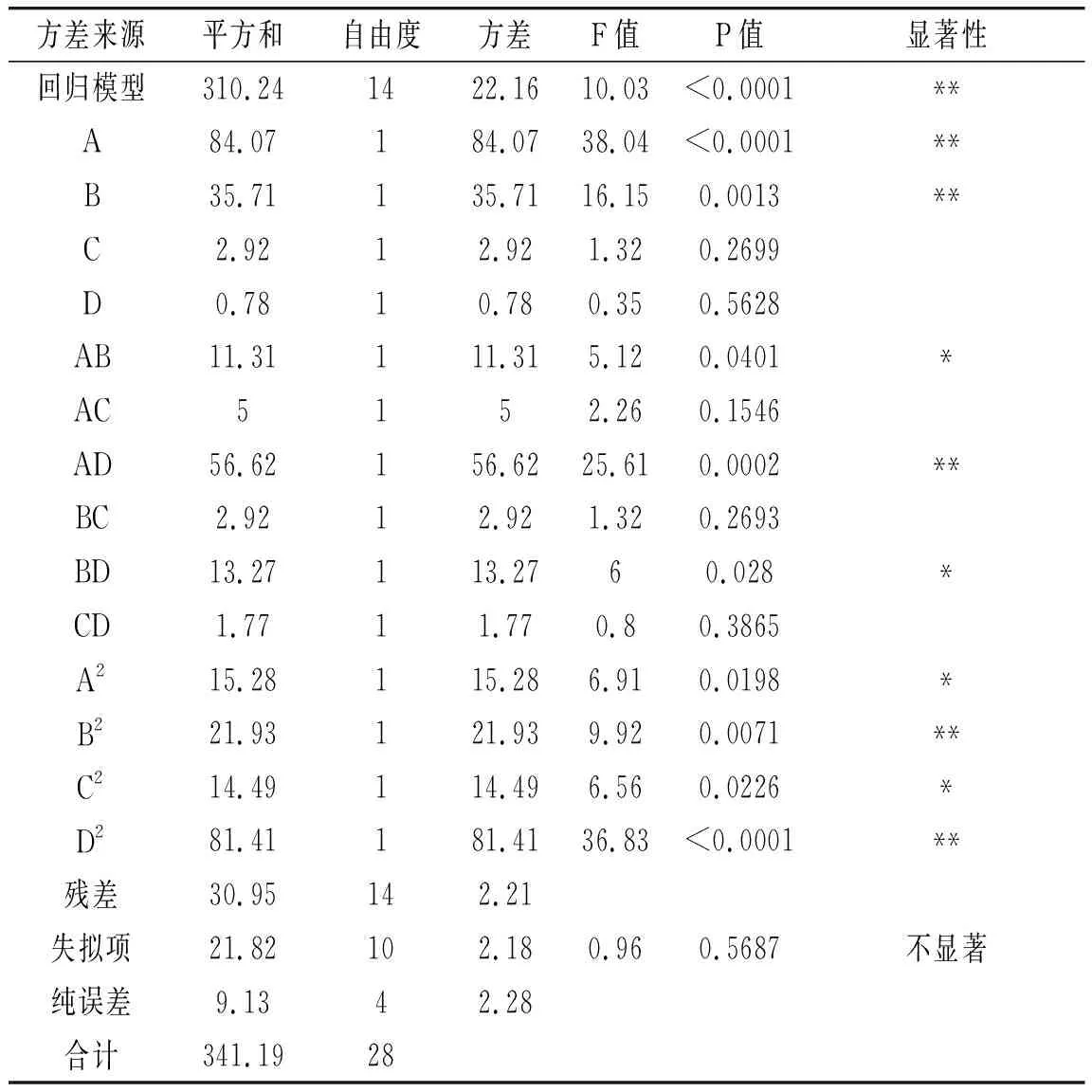
表4 回归模型方差分析Table 4 Analysis of variance of regression model
回归模型中一次项A和B、交互项AD及二次项B2和D2的P值均小于0.01,对钙螯合率的影响极显著,交互项AB和BD及二次项A2和C2的P值均小于0.05,对钙螯合率的影响显著(P<0.05)。通过比较各因素的 F值大小可判定各因素的主次关系,F值越大,则该因素对试验结果的影响越大[19],因此各因素对钙螯合率的影响主次为A>B>C>D,即摩尔比>料液比>超声时间>反应温度。
2.3.1 响应面结果分析
响应曲面分析法优化图形为响应值与对应的因素间构成的三维图及在二维平面上的等高线图,综合直观地反映各因素对响应值的影响,每个响应面对其中两个因素进行分析,其他试验因素固定在零水平上。响应面坡度越陡,表明该响应值试验因素的变化越敏感,该试验因素对响应值的影响越大;反之则表明该试验因素对响应值的影响越小[20];等高线呈圆形表示两因素交互作用不显著,而呈椭圆形或马鞍形则表示两因素交互作用显著[21]。由图6可知,摩尔比和反应温度、摩尔比和料液比及料液比和反应温度对谷氨酸螯合钙螯合率的交互作用显著,与上述方差分析的结果一致。
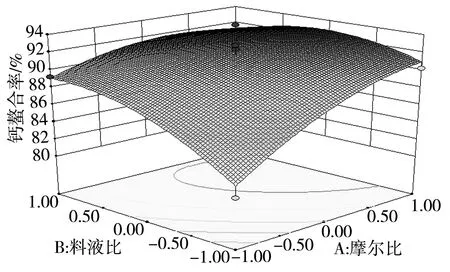
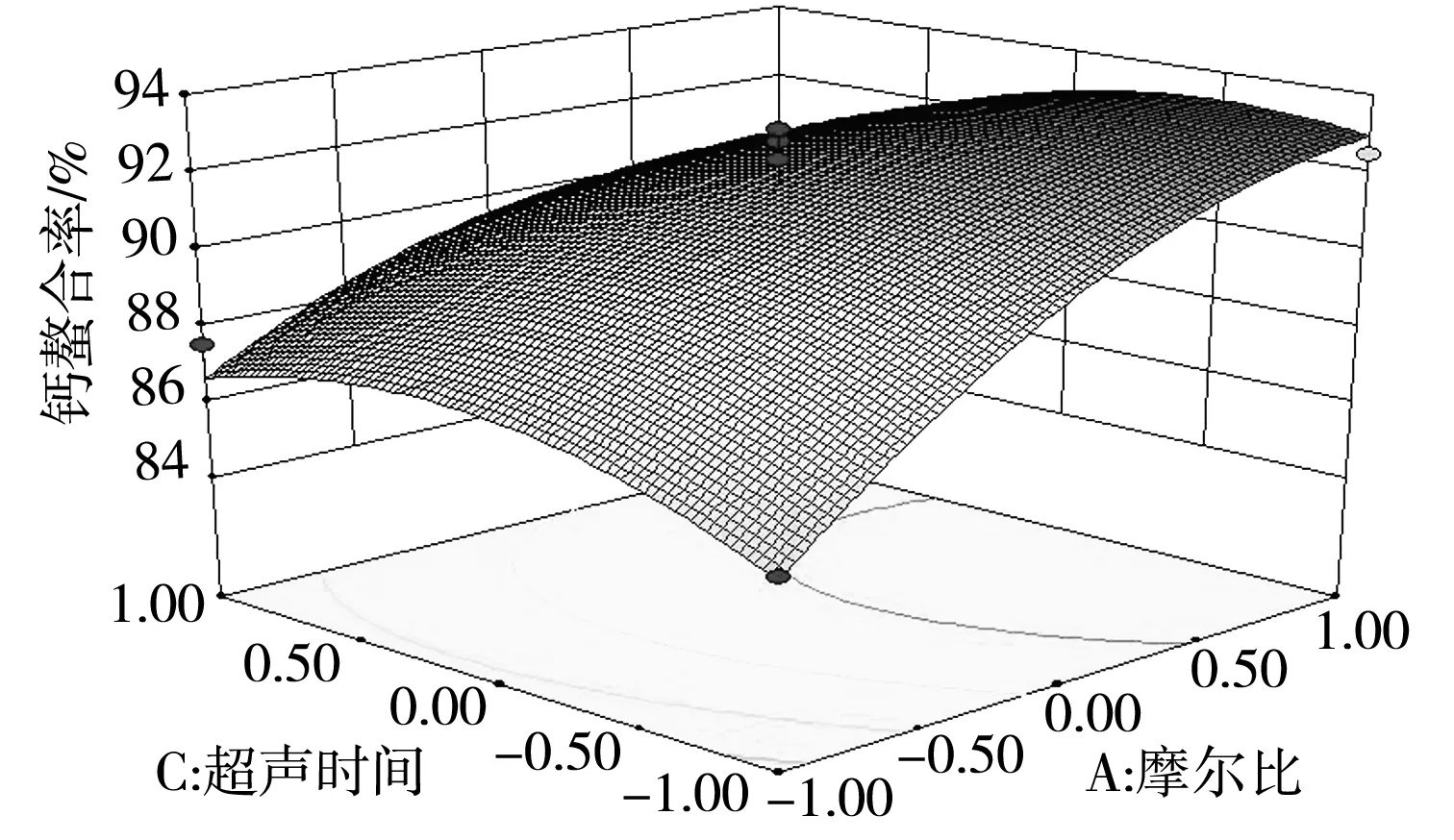
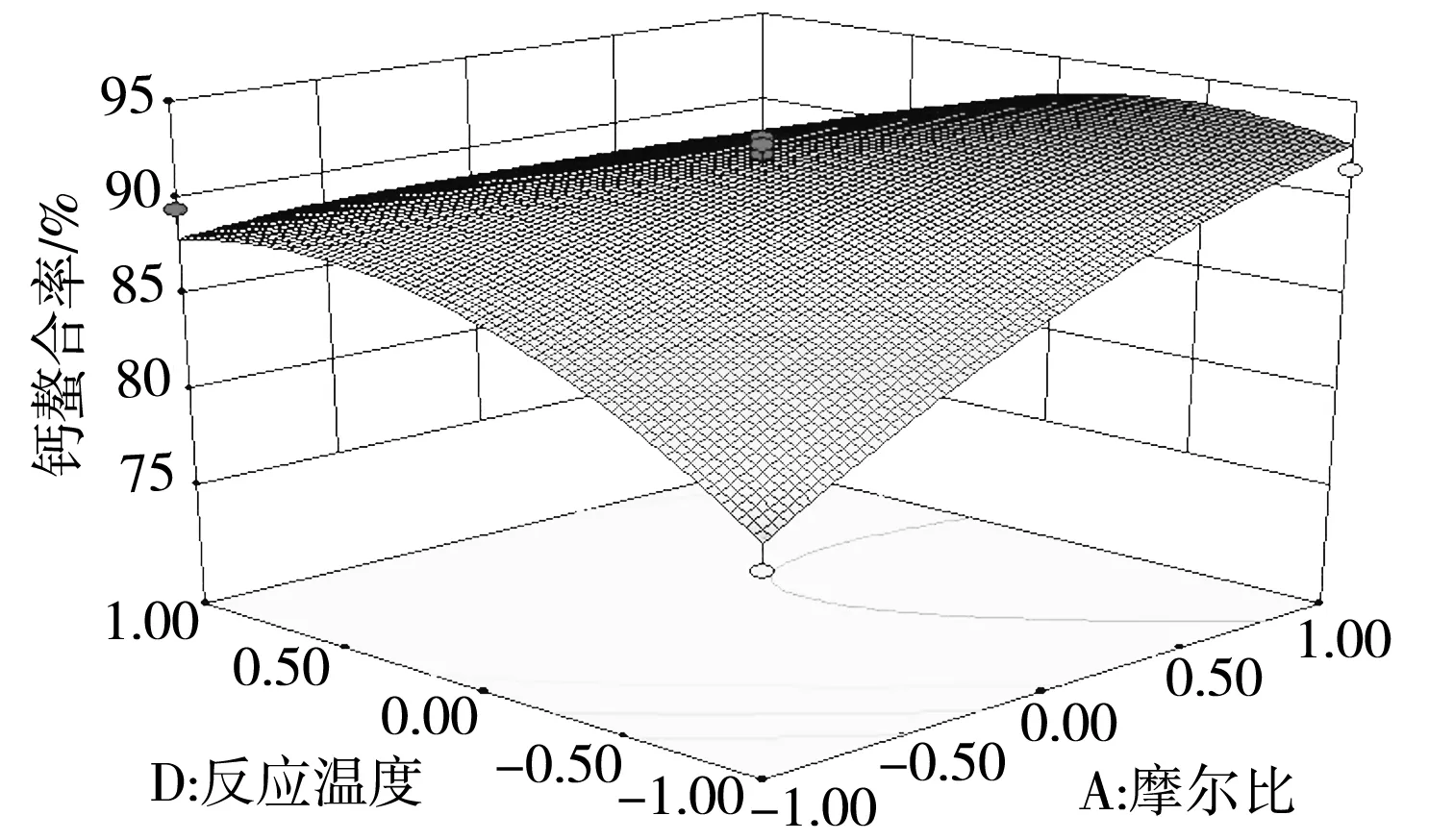
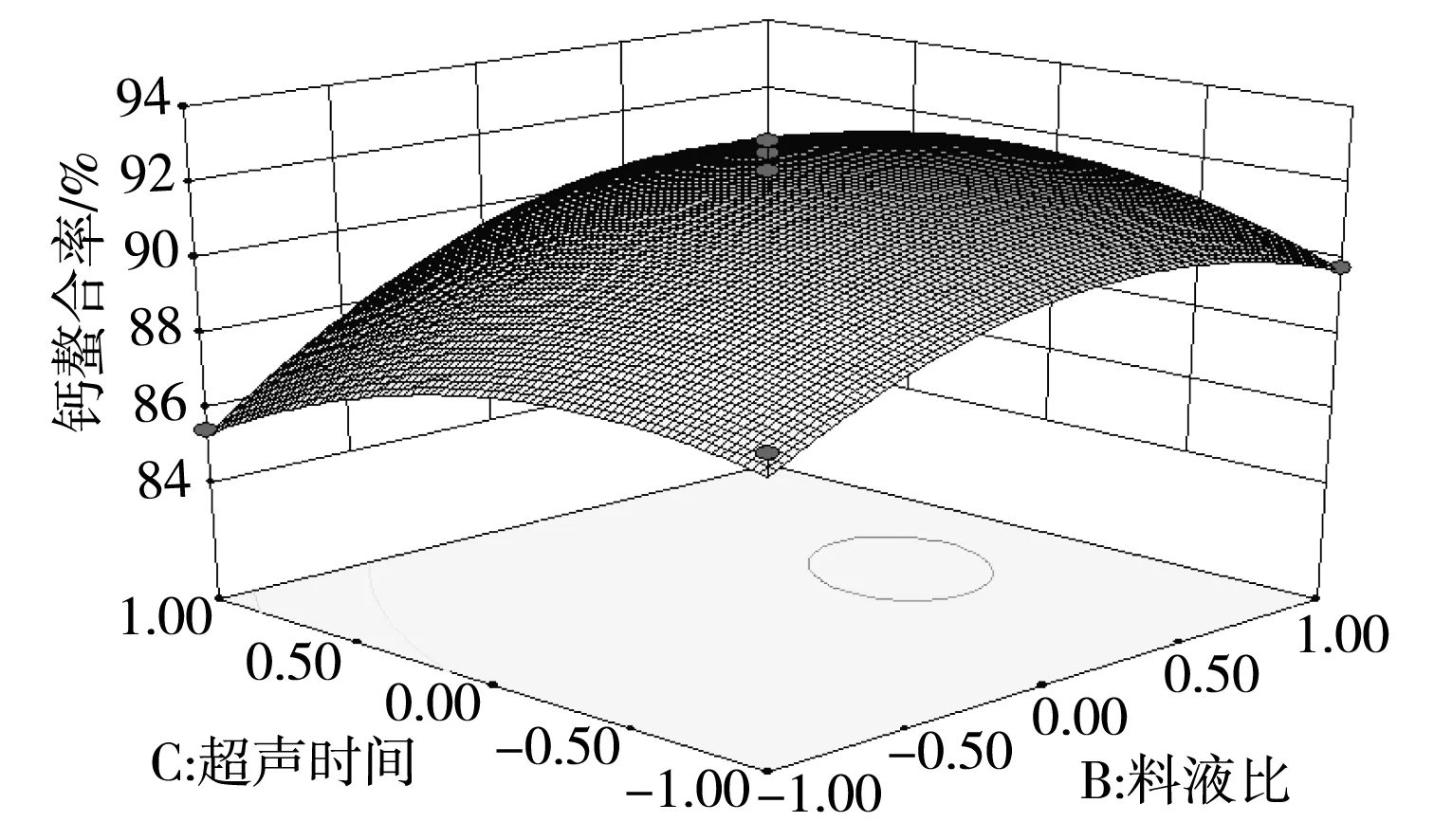
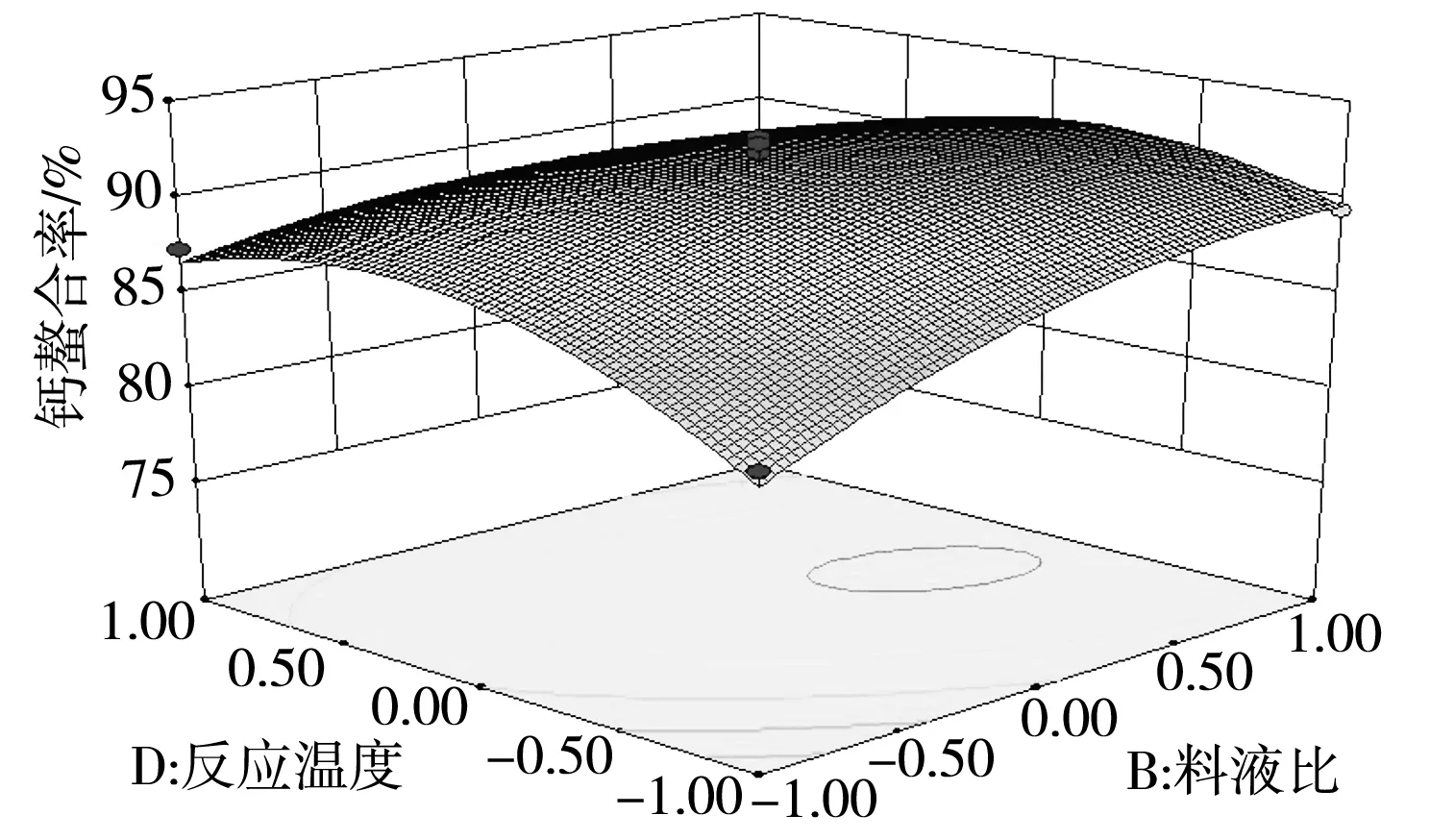

图6 试验因素交互作用对钙螯合率的影响Fig.6 Effect of interaction of test factors on the chelation rate of calcium
2.3.2 响应面结果及验证
通过回归模型的预测,谷氨酸螯合钙理论的最佳制备工艺条件为摩尔比4∶1、料液比1∶30.85、超声时间23.25 min、反应温度59.9 ℃,此条件下谷氨酸螯合钙的螯合率为94.02%。考虑实际操作的局限性,工艺最终修正为摩尔比4∶1、料液比1∶31、超声时间23 min、反应温度60 ℃。在此条件下进行验证,并与取消超声辅助步骤(反应23 min)试验组进行对比,每组平行测定3次。测得谷氨酸螯合钙的螯合产率为93.68%,与预测值94.02%接近,说明该模型与实际情况的拟合度较好,该模型能较好地预测实际谷氨酸螯合钙的螯合率。取消超声辅助步骤试验组的谷氨酸螯合钙的螯合率76.15%,比超声辅助组少17.53%。
3 结论
根据单因素试验结果,利用Design-Expert V8.0.6软件进行响应面分析,各因素的效应关系为摩尔比>料液比>超声时间>反应温度,摩尔比和反应温度的交互作用对谷氨酸螯合钙的螯合产率影响最为明显;其最优制备工艺为摩尔比4∶1、料液比1∶31、超声时间23 min、反应温度60 ℃,在此条件下,谷氨酸螯合钙的螯合产率为93.68%,且比取消超声辅助步骤试验组高17.53%,因此超声波辅助制备工艺可显著提升虾壳谷氨酸螯合钙的螯合率。本试验以小龙虾副产物虾壳和谷氨酸为原料,在超声波的辅助下制备谷氨酸螯合钙,为综合利用我国丰富的虾壳资源提供了参考。

