糖尿病视网膜病变患者扩张型毛细血管的发生率、眼底影像学特征及其影响因素△
张 怡 姚 静 王建明 庾 苗 郭 晓 周爱意
糖尿病视网膜病变(DR)是导致糖尿病患者视力下降的首要原因[1]。微血管瘤是DR最常见的病理表现[2-3]。近年来,扩张型毛细血管逐渐被人们认识,它是一类较微血管瘤更大的糖尿病相关眼底血管异常[4]。扩张型毛细血管可由毛细血管、动脉、静脉或侧支血管局部薄弱的血管壁内皮细胞增殖发育而来。它不易被荧光素眼底血管造影(FFA)检出,而易被吲哚菁绿血管造影(ICGA)检出[4]。目前,关于扩张型毛细血管的研究较少,其在DR患者中的发生率也未被详细报道。研究发现,针对扩张型毛细血管的激光光凝治疗能改善糖尿病性黄斑水肿(DME)患者的解剖学表现和视力,对顽固性DME亦有效[5-6]。本研究探讨DR患者扩张型毛细血管的发生率、眼底影像学特征及其影响因素,希望能加深人们对扩张型毛细血管的认识。
1 资料与方法
1.1 一般资料选取2020年5月至2021年5月就诊于西安交通大学第二附属医院眼科并确诊为DR的患者147例230眼。其中,合并DME者65眼,不合并DME者165眼。2型糖尿病诊断标准:既往诊断为2型糖尿病者或者非同日3次空腹静脉血糖>7.0 mmol·L-1且随机血糖>11.1 mmol·L-1的首诊患者。DR诊断标准:(1)诊断为2型糖尿病;(2)符合国际眼科协会发布的DR诊断标准[7],眼底检查视网膜有典型的微血管瘤、渗出、出血、静脉串珠样改变及视网膜内微血管异常,FFA显示片状无灌注区,或发生增生性玻璃体视网膜病变。
1.2 患者纳入和排除标准纳入标准:(1)符合DR诊断标准;(2)年龄20~80岁;(3)眼底结构清晰者。排除标准:(1)出现明显的屈光介质混浊影响检查者;(2)眼压异常者;(3)患有其他严重心脑血管疾病影响研究者;(4)合并其他严重眼部疾病者。本研究通过了西安交通大学第二附属医院医学伦理委员会的审查(批件号:2021185),研究过程遵循《赫尔辛基宣言》的要求。
1.3 检查方法受检患者使用复方托吡卡胺滴眼液充分散瞳,先拍摄眼底彩照及OCT图像。荧光素钠过敏试验反应为阴性后行FFA和ICGA同步眼底血管造影,选择 FFA+ICGA 同步模式,将 100 g·L-1荧光素钠5 mL及12.5 g·L-1吲哚菁绿2 mL混合液通过肘前静脉快速推注入患者体内并开始计时,拍摄时间大于30 min,造影后将图片储存,供分析使用。ICGA 3 min内的影像定义为早期像;3~10 min为中期像;10 min后为晚期像。
1.4 观察指标观察患者的ICGA图像,判定是否存在扩张型毛细血管。其中扩张型毛细血管在ICGA图像中的表现为:于ICGA中期开始出现并逐渐增强,晚期持续存在且与背景荧光形成强对比度的高荧光点(直径≥150 cm)[4]。观察扩张型毛细血管在ICGA检查中的特征,包括扩张型毛细血管的大小、最早显影时间以及形态学表现。观察OCT图像中是否存在DME并记录其类型,包括浆液性视网膜脱离(SRD)型、囊样黄斑水肿(CME)型、弥漫性视网膜增厚(DRT)型及混合型,以及扩张型毛细血管对应部位的OCT特征。统计DR患眼中、合并或不合并DME的DR患眼中以及不同类型DME患眼中扩张型毛细血管的发生率,并总结扩张型毛细血管的眼底影像学特征。
为研究扩张型毛细血管与硬性渗出的关系,观察患者眼底彩照中硬性渗出的分级,其中0级为后极部没有明显的硬性渗出,1级为细小点状的硬性渗出,2级为聚集成片的大颗粒硬性渗出,3级为聚集成环形或近中心凹的大量硬性渗出。统计并比较不同级别硬性渗出患眼中扩张型毛细血管的发生率。为研究扩张型毛细血管与血糖指标的关系,收集研究对象生物化学检查中血糖相关指标,包括空腹血糖、糖化白蛋白、血清白蛋白、糖化血清白蛋白含量,对比有扩张型毛细血管眼患者和无扩张型毛细血管眼患者血糖相关指标数据。
1.5 统计学方法采用 SPSS 23.0统计学软件进行统计分析。计量资料采用均数±标准差表示 ,计数资料以率(%)表示。计量资料若符合正态分布,则采用单因素方差分析,不符合正态分布,则采用Kruskal-WalisH检验。两组间率的比较采用χ2检验。检验水准:α=0.05。
2 结果
2.1 DR患者扩张型毛细血管的发生率本研究230眼DR患眼中扩张型毛细血管的发生率为39.6%。在合并DME的DR患眼(65眼)中扩张型毛细血管的发生率为53.8%,而在未合并DME的DR患眼(165眼)中发生率为33.9%;合并DME的DR患眼的发生率高于未合并DME的DR患眼,差异有统计学意义(χ2=7.728,P=0.005)。
合并DME的DR患眼中SRD型12眼,CME型25眼,DRT型7眼,混合型20眼,在合并不同类型DME的DR患眼中扩张型毛细血管的发生率分别为58.3%、44.0%、14.3%、70.0%。其中,合并混合型DME的DR患眼中扩张型毛细血管的发生率最高(P=0.038)。
2.2 扩张型毛细血管的眼底影像学特征本研究中,DR患眼扩张型毛细血管的直径为150~450 μm。在ICGA检查中,扩张型毛细血管开始显影时间为3 min 57 s~7 min 31 s,平均开始显影时间为4 min 58 s,之后染色逐渐增强呈现高荧光,持续至10 min后仍不衰退,并与晚期低背景荧光形成强烈对比。图1所示为1例典型扩张型毛细血管的眼底影像学表现。
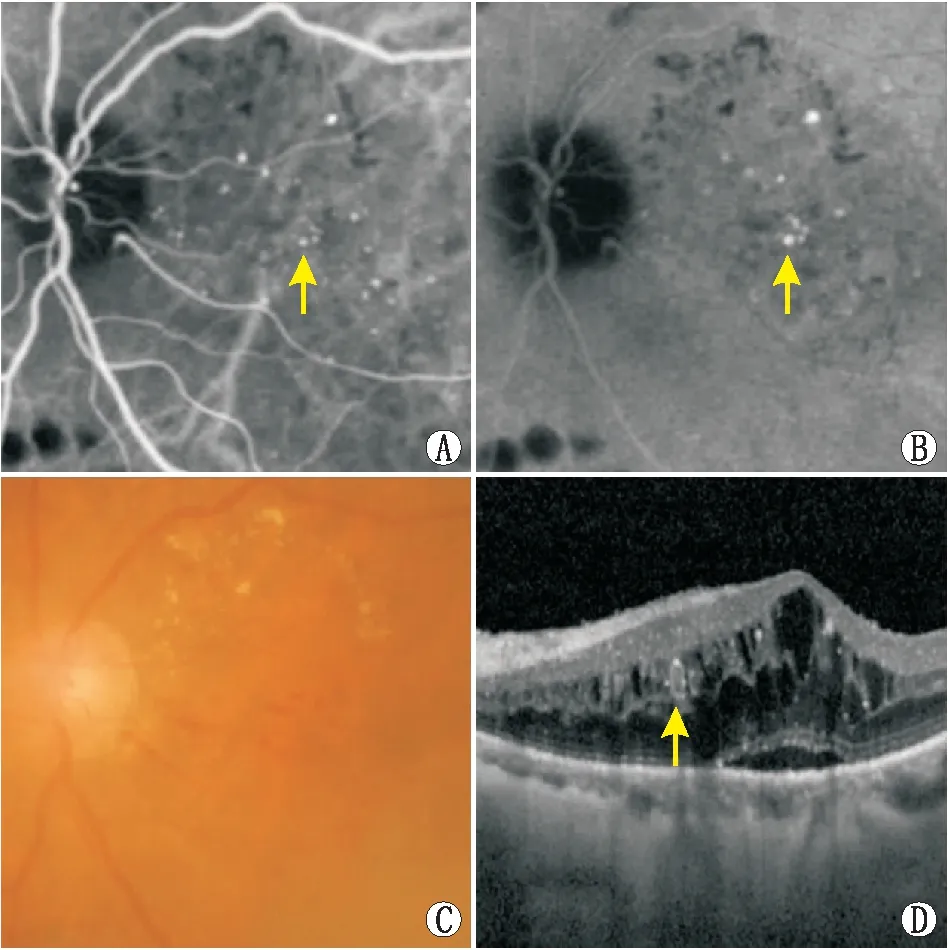
图1 1例典型扩张型毛细血管的眼底影像学特征 A:ICGA计时3 min 45 s扩张型毛细血管开始显影(黄色箭头);B:ICGA计时12 min 46 s扩张型毛细血管体积更大,亮度更高,与背景荧光的对比度更强(黄色箭头);C:眼底彩照可见扩张型毛细血管所在部位周围为聚集成近环形的硬性渗出(3级硬性渗出);D:扩张型毛细血管对应部位的OCT图像,该DR患眼合并混合型DME,扩张型毛细血管在OCT图像中的表现为视网膜层间具有高反射管壁的类圆形管腔,腔内为欠均匀的中高反射物质(黄色箭头)。
通过对91眼扩张型毛细血管的ICGA形态学特征的观察,可将其分为两种类型:(1)孤立的圆形扩张型毛细血管(图2),表现为单独存在的圆形高荧光点,直径通常为200~450 μm,此型较常见,占72.5%;(2)簇状扩张型毛细血管(图3),表现为聚集在一起的高荧光点,直径通常为150~200 μm,此型占27.5%。
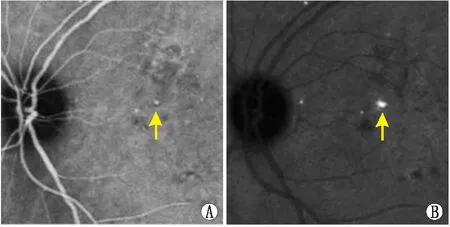
图2 1例孤立的圆形扩张型毛细血管 A:ICGA计时4 min 29 s扩张型毛细血管开始显影,呈孤立的圆形(黄色箭头);B: ICGA计时15 min 16 s扩张型毛细血管体积更大,亮度更高,与背景荧光的对比度更强(黄色箭头)。
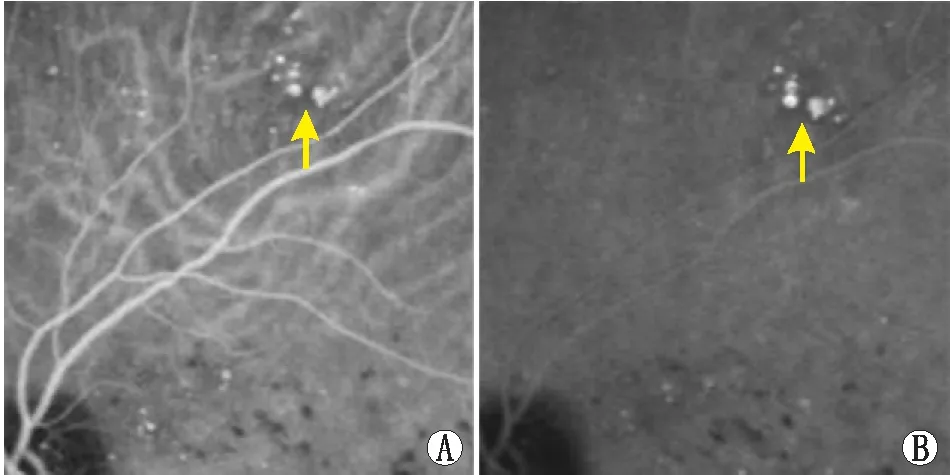
图3 1例簇状扩张型毛细血管 A:ICGA计时3 min 57 s扩张型毛细血管开始显影,若干个扩张型毛细血管呈簇状聚集在一起(黄色箭头);B:ICGA计时13 min 5 s扩张型毛细血管体积更大,亮度更高,与背景荧光的对比度更强(黄色箭头)。
2.3 扩张型毛细血管的影响因素
2.3.1 扩张型毛细血管与硬性渗出的关系在230眼DR患眼中,不同硬性渗出分级的患眼分别为:0级121眼,1级59眼,2级36眼,3级14眼;其中,同时存在扩张型毛细血管的眼数分别为:0级31眼、1级25眼、2级22眼、3级13眼。硬性渗出越严重,出现扩张型毛细血管的可能性越大(线性关联值为32.754,P<0.001)。
2.3.2 扩张型毛细血管的发生与血糖指标的关系与无扩张型毛细血管眼相比,有扩张型毛细血管眼患者的糖化血清白蛋白、糖化白蛋白含量更高,差异均有统计学意义(均为P<0.05)。两组患者空腹血糖、血清白蛋白含量差异均无统计学意义(均为P>0.05)(表1)。
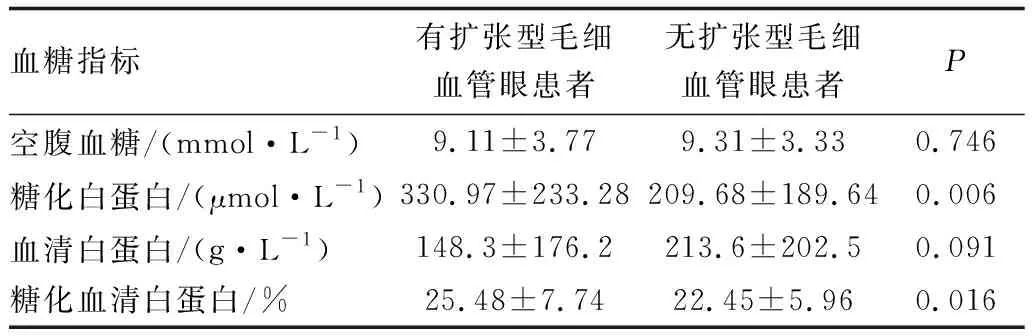
表1 扩张型毛细血管的发生与血糖指标的关系
3 讨论
对DR的治疗目前仍无特别有效的方法,全视网膜激光光凝术会导致患者视野缩小,视敏度下降;玻璃体内注射抗VEGF药物对有些患者效果较差;玻璃体切割术会造成较大的创伤且疗效有限。近年来,有研究报道针对扩张型毛细血管的眼底激光光凝对合并DME的DR患者有较好疗效[5-6]。因此,提高眼科医师对扩张型毛细血管的认知很有必要。
本次我们对230眼DR患眼研究发现,扩张型毛细血管的发生率高达39.6%;在合并DME的DR患眼中,扩张型毛细血管的发生率更是高达53.8%。DME是引起DR患者视力下降的最常见原因[8],扩张型毛细血管可能通过促进视网膜血管壁的功能破坏而导致局部渗漏增加。但是,并不是所有扩张型毛细血管都伴发黄斑水肿[9],这可能与扩张型毛细血管所在的位置、大小及黄斑区其他细胞的调节等多方面因素有关。本次我们还发现,合并不同类型DME的DR患眼中扩张型毛细血管的发生率不同,由高到低分别为混合型、SRD型、CME型、DRT型。既往研究表明,不同类型DME的发病机制有所差异。SRD型主要是由于血-视网膜外屏障的破坏所导致,与视网膜色素上皮功能受损密切相关;而DRT型和CME型主要是由血-视网膜内屏障破坏而引起[10-12]。本研究中混合型主要表现为SRD和CME同时存在,即血-视网膜内、外屏障的损害同时发生。我们推测,在这种情况下,血管壁受损越严重,局部血管内皮细胞异常增殖和迁移的概率也就越高,故混合型DME中扩张型毛细血管更为常见。
本研究还总结了扩张型毛细血管在ICGA的特征性表现:扩张型毛细血管一般在ICGA 计时3 min后开始出现并增大,之后其染色逐渐增强并呈现高荧光,持续至10 min后仍不衰退,并与造影晚期逐渐降低的背景荧光形成强烈对比。此外,我们在OCT图像上还发现,扩张型毛细血管对应部位往往有管壁明晰的类圆形管腔,腔内常填充不均匀的中高反射物质,这与既往文献报道的扩张型毛细血管的OCT图像特征相一致[2]。腔内物质可能为脂质、蛋白、微血栓等,它们均与吲哚菁绿具有较强的亲和力[13]。同时,由于吲哚菁绿还能染色管腔壁的纤维蛋白原[14],从而形成管腔的晚期着色,进而有可能造成扩张型毛细血管延迟性染色的特点。
为了加深对扩张型毛细血管的认知,我们又进一步探讨了扩张型毛细血管可能的影响因素,发现扩张型毛细血管与硬性渗出关系密切,硬性渗出程度越重,越容易出现扩张型毛细血管,提示严重硬性渗出是扩张型毛细血管相关的一个筛检特征。这不难理解,硬性渗出的出现往往提示血-视网膜屏障遭受较严重的破坏,使得脂蛋白等大分子物质从血管中漏出[15],硬性渗出处及邻近组织缺血缺氧,从而促进了扩张型毛细血管的形成。另外,我们还分析了扩张型毛细血管与血糖指标的关系,发现有扩张型毛细血管眼患者较无扩张型毛细血管眼患者的糖化血清白蛋白、糖化白蛋白更高,由于这两者均是反映糖尿病患者近2~3周血糖控制水平的指标[16-19],故该研究结果提示,长期血糖控制不良的糖尿病患者可能更容易发生扩张型毛细血管。
综上所述,本研究发现,扩张型毛细血管在DR患眼中的发生率较高,尤其是合并DME的DR患眼。其中,合并混合型DME患眼中扩张型毛细血管的发生率最高;扩张型毛细血管依其在ICGA中的形态学表现可分为孤立的圆形扩张型毛细血管和簇状扩张型毛细血管两种类型;严重的硬性渗出和较差的血糖控制水平与扩张型毛细血管的发生可能具有一定关系。

