人工智能在房颤管理中的应用进展
李小荣 杨兵
经过60多年的发展,人工智能正迅速发展,并深刻改变着传统医疗体系的诊治模式。房颤是临床最常见的心律失常之一,随着人口老龄化加剧,其患病率逐年升高。近期北京安贞医院牵头的一项全国大型社区调查研究显示,在我国成年人(≥45岁)中,房颤发病率约1.8%,估测近800万人罹患房颤[1]。本文以房颤为切入点,深入阐述人工智能在房颤管理中的应用进展。
1 人工智能概述
1956年,美国计算机科学家John McCarthy首次提出了人工智能的术语和原理[2]。人工智能是指应用计算机科学的理论与方法,使机器模仿人类利用知识完成一定行为的计算模拟过程[3],目前实现人工智能的技术手段主要有机器学习和深度学习。机器学习是人工智能的重要组成部分,是计算机基于算法,从大量数据中学习训练获得经验,形成某种模型,并利用模型预测结果的方法[4]。而深度学习是机器学习的一种特殊形式,它是让机器能够像人脑神经网络一样实现对数据的深度挖掘和解释的方法[4],其代表算法之一为卷积神经网络(convolutional neural network,CNN)。深度学习的主要优势在于以下几方面:①数据依赖,即只要拥有充足的数据就可进行学习研究,且随着数据规模的增大,深度学习的性能也不断增强;②特征处理,即深度学习能自动从数据中直接获取特征,而机器学习中应用的特征多需专家确定,其算法性能依赖于所确定特征的准确度。当然,因为深度学习需进行大量运算,所以更依赖于GPU等高端硬件;深度学习算法中涉及的参数很多,需要消耗更长的时间。人工智能医疗的技术流程见图1。

图1 人工智能医疗的技术流程
2 人工智能在房颤诊治管理中的应用
人工智能在房颤诊治管理中的应用,可以归纳为房颤诊断、预测、治疗支持、预后预测等。见图2。
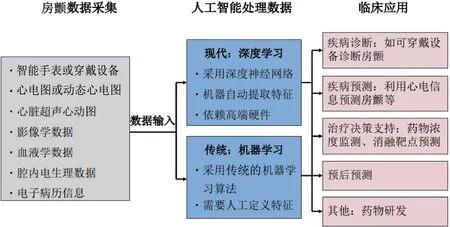
图2 人工智能在房颤管理中的应用
2.1 房颤诊断
心电信息采集简单、数据量极大,所以,心电检测也成为人工智能在心血管领域应用的主要阵地。随着移动设备、可穿戴传感器和软件应用程序的大规模应用,人们可以通过心电检测发现包括房颤在内的各类心律失常。基于深度学习的心电人工智能,可以准确掌握心电图自身的特点和充分理解专家判读心电图的思考过程,将人类百年来积累的心电知识和机器的数据学习能力进行有机结合,建立一套诊断能力达到临床医生平均水平的心电诊断系统,其操作方便、价格相对低廉,且能对心电数据进行实时分析。HANNUN等[5]使用人工智能-深度神经网络对来自53 877例患者的91 232条单导联动态心电图记录的大型临床数据集进行心律分类,结果发现人工智能-心电图(artifical intelligenceenabled ECG,AI-ECG)可以诊断出包括房颤、心房扑动、房室阻滞、交界性心律在内的12种心律,其ROC曲线下面积AUC值平均达0.97,F1平均得分(阳性预测值和敏感性的平均值)高于心脏病专家诊断时F1的平均值(0.837vs.0.780)。我国GUO等[6]利用基于光电容积脉搏波描记法(photoplethysmographic,PPG)的mHealth技术开展房颤筛查研究(HUAWEI Heart Study),结果显示,在应用华为智能手环或手表的187 912例用户中,筛查出424例(0.23%)“疑似”房颤患者,其中,262例接受了远程管理团队和医生的随访后,最终227例确诊为房颤,其阳性预测值可达91.6%。
2.2 房颤预测
2.2.1 基于心电图的房颤预测 阵发性房颤的诊断依赖于房颤发作时的心电图,而人工智能技术可以根据阵发性房颤患者平素未发作时获得的窦性心律心电图,识别出房颤高危个体。《世界心脏联盟房颤路线图(2020年更新版)》指出,除常规心电检查外,还可以利用现代人工智能技术,根据现有的临床标本、样本或数据(包括心电图数据)有效预测房颤[7]。ATTIA等[8]纳入了自1993年12月31日至2017年7月21日美国梅奥诊所心电图室180 922例患者的649 931份窦性心律心电图,根据窦性心律的P波预测房颤,用深度学习算法构建和优化房颤预测模型,结果显示该模型在单次人工智能窦性心律下心电图预测房颤的AUC值为0.87,敏感性为79%,特异性为79.5%。BAEK等[9]开发的递归神经网络深度学习算法,通过学习房颤未发作时标准12导联窦性心律心电图的细微差异来预测房颤,结果显示AI-ECG上QRS波群出现前的0.24 s内是检测阵发性房颤细微变化的最佳时间窗。人工智能算法还可仅利用窦性心律心电图预测人群未来是否会发生房颤,而无须其他临床数据支持。CHRISTOPOULOS等[10]使用AI-ECG计算梅奥诊所临床研究老年人群中房颤的发生率,该人群在基线访视时无房颤病史,共有1 936例参与者被纳入分析,平均75.8岁;基线检查时AI-ECG房颤模型输出>0.5的参与者,2、10年的房颤累积发生率分别为21.5%、52.2%。因此,AI-ECG作为一种低成本的筛查手段,可以根据窦性心律心电图识别阵发性房颤和预测房颤易发患者。
2.2.2 基于照片或视频的房颤预测 古有扁鹊通过“望色、听声”即可得知蔡桓公的疾病状态,而今借助先进的人工智能技术,不需要病史或查体,也能“看脸识病”。香港中文大学YAN等[11]的研究纳入20例永久性房颤患者[平均(76.6±7.6)岁,男12例(60%)]和24例窦性心律对照组人群[平均(56.8±20.2)岁,男14例(58.3%)],通过使用一台数码摄像机以视频方式记录患者面部表情,分析无身体接触的面部PPG信号,经过训练的深度CNN可据此检测出患者是否有房颤,其与心电图之间的一致性良好(95.9%),总敏感性为93.8%(95%CI88.9%~96.6%),特异性为98.1%(95%CI94.6%~99.4%)。
2.3 房颤风险评估
脑卒中是房颤的主要并发症,目前指南推荐以CHA2DS2-VASc评分作为房颤患者脑卒中风险分层的依据,以确定是否需要启动抗凝治疗。该评分系统基于简单的临床变量,易于临床推广,但其仅考虑人口学特征、病史和共存疾病的因素,模型过于简单,不能反映房颤血栓栓塞的复杂发病机制,以及房颤患者中其他关键的表型特征,如房颤的类型和负荷、电生理特征、左心房纤维化程度、左心耳的解剖和功能、循环生物因素(心肌标志物、炎症、促凝因子)和心电图特征(如P波振幅、持续时间、轴),而上述都是脑卒中风险增加的重要因素。HAN等[12]建立人工智能模型后纳入3 114例非脑卒中房颤患者作为对照组,将其与71例脑卒中房颤患者进行验证,验证数据集中的CNN模型表现最好(AUC=0.702),而CHA2DS2-VASc的AUC<0.5。因此对房颤患者可以使用同时纳入结构化和非结构化数据的人工智能模型自动进行脑卒中风险评估,以识别高危患者并及时启动抗凝治疗[13]。
2.4 房颤治疗辅助支持
2.4.1 药物浓度监测和预测 抗心律失常药物有致心律失常风险,因此监测其血药浓度至关重要。ATTIA等[14]从42例(男、女各21例)接受多非利特或安慰剂治疗的健康受试者中获得连续心电图和血药浓度,开发了一种深度学习算法以评估体表心电图(QTc)形态学变化与多非利特血浆浓度的关系;结果显示,QTc的线性模型与多非利特血浆药物浓度之间有很好的相关性(r=0.64)。CHANG等[15]的研究纳入了61例地高辛中毒患者和177 066例急诊患者的心电图,结果显示人工智能在验证队列和人机竞争中的AUC值分别为0.912和0.929,敏感性和特异性分别达到84.6%和94.6%。更有趣的是,仅使用Ⅰ导联的人工智能系统(AUC=0.960)并不比使用完整12导联(AUC=0.912)的差。因此,基于心电图的人工智能可用于预测血浆多非利特、地高辛等房颤治疗药物的浓度,从而经济、快速、方便地监测临床抗心律失常药物的浓度。
2.4.2 导管消融的决策支持 肺静脉电隔离是目前房颤消融治疗的基石,但非肺静脉触发灶在部分患者中也起着重要的作用。台北荣民总医院LIU等[16]回顾性分析了521例经导管消融治疗的阵发性房颤患者,其中358例未复发患者(单纯肺静脉触发者298例,占83.2%;非肺静脉触发者±肺静脉触发者60例,占16.8%)的肺静脉CT成像(PV-CT)数据被用来进行深度学习,并创建非肺静脉触发灶的预测模型,结果显示人工智能模型预测非肺静脉触发的准确率为(82.4±2.0)%,敏感性为(64.3±5.4)%,特异性为(88.4±1.9)%。利用消融前PV-CT的深度学习模型可在消融前识别非肺静脉触发患者,并预测阵发性房颤导管消融的触发灶。ZOLOTAREV等[17]的研究亦发现,与传统标测相比,基于傅里叶谱特征预训练的机器学习模型,可以有效地将人离体心脏的心房电图分类为房颤驱动或非驱动灶,从而提高房颤患者靶向消融的准确性。房颤消融时,构建精准的左心房模型至关重要,基于模型的FAM(m-FAM)是CARTO系统开发的一个新模块,其将机器学习技术应用于左心房重建。SCHWARTZ等[18]的研究显示,无论使用何种导管进行标测,m-FAM模块均可快速、精确地重建左心房和肺静脉解剖结构,从而安全地指导房颤消融。
2.4.3 综合管理 心电图和动态心电图是既往最常用的监测房颤复发的工具,但是报告的及时性、家庭普及性均不高。目前,基于人工智能的移动设备用于心电监测有望规模化应用于术后随访,更早地检出复发房颤,有利于房颤的长期综合管理。顾赛男等[19]研究显示,非瓣膜性房颤患者消融治疗后利用“大拇指”心电监测仪进行监测,人工智能算法诊断房颤的敏感性和特异性分别为96.5%和99.6%。HUAWEI Heart Study对应用移动医疗技术的干预组(1 646例)和常规治疗组(1 678例)的临床结局进行比较和分析,其中干预组通过管理平台接受医生的管理;随访12个月后,与对照组相比,干预组的缺血性脑卒中或全身血栓栓塞、死亡和再住院的主要复合终点发生率更低(6.0%vs.1.9%),住院率也更低(4.5%vs.1.2%)[20]。由此可见,移动健康技术可用于改善房颤筛查和优化综合护理。
2.5 房颤预后判断
2.5.1 房颤消融后再住院预测 由于再发房颤、心房扑动和手术并发症等原因,接受导管消融治疗的房颤患者30 d再入院率约10%[21]。HUNG等[22]研究分析了2013年美国全国房颤患者再入院数据库的数据,利用K-近邻、决策树、支持向量机等多种机器学习算法建立预测模型,探讨了再入院的危险因素;结果发现,预测患者30 d再入院最重要的变量是年龄、出院总次数以及患者病历记录中的疾病数目等;在所使用的机器学习算法中,K-近邻算法预测准确率最高,达85%。
2.5.2 主要心血管不良事件预测 GOTO等[23]利用GARFIELD-AF登记的数据开发了一种新的人工智能模型,用于预测房颤患者的临床结局;研究发现,接受维生素K拮抗剂治疗的新诊断房颤患者30 d内至少进行3次凝血酶原时间测量,该人工智能模型通过捕捉连续凝血酶原时间测量中的重要信息,预测患者一年内大出血、脑卒中或全身性栓塞和全因死亡的c统计量分别为0.75、0.70和0.61,对主要出血的预测准确率最高。
3 人工智能应用于医疗领域存在的问题
人工智能在医疗领域的研究与临床应用均处于起步阶段,虽然前景广阔,但在发展过程中仍面临着一些困难和争议[24]。
3.1 质量控制问题
首先,当前人工智能在医学领域中的应用研究大多数是非随机、非前瞻性的,存在高偏差风险[25]。其次,虽然大数据可以增强机器学习模型的性能,但当使用深度学习卷积模型时,非线性数据转换和多重卷积导致数据内部处理过程很难追踪,而输入数据的哪些方面对模型输出的影响最大也难以判断。从某种意义上说,深度学习算法的处理过程就是一个“黑匣子”。因此,深度学习算法的可解释性是当前的一个重要研究领域[13]。
3.2 伦理学问题
基于人工智能的可穿戴设备是电子消费品,价格较高,在不同收入、年龄人群中的接受程度都存在差异。此外,人工智能的参与会不会产生假阳性结果,带来过度诊断与过度治疗,甚至导致伤害尚属未知。尤其值得注意的是,目前多数人工智能研发机构属于私人公司,这类公司如果存储有大量敏感的医疗数据和个人信息,是否会引发道德和法律问题[26]?如果基于人工智能的医疗应用被犯罪分子利用,则可能会导致巨大灾难。
3.3 结果推广问题
首先,人工智能医疗基于算法和既往的大量数据,依据数据的局部特征进行识别,其对个体的整体属性、罕见病或未见过的场景则无法识别。其次,许多研究基于单中心、回顾性的临床数据,模型的泛化能力较差。再次,人工智能模型对数据质量的高要求,也限制了其预测的准确性和在基层的可推广性。
3.4 弱化医护地位问题
人工智能医疗的快速发展,一定程度上可以减轻医护工作负担,帮助医护管理患者,与此同时,可能会弱化医护专业的地位。但鉴于医学科学的复杂性和人们对疾病认识的局限性,人工智能完全取代医护专业人员的工作是不可能的。
4 小结
利用人工智能,基于计算机算法可以优化诊断过程、提高决策能力,有望彻底改变传统的医疗诊治模式。从房颤管理角度出发,人工智能可以通过可穿戴设备、远程心电网络平台筛查出房颤患者;通过心电图、超声心动图、影像学及血液学检查的特征预测房颤,并辅助临床医生预测消融靶点、制定消融方案,甚至开展机器人主导下的消融;在药物治疗过程中,可以利用人工智能监测抗心律失常药物的血药浓度;随访期间,基于人工智能的辅助系统有助于预测主要心血管不良事件;人工智能甚至可以预测治疗复杂房颤的药物组合,或结合蛋白质组学寻找新的药物研发靶点。当然,人工智能的研究和应用均处于起步阶段,存在质量控制、结果推广等方面的诸多问题,需要在发展过程中继续探索解决之道。

