一测多评法同时测定蒲公英配方颗粒中5种成分的含量*
施文婷,邓桂海,文珊,黎桃敏,张兰兰,刘权震,梁志毅
(广东一方制药有限公司/广东省中药配方颗粒企业重点实验室,广东 佛山 528244)
蒲公英是菊科植物蒲公英(Taraxacum mongolicum Hand.-Mazz.)、碱地蒲公英(Taraxacum borealisinense Kitam.)或同属数种植物的干燥全草[1]。其主要产于北半球温带至亚热带地区,在我国主要分布于华北、东北、西北、西南等地区[2]。现代药理研究表明,蒲公英含有酚酸类、黄酮类、多糖类、萜类及甾醇类等多种有效成分[3-5],具有抗癌、抗氧化、降血糖、抗血栓、免疫调节等多重药理作用,同时蒲公英具有清热解毒、健胃消炎、散结、利尿活血的功效,临床上主要用于治疗炎症、疔毒痈肿、肿瘤、高脂血症、前列腺等疾病[6-10]。
蒲公英配方颗粒由蒲公英药材炮制成饮片后,经过提取、浓缩和制剂工艺精制而成,具有药性强、药效好、免煎煮、服用方便等优势,临床应用广泛[11]。一测多评法借助相对校正因子,只需测定一个成分(内标物),即可实现对多个有效成分的定量分析,同时降低了检测成本,在中药质量控制方面得到广泛应用[12-13]。本研究通过建立一测多评法,以咖啡酸为内标物,同时测定蒲公英配方颗粒中单咖啡酰酒石酸、新绿原酸、绿原酸和菊苣酸的含量,以期为蒲公英配方颗粒的质量控制及后续研究提供参考。
1 仪器与试药
1.1 仪器 Thermo U3000型高效液相色谱仪(美国赛默飞公司);Waters Arc型高效液相色谱仪(美国沃特世公司);Milli-Q Direct型超纯水系统(德国默克公司);XP26型百万分之一天平、ME204E型万分之一天平均购自瑞士梅特勒-托利多仪器有限公司;KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药 绿原酸对照品(批号:110753-201817,质量分数为96.80%)、咖啡酸对照品(批号:110885-201703,质量分数为99.7%)均购自中国食品药品检定研究院;单咖啡酰酒石酸对照品(批号:wkq20043006,质量分数为99.10%)、新绿原酸对照品(批号:wkq18030107,质量分数为98.00%)、菊苣酸对照品(批号:wkq20030403,质量分数为98.56%)均购自四川省维克奇生物科技有限公司;乙腈、甲醇为色谱纯均购自德国默克公司;醋酸为色谱纯(天津市科密欧化学试剂有限公司);其他试剂为分析纯。本研究所用10批蒲公英配方颗粒(编号:S1~S10)由广东一方制药有限公司提供。
2 方法与结果
2.1 色谱条件[14]采用Waters Xbridge C18色谱柱(250 mm×4.6 mm,5.0 μm,美国沃特世公司),流动相为乙腈(A)-0.5%醋酸溶液(B),梯度洗脱(0~25 min,5%~15%A;25~35 min,15%~35%A;35~50 min,35%A),检测波长为323 nm,柱温为35 ℃,进样量为10 μL,流速为1.0 mL/min。
2.2 混合对照品溶液的制备 分别取单咖啡酰酒石酸、新绿原酸、绿原酸、咖啡酸、菊苣酸对照品适量,精密称定,加入50%甲醇定容,制成质量浓度分别为556.248 0、53.468 8、54.046 6、54.840 8、388.864 0 μg/mL的混合对照品贮备液。
2.3 供试品溶液的制备[12]取蒲公英配方颗粒约0.2 g,精密称定样品质量,置于100 mL的具塞锥形瓶中,精密加入水50 mL,密塞,称定总质量,超声波提取目标成分30 min后,取出,放冷后再称质量,补足减失的水溶液质量,摇匀,滤过,取续滤液,即得供试品溶液。
2.4 方法学考察
2.4.1 专属性试验[15]分别精密吸取空白溶剂、混合对照品溶液及供试品溶液,按“2.1”项下色谱条件进样测定。结果显示,空白溶剂色谱图中,在单咖啡酰酒石酸、新绿原酸、绿原酸、咖啡酸、菊苣酸的出峰位置无吸收峰;供试品溶液色谱中,在与混合对照品溶液色谱相同保留时间处有相应色谱峰,表明该方法专属性良好。(见图1)
2.4.2 线性关系考察[12]精密量取0.1、0.2、0.5、1.0、2.5、5.0、10.0 mL的单咖啡酰酒石酸(556.248 0 μg/mL)、新绿原酸(53.468 8 μg/mL)、绿原酸(质54.046 6 μg/mL)、咖啡酸(54.840 8 μg/mL)、菊苣酸(388.864 0 μg/mL)混合对照品溶液,置于容量瓶中,缓慢滴加50%甲醇溶液定容至10 mL的刻度线处,制成系列浓度的混合对照品溶液,按“2.1”项下色谱条件进样测定,记录单咖啡酰酒石酸、新绿原酸、绿原酸、咖啡酸、菊苣酸的峰面积。以对照品溶液质量浓度为横坐标(x),峰面积为纵坐标(y)进行线性回归。结果表明各成分的线性关系在其相应的质量浓度范围内均有良好的线性关系。(见表1)
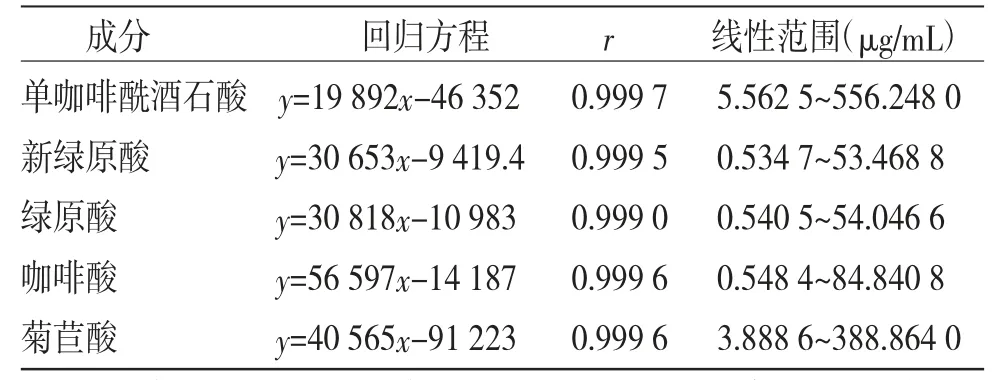
表1 线性关系考察结果
续表1:
2.4.3 精密度试验[15]精密吸取“2.2”项下混合对照品溶液,按“2.1”项下色谱条件连续进样6次,计算得单咖啡酰酒石酸、新绿原酸、绿原酸、咖啡酸、菊苣酸色谱峰峰面积的RSD均小于3%,表明仪器精密度良好。
2.4.4 稳定性试验[15]取蒲公英配方颗粒样品适量,精密称定,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件分别于制备0、2、4、8、12、24 h后进样测定,计算得单咖啡酰酒石酸、新绿原酸、绿原酸、咖啡酸、菊苣酸色谱峰峰面积的RSD均小于3%,表明供试品溶液在24 h内稳定性良好。
2.4.5 重复性试验[15]取蒲公英配方颗粒样品适量,精密称定,按“2.3”项下方法平行制备6份供试品溶液,按“2.1”项下色谱条件进样测定,计算得单咖啡酰酒石酸、新绿原酸、绿原酸、咖啡酸、菊苣酸色谱峰峰面积的RSD均小于3%,表明该方法重复性良好。
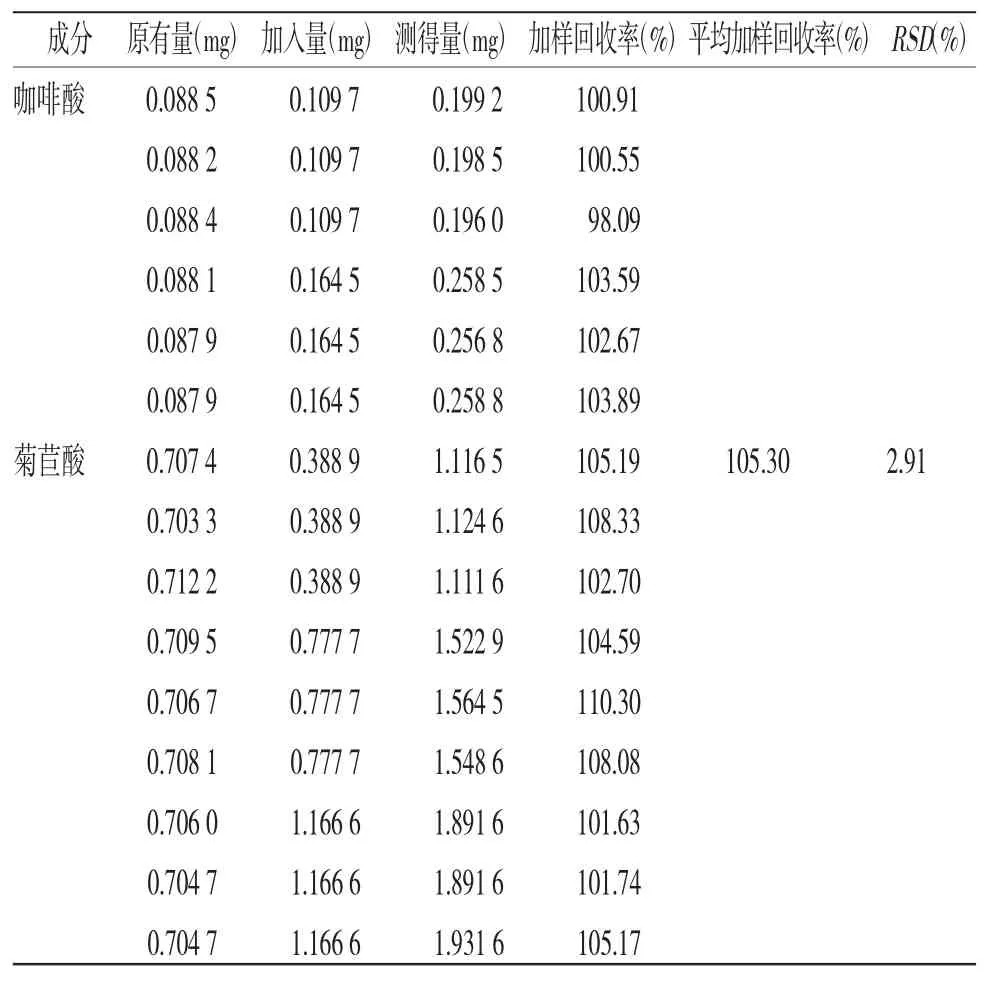
2.4.6 加样回收率试验[12]取同一批次已知成分含量的蒲公英配方颗粒共9份,研细,每份取约0.5 g,精密称定后分别置于锥形瓶100 mL中,每组分别加入单咖啡酰酒石酸、新绿原酸、绿原酸、咖啡酸、菊苣酸对照品溶液,加入量为蒲公英配方颗粒中各成分含量的50%、100%和150%,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,记录峰面积,计算加样回收率及RSD。平均回收率:单咖啡酰酒石酸为105.20%(RSD=1.76%);新绿原酸为106.83%(RSD=2.40%);绿原酸为106.89%(RSD=1.77%);咖啡酸为102.60%(RSD=2.51%);菊苣酸为105.30%(RSD=2.91%)。表明该方法准确度良好。(见表2)

表2 5 种成分的加样回收率试验结果(n=9)
2.5 相对校正因子的确定[16-17]精密吸取“2.4.2”项下混合对照品溶液,按“2.1”项下色谱条件进样测定,以咖啡酸为内标物,计算其他4种成分的相对校正因子(fs/k),公式为fs/k=fs/fk=(As×Ck)/(Ak×Cs)。其中As为内标物峰面积,Cs为内标物质量浓度,Ak为待测成分峰面积,Ck为待测成分质量浓度。结果见表3。
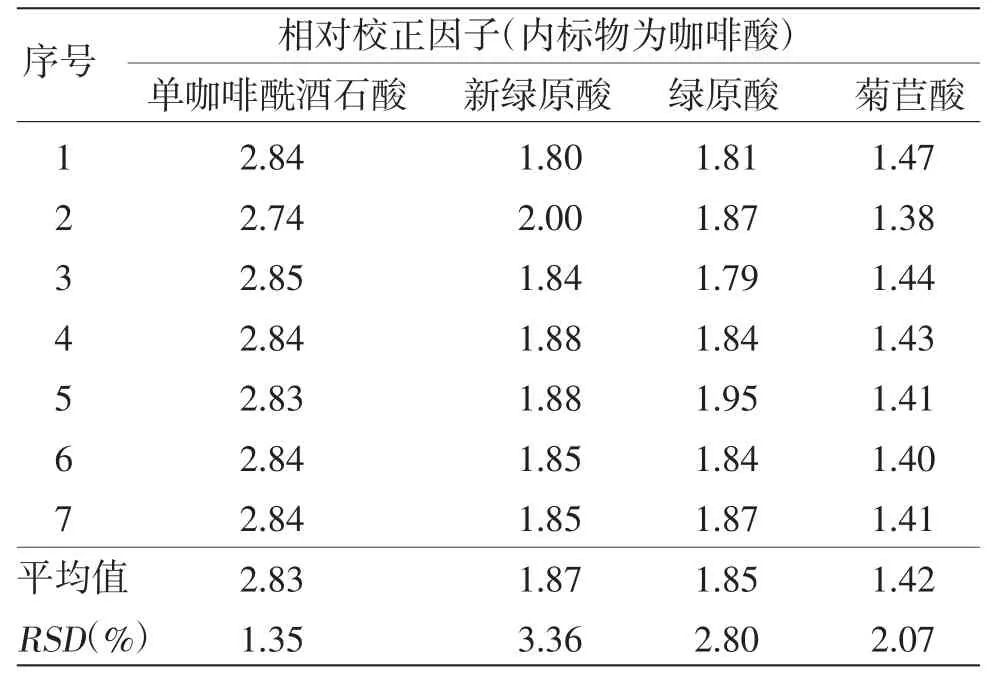
表3 各成分相对校正因子(n=7)
2.6 耐用性和系统适应性试验
2.6.1 不同色谱系统及色谱柱对相对校正因子的影响[18]以咖啡酸为内标物,考察其他4种成分在Thermo U3000型、Waters Arc型2种高效液相色谱系统,以及Waters Xbridge C18(250 mm×4.6 mm,5 μm)、Agilent ZORBAX Extend-C18(250 mm×4.6 mm,5 μm)、YMC Triart C18(250 mm×4.6 mm,5 μm)3种色谱柱下的相对校正因子。结果见表4。各成分的RSD均小于3%,表明不同色谱系统和色谱柱对各成分相对校正因子无显著影响。
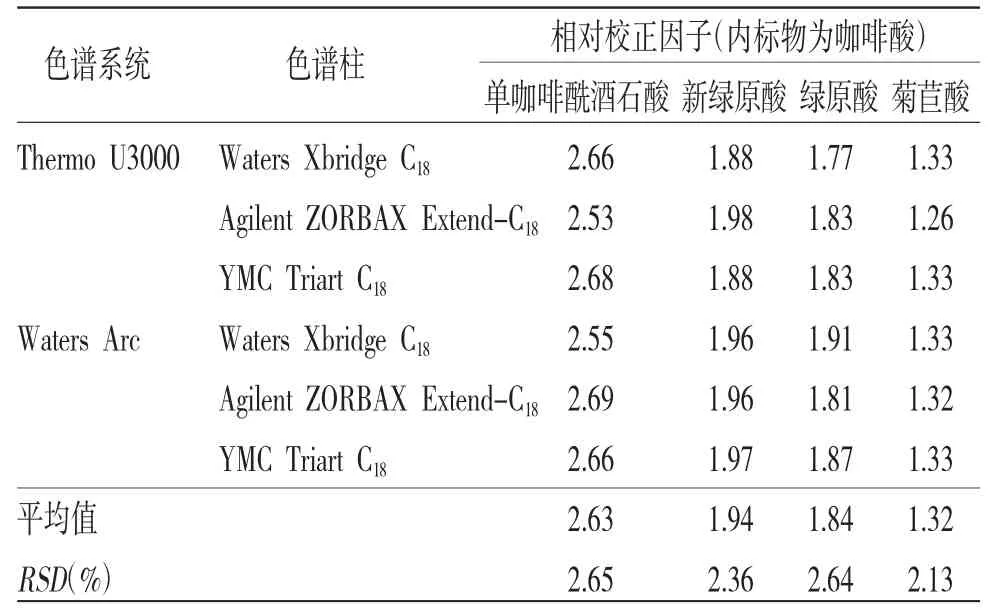
表4 不同色谱系统、色谱柱对相对校正因子的影响
2.6.2 不同柱温对相对校正因子的影响[18]采用Waters Arc型高效液相色谱仪、Waters Xbridge C18色谱柱,考察柱温25、30、35、40 ℃对各成分相对校正因子的影响。结果见表5。不同柱温条件下各成分的RSD均小于3%,表明柱温对各成分相对校正因子无显著影响。
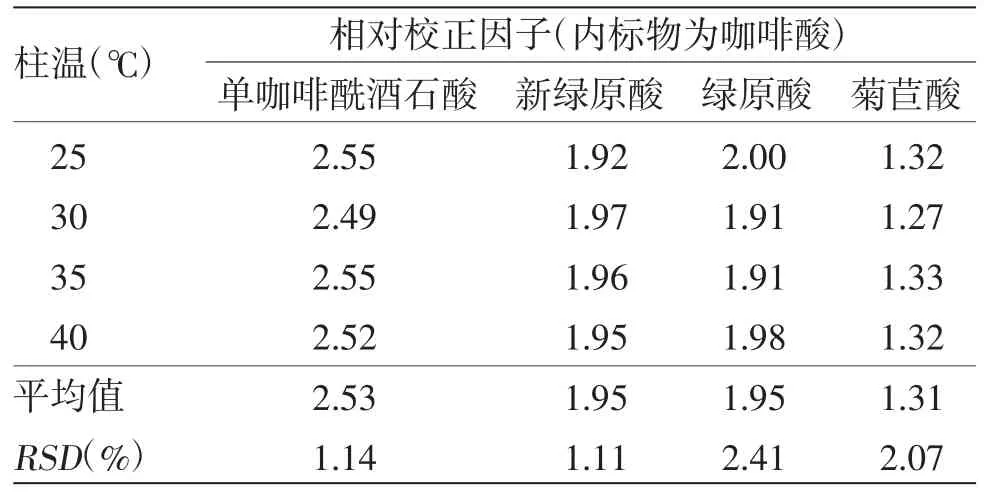
表5 不同柱温对相对校正因子的影响
2.6.3 不同流速对相对校正因子的影响[18]采用Waters Arc型高效液相色谱仪、Waters Xbridge C18色谱柱,考察流速0.8、1.0、1.2 mL/min对各成分相对校正因子的影响。结果显示不同流速条件下各成分的RSD均小于3%,表明不同流速对各成分相对校正因子无显著影响。(见表6)

表6 不同流速对相对校正因子的影响
2.6.4 不同进样体积对相对校正因子的影响[18]采用Waters Arc型高效液相色谱仪、Waters Xbridge C18色谱柱,考察进样体积2、4、6、8、10、15 μL对各成分相对校正因子的影响。结果显示各成分的RSD均小于3%,表明进样体积的波动对各成分相对校正因子无显著影响。(见表7)
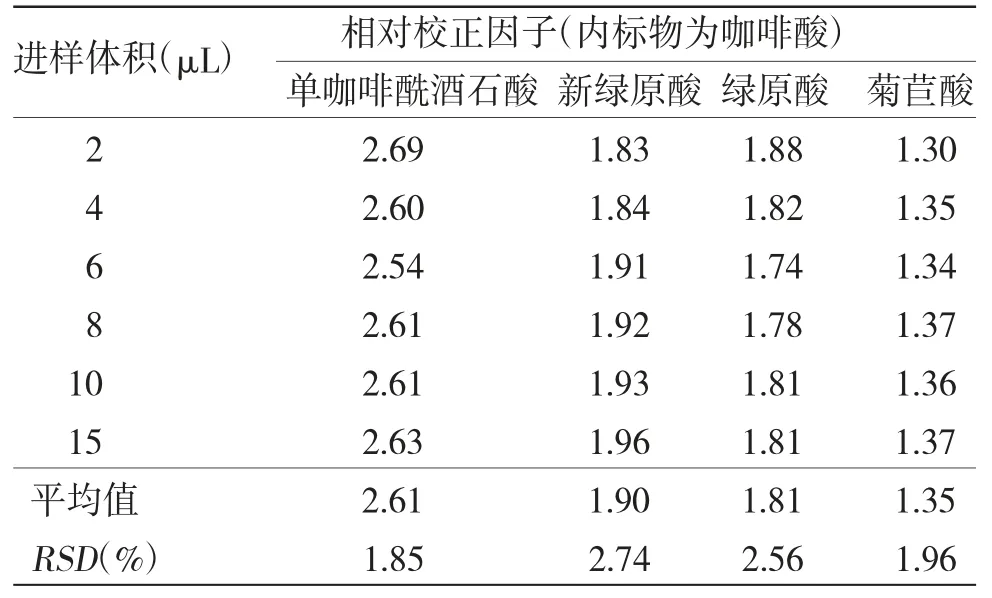
表7 不同进样体积对相对校正因子的影响
2.7 待测成分色谱峰的定位[19]在QAMS的应用中,目前常用的色谱峰定位方法有相对保留值法、保留时间差法、时间校正法、对照提取物法等方法。保留时间差法计算公式:Δti/s=ti-ts。相对保留值法计算公式:ti/s=ti/ts。本实验采用相对保留时间进行待测组分色谱峰的定位,以咖啡酸为内标物,考察其他4种成分在Thermo U3000型和Waters Arc型2种高效液相色谱系统,以及3根不同厂家的色谱柱(Waters Xbridge C18、Agilent ZORBAX Extend-C18、YMC Triart C18)的相对保留时间。采用相对保留值法各成分的RSD均小于3%,表明采用相对保留值法对待测成分的定位是可行的。(见表8)
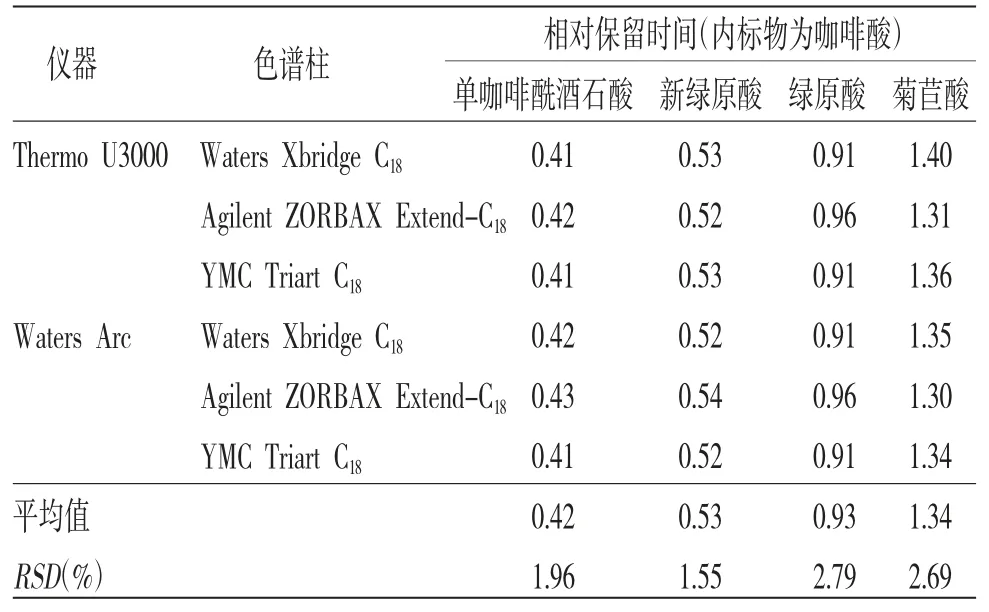
表8 各成分相对保留时间
2.8 一测多评法与外标法测定结果比较 取10批蒲公英配方颗粒适量,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,分别采用外标法和一测多评法测定各成分含量,利用SPSS 20.0软件对两组检测结果进行配对t检验及Pearson相关性分析。两种方法之间的相关系数r均为1.000,表明两种方法测定结果比较,差异无统计学意义(P>0.05),建立的一测多评法具有较好的可信度。(见表9)
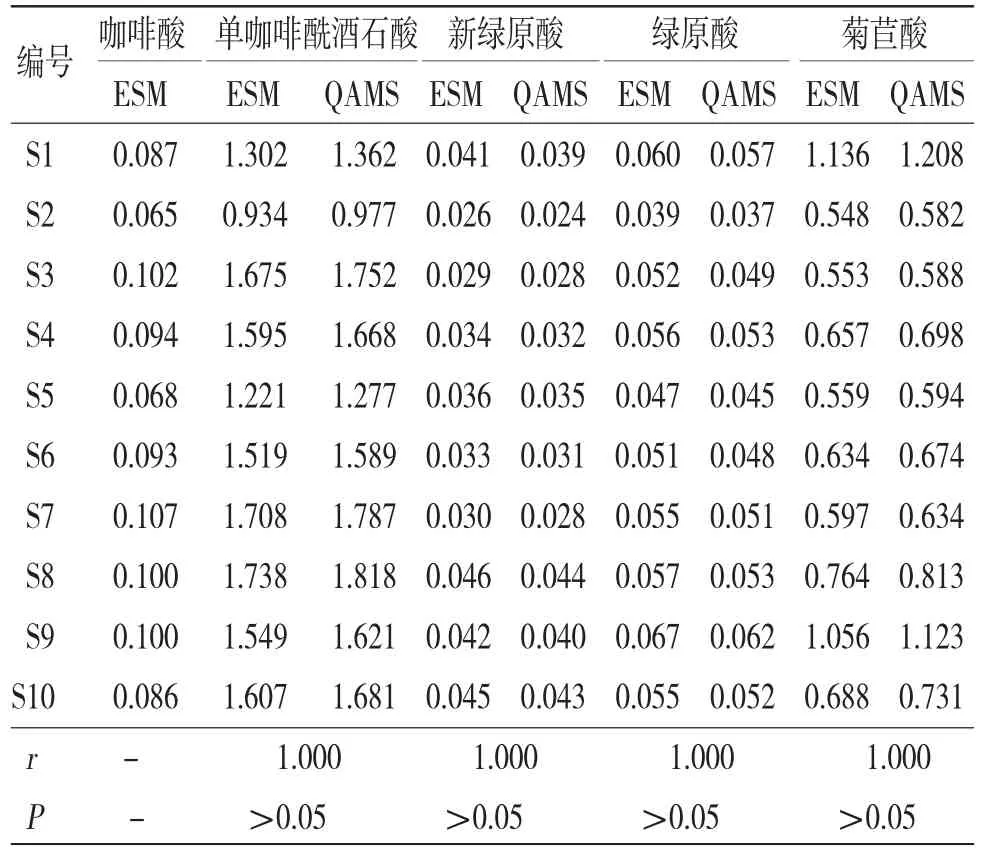
表9 外标法与一测多评测定结果比较(%,n=3)
3 讨 论
蒲公英作为一种药食同源植物,在我国传统食用和药用方面的应用已有几千年历史。蒲公英含有多种有效成分,其中酚酸类成分如单咖啡酰酒石酸、新绿原酸、绿原酸和菊苣酸等为其主要活性成分,具有抗氧化、免疫调节、降血糖和抑制肿瘤等多重药理作用[20-22]。蒲公英配方颗粒国家标准属于国家药品监督管理局首批颁布的160个中药配方颗粒国家标准之一,已于2021年11月1日正式实施。中药配方颗粒国家标准的执行将有助于实现安全性、有效性等多方面的整体质量控制。本研究在此基础上,采用QAMS法同时测定了蒲公英配方颗粒中5种有效成分的含量,并对QAMS法的可行性与适用性进行了探讨。计算结果与外标法实测结果无明显差异,表明所建立的QAMS方法经济、稳定、可行,可为蒲公英配方颗粒的质量控制、谱效相关研究提供基础,并为其他品种质量评价研究提供范例。
——评析绿原《幸福》

