卡瑞利珠单抗联合化疗治疗晚期NSCLC患者的治疗效果
韩璐 厉锋
我国是肺癌的高发国家,常见的类型主要为非小细胞肺癌(Non-small cell lung cancer,NSCLC),虽然目前新的诊断技术及治疗技术得到了不断提高,但NSCLC 的早期诊断率仍较低,大部分病人诊断时已为晚期,无法通过手术治愈,只能选择有效的化疗方案进行治疗[1-2]。癌症患者普遍存在着免疫功能低下现象,化疗药物能进一步对细胞免疫功能造成破坏,从而导致患者抵抗力更低,不利于患者预后[3-4]。近年来,免疫疗法在肿瘤患者化疗过程中的作用也受到较多临床关注,具有稳定机体免疫内环境、提高疗效、延长生存期等优势[5]。卡瑞利珠单抗已被我国药品监督管理局批准上市,属于一种人源化抗程序性死亡受体(Programmed death receptor,PD-1),具有加强机体抗肿瘤免疫功能的作用[6]。因此,本研究旨在探讨卡瑞利珠单抗联合化疗治疗晚期NSCLC 患者的治疗效果,现将结果报道如下。
1 资料与方法
1.1 一般资料
纳入2019年5月至2021年5月徐州市肿瘤医院接受化疗的80 例晚期NSCLC 患者进行研究。纳入标准:①经检查确诊为NSCLC,临床分期Ⅲ~Ⅳ期[7];②美国东部肿瘤协作组(Eastern Oncology Collaborative Group,ECOG)[7]评分0~1 分,经评估预计生存期>3 个月;③近3 个月内未使用过免疫增强剂、免疫抑制剂等药物;④化疗前血常规检查正常。排除标准:①伴有表皮生长因子受体、间变淋巴瘤激酶基因突变情况;②合并感染;③合并其他恶性肿瘤;④合并先天或者后天的细胞免疫功能障碍、免疫系统疾病;⑤合并严重肝、肾、心脑血管系统等疾病,无法耐受化疗治疗;⑥合并凝血功能障碍、严重贫血者;⑦经评估对研究药物有应用禁忌症;⑧精神障碍。依照随机数表法分为试验组与对照组,各40 例,两组一般资料情况见表1,两组基本资料差异无统计学意义(P>0.05)。本研究已经由院伦理委员会批准。所有患者及家属均签署研究知情同意书。
表1 两组一般资料比较[n(%),(±s)]Table 1 Comparison of general data between the two groups[n(%),(±s)]
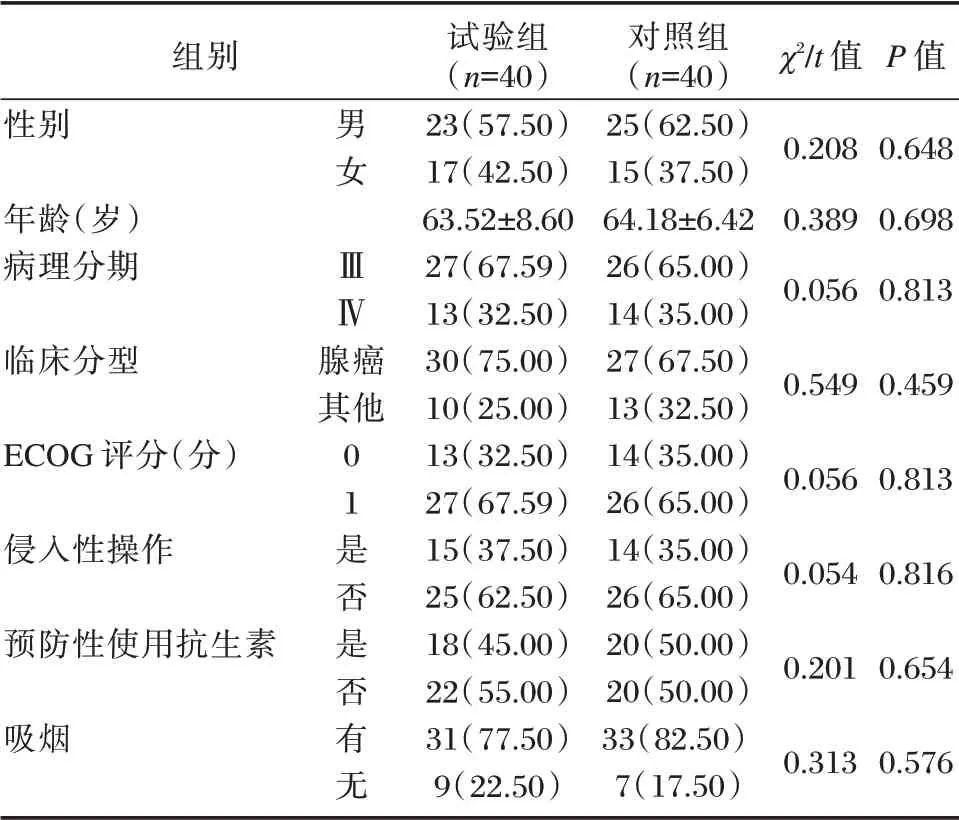
表1 两组一般资料比较[n(%),(±s)]Table 1 Comparison of general data between the two groups[n(%),(±s)]
组别性别χ2/t 值P 值年龄(岁)病理分期0.208 0.389 0.056 0.648 0.698 0.813临床分型男女ⅢⅣ腺癌其他0.5490.459 ECOG 评分(分)0.0560.813侵入性操作0.0540.816预防性使用抗生素0.2010.654吸烟0 1是否是否有无试验组(n=40)23(57.50)17(42.50)63.52±8.60 27(67.59)13(32.50)30(75.00)10(25.00)13(32.50)27(67.59)15(37.50)25(62.50)18(45.00)22(55.00)31(77.50)9(22.50)对照组(n=40)25(62.50)15(37.50)64.18±6.42 26(65.00)14(35.00)27(67.50)13(32.50)14(35.00)26(65.00)14(35.00)26(65.00)20(50.00)20(50.00)33(82.50)7(17.50)0.3130.576
1.2 方法
对照组采用培美曲塞(齐鲁制药有限公司生产,国药准字H20060672)联合顺铂(云南植物药业有限公司生产,国药准字H53021740)进行化疗,第1 天给予培美曲塞500 mg/m2静脉输注,第1~3 天给予顺铂25 mg/m2静脉输注治疗;试验组联合卡瑞利珠单抗(苏州盛迪亚生物医药有限公司生产,国药准字S20190027)进行治疗,仅第1 天给药,静脉注射200 mg。两组的化疗周期均为21 d,连续治疗3 个化疗周期。
1.3 观察指标
1.3.1 临床疗效
治疗3 个周期后评价疗效,完全缓解:病灶得到完全消失,持续时间>4 周;部分缓解:病灶较治疗前缩小程度≥50%,持续时间>4 周;疾病稳定:病灶较治疗前缩小程度<50%,或者增大程度<25%;疾病进展:病灶较治疗前出现≥25%的增加,或出现新病灶;统计疾病缓解率,为完全缓解、部分缓解之和[8]。
1.3.2 免疫功能
治疗前及治疗后,于无菌条件采集3 mL 外周血,添加人淋巴细胞分离液,置于1 500 r/min 的条件下离心处理,离心半径10 cm,提取中间层的细胞,加入对应的抗体,使用流式细胞仪(美国BD 公司,FACSCaliur 型)测量CD3+、CD4+、CD4+/CD8+及自然杀伤细胞(Natural killer cell,NK)细胞的表达。
1.3.3 血液指标、炎症因子
治疗前及治疗后,采集清晨空腹静脉血6 mL,采用西门子全自动血细胞分析仪测量网织红细胞百分数(Reticulocyte percentage,Retic%)、血小板计数(Platelet count,PLT)、中性粒细胞数(Neutrophil count,Neu)的表达;并采用免疫荧光法对降钙素原(Calcitonin original,PCT)、C 反应蛋白(C-reactive protein,CRP)的表达进行测定,酶联免疫吸附法测定白细胞介素-6(Interleukin-6,IL-6)的表达,试剂盒均购于武汉优尔生商贸有限公司。
1.4 统计学方法
应用SPSS 20.0 软件包进行统计学分析;计量资料以()表示,组内比较采用配对样本t检验,组间比较采用独立样本t检验;计数资料以n(%)表示,采用χ2检验;P<0.05 表示差异有统计学意义。
2 结果
2.1 两组临床疗效比较
试验组临床疗效总缓解率高于对照组,差异有统计学意义(P<0.05)。见表2。
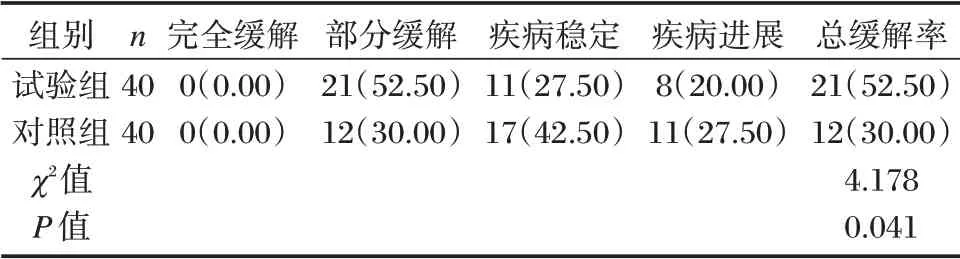
表2 两组临床疗效比较[n(%)]Table 2 Comparison of clinical efficacy between the two groups[n(%)]
2.2 两组细胞免疫功能比较
治疗后,两组细胞免疫功能指标和治疗前比较,差异有统计学意义(P<0.05);试验组治疗后CD3+、CD4+、CD4+/CD8+及NK 细胞数量均高于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组细胞免疫功能比较(±s)Table 3 Comparison of cellular immune function between the two groups(±s)
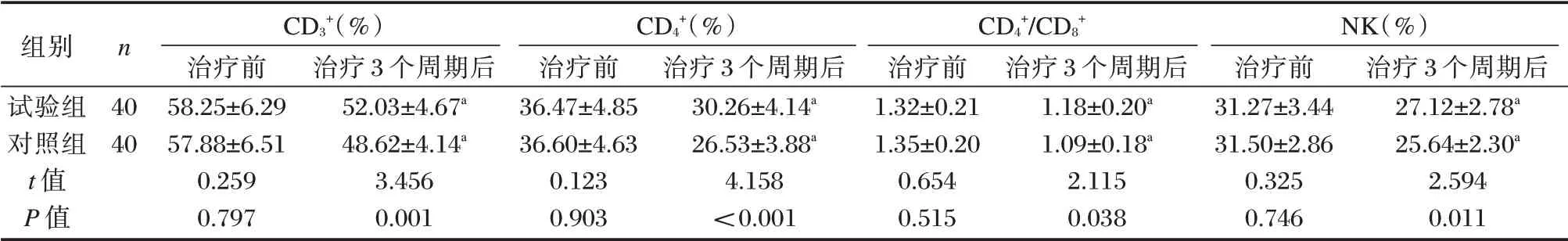
表3 两组细胞免疫功能比较(±s)Table 3 Comparison of cellular immune function between the two groups(±s)
注:与本组治疗前对比,aP<0.05。
组别试验组对照组t 值P 值n 40 40 CD3+(%)治疗前58.25±6.29 57.88±6.51 0.259 0.797治疗3 个周期后52.03±4.67a 48.62±4.14a 3.456 0.001 CD4+(%)治疗前36.47±4.85 36.60±4.63 0.123 0.903治疗3 个周期后30.26±4.14a 26.53±3.88a 4.158<0.001 CD4+/CD8+治疗前1.32±0.21 1.35±0.20 0.654 0.515治疗3 个周期后1.18±0.20a 1.09±0.18a 2.115 0.038 NK(%)治疗前31.27±3.44 31.50±2.86 0.325 0.746治疗3 个周期后27.12±2.78a 25.64±2.30a 2.594 0.011
2.3 两组血液指标比较
治疗后,两组的Retic%、PLT、Neu 均低于治疗前;治疗后,试验组各指标结果均高于对照组,差异有统计学意义(P<0.05)。见表4。
表4 两组血液指标比较(±s)Table 4 Comparison of blood indexes between the two groups(±s)
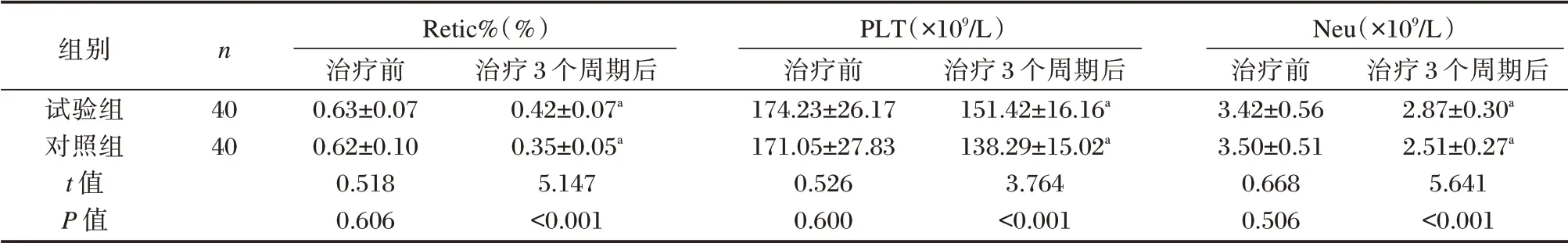
表4 两组血液指标比较(±s)Table 4 Comparison of blood indexes between the two groups(±s)
注:与本组治疗前对比,aP<0.05。
组别试验组对照组t 值P 值n 40 40 Retic%(%)治疗前0.63±0.07 0.62±0.10 0.518 0.606治疗3 个周期后0.42±0.07a 0.35±0.05a 5.147<0.001 PLT(×109/L)治疗前174.23±26.17 171.05±27.83 0.526 0.600治疗3 个周期后151.42±16.16a 138.29±15.02a 3.764<0.001 Neu(×109/L)治疗前3.42±0.56 3.50±0.51 0.668 0.506治疗3 个周期后2.87±0.30a 2.51±0.27a 5.641<0.001
2.4 两组炎症因子指标比较
治疗后,两组的PCT、CRP、IL-6 均高于治疗前;治疗后,试验组各指标结果低于对照组,差异有统计学意义(P<0.05),见表5。
表5 两组炎症因子指标比较(±s)Table 5 Comparison of inflammatory factors between the two groups(±s)
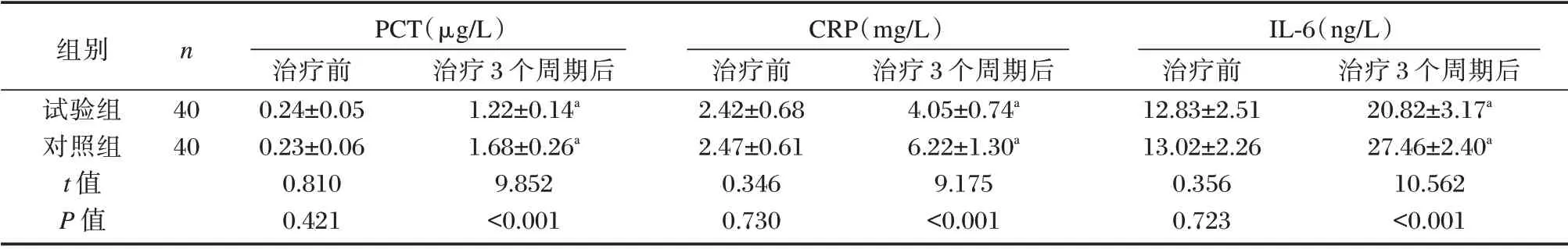
表5 两组炎症因子指标比较(±s)Table 5 Comparison of inflammatory factors between the two groups(±s)
注:与本组治疗前对比,aP<0.05。
组别试验组对照组t 值P 值n 40 40 PCT(μg/L)治疗前0.24±0.05 0.23±0.06 0.810 0.421治疗3 个周期后1.22±0.14a 1.68±0.26a 9.852<0.001 CRP(mg/L)治疗前2.42±0.68 2.47±0.61 0.346 0.730治疗3 个周期后4.05±0.74a 6.22±1.30a 9.175<0.001 IL-6(ng/L)治疗前12.83±2.51 13.02±2.26 0.356 0.723治疗3 个周期后20.82±3.17a 27.46±2.40a 10.562<0.001
3 讨论
NSCLC 在肺癌中的比例占有80%左右,具有发病率高、病程短、患者预后差等特点,且通常难以早期及时的发现病灶,以至于较多患者在就诊时已错过了根治性手术的最佳时机,需接受化疗以延长总体生存期、提高患者的生活质量[9-10]。临床针对NSCLC 患者的治疗主要采取以铂类药物为基础的化疗方案,有助于抑制肿瘤进展,但有较多报道中也发现,化疗药物在杀伤肿瘤细胞期间,也容易对机体正常细胞产生毒性作用,致使机体抵抗力降低,而抵抗能力的降低也会导致机体更易于受到肿瘤细胞的侵袭,不利于患者病情的早期恢复,在一定程度上也增加了临床治疗难度[11]。
近年来,各类免疫制剂在肿瘤患者的治疗中也不断兴起,也有较多PD-1 药物获批应用于临床,并体现出疗效持久、不良反应少等特点[12]。卡瑞利珠单抗是我国自主研发的一种PD-1 药物,其作为PD-1阻断剂,给药后能够和人PD-1 受体相互结合,并对PD-1/PD-L1 通路进行阻断,从而产生一种肿瘤免疫治疗的基础,该药物目前也逐渐在一些恶性肿瘤患者中开展临床试验。有研究称,卡瑞利珠单抗联合化疗能明显提高胃癌患者的疗效,并积极提高生活质量[13]。Qin S 等[14]一项多中心、开放性试验中发现,晚期肝细胞癌应用卡瑞利珠单抗后,疾病客观缓解率较高,6 个月总生存率高达74.4%,体现出较好的抗肿瘤活性,同时在副反应反应也具有可控性。也有实验将卡瑞利珠单抗应用于晚期NSCLC 患者的治疗,研究显示近期的客观有效率、疾病控制率分别为50.0%、72.5%,证实疗效可靠[15]。
本研究结果发现,试验组的临床疗效总缓解率和对照组相比更高,结果和吴克林等[16]研究具有相似性。同时本研究也显示,两组患者治疗后CD3+、CD4+、CD4+/CD8+、NK 细胞数量、Retic%、PLT、Neu 均出现降低,而PCT、CRP、IL-6 升高,表明化疗对机体的免疫功能、血液系统等均会产生一定毒性作用,然而试验组上述指标的变化幅度较对照组相比更小,主要原因是由于,卡瑞利珠单抗可通过和PD-1 进行靶向结合,对PD-1 通路所介导的T 细胞免疫抑制效应起到阻断作用,重建免疫系统功能,同时在提高机体免疫功能后,能够加强机体抗病能力,从而提高机体的抗肿瘤功能,更好的对病情进展起到抑制作用。因此笔者建议,今后在NSCLC 患者化疗期间,可根据患者自身情况合理应用卡瑞利珠单抗配合化疗,有助于避免化疗所导致的免疫功能降低等情况,积极改善患者治疗结局。但本研究也有一些缺点,例如未观察长期应用卡瑞利珠单抗对患者生存期方面的影响等,也有待开展更高质量的试验。
综上所述,卡瑞利珠单抗联合化疗治疗晚期NSCLC 患者的作用明显,能有效提高细胞免疫功能,改善血液指标及炎症因子的表达,临床应用价值高。

