Fenton 氧化法与Ca(OH)2-CaCl2 沉淀法联合处理锂电池高氟废水的应用研究
张浩纯
(广东广深环保科技股份有限公司,广州 510500)
在新能源汽车和工业储能等新兴应用市场的发展带动下,全球锂电池电解液市场需求稳步增长,电解液生产过程中产生的工业废水也逐年递增。氟离子是废水中的主要污染物之一,其浓度高,若不能有效处理,直接排放到环境中将造成严重的污染。锂电池电解液生产的原材料成分复杂且种类繁多,其产生的高氟废水同时含有无机氟化物和有机氟化物,该废水具有一定的生物毒性,且较难通过沉淀完全处理。因此,高氟废水的处理引起研究者的重视和广泛关注[1]。
高氟废水中的无机氟化物可通过钙法沉淀去除,CaF2的溶度积常数为2.7×10-11,表明钙盐的除氟效果很好,同时钙盐价格相对便宜,因此钙盐沉淀法是最常用的除氟方法。但是,有机氟化物的抗降解性较高,使得其在废水中较难去除。另外,氟原子半径小,F-C 化学键键能大,电负性较强,其在强酸、强碱、高温等条件下均难以被破坏。因而,研究含有无机氟化物和有机氟化物的高氟废水高效处理工艺具有重要意义。
1 项目废水处理工艺流程
某企业主要生产锂电池电解液的添加剂,其生产废水的主要污染物为氟化物,且浓度较高。废水处理后,出水水质要求达到《水污染物排放限值》(DB44/26—2001)的标准,即氟化物浓度不大于10 mg/L。从原水指标来看,本项目含氟废水pH 为8.5,氟化物浓度为1 080 mg/L。
高氟废水通过调节池调节水质水量后,首先泵入一级钙法除氟系统,通过投加Ca(OH)2溶液调节pH,使其保持在8~9,再投加CaCl2溶液去除废水中的部分无机氟化物。沉淀后的上清液自流进入Fenton 氧化反应系统,通过投加硫酸溶液调节pH,使其保持在3~4,以满足Fenton 氧化条件,再投加H2O2溶液和FeSO4溶液进行Fenton 氧化反应,将有机氟化物转化为无机氟化物。最后进行二级钙法除氟,去除废水中的无机氟化物,最终沉淀后的上清液自流至后续生化系统,所有污染物指标达到排放标准后,出水外排。
2 废水处理试验结果分析
首先控制H2O2溶液(浓度30%)和FeSO4溶液(浓度10%)的投加量,利用Fenton 氧化法将高氟废水中有机氟化物转化为无机氟化物,然后控制Ca(OH)2溶液(浓度15%)和CaCl2溶液(浓度10%)的投加量,运用Ca(OH)2-CaCl2沉淀法去除高氟废水中氟化物。下面通过开展试验,分析其最佳反应条件。
2.1 Fenton 氧化效率
采用Fenton 氧化法对废水中的有机氟化物进行深度处理,将其转化为无机氟化物,研究H2O2溶液和FeSO4溶液的投加量对Fenton 氧化效果的影响。
2.1.1 H2O2投加量的影响
控制Fenton 氧化系统的pH 为4,统一投加FeSO4溶液250 mg/L,通过改变H2O2溶液的投加量,研究其对Fenton 氧化效果的影响,试验结果如表1所示。

表1 H2O2 溶液投加量对Fenton 氧化效果的影响
随着H2O2溶液的投加量增加,羟基自由基(·OH)的生成量增加,有机氟化物在过量·OH 的作用下得到充分的氧化分解。但是,当H2O2溶液的投加量大于40 mg/L 时,氟离子浓度开始出现明显下降。经分析,过量投加H2O2会导致过量的H2O2与·OH 反应生成氢过氧自由基(HOO·),HOO·会抑制·OH的氧化作用,从而降低H2O2的有效利用率[3],造成药剂浪费,增加运行成本。在实际运行过程中,H2O2投加量可以控制在40 mg/L 左右。
2.1.2 FeSO4投加量的影响
控制Fenton 氧化系统的pH 为4,统一投加H2O2溶液40 mg/L,通过改变FeSO4溶液的投加量,研究其对Fenton 氧化效果的影响,如表2 所示。

表2 FeSO4 溶液投加量对Fenton 氧化效果的影响
随着FeSO4溶液投加量的增加,脱氟效率呈现先增强后减弱的变化趋势。过少的FeSO4溶液投加量不利于·OH 生成,但FeSO4溶液过量投加时,Fe2+会与·OH 反应生成Fe3+和OH-,易生成Fe(OH)3沉淀,不利于H2O2催化分解(产生·OH),同时消耗部分·OH,造成药剂浪费,增加运行成本。在实际运行过程中,FeSO4溶液的投加量可以控制在250 mg/L左右。
综上,高氟废水中的有机氟化物可通过Fenton氧化法转化成无机氟化物,从Fenton 氧化除氟系统的最佳反应条件来看,pH 为4 时,H2O2溶液投加量为40 mg/L,FeSO4溶液投加量为250 mg/L。
2.2 钙法除氟效率
高氟废水常采用的处理方法有化学沉淀法、离子交换法和膜分离法等[2]。其中,化学沉淀法常采用钙盐与氟离子反应生成CaF2沉淀。但考虑到Ca(OH)2的溶解度较低,本研究采用Ca(OH)2-CaCl2沉淀法进行联合处理[3],为反应提供更多钙离子。下面通过开展试验,探讨改良钙法脱氟的最佳反应条件。
2.2.1 Ca(OH)2投加量的影响
高氟废水经过Fenton 氧化后,投加Ca(OH)2溶液进行钙法除氟反应,同时记录pH、Ca(OH)2溶液投加量和氟离子浓度,研究不同Ca(OH)2溶液投加量对钙法除氟效果的影响,如表3 所示。
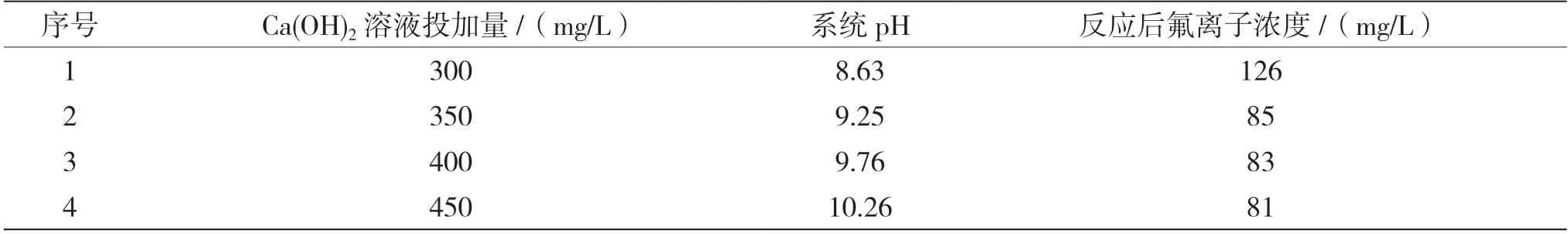
表3 Ca(OH)2 溶液投加量对钙法除氟的影响
当系统pH 为9.25,Ca(OH)2溶液投加量为350 mg/L时,除氟效果最佳,氟离子去除率最高。但随着投加量的增加,系统除氟效果未明显增强,最终趋于平稳,使得出水水质仍未达到排放标准。若继续投加大量的Ca(OH)2溶液,则不利于实际运行,且会导致运行成本增高,性价比较低。
2.2.2 CaCl2投加量的影响
控制钙法除氟系统的pH 为9.25,统一投加Ca(OH)2溶液350 mg/L,通过改变CaCl2溶液的投加量,研究其对钙法除氟效果的影响,如表4 所示。

表4 CaCl2 溶液投加量对钙法除氟的影响
随着CaCl2溶液的投加量增加,系统的Ca2+浓度逐渐提高,除氟效率大大提升,出水可满足排放标准。当CaCl2溶液投加量为450 mg/L 时,系统除氟效率较高,出水达到排放标准。在Ca(OH)2-CaCl2体系的联合作用下,随着钙离子含量的增加,氟离子与钙离子形成氟化钙沉淀,废水中的氟化物浓度下降明显。研究表明,选择适宜的混合盐具有较高的经济性。同时投加Ca(OH)2与CaCl2处理高氟废水时,未溶解的Ca(OH)2起到凝结核作用,使得沉淀后上清液更加清澈[4]。
3 结论
处理高氟废水时,首先要分析氟化物的存在形式,考虑有机氟化物的存在,避免过量投加药剂导致运行成本增加。Fenton 氧化法可将高氟废水中的有机氟化物氧化成无机氟化物,从系统最佳反应条件来看,当废水pH 为4 时,H2O2溶液和FeSO4溶液的投加量分别为40 mg/L、250 mg/L。当系统pH为9.25,Ca(OH)2溶液投加量为350 mg/L,CaCl2溶液投加量为450 mg/L 时,Ca(OH)2-CaCl2混合钙盐能够获得较高的除氟效率,使得出水氟化物浓度低于10 mg/L,保证出水稳定达标。高氟废水采用Ca(OH)2-CaCl2沉淀法进行联合处理时,CaF2沉淀明显增多,且废水中的氟化物浓度下降明显,该方法在实际应用中具有较高的经济性。另外,钙盐与氟离子反应生成的CaF2沉淀物会以未溶解的Ca(OH)2颗粒为凝结核,发生自絮凝,从而降低出水浊度。

