HPLC-MS/MS法鉴定落新妇苷在大鼠尿中的代谢产物
王文艳,仝瑶瑶,张林琪,宋吉伦,李贵生,,刘万卉
(1.烟台大学药学院,山东烟台 264005;2.山东绿叶制药天然药物研究中心,山东烟台 264005)
HPLC-MS/MS法鉴定落新妇苷在大鼠尿中的代谢产物
王文艳1,仝瑶瑶1,张林琪1,宋吉伦2,李贵生1,2,刘万卉1
(1.烟台大学药学院,山东烟台 264005;2.山东绿叶制药天然药物研究中心,山东烟台 264005)
为鉴定大鼠给药落新妇苷后尿中的主要代谢产物,收集其尿样,用聚酰胺固相萃取小柱处理后进样,采用高效液相色谱-串联质谱(HPLC-MS/MS)法分析。电喷雾离子源在负离子模式下进行扫描,借助碰撞诱导解离方式进行落新妇苷在大鼠体内主要代谢产物的结构确证。共鉴定出6个落新妇苷在大鼠尿中的代谢产物,分别为落新妇苷异构体(M1)、3′-O-甲基化落新妇苷(M2)、3′-O-甲基化落新妇苷异构体(M3)、槲皮素-鼠李糖苷(M4)、葡萄糖醛酸化落新妇苷 (M5)、3′-O-甲基化落新妇苷-葡萄糖醛酸化物(M6)。该方法对落新妇苷在大鼠体内的代谢进行了初步研究,并报道了落新妇苷在大鼠尿中的另外4个代谢产物M1、M3、M4、M6。
落新妇苷;代谢产物;高效液相色谱-串联质谱法(HPLC-MS/MS);聚酰胺固相萃取小柱
落新妇苷(3-O-α-l-鼠李糖-5,7,3′,4′-4 羟基二氢黄酮醇)为中药材土茯苓的提取物[1-2]。研究发现,落新妇苷在体内外有许多有益的药理药效作用,如抗菌活性[3]、免疫抑制活性[4]、抑制肝癌细胞系的扩增[5]。另外,落新妇苷有类似于刀豆蛋白A的抗炎作用,但没有副作用[6]。有研究报道了落新妇苷单剂量静注给药或灌胃给药兔子后的药动学特性[7]。落新妇苷灌胃给药后迅速被吸收,生物利用度低于10%。有学者以99 mg/kg剂量灌胃给药大鼠后,在鼠尿中鉴定出落新妇苷的代谢产物为 3′-O-甲基-落新妇苷[8]。为了更全面的了解落新妇苷的体内代谢情况,我们进行了大鼠静注给药落新妇苷(10 mg/kg)后的代谢途径研究。鼠尿样经自制的聚酰胺固相萃取小柱处理后,采用高效液相色谱-串联质谱(HPLC-MS/MS)法进行检测,通过色谱及质谱数据推测代谢物的结构。
1 实验部分
1.1 主要仪器与装置
Agilent 1100 HPLC:美国安捷伦公司产品,配有在线脱气机、四元梯度泵、自动进样器、柱温箱和VWD检测器;TSQ Quantum Access三重四极杆质谱仪:美国 ThermoFisher公司产品,配有电喷雾离子源及Xcalibur1.4数据处理系统。
1.2 主要材料与试剂
落新妇苷(纯度>98%):由山东绿叶制药天然药物研究中心提供;甲醇(色谱纯):德国Merck公司产品;试验用水为去离子双蒸水;聚酰胺(粒径30~50μm):购自北京百灵威化学技术有限公司。
1.3 动物实验
5只(235±11)g雄性 SD大鼠:由山东绿叶制药有限公司实验动物中心提供。动物饲养在代谢笼中,水和食物可以自由获得。每只鼠尾静脉注射给药 10 mg/kg落新妇苷,给药前(-12~0 h)收集空白尿样,给药后(0~12 h)收集尿样,收集到尿样后立即储存于-20℃冰箱中 ,待测。
1.4 实验条件
1.4.1 色谱条件 Supelco Discovery C 18色谱柱(150 mm×2.1 mm×5μm),柱温30 ℃。以90%甲醇作为A相,5%甲醇作为B相,按如下设置进行梯度洗脱:0 min,100%B;6 min,90%B;12 min,60%B,保持 2 min;20 min,5%B,保持 3 min;24 min,100%B,保持7 min。紫外检测波长设置为290 nm。
1.4.2 质谱条件 电喷雾离子源负离子检测模式,喷雾电压3 500 V,鞘气压力2.41×105Pa;辅气压力3.45×104Pa,毛细管温度350℃,碰撞诱导解离电压23 V,氩气压力0.2 Pa。
1.5 样品处理
尿样在冰水浴中融化后,8 000 r·min-1离心10 min,聚酰胺固相萃取小柱(200 mg)依次用4 mL甲醇活化和4 mL水平衡,然后将1 mL尿样上样到小柱上,再用2 mL水和4 mL甲醇洗脱小柱,收集甲醇洗脱相,在40℃用氮气流吹干。残留物用50%甲醇水复溶后,10μL进样,HPLC-MS/MS分析。
2 结果与讨论
2.1 HPLC-MS/MS鉴定落新妇苷的代谢产物
为了消除内源性物质的干扰,鼠尿样用自制的聚酰胺固相萃取小柱处理,聚酰胺基质处理含有羟基或羧基基团的化合物。与采用0.45μm滤膜过滤或乙腈沉淀蛋白预处理的尿样方法比较,采用聚酰胺固相萃取小柱处理尿样后,明显减少了基质干扰,并且有利于减少样品对质谱仪器的污染。高灵敏度的 ESI电离源结合串联四极质谱为推断落新妇苷代谢物的结构特性提供了信息。空白尿样及落新妇苷尿样的典型HPLC-UV色谱图和 TIC(总离子流)图示于图1。与空白尿样比较,静注给药落新妇苷后,在鼠尿样中可发现落新妇苷(M0)及其6个代谢产物M1~M6。
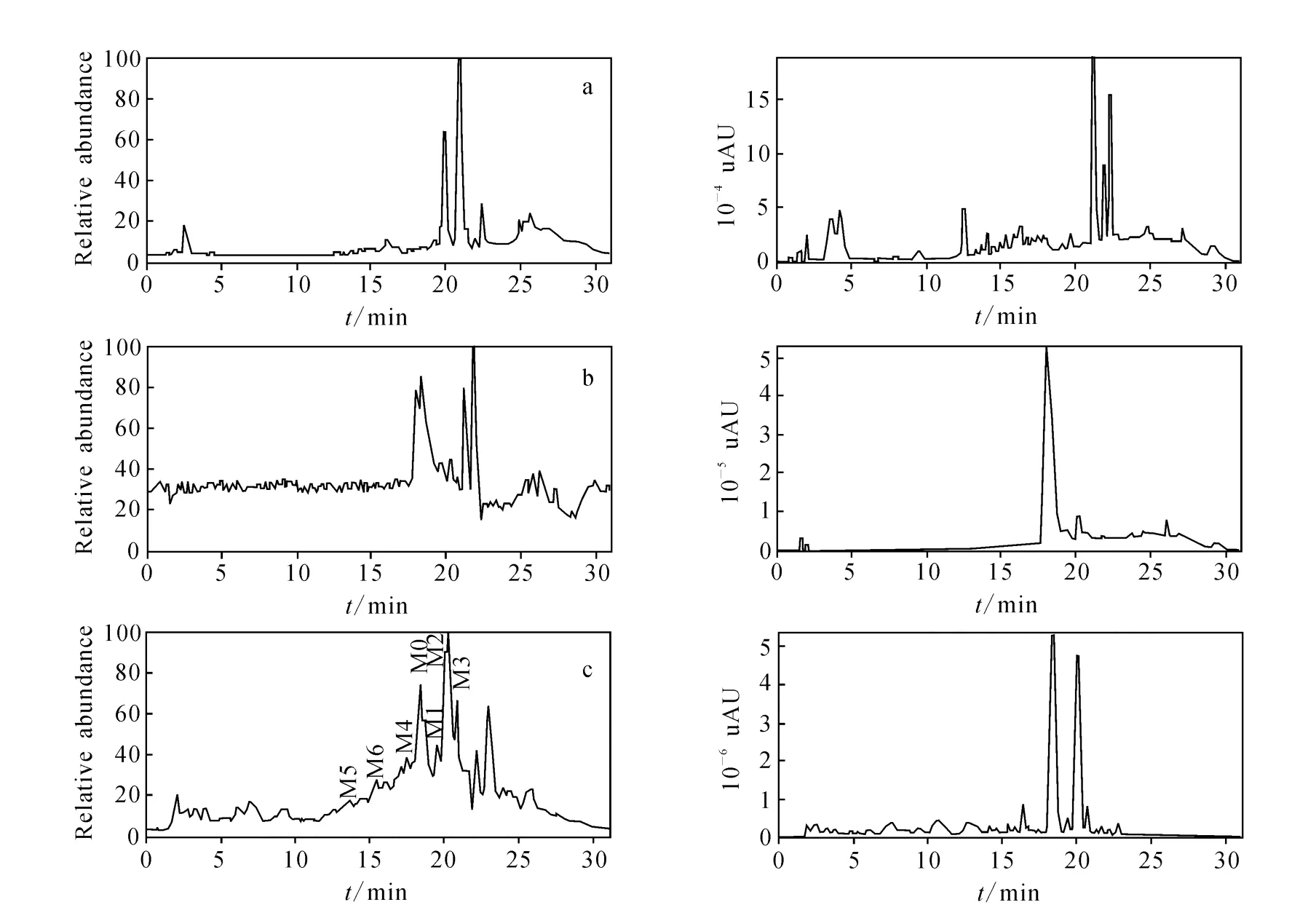
图1 尿样经SPE预处理后的 HPLC-UV和TIC图a.空白鼠尿;b.添加落新妇苷标准品的空白鼠尿;c.静注给药落新妇苷后的鼠尿样Fig.1 HPLC-UVand TIC chromatograms of SPE extract a.blank rat urine;b.blank rat urine spiked with an astilbin standard;c.urine sample after intravenous administration of astilbin
2.2 落新妇苷M0及其代谢产物M1
负离子电喷雾质模式下,扫描落新妇苷的准分子离子峰为[M-H]-m/z449,色谱保留时间为18.4 min,经碰撞诱导解离(CID),其产生的碎片离子为m/z303、285、179及151,示于图2。m/z449丢失鼠李糖(Rha,146,C6H10O4)产生碎片离子m/z303,其进一步碎裂产生碎片离子m/z285和m/z179,分别丢失了 18 u(H2O)和124 u(C6H4O3)。m/z179进一步碎裂产生m/z151,丢失28 u(CO)。代谢物M1的色谱保留时间为19.5 min,其裂解过程及产生的碎片与落新妇苷一致,所以推断M1为落新妇苷的同分异构体。落新妇苷及其代谢产物M1的二级质谱裂解途径示于图3。有研究报道,在土茯苓提取物中,落新妇苷还有3个同分异构体,分别为新落新妇苷、异落新妇苷、新异落新妇苷[9-10]。本实验发现,落新妇苷在体内可以转化为它的同分异构体。
2.3 落新妇苷代谢产物M2和M3
落新妇苷代谢产物M2、M3的色谱保留时间分别为20.2 min和 20.9 min,它们的准分子离子峰为[M-H]-m/z463,比落新妇苷[MH]-的m/z高14 u,经碰撞诱导解离反应产生一系列的碎片离子,分别为m/z317、299、289、179和151,示于图4。m/z463丢失 Rha产生碎片离子m/z317,其进一步碎裂产生m/z299、289和 179碎片离子,它们分别丢失 18 u(H2O),28 u(CO)和138 u(C2H2O)。m/z179丢失28 u(CO)产生碎片离子m/z151。结果表明,M2和M3分别是落新妇苷及其同分异构体的甲基化产物。有文献[8]鉴定,落新妇苷灌胃给药大鼠后,鼠尿中的甲基化代谢产物为3′-O-甲基-落新妇苷。落新妇苷及其同分异构体的甲基化代谢物的质谱裂解途径示于图5。
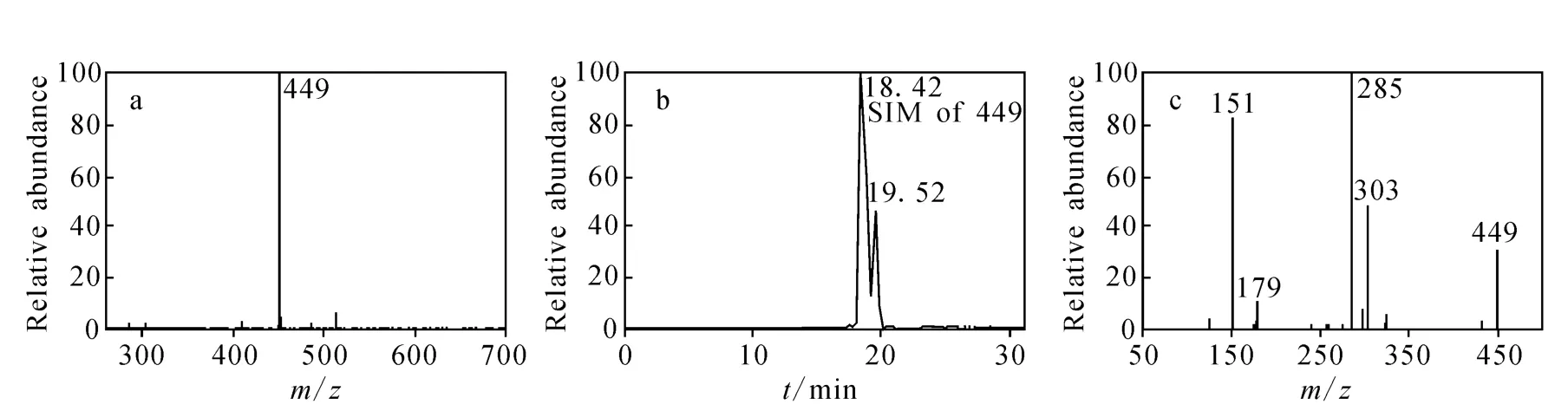
图2 落新妇苷及其异构体(M0,M1,m/z449)的 HPLC-MS/MS图a.扫描质谱图;b.SIM色谱图;c.CID碎片离子Fig.2 HPLC-MS/MS spectrum of astilbin and its stereoisomer(M0 and M1,m/z449)a.mass scan spectra;b.selected ion monitoring(SIM)chromatogram;c.CID product ion spectra
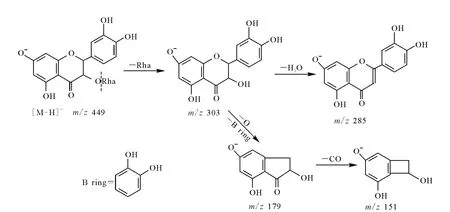
图3 落新妇苷m/z449离子的可能裂解机理Fig.3 Proposed decomposition process ofm/z449[M-H]-ion of astilbin
2.4 落新妇苷代谢产物M4
代谢产物M4的准分子离子峰为[M-H]-m/z447,色谱保留时间为17.4 min。经碰撞诱导解离后产生的碎片离子m/z301,它是m/z447丢失Rha产生的,示于图6。m/z447比落新妇苷[M-H]-的m/z少2 u,即m/z449丢失2 u(H2)。因此推断落新妇苷在体内进行了脱氢反应,这样二氢黄酮苷氧化为黄酮苷,推断M4为槲皮素-鼠李糖苷,并且有文献[11]报道槲皮素-鼠李糖苷的多反应监测离子对为m/z447/301,这与图 6c中m/z447的 CID图谱相符。
2.5 落新妇苷代谢产物M5
代谢产物M5的液相色谱保留时间为12.6 min,准分子离子峰为[M-H]-m/z625,比落新妇苷[M-H]-的m/z高176 u,示于图7。经碰撞诱导解离M5产生一系列的碎片离子m/z449、303和285,相应为落新妇苷[M-H]-及其碎片的质谱峰,而且葡萄糖醛酸基团的特征峰为m/z176,因此代谢物M5鉴定为葡萄糖醛酸化落新妇苷。文献[8]报道大鼠灌胃给药落新妇苷后,在鼠胆汁中发现了葡萄糖醛酸化落新妇苷,但在血浆和尿样中未发现该代谢物。
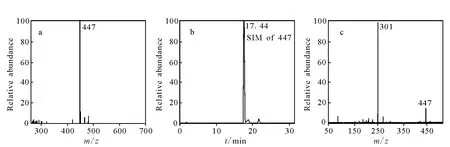
图6 槲皮素-鼠李糖苷(M4,m/z447)的 HPLC-MS/MS图a.扫描质谱图;b.SIM色谱图;c.CID碎片离子Fig.6 HPLC-MS/MS spectrum of quercetin rhamnoside(M4,m/z447)a.mass scan spectra;b.selected ion monitoring(SIM)chromatogram;c.CID product ion spectra
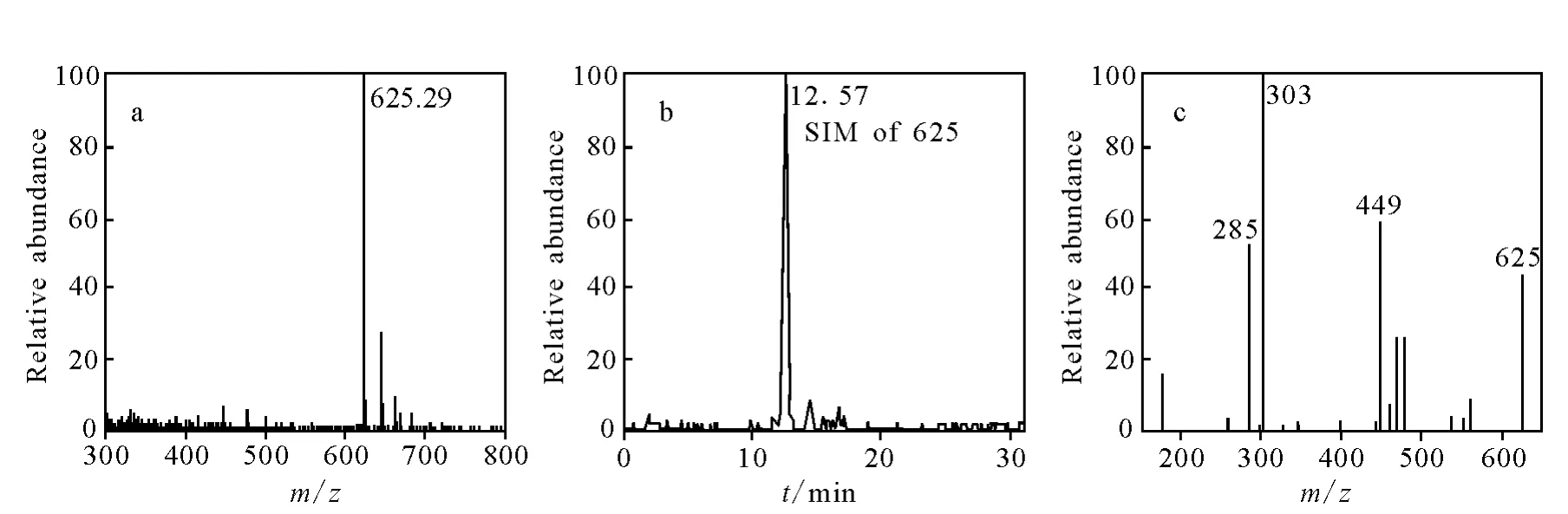
图7 葡萄糖醛酸化落新妇苷(M5,m/z625)的 HPLC-MS/MS图a.扫描质谱图;b.SIM色谱图;c.CID碎片离子Fig.7 HPLC-MS/MS spectrum of astilbin glucuronide(M5,m/z625)obtained using negative ion electrospray and CID a.mass scan spectra;b.selected ion monitoring(SIM)chromatogram;c.CID product ion spectra
2.6 落新妇苷代谢产物M6
代谢产物M6的液相色谱保留时间为13.5 min,其准分子离子峰为 [M-H]-m/z639,比甲基化落新妇苷[M-H]-高176 u。经碰撞诱导解离后,M6产生一系列碎片离子m/z463、317、299和289,它们为甲基化落新妇苷及其碎片的离子峰,示于图8。因此,推断代谢物 M6为甲基化落新妇苷的葡萄糖醛酸化物,即3′-O-甲基-落新妇苷-葡萄糖醛酸化物。
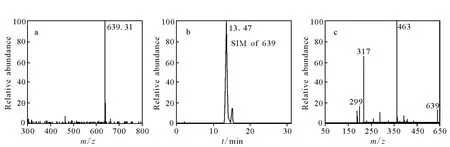
图8 甲基化落新妇苷的葡萄糖醛酸化物(M5,m/z639)的 HPLC-MS/MS图a.扫描质谱图;b.SIM色谱图;c.CID碎片离子Fig.8 HPLC-MS/MS spectrum of methylastilbin glucuronide(M6,m/z639)a.mass scan spectra;b.selected ion monitoring(SIM)chromatogram;c.CID product ion spectra
3 结论
落新妇苷静脉注射给药大鼠后,鼠尿样经聚酰胺固相萃取小柱处理后,采用 HPLC-MS/MS法鉴定的落新妇苷代谢产物主要为落新妇苷异构体 (M1)、3′-O-甲基-落新妇苷 (M2)、3′-O-甲基-落新妇苷异构体(M3)、槲皮素-鼠李糖苷(M4)、葡萄糖醛酸化落新妇苷(M5)和 3′-O-甲基-落新妇苷-葡萄糖醛酸化物(M6)。落新妇苷在大鼠体内的代谢途径推断示于图9。M2和M5有文献[8]报道,其余4种代谢产物 (M1、M3、M4、M6)未在鼠尿中落新妇苷代谢物的报道中发现,表明落新妇苷在鼠体内除发生了甲基化和葡萄醛酸化代谢反应外,还可进行异构化和脱氢化代谢反应。推测落新妇苷的代谢途径有助于理解落新妇苷的作用机制,并为以后的临床试验提供有益信息。

图9 落新妇苷在鼠体内的可能代谢途径Fig.9 Proposed metabolic pathw ay of astilbin in vivo in the rat
[1]易以军,曹正中,杨大龙,等.土茯苓化学成分研究(Ⅳ)[J].药学学报,1998,33(11):873-875.
[2]陈广耀,沈连生,江佩芬.土茯苓中二氢黄酮醇苷的研究[J].中国中药杂志,1996,21(6):355-357.
[3]MOULARIB,PELLEQUER Y,LBOUTOUNNE H,et al.Isolation and in vitro antibacterial activity of astilbin,the bioactive flavanone from the leaves ofHarunganamadagascariensisLam. ex Poir.(Hypericaceae)[J].J Ethnopharmacol,2006,106:272-278.
[4]CHINEN J,FINKELMAN F,SHEARER W T.Advances in basic and clinical immunology[J].J Allergy Clin Immunol,2006,118:489-495.
[5]SA F,GAO J L,FUNG K P,et al.Anti-proliferative and pro-apoptotic effect ofSmilax glabraRoxb.extract on hepatoma cell lines[J].Chem Biol Interact,2008,171:1-14.
[6]CAI Y,CHEN T,XU Q.Astilbin suppresses collagen-induced arthritis via the dysfunction of lymphocytes[J].Inflamm Res,2003,52:334-340.
[7]GUO J,XU Q,CHEN T.Quantitative determination of astilbin in rabbit plasma by liquid chromatography[J].J Chromatogr B Analyt Technol Biomed Life Sci,2004,805:357-360.
[8]GUO J,QIAN F,LI J,et al.Identification of a new metabolite of astilbin,3’-O-methylastilbin,and its immunosuppressive activity against contact dermatitis[J]. Clin Chem,2007,53 (3):465-471.
[9]袁久志,窦德强,陈英杰,等.土茯苓二氢黄酮醇类成分研究[J].中国中药杂志,2004,29(9):867-870.
[10]王映红,李 磊,张宏桂,等.HPLC-MS与 HPLC-1H-NMR联用鉴定土茯苓中的二氢黄酮醇苷异构体[J].中国中药杂志,2008,33(11):1 281-1 284.
[11]潘 见,杨 毅,夏潇潇,等.高效液相色谱-串联质谱测定砀山酥梨中的酚类物质[J].食品科学,2006,27(12):578-581.
Identification of the Major Metabolites of Astilbin in Rat Urine by HPLC-MS/MS
WANG Wen-yan1,TONG Yao-yao1,ZHANG Lin-qi1,SONGJi-lun2,LI Gui-sheng1,2,LIU Wan-hui1
(1.School ofPharmacy,Yantai University,Yantai264005,China;2.Research Center of N atural Medicine of Shandong L uye Pharmaceutical,Yantai264005,China)
To identify the major metabolites of astilbin in rats,urine samples were collected after intragastric administration of astilbin.The urine samples were pretreated by solidphase extraction using polyamide cartridges,and then were analyzed by high performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS).Electrospray ionization source operated in negative mode for scan and collision induced dissociation were used to elucidate the structures of the major metabolites of astilbin.The data indicated that the main urine metabolites of astilbin are stereoisomers of astilbin(M1),3′-O-methylastilbin(M2),a stereoisomer of 3′-O-methylastilbin(M3),quercetin rhamnoside(M4),astilbin glucuronide(M5),3′-O-methylastilbin glucuronide(M6).Metabolites of M1,M3,M4 and M6 are reported from rat urine.
book=37,ebook=37
astilbin;metabolite;high performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS);polyamide solid-phase extraction
O 657.63
A
1004-2997(2011)01-0036-07
2010-01-27;
2010-05-31
王文艳(1976~),女(蒙古族),内蒙古赤峰人,博士,讲师,从事药物代谢动力学研究。
E-mail:wangwenyan345@yahoo.com.cn
刘万卉(1964~),男(土家族),湖南人,博士,教授,从事药物分析研究。E-mail:PAL05@ytu.edu.cn

