四-β-(氨甲基)酞菁锌盐酸盐的合成及光物理光化学性质研究
许秀枝 王 艰 李柱来*, 严文锦 蚩会丽 陈文斌 卓世昌 陈耐生
(1福建医科大学药学院,福州 350004)(22007级福建医科大学药学院药物分析本科生,福州 350004)(3福州大学功能材料研究所,福州 350002)
四-β-(氨甲基)酞菁锌盐酸盐的合成及光物理光化学性质研究
许秀枝1王 艰1李柱来*,1严文锦1蚩会丽1陈文斌2卓世昌2陈耐生*,3
(1福建医科大学药学院,福州 350004)(22007级福建医科大学药学院药物分析本科生,福州 350004)(3福州大学功能材料研究所,福州 350002)
四-β-(邻苯二甲酰亚胺甲基)酞菁锌(ZnPcP4)与85%水合肼反应得到四-β-(氨甲基)酞菁锌(ZnPcN4,分子式C36H28N12Zn),其盐酸盐为ZnPcN4·HCl。测试合成得到的标题化合物紫外-可见电子吸收光谱,荧光光谱和单线态氧生成速率。标题化合物在水中聚集,在90%1,2-丙二醇/水中主要以单体形式存在。目标酞菁锌配合物在90%DMF/水的中性溶液存在聚集体,在弱酸性条件下,随酸度增大,675 nm处Q带单体吸收峰升高,在DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)溶液中10-5mol·L-1的酞菁配合物基本上没有聚集;在强酸性条件下,随酸度增大,675 nm处Q带单体吸收峰下降的同时,在713 nm处酞菁单质子化吸收峰强度有所增加。ZnPcN4·HCl在DMF体系中聚集,荧光量子产率和单线态氧量子产率变小,但其在DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)体系中主要以单体形式存在,荧光量子产率为0.19,单线态氧量子产率0.58,光敏活性与标准无取代酞菁锌相近。
酞菁锌;聚集;单线态氧;质子化
光动力治疗(PDT)是目前公认的有效治疗癌症的方法之一,光动力治疗的关键物质是光敏剂。在化学合成的光敏剂中,酞菁类被认为是最有希望的新一代光敏剂之一。理想的光敏剂应具备以下特点[1]:①组分单一,结构明确,性质稳定;②在光照时具有强的光毒性,对机体无副作用、安全;③与正常组织相比,在靶组织内有相对的选择性摄取,而又不会在体内滞留过久;④光敏活性高,其三线态寿命长,产生1O2而且产率高;⑤在治疗窗口(600~900 nm)有强吸收,以利于治疗时使用对人体组织穿透较深的波长;⑥在生理pH值可溶解。由于酞菁环上取代基影响到药物在体内的转运和肿瘤组织对药物的摄取以及穿透癌细胞的能力等,因此,它是决定其性能的重要因素,如何进一步提高光敏剂对病变组织的靶向性是目前研究的热点之一。亲脂性酞菁难代谢,易造成皮肤光毒性[2],水溶性或两亲性酞菁如磺基、羧基、膦基等取代的阴离子型[3-10]和吡啶基、喹啉基、二甲胺基乙氧基等取代的阳离子型[11-15]等,带正电性的光敏剂可直接作用于线粒体,有利于癌症治疗。取代基中两亲性基团既可与白蛋白结合有助于其在体内输运,又能提高被病变组织摄取能力。基于这个认识,具有两亲性的氨基与蛋白质间可能有强的相互作用,并能共价连接到单克隆抗体上,而引起人们的关注。本文选择邻苯二甲酰亚胺作为氨基的前驱体,缩合得到的酞菁配合物通过水合肼转化成氨甲基取代酞菁,其盐酸盐为 ZnPcN4·HCl(Scheme 1),对其光物理和光化学性质进行了初步的研究。
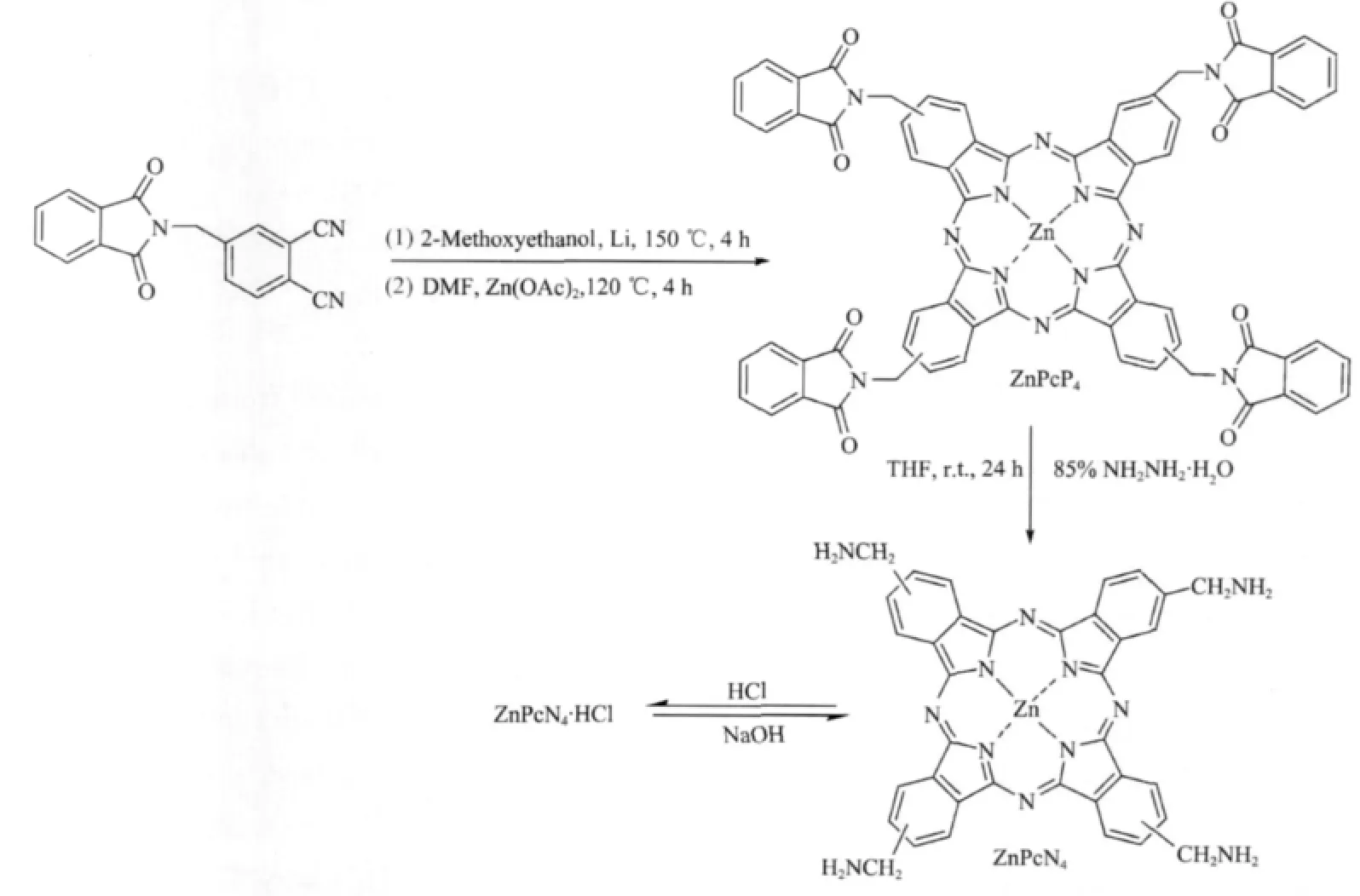
Scheme 1 Synthesis of β-tetrakis(aminomethyl)phthalocyaninato zinc(Ⅱ) and its hydrochloride
1 实验部分
1.1 仪器与试剂
仪器:傅立叶变换红外光谱仪(美国 Perkin-Elmer公司);UV-2450型紫外可见分光光度计(日本岛津公司);970-CRT荧光分光光度计(上海精密科学仪器有限公司);Vario ELⅢ型元素分析仪(德国Element公司);DECAX-30000 LCQ Deca XP 液质电喷雾离子阱质谱仪(德国ThermoFinnigan公司);FDLCE-1型液晶电光效应实验仪(上海复旦天欣科教仪器有限公司);LC-20AT高效液相色谱分析仪(日本岛津公司,SPD-20A紫外检测器)。
试剂:9,10-二甲基蒽(DMA)(德国 Augsburg公司,纯度99%)和酞菁锌(ZnPc)为(Alfa Aesar公司,纯度95%)由福建医科大学药学院黄丽英课题组提供。邻苯二甲酰亚胺甲基邻苯二甲腈为实验室自制,DMF、甲醇等其他试剂由国药集团化学试剂有限公司生产,均为分析纯试剂。实验用水为双蒸水。
1.2 合 成
四-β-(邻苯二甲酰亚胺甲基)酞菁锌(ZnPcP4)的合成:根据文献[16],于500 mL三口烧瓶中,加入新蒸的干燥乙二醇乙醚250 mL和金属锂120 mg,5 g邻苯二甲酰亚胺甲基邻苯二甲腈,升温至150℃,反应4 h。反应结束后,减压蒸出溶剂,后往溶液中加入300 mL DMF和20 g无水醋酸锌,在120℃反应4 h,减压蒸馏除去大部分溶剂后冷却至室温。将残余液直接转移到硅胶柱上进行纯化,用四氢呋喃进行洗脱收集主要组分,减压浓缩后再次经硅胶柱纯化,最后残留物用DMF进行洗脱,两组分分别用甲醇析出,过滤,甲醇洗涤,干燥,共得产物2 g,记为ZnPcP4。 IR ν(cm-1):2 926,2 854(-CH2-),1 771,1 716(邻苯二甲酰亚胺,C=O),1 392,1 338,1 165,1 100,950,727 cm-1。红外光谱的数据与目标产物相符。
四-β-(氨甲基)酞菁锌(ZnPcN4)的合成:参照文献[17-18],于250 mL三口烧瓶中,将酞菁锌配合物ZnPcP4(1.09 g,0.9 mol)和肼(2.4 mL,77 mmol)加入到100 mL THF中,室温搅拌24 h,旋转蒸发除去溶剂。 将所得固体溶于 0.1 mol·L-1HCl中,过滤除去白色固体,所得蓝色滤液用0.1 mol·L-1NaOH溶液调节至pH值为7。静置24 h,过滤,所得滤饼水洗2次,甲醇洗涤3次。固体40℃真空干燥后,称重,计算产率(0.67 g,90%)。 IR ν:3430~3240(NH),2 925,2849(-CH2-),1666,1612,1574,1489,1382,1336,1094,1052,1100,927,831,745 cm-1。 m/z:693(MH)+。 元素分析按 C36H28N12Zn 的计算值(%):C(62.30),H(4.07),N(24.22); 实 验 值 (%):C(62.09),H(4.31),N(24.14)。
四-β-(氨甲基)酞菁锌盐酸盐(ZnPcN4·HCl)的合成:取上述合成得到的四-β-(氨甲基)酞菁锌(ZnPcN4)0.2 g,用 0.1 mol·L-1HCl溶解,加入 1 倍量的无水乙醇减压蒸干,然后加入甲苯通过减压蒸馏除去残余的水和盐酸,固体40℃真空干燥。产物记为ZnPcN4·HCl。产物通过HPLC检测为单一组分(图1):配制一定浓度的此酞菁锌化合物水溶液,取20 μL 进 样 , 用 YMC-Triart C18(4.6×150 mm,S-5 μm,12 nm)色谱柱进行分析,洗脱液为 1.2 mmol·L-1HCl和乙腈混合溶液,流速 1.0 mL·min-1,采用梯度洗脱,675 nm检测。具体流程设置见表1。

表1 ZnPcN4·HCl色谱分析流程表Table 1 Analysis flow-sheet of ZnPcN4·HCl by HPLC
1.3 紫外-可见电子吸收光谱测定
分别配制 ZnPcN4·HCl的水母液(1 mmol·L-1)。
不同溶剂体系中标题酞菁锌配合物溶液的配制:从母液中各取50 μL于10 mL容量瓶中,分别加入不同溶剂配制溶液用于紫外-可见电子吸收光谱测定。(1)加入 9 mL DMF,用水定容;(2)加入 9 mL 1,2-丙二醇, 用水定容;(3) 加入 2 mL 1,2-丙二醇,0.2 mL CEL,用水定容;(4)直接加水定容。
不同酸度体系中标题酞菁锌配合物溶液的配制:从母液中各取50 μL于10 mL容量瓶中,加入9 mL DMF,然后分别加入不同浓度的盐酸溶液,最后用水定容。
不同浓度标题酞菁锌配合物溶液的配制:从母液中各取 5.5、27.5、55、110、165 μL 于 10 mL 容量瓶 中 , 加 入 9 mL DMF,0.12 mol·L-1HCl 溶 液100 μL,用水定容。
实验在室温下进行。
1.4 荧光量子产率测定
配制 ZnPcN4·HCl的 DMF 母液(0.5 mmol·L-1)。采用稀释法配制 ZnPcN4·HCl(2.5 μmol·L-1)的 DMF溶液:从母液中取50 μL于10 mL容量瓶中,用DMF 定容。 ZnPcN4·HCl/DMF/water(10%,V/V)/HCl(1.2 mmol·L-1) 溶液的配制: 从母液中取 50 μL 于10 mL 容量瓶中, 加入 8.95 mL DMF,0.12 mol·L-1HCl溶液100 μL,用水定容。以610 nm为荧光激发波长,在室温(15~30℃)下,扫描荧光发射光谱。以ZnPc为标准物,采用下式求出ZnPcN4·HCl在不同溶剂体系中的荧光量子产率(ΦF)[19]。
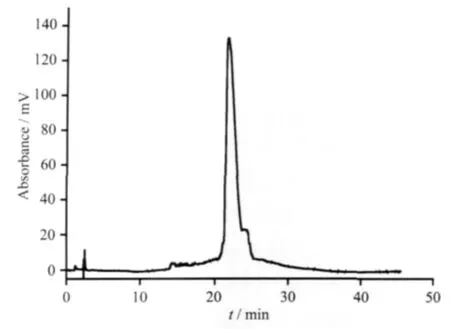
图1 产物ZnPcN4.HCl的高效液相色谱图Fig.1 HPLC chromatograms of ZnPcN4·HCl
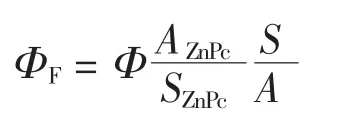
式中:Φ:ZnPc的荧光量子产率,以DMF为溶剂 Φ =0.32[20], 以 DMF/water(10% ,V/V)/HCl(1.2 mmol·L-1)为溶剂 Φ=0.28[21];ΦF:ZnPcN4·HCl的荧光量子产率;AZnPc:标准物ZnPc在610 nm处的吸光度;SZnPc:标准物ZnPc荧光发射光谱的积分面积;A:ZnPcN4·HCl在 610 nm 处的吸光度;S:ZnPcN4·HCl荧光发射光谱的积分面积。
1.5 单线态氧测定条件
本文以DMA为1O2捕获剂,DMA可以选择性地与1O2作用形成稳定性强的化合物(9,10-二甲基-9,10-二氢-9,10-环二氧蒽), 其在 374 nm 处无紫外吸收,该反应过程如下:

1.5.1 供试品及标准物ZnPc溶液的制备
配制 ZnPc 的 DMF 母液(0.5 mmol·L-1);DMA 的DMF 溶液(0.15 mmol·L-1)。ZnPcN4·HCl的 DMF 母液(0.5 mmol·L-1)为上述 1.4 中配制。
体系1:分别采用稀释法配制ZnPc+DMA(5 μmol·L-1,74.5 μmol·L-1) 和 ZnPcN4·HCl+DMA(5 μmol·L-1,74.5 μmol·L-1)溶液:从各自母液中取 100 μL 于 10 mL 容量瓶中,各加入 DMA(0.15 mmol·L-1)的DMF母液5 mL,用DMF定容。然后从中各取出3.00 mL于紫外-可见电子吸收光谱用比色皿中,置于下述1.5.2光照装置槽中进行测定。
体系2:分别采用稀释法配制ZnPc+DMA(5 μmol·L-1,74.5 μmol·L-1)/DMF/water(10% ,V/V)/HCl(1.2 mmol·L-1) 和 ZnPcN4·HCl+DMA(5 μmol·L-1,74.5 μmol·L-1)/DMF/water(10% ,V/V)/HCl(1.2 mmol·L-1)溶液:分别从母液中取100 μL于10 mL容量瓶中,各加入 DMA(0.15 mmol·L-1)的 DMF 母液5 mL、3.9 mL DMF、0.12 mol·L-1HCl溶液 100 μL,用水定容。然后从中各取出3.00 mL于紫外-可见电子吸收光谱用比色皿中,置于下述1.5.2光照装置槽中进行测定。
DMA 空白溶液的配制:(1)从 DMA(0.15 mmol·L-1)的DMF母液中取5 mL于10 mL容量瓶中,用DMF定容,用于体系1的对照实验;(2)从DMA(0.15 mmol·L-1)的DMF母液中取5 mL于10 mL容量瓶中, 然后加入 4 mL DMF、0.12 mol·L-1HCl溶液100 μL,用水定容,用于体系2的对照实验。从中各取出3.00 mL于紫外-可见电子吸收光谱用比色皿中,置于下述1.5.2光照装置槽中进行测定。
1.5.2 光照装置
此装置由福建医科大学药学院黄丽英课题组提供[22]。将所配溶液精密量取3.00 mL于光路径为1 cm石英比色皿中,在空气中,以100 W碘钨灯光为照射光源,光线经循环水槽滤去紫外和红外辐射、一组凸透镜将光源转化为平行光、一块650 nm的玻璃滤光片至石英比色皿。光功率用液晶电光效应实验仪测定为80 mW·cm-2。
1.5.3 UV-Vis法测定单线态氧量子产率
室温条件下(15~30℃),所配置的供试品及对照品溶液经过上述光照装置照射,每隔5 min测定供试品及对照品溶液中吸光度的变化(即在401 nm处吸光度的变化)[23]。DMA的消耗速率符合一级动力学,可用如下方程[24]表示:

(1)式中:A0:起始浓度吸光度;At:某一时刻吸光度;t:光照射时间;KDMA:DMA 消耗速率常数。光敏剂吸收光子的速率Kpho(The rate of absorption of photons by the sensitizer,Kpho),可以用下式求得[24]:
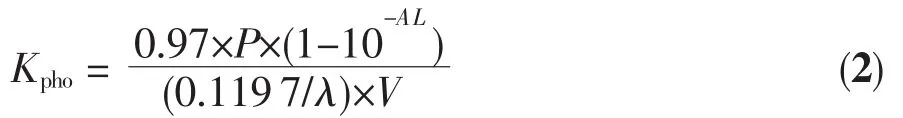
(2)式中:P:光照装置照射于样品上的光功率(mW);A:光敏剂于固定波长λ处的吸光度;λ:光照装置照射于样品上的光波长即650 nm;L:光束照射在样品上的光路径长度(1 m);V:样品的体积(mL);因子0.97是激光在空气和玻璃接触面反射光的校正系数。因子0.119 7/λ是1 mol光子的能量,也称为一爱因斯坦。
单线态氧的量子产率与DMA消耗的速率及光敏剂吸收光子的速率的比值成正比,即与KDMA/Kpho成正比。已知光敏剂ZnPc在DMF溶液中的ΦΔ=0.56[21,23], 通过以下公式计算即可算出 ZnPcN4·HCl的单线态氧量子产率:
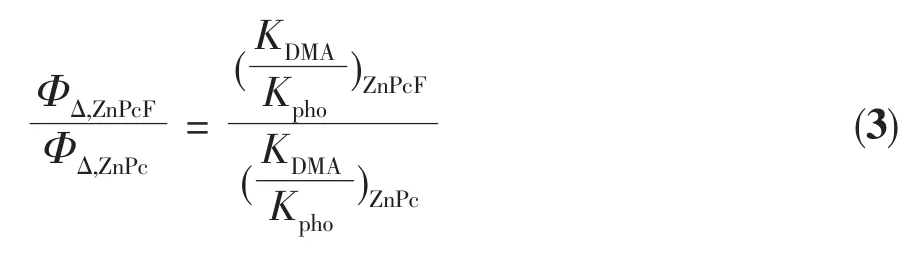
2 结果与讨论
2.1 紫外-可见电子吸收光谱
图2是ZnPcN4·HCl在水溶液及混合溶液中的紫外-可见电子吸收光谱。酞菁及金属配合物电子吸收光谱在200~400 nm和600~800 nm有2个很强的吸收带,分别称为B带和Q带,分别对应于其电子能级中的a2u→eg跃迁和a1u→eg跃迁。标题酞菁锌配合物在长波长方向有2个典型的特征吸收峰,632 nm处是酞菁聚集体的吸收峰,675 nm处为酞菁Q带单体吸收峰[25-27]。标题配合物易溶于水,其可见吸收光谱见图2a,单体的吸收峰强度明显低于聚集体,说明在水溶液中产生了严重的聚集。含O配位基团溶剂(ROH、DMF等)对酞菁的聚集有解聚作用(图 2,b、c、d):90%1,2-丙二醇/H2O 中主要以单体形式存在,90%DMF/H2O和 20%1,2-丙二醇/2%CEL/H2O中单体聚集体共存。从吸收峰的强度来看,同等比例条件下 1,2-丙二醇/H2O混合液对聚集体的解聚作用要优于DMF/H2O混合液;1,2-丙二醇/H2O混合液中随着醇含量增加,水含量减少,675 nm处的吸收峰升高,632 nm处吸收峰降低,表明聚集体浓度随着水含量减少而逐渐减少。上述实验表明水在酞菁聚集过程中起了主要作用。
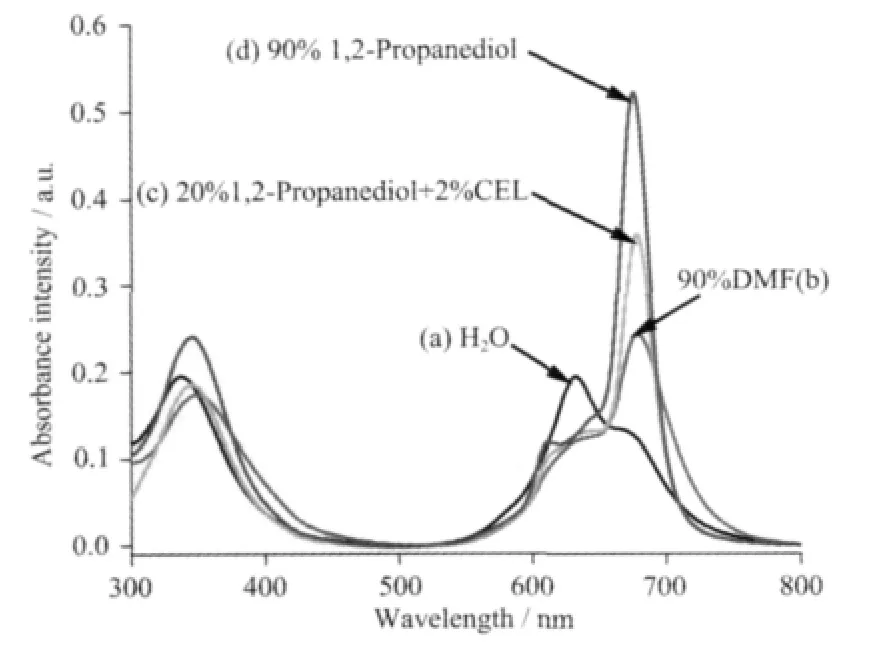
图 2 ZnPcN4·HCl(5 μmol·L-1)在不同溶剂中的紫外-可见电子吸收光谱Fig.2 UV-Vis spectra of ZnPcN4·HCl(5 μmol·L-1)in different solvents
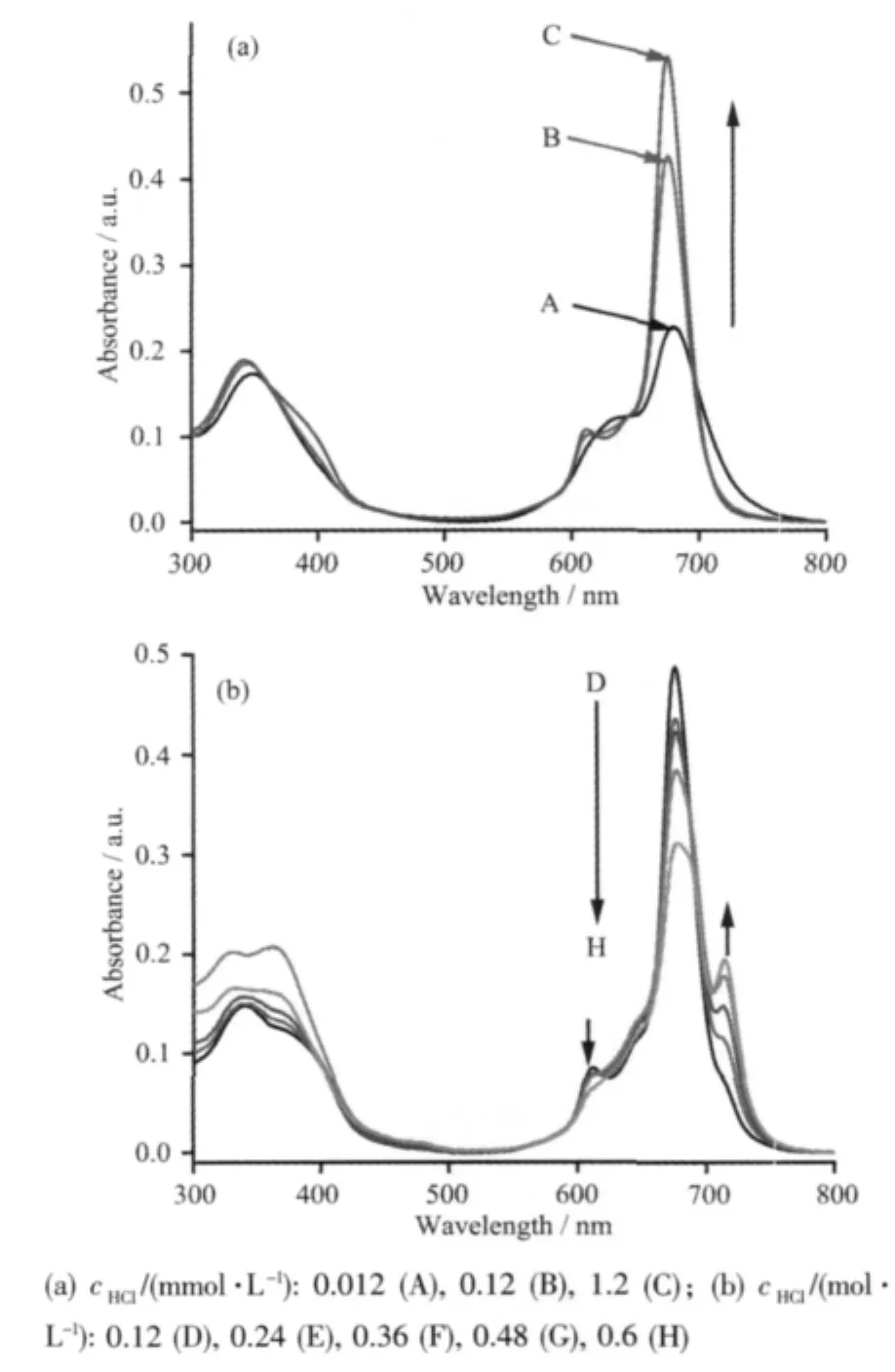
图 3 ZnPcN4·HCl(5 μmol·L-1)/DMF/water(10%,V/V)/HCl在不同酸度值中的紫外-可见电子吸收光谱Fig.3 UV-Vis spectral changes observed on increase in acidity of ZnPcN4·HCl in DMF/water(10%,V/V)/HCl system
图 3 是 ZnPcN4·HCl(5 μmol·L-1)/DMF/water(10%,V/V)/HCl在不同pH值中的紫外-可见电子吸收光谱。从图3a中可以看出,在弱酸性条件下随着酸度的增大,675 nm处Q带单体吸收峰逐渐增强;从图3b中可以看出,在强酸性条件下随着酸度的增大,675 nm处Q带吸收峰逐渐降低的同时,在713 nm处出现新的吸收峰,且此新吸收峰强度随酸度增加逐渐增大,这个峰可以归属于酞菁外周氮原子质子化[24]。这些结果表明酸度对目标酞菁锌配合物在DMF/water(10%,V/V)混合溶液中的存在状态起了重要作用。
标题化合物在DMF/water(10%,V/V)混合溶液中虽然单体含量相对较大,但是单体与聚集体的吸光度比值相对较小,酞菁分子间聚集程度较大,虽然标题酞菁锌配合物周环上的氨基与盐酸作用形成盐酸盐,铵盐带正电荷可相互排斥,但只有4个正电荷仍未能阻止酞菁配合物的聚集[28]。随着酸度的增大,标题化合物在632 nm处聚集体的吸收峰强度逐渐减弱,在675 nm处单体的吸收峰强度逐渐增强,在pH值约为3时单体与聚集体的吸光度比值最大。可能是由于酸度增大,溶剂分子水或DMF中的O原子质子化,带正电荷溶剂分子促进酞菁分子间相互排斥作用,使目标酞菁锌配合物在DMF/water(10%,V/V)混合溶液中进一步解聚,当酸度增大到pH值约为3时,酞菁锌配合物主要以单体形式存在。
酞菁外周桥联的4个氮原子呈弱碱性,在酸性介质中能参与酸碱相互作用,可与1~4个H+结合形成质子化酞菁。
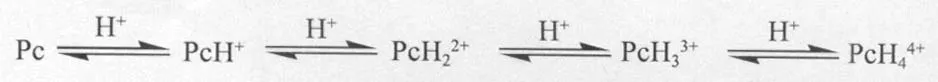
酞菁氮原子单质子化会导致Q带分裂和红移[21,29-31]。单质子化在~680 nm和~710 nm处有2个吸收带,如无取代酞菁锌在 DMF/H2SO41.84 mol·L-1介质中质子化光谱[29]。朱晓利[31]研究了在多种酞菁锌配合物CH2Cl2溶液中添加三氟乙酸紫外-可见电子吸收光谱和荧光光谱变化,随着三氟乙酸的增加,酞菁锌配合物的Q带单体吸收峰出现不同程度的下降,在Q带右侧方向出现新的单质子化吸收峰且强度逐渐增大。本文是在DMF/water(10%,V/V)混合溶液中添加盐酸,随着酸度增大,标题化合物也发生质子化,所测单质子化结果与文献报道的相一致。
图4为不同浓度的标题化合物在DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)中的紫外-可见电子吸收光谱图,图中标题酞菁锌配合物在675 nm处单体吸收峰强度随浓度增大逐渐增加,在所测浓度范围(10-5mol·L-1)中,酞菁单体的吸收峰强度和浓度的关系符合Beer-Lambert定律,结果表明标题化合物在 DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)弱酸性溶液体系中10-5mol·L-1浓度范围内基本没有聚集。
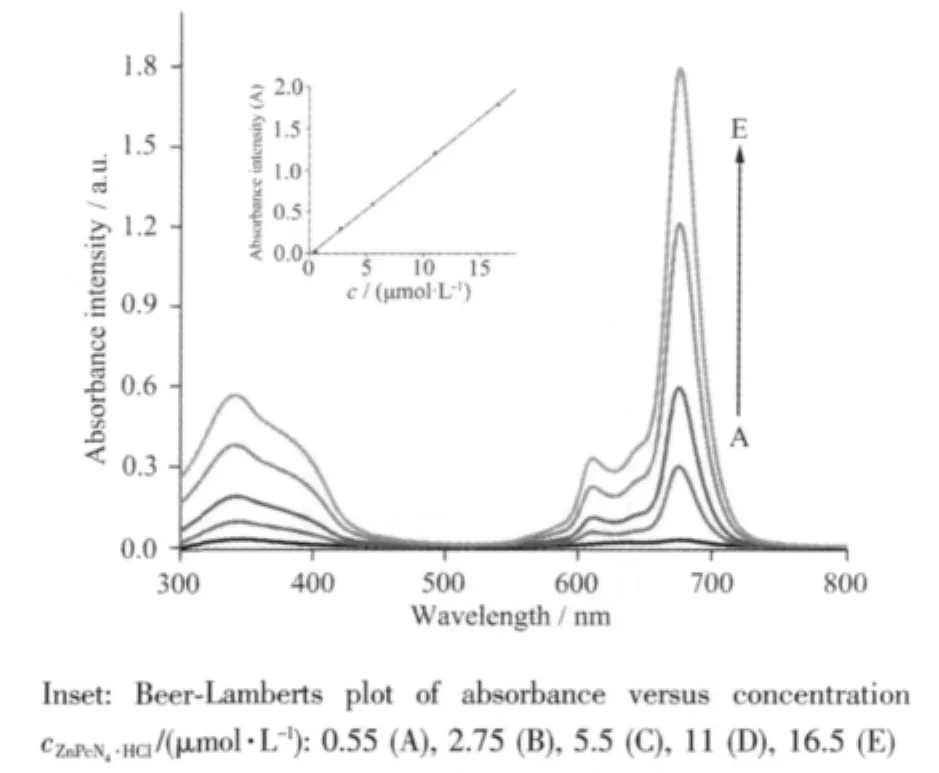
图 4 ZnPcN4·HCl/DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)不同浓度紫外-可见电子吸收光谱图Fig.4 UV-Vis spectral changes observed on increase in the concentration of ZnPcN4·HCl in DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)system
2.2 荧光量子产率
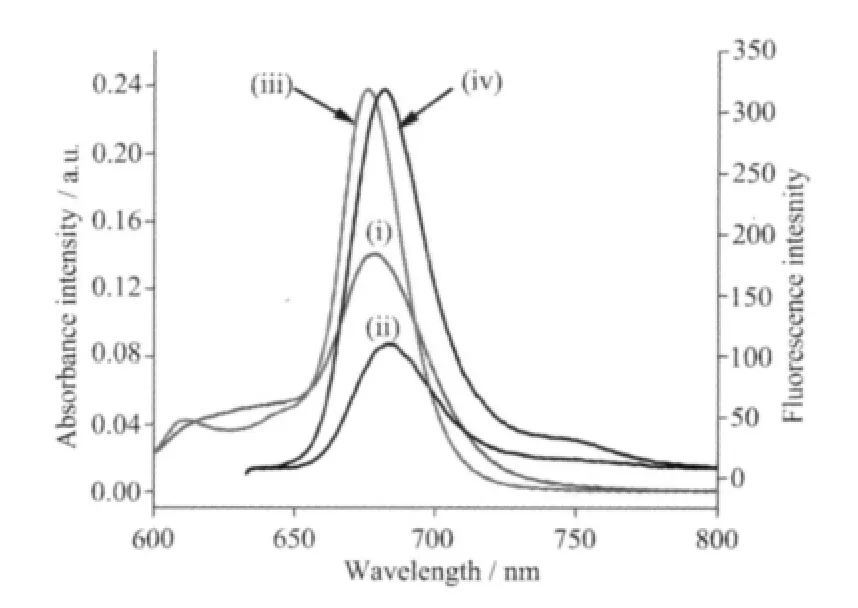
图5 (Ⅰ)和(Ⅱ)是ZnPcN4·HCl/DMF体系中的紫外-可见电子吸收光谱和荧光发射光谱(ⅲ)和(ⅳ)是ZnPcN4·HCl/DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)体系中的紫外-可见电子吸收光谱和荧光发射光谱(λex=610 nm)(cZnPcN4·HCl=2.5 μmol·L-1)Fig.5 Absorption spectra(ⅰ) and fluorescence emission spectra(ⅱ) of ZnPcN4·HCl in DMF.The absorption spectra(ⅲ) and fluorescence emission spectra(ⅳ)of ZnPcN4·HCl in DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)systems.(λex=610 nm)
图 5 是 ZnPcN4·HCl在 DMF 和 DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)体系中的紫外-可见电子吸收光谱和荧光发射光谱(λex=610 nm)图。标题化合物在纯DMF体系中会发生聚集(图5ⅰ),聚集体的存在会消耗激发态的能量,使得荧光发射强度下降(图5ⅱ),荧光量子产率降低(表2)。标题化合物在DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)体系中基本不聚集,Q带最大吸收光谱处紫外-可见电子吸收光谱和荧光光谱存在镜像对应关系(图5ⅲ,ⅳ),表2是其相应的激发单线态光物理数据,从表中可知标题化合物单体最大吸收波长675 nm,最大发射波长681 nm,荧光发射光谱较相应的吸收光谱略微红移,Stokes位移 6 nm。 荧光量子产率 0.19,ZnPcN4<ZnPc,说明标题化合物ZnPcN4·HCl第一激发单线态的荧光辐射跃迁概率相对无取代锌酞菁要小。这些结果与文献[28]报道的阳离子酞菁AzaPc性质相似。

表2 酞菁锌配合物ZnPcN4·HCl激发单线态光物理数据Table 2 Absorption,emission,fluorescence quantum yield values for ZnPcN4·HCl
2.3 单线态氧生成速率
图 6 是 ZnPcN4·HCl/DMA/DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)溶液吸光强度值随光照时间变化图。从图中可以看出所测含标题酞菁锌光敏剂的DMA溶液在360、380和401 nm处的吸光度值均随光照时间逐渐变小,标题配合物在401 nm处吸收很小,故可直接利用DMA在401 nm处的吸光度随时间变化作图,所测DMA溶液的吸光度值ln(A0/At)与光照时间呈一级动力学关系(图7,表3),线性拟合斜率为 KDMA+ZnPcN4·HCl=3.482 04×10-4s-1。 在此光照条件下,标题物酞菁锌基本不衰减,故可排除光敏剂本身光吸收的干扰。但空白DMA其在酸性DMF溶液中的有一定程度的衰减,衰减速率为KDMA=8.121 98×10-5s-1,因此不可以忽略DMA自身氧化带来的干扰。扣除DMA自身衰减,标题配合物ZnPcN4·HCl的衰减速率常数为 KZnPcN4·HCl=2.669 842×10-4s-1。 标题酞菁锌配合物和无取代酞菁锌ZnPc溶液于650 nm处的吸光度值分别为0.117 37和0.130 46,通过公式(2)(3)计算得 ΦΔZnPcN4·HCl=0.58,此单线态氧生成速率与无取代酞菁锌相近,说明酞菁周环烷基取代对酞菁光化学性质影响不大。
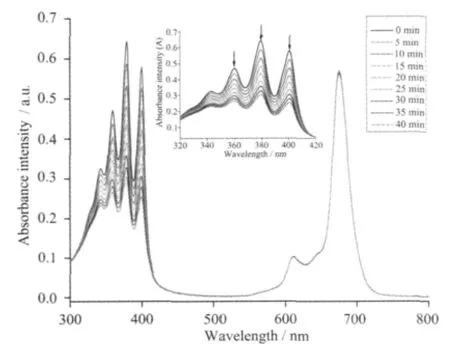
图6 ZnPcN4·HCl(5.0 μmol·L-1)/DMA(74.5 μmol·L-1)/DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)溶液吸光强度值随光照时间变化图Fig.6 A typical spectrum for the determination of singlet oxygen quantum yield of ZnPcN4·HCl in DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)using DMA as a singlet oxygen quencher.c(ZnPcN4·HCl)=5 μmol·L-1
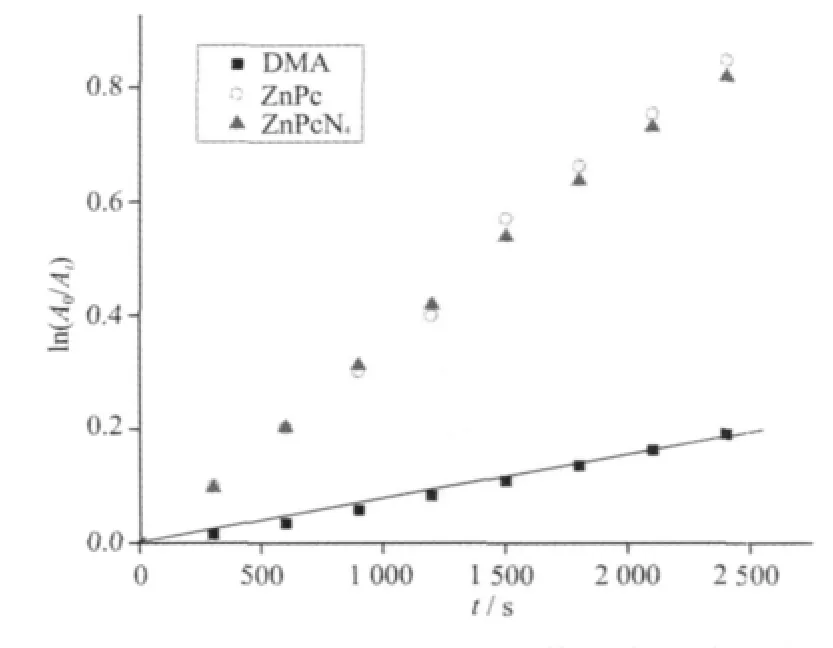
图7 DMA吸光度的ln(A0/At)值对光照时间图(λ=401 nm)Fig.7 Plots of ln(A0/At)vs.irradiation time for the photooxidation of DMA photosensitized by ZnPc and ZnPcN4·HCl(λ=401 nm)

表3 酞菁锌配合物光敏消耗DMA速率常数和单线态氧量子产率Table 3 Rate of photooxidation of DMA photosensitized by ZnPcN4·HCl and singlet oxygen quantum yield values
但是,ZnPcN4·HCl单线态氧量子产率在纯DMF体系中只有 0.19(表 2),相比在 90%DMF/10%H2O/HCl(1.2 mmol·L-1)体系中小得多,主要是由于标题配合物在DMF中大部分是以聚集体形式存在,单体含量少,聚集体的存在会消耗激发态的能量,激发态与单质氧作用几率减少,生成单线态氧能力下降。这与其在纯DMF溶剂中荧光量子产率小于在 DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)体系中的结果相一致,说明聚集对酞菁配合物的性质有很大影响。
3 结 论
通过Gabrie合成法合成得到氨甲基取代酞菁锌配合物(ZnPcN4),所得产物的盐酸盐ZnPcN4·HCl在水溶液中主要以聚集体存在,在90%1,2-丙二醇/H2O中主要以单体形式存在。目标酞菁锌配合物在90%DMF/水的中性溶液存在聚集体,但在弱酸性条件下,随酸度增大,675 nm处Q带单体吸收峰升高,在 DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)溶液中10-5mol·L-1的酞菁配合物基本没有聚集;在强酸性条件下,随酸度增大,675 nm处Q带单体吸收峰下降的同时,在713 nm处酞菁单质子化吸收峰强度有所增加。若ZnPcN4·HCl在DMF体系中聚集,则荧光量子产率和单线态氧量子产率变小,在主要以单体形式存在时,其荧光量子产率为0.19,单线态氧量子产率0.58,光敏活性与无取代酞菁锌相近。
[1]Lang K,Mosinger J,Wagnerová D M.Coord.Chem.Rev.,2004,248,321-350
[2]Jori G.J Photochem.Photobiol.B,Biol.,1996,36:87-93
[3]HUANG Jin-Ling(黄金陵),CHEN Nai-Sheng(陈耐生),HUANG Jian-Dong(黄剑东),et al.Sci.China Ser.B(Zhonggou Kexue B),2000,30(6):481-488
[4]Choi C F,Tsang P T,Huang J D,et al.Chem.Commun.,2004,2236-2237
[5]LU Shan(卢珊),WEI Shao-Hua(魏少华),ZHOU Jia-Hong(周家宏),et al.J.Nanjing Normal Univ.:Nat.Sci.(Nanjing Shida Xuebao),2006,29(1):59-61
[6]ZHANG Pei(张 沛),ZHANG Shu-Fen(张 淑 芬).Fine Chem Icals(Jingxi Huagong),2009,26(12):1240-1244
[7]Masilela N,Nyokong T.Dyes Pigm.,2010,84:242-248
[8]WEI Yan(魏彦),CHEN Wei(陈伟),WANG Yu(王玉),et al.Imag.Sci.Photochem.(Yingxiang Kexue Yu Guanghuaxue),2010,28(5):362-367
[9]HUANG Xian-Wen(黄显雯),LÜ Wang-Yang(吕汪洋),YAO Yu-Yuan(姚玉元),et al.J.Zhejiang Sci-Tech Univ.(Zhejiang Ligong Daxue Xuebao),2010,27(1):1-5
[10]Peng Y R,Lin P P,Lin J H,et al.Mater.Lett.,2009,63:914-916
[11]Murphy M P.J.Trends Biotechnol.,1997,15(8):326-330
[12]Li H R,Jensen T J,Fronczek F R,et al.J.Med.Chem.,2008,51:502-511
[13]CHEN Jin-Can(陈锦灿),CHEN Hong-Wei(陈宏炜),LI Yong-Dong(李永东),et al.Chem.J.Chinese Universities(GongdengXuexiaoHuaxueXuebao),2008,29(11):2131-2137
[14]Duan W B,Lo P C,Duan L,et al.Bioorg.Med.Chem.,2010,18:2672-2677
[15]LI Chun-Yan(李春艳),RUAN Guan-Yu(阮冠宇),SHAN Li(单丽),etal.J.FujianMed.Univ.(FujianYikeDaxueXuebao),2010,44(4):244-248
[16]XU Xiu-Zhi(许秀枝).Thesis for the Doctorate of Fuzhou University(福州大学博士论文).2006.
[17]Fernández D A,Dicelio L E,Awruch J.J.Heterocycl.Chem.,1995,32:519-522
[18]Rodríguez M E,Strassert C A,Dicelio L E,et al.J.Heterocycl.Chem.,2001,38:387-389
[19]Modibane D K,Nyokong T.Polyhedron,2009,28:479-484
[20]HUANG Zi-Yang(黄紫洋),HUANG Jian-Dong(黄剑东),CHENG Nai-Sheng(陈耐生),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(1):55-60
[21]Cormick M P,Rovera M,Durantini E D,et al.J.Photochem.Photobiol.A,2008,194:220-229
[22]WU Xiao-Shan(吴晓珊),HUANG Li-Ying(黄丽英),ZHANG Jin-Que(张锦雀).Chin.JMAP(Zhongguo Xiandai Yingyong Yaoxue),2010,27(10):864-868
[23]Kluson P,Drobek M,Kalaji A,et al.J Photochem.Photobiol.A,2008,199:267-273
[24]Lavi A,Weitman H,Holmes R T,et al.Biophys.J.,2002,82(4):2101-2110
[25]Dupouy E A,Lazzeri D,Durantini E N.Photochem.Photobiol.Sci.,2004,3:992-998
[26]Kostka M,Zimcik P,Miletin M,et al.J.Photochem.Photobiol.A,2006,178:16-25
[27]Erdoğmus A,Nyokong T.Dyes Pigm.,2010,86:174-181
[28]Zimcik P,Miletin M,Musil Z,et al.J.Photochem.Photobiol.A,2006,183:59-69
[29]LIU Jian-Bo(刘剑波),ZHAO Yu(赵瑜),ZHAO Fu-Qun(赵福群).Acta Phys.-Chem.Sin.(Wuli Huaxue Xuebao),1996,12(3):202-207
[30]Ogunsipe A,Nyokong T.J.Mol.Struct.,2004,689:89-97
[31]Zhu Xiao-Li(朱晓利).Thesis for the Master of Fuzhou University(福州大学硕士论文).2006.
Synthesis,Photophysical and Photochemical Properties of β-Tetrakis(aminomethyl)phthalocyaninato Zinc(Ⅱ)Hydrochloride
XU Xiu-Zhi1WANG Jian1LI Zhu-Lai*,1YAN Wen-Jin1CHI Hui-Li1CHEN Wen-Bin2ZHUO Shi-Chang2CHEN Nai-Sheng*,3
(1Faculty of Pharmacy,Fujian Medical University,Fuzhou 350004,China)(2Undergraduate,Faculty of Pharmacy,Fujian Medical University,Fuzhou 350004,China)(3Institute on Research of Functional Materials,Fuzhou University,Fuzhou 350002,China)
β-Tetrakis(aminomethyl)phthalocyaninato zinc(Ⅱ) (ZnPcN4)was synthesized from the reaction of β-tetrakis(phthalimidomethyl)phthalocyaninato zinc(Ⅱ) (ZnPcP4)with 85%NH2NH2·H2O and the hydrochloride of ZnPcN4(ZnPcN4·HCl)was obtained.UV-Visible electronic absorption spectra,fluorescence spectra and singlet oxygen quantum yield of ZnPcN4·HCl were determined.ZnPcN4·HCl was found to be aggregated in aqueous media but was partially or fully disaggregated on addition of DMF or ROH to the water solution.In the DMF/water(10%,V/V)/HCl media,as the concentration of HCl increased,the absorbance intensity of monomer increased gradually in the weak acid solution.It is no aggregation in DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)media in the concentration of 10-5mol·L-1.However,in the strong acid solution,as the concentration of HCl increased,the absorbance intensity of monomer decreased gradually,meanwhile the absorbance intensity of monoprotonation peak at 713 nm increased to a small extent.The maximum absorbance and emission wavelength of ZnPcN4·HCl is 675 nm and 681 nm in DMF/water(10%,V/V)/HCl(1.2 mmol·L-1)media,respectively.ZnPcN4·HCl was found to be aggregated in DMF,so its fluorescence quantum yield and singlet oxygen quantum yield were small.A value of 0.19 was calculated for thefluorescence quantum yield of this photosensitizer in DMF/water(10%,V/V)/HCl(1.2 mmol·L-1).The photodynamic activity of ZnPcN4·HCl was evaluated using 9,10-dimethylanthracene(DMA).The singlet oxygen quantum yield was 0.58 close to ZnPc with a promising anti-tumor photosensitizer for the further research.
phthalocyaninatozinc;aggregation;singlet oxygen;protonation
O614.24+1;O627.23
:A
:1001-4861(2011)05-0877-09
2010-10-08。收修改稿日期:2010-11-26。
福建省青年人才创新基金(No.2007F3038)和福建医科大学青年骨干教师基金(2009-2011)资助项目。
*通讯联系人。 E-mail:lizhulai@126.com,nschen@fzu.edu.cn;会员登记号:M041400053S。

