Beckman AU680生化分析仪性能评价及溯源
李 鑫,周春洁,武军梅,刘凤霞(重庆市江津区中医院检验科 402260)
由于日益增加的标本检测量,科室目前生化分析仪的测试速度难以满足大批量临床样本检测的需要,本科室引进1台Beckman AU680全自动生化分析仪。该生化分析仪在带来快速、高效的同时,仪器的测定误差难免,对仪器性能评价是必要的,以保证检验结果的准确、可靠[1]。本文遵照美国临床和实验室标准协会(CLSI)部分文件的要求,对Beckman AU680生化分析仪及其原装试剂、校准品组成封闭检测系统的碱性磷酸酶(ALP)、天门冬氨酸氨基转移酶(AST,采用速率法)、血清总胆红素(TBil,采用终点法)、非原装试剂血肌酐(Cr,采用两点终点法)共4个检测项目的精密度、准确度、线性及携带污染进行评价,并对钾(K+)、钠(Na+)、氯(Cl-)离子选择电极法与Olympus AU2700进行对比分析,现将结果报道如下。
1 材料与方法
1.1 材料
1.1.1 仪器 Beckman AU680生化分析仪、Olympus AU2700生化分析仪。
1.1.2 试剂、标准品及质控品 ALP、AST、TBil的试剂均由Beckman公司提供:ALP批号为1906,AST批号为1565,TBil批号为1566。Beckman公司提供的校准品,批号为66300,能溯源到Beckman Coulter Master Calibrator;两个水平质控血清批号分别为0029 H和0030F。Cr的试剂由利德曼公司提供,批号为111183K。其校准品由上海长征公司提供,批号为663 UN,能溯源到NIST SRM 909B;质控血清批号为678UN-2。电解质试剂全为配套试剂,其能溯源到 NIST SRM 2201/2202。
1.1.3 精密度分析稳定的实验样品 采用本院患者新鲜血清,混合后分装冷冻保存。
1.2 方法
1.2.1 分析方法 ALP、AST、TBil、Cr检测方法及参数见各自批号的相应试剂说明书,K+、Na+、Cl-采用离子选择电极法。评价前分析者已经熟悉分析方法、仪器使用和评价方案,对仪器进行常规维护以保证仪器处于良好状态。使用相应校准品对各检测项目进行校准,每天进行试剂空白测定和电解质校准,并按经典的Westgard多规则质控方法进行Beckman两水平质控品及长征质控品分析,质控在控才进行下一步实验。
1.2.2 精密度实验 精密度依照 CLSI的 EP5-A2[2]文件要求,收集本院患者新鲜血清混合,因为混合样本稳定较困难,所以精密度实验采用5个工作日完成。每天做两批实验(上午一批,下午一批,时间间隔大于2 h),每个批次测8个样本。每样本做双份重复测试,随机插入常规标本中。获取80个数据。从所有80个结果计算出总精密度。以批内精密度的CV或SD<1/4CLIA′88,总精密度的CV 或SD<1/3CLIA′88为可接受的精密度最低水平[3]。
1.2.3 准确度实验 准确度分两个方案:(1)ALP、AST、TBil、Cr测定采用测定相应配套质控品,与质控品结果进行对照。每个水平进行5次(或天)测定,计算其平均值是否在质控范围内。(2)K+、Na+、Cl-测定采用《患者样本方法比较和偏倚估计》。依照CLSI的EP9-A2[4]文件的要求,由于Olympus AU2700生化分析仪性能和准确度已证实,且长期参加室间质评结果优秀,以其测定结果为X值,新购置Beckman 680生化分析仪测定结果为Y,进行线性回归统计^Y=b X+a,b和a分别表示两种仪器间的比例误差和恒定误差。r表示两仪器的相关系数,当r≥0.975或r2≥0.95,认为X范围是合适的。以CLIA′88规定的室间质量评价允许误差范围的1/2为标准[5],在不同医学决定水平分别判断仪器的偏倚临床是否可以接受性。
1.2.4 线性实验 线性实验依照CLSI的EP6-A[6]文件的要求,按不同项目收集近20 d来患者血清最高值(H)和正常值或低值(L),但高值样本较少。对收集的高值样本和低值样本,采用不同比例进行混合,形成9管系列样品,分别用AU680生化分析仪进行检测,每样品测两次取均值作为实测值X,以Y表示各样品的预期值,进行回归分析,得到Y=b X+a,若b在0.95范围内,a近于0(统计学上无差异),则可判断线性范围验证成功[7]。
1.2.5 携带污染率 在Beckman AU680生化分析仪上,选取高浓度定值血清样本连续测定3次,测定值分别为H1、H2、H3;再取低浓度定值血清样本连续测定3次,测定值分别为L1、L2、L3。按公式计算携带污染率[8]。携带污染率=(L1-L3)/(H3-L3)×100%。
1.3 统计学处理 使用Excel 2007软件,对原始数据进行统计处理及相关线性分析。
2 结 果
2.1 精密度实验结果 ALP、AST、TBil、Cr、K+、Na+、Cl-的批内精密度的CV或SD均小于1/4CLIA′88,总精密度的CV或SD均小于1/3CLIA′88,在质量目标的可接受范围内,见表1。
2.2 准确度实验结果 (1)ALP、AST、TB、CR 4个项目的质控品测试均在质控范围内,Beckman AU680生化分析仪各检测项目不同医学决定水平上的相对偏倚除AST外均小于或等于1/2CLIA′88,达到了本研究预期的质量目标(表2),但AST在控结果尚可,在日后的工作中注意查找原因。(2)K+、Na+、Cl-:Cl-在Beckman AU680生化分析仪检测结果均与Olympus AU2700生化分析仪检测结果呈明显相关,相关系数r≥0.95,表明X范围是较合适的,其分布范围较宽,结果在接受标准范围内,则说不同检测系统间检测结果可比;但Na+的结果相关系数r<0.95,则说明不同检测系统间检测结果相关性差,无法保证检测结果的准确性,可以通过相关回归来拟合两者的线性方程,见表3。
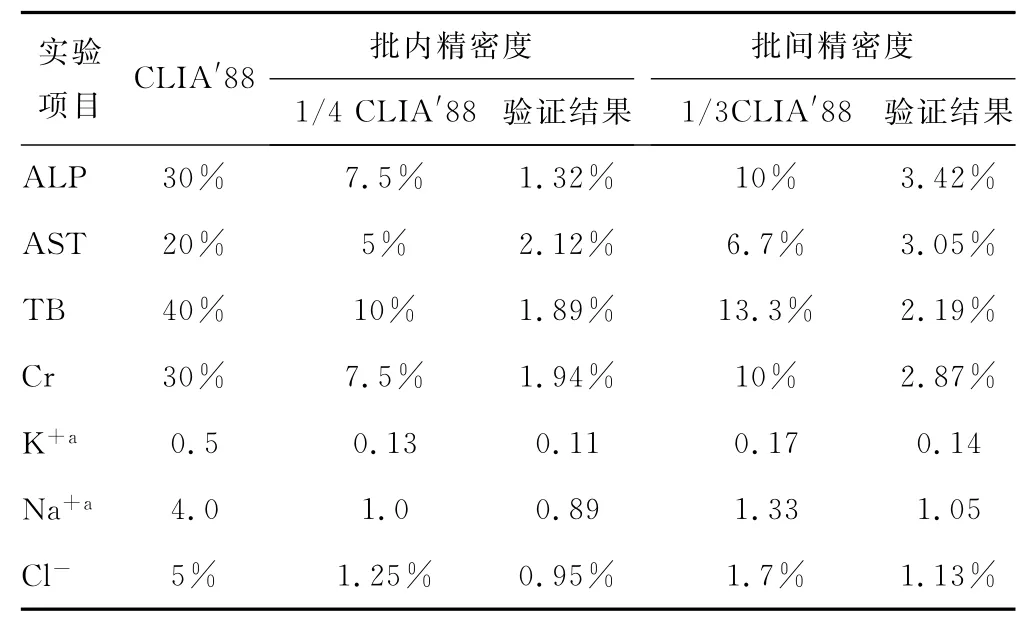
表1 ALP等项目的精密度实验结果
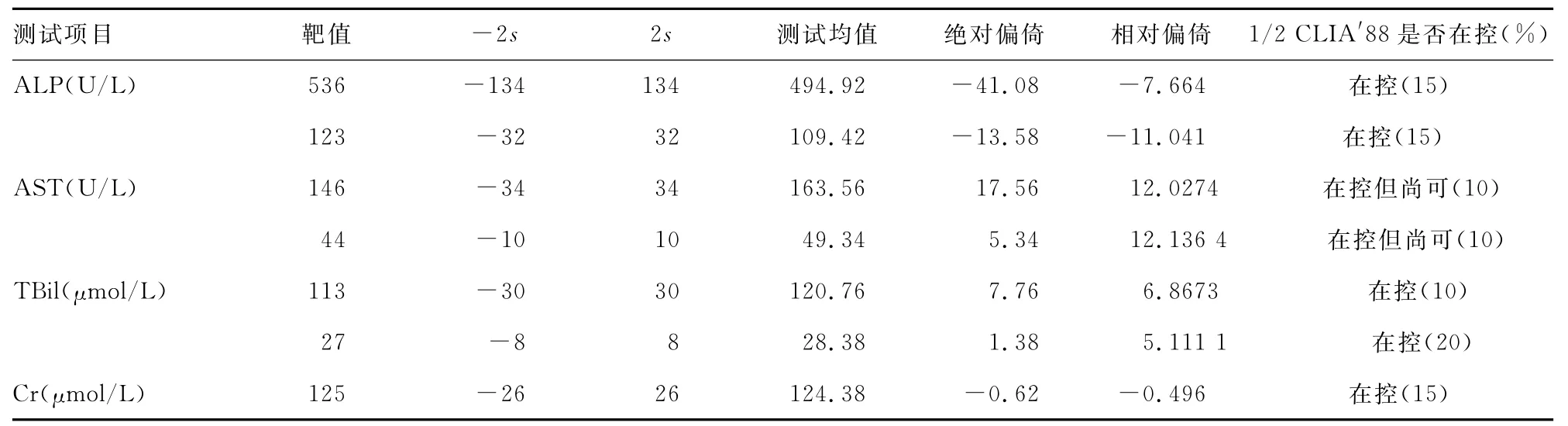
表2 ALP等项目的准确度实验结果
2.3 线性实验结果 高低值样本收集后,混合方案见表4。Beckman AU680生化分析仪ALP、AST、TBil、Cr的线性实验中,r2>0.95、0.95<b<1.05均在可接受范围内,各检测项目在该实验涉及浓度范围内呈线形,见表5。
2.4 携带污染率 ALP、AST、TB、CR 4项目的携带污染率较小,均小于2%,相比较而言,Cr的携带污染最大,为1.65%,见表6。

表3 K+等项目的相关性及线性回归结果

表4 ALP等项目的线性实验高低值混合方案
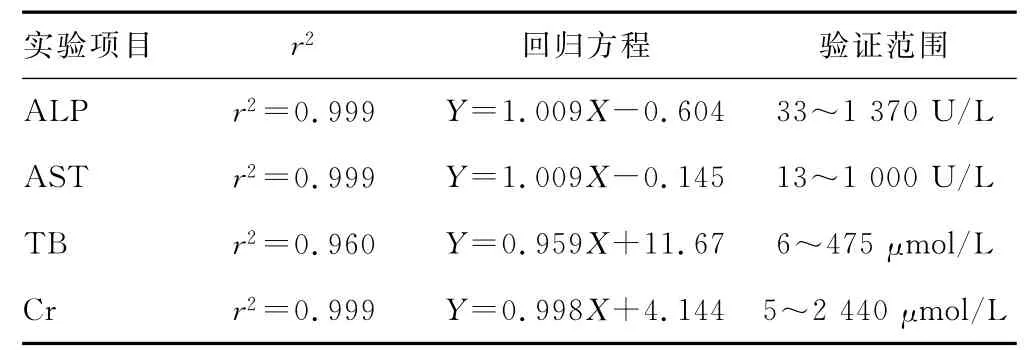
表5 ALP等项目的线性实验结果
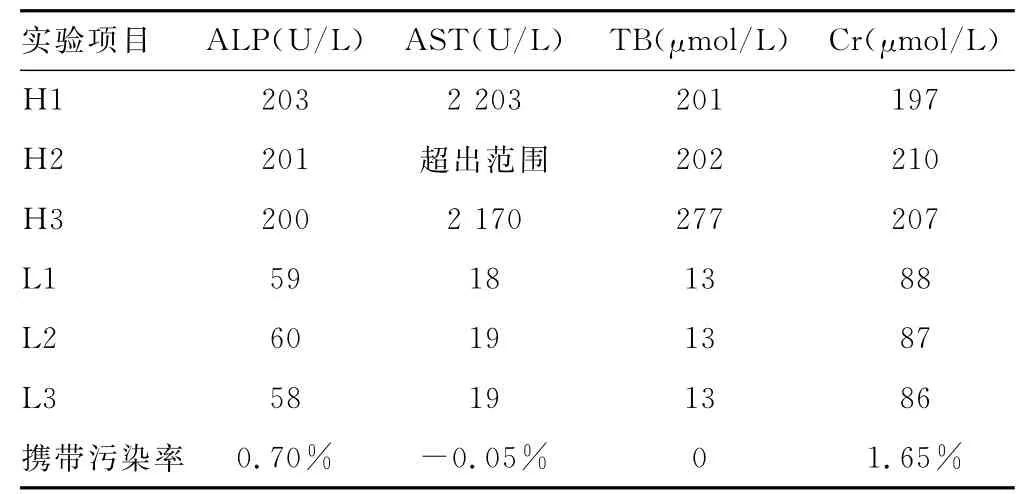
表6 ALP等项目的携带污染实验结果
3 讨 论
医学实验室-质量和能力的专用要求ISO15189[9]设备(在安装时及常规使用中)应显示出能够达到规定的性能标准,并且符合相关检验所要求的规格。CLIA强调医学检验部门必须对于检测系统的性能参数进行验证,至少包括精密度、准确度、可报告范围和临床参考区间。
本文依照CLSI的EP5-A2、EP9-A2和EP6-A 文件的要求,以不同方法、不同波长、不同检测单元、试剂配套与否等原则,本科室选取了 ALP、AST、TBil、Cr、K+、Na+、Cl-共7个检测项目的精密度、准确度、线性对Beckman AU680检测系统进行评价。仪器试剂生产厂商常采用不同浓度范围的新鲜患者血清与参考实验室的参考方法进行比对来实现其检测系统结果的溯源性[10]。为了将其检测结果的溯源性继续向用户传递,厂商提供了针对该检测系统配套的校准品,并对校准品进行了极其严密的定值。因而准确度确认较为简便的方法可使用不同批号的校准品或直接使用“正确度验证品”进行准确度验证。但遗憾的是试剂厂商只有在上一个批号的校准品即将过期时才会有新批号的校准品上市,因而实际工作中很难做到用一个批号的校准品校准而用另一个批号的校准品进行准确度评价;同时基质效应极小的“正确度验证品”由于项目局限和昂贵的价格并未在国内广泛使用。本实验室ALP、AST、TBil、Cr 4项目测定质控品,可完成相应项目的准确度测定,还能检测本科室的室内质量控制。根据CLSI的EP9-A2文件的要求,将Beckman AU680的ISE 3个检测项目分别与分析性能和准确度已在本实验室得到确证的Olympus AU2700检测系统进行比对,同时完成了准确度评价和同一检测项目在不同设备间的比对工作。线性实验的关键为在日常工作中留取高值和低值的标本。在评价实验中如果b<0.95或b>1.05,有可能b与1之间差异有统计学意义,为做出正确判断,可对所有实验结果作分析:试着舍去某组数据,另进行回归统计。若缩小分析范围后,回归方程明显改善,b近于1,a趋于0(差异无统计学意义),则缩小的分析范围是真实的线性范围。由于K+、Na+、Cl-生理波动范围明显窄于电解质线性宽度,加之高低值标本不易收集,本研究对K+、Na+、Cl-线性范围未行评价。而ALP、AST、TBil在评价实验中线性未超出厂商的声明,或在试剂厂商表示的线性上下限的10%以内,但实际工作中仍以厂商声明的线性为准,因为在实际工作中很少遇到超出所做的线性,若对于超过厂商声明的线性样品,本实验室仍建议稀释后重测。
以上实验结果表明,Beckman AU680生化分析仪达到本实验室性能要求,能够在本实验室准确快速的应用。对于大型生化分析仪,特别是多模块多检测系统的组合式高速生化分析仪,在不同的运行环境、操作情况下性能指标可能会存在一定的差异,必须在使用前进行常规性能评价或验证,在确保在同一仪器内多个检测系统结果一致性的前提下,才能进一步保证同一实验室中不同仪器结果的一致性,为实验室全面质量保证奠定基础。
[1]夏勇,李卫宁.Olympus AU5400生化分析仪性能的评价[J].检验医学与临床,2009,6(18):1539-1542.
[2]Clinical and laboratory standards Institue.Evaluation precision performance of quantitative measurement methods;approved guideline-seconded ition.document EP5-A2[S].Wayne,PA:CLSI,2004.
[3]庄俊华,黄宪章,翟培军.医学实验室质量体系文件编写指南[M].北京:人民卫生出版社,2006:193.
[4]Clinical and laboratory standards Institue.Method Comparison and biasa estimation using patient samples;tentative guideline-second edition.document EP9-A2[S].Wayne,PA:CLSI,2002.
[5]张秀明,庄俊华,徐宁,等.不同检测系统血清酶测定结果的偏倚评估与可比性研究[J].中华检验医学杂志,2006,29(16):346-349.
[6]Clinical and laboratory standards Institue.Evaluation of the linearity of quantitative analytical methods,proposed:astatistical approach;Approved Guideline.document EP6-A[S].Wayne,PA:CLSI,2003.
[7]冯仁丰.临床检验质量管理技术基础[M].上海:上海科学技术文献出版社,2003:66-68.
[8]顾柄权,刘树林.美国 MD-100自动生化分析仪性能评价[J].陕西医学检验,2000,15(3):37.
[9]CNAS-CL02.ISO15189:医学实验室质量和能力认可准则[S].北京:中国标准出版社,2008.
[10]刘小娟,黄亨建.罗氏生化试剂用于奥林巴斯全自动生化分析仪的溯源性分析[J].华西医学,2004,19(3):401-402.