Fe2 O3/TiO2复合光催化剂的制备及其表征
刘 红,陈仕祥,彭秀达,王 翠
(武汉科技大学资源与环境工程学院,湖北武汉,430081)
以TiO2为代表的半导体光催化剂用于污水处理越来越受到普遍关注。TiO2在紫外光作用下能产生氧化能力很强的羟基自由基,可使有机污染物氧化后生成CO2、H2O及其它简单无机离子[1]。但由于TiO2光催化剂禁带较宽,只对紫外光响应,光激发产生的电子-空穴对容易复合,其催化效率较低。改进研究发现,用能隙较窄的半导体与TiO2复合制成的光催化剂,可使光催化活性得以提高[2-5]。有关复合半导体光催化剂的研究报道很多[6-15],这些复合半导体光催化剂几乎都表现出高于单一半导体光催化活性的性质。上述复合光催化剂的制备大多采用浸渍法、水热法和混合溶胶法。微乳液法是近年来兴起的一种合成纳米材料的理想方法,具有反应条件温和、实验装置简单、操作方便、应用领域广等优点[16]。
本文以九水硝酸铁为铁源、硫酸钛为钛源,采用微乳液法制备Fe2O3/TiO2复合光催化剂,并用SEM、FTIR、XRD、BET和甲基橙降解率对复合光催化剂性能进行表征,考察不同制备条件下复合光催化剂的活性。
1 实验
1.1 试剂
试剂为十二烷基硫酸钠(SDS)、正庚烷、正丁醇、硫酸钛、九水硝酸铁、氨水和甲基橙,均为分析纯。
1.2 Fe2 O3/TiO2复合光催化剂制备
将4 g十二烷基硫酸钠、5 m L正丁醇与30 m L正庚烷混合并搅拌均匀,按照一定Fe与Ti的摩尔比,在快速搅拌下缓慢滴加一定体积的九水硝酸铁和硫酸钛水溶液,得到澄清的微乳液,用氨水调节微乳液p H值至6,超声波分散30 min,放入内衬为聚四氟乙烯的不锈钢密闭反应釜中,在160℃下水热合成2 h,冷却至室温,取出产物进行抽滤,所得固体用蒸馏水和无水乙醇洗涤,干燥后充分研磨,再于一定温度下煅烧1.5 h,自然冷却后得到Fe2O3/TiO2复合光催化剂。
1.3 光催化活性评定
光催化活性测定在圆形玻璃缸中进行,以300 W高压汞灯为紫外光源,反应液液面与紫外灯距离为10 cm。室温下,将0.05 g光催化剂加入到100 m L浓度为25 mg/L的甲基橙溶液中,关闭紫外光源,在光催化反应器暗环境内搅拌0.5 h,进行吸附,打开紫外光源,15 min后移取约10 m L混合液,离心分离,取上层清液,用日本岛津公司UV2550型分光光度计测定吸光度,用甲基橙的降解率来评定光催化剂的活性。降解率计算公式为
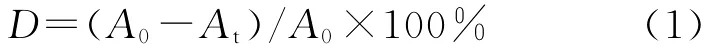
式中:A0、At分别为反应前后甲基橙溶液的吸光度。
1.4 结构与性能表征
用日本理学公司D/MAX-ⅢA型全自动X射线衍射仪进行晶相分析(Cu Kα辐射,40 k V/50 m A,扫描范围5°~70°),用德国VERTEX 70型傅立叶红外光谱仪进行结构分析,用德国Nava 400 Nano扫描电镜观察微观形貌,用美国贝克曼库尔特公司SA3100比表面积和孔径分析仪对样品的比表面积、孔径和孔容进行表征,采用多点BET法和BJH法,利用相对压力为0.05~0.2所对应的N2吸附数据计算总孔体积和比表面积。
2 结果与讨论
2.1 Fe2 O3/TiO2晶相转变
Fe/Ti摩尔比为1∶3时,不同煅烧温度下所制Fe2O3/TiO2样品XRD图谱如图1所示。从图1中可看出,经300℃煅烧后的Fe2O3/TiO2样品,其锐钛矿相TiO2的特征峰位于25.3°处;当煅烧温度为500℃时,代表锐钛矿相的几个最强特征衍射峰已非常明显,同时还有少量的金红石相出现;随着煅烧温度进一步升高,金红石相逐渐增多,锐钛矿相所占比例相对减少。此外,500℃煅烧过的Fe2O3/TiO2在25.3°处的锐钛矿相TiO2特征衍射峰最为尖锐,表明此时晶型结构最好;600℃时,金红石相特征峰不仅增多,衍射峰强度也在进一步增大,明显呈现出TiO2由锐钛相向金红石相转变的趋势。
随煅烧温度不断升高,Fe2O3/TiO2由浅黄色变为深红色,表明有铁的氧化物生成。从图1中可看出,样品在500℃时出现了α-Fe2O3的特征衍射峰,并且在600℃下其进一步增多。

2.2 Fe2 O3/TiO2红外光谱分析
经500℃×1.5 h煅烧,TiO2和不同Fe/Ti摩尔比时所制Fe2O3/TiO2样品红外光谱如图2所示。从图2可看出,3 742 cm-1和1 650 cm-1处的吸收峰属于O—H的弯曲振动吸收峰,3 422 cm-1处的宽峰是是由O—H的伸缩振动引起的[17]。此外,2 923 cm-1处的峰为C—H键的伸缩振动引起[18],表明有少量的有机物残留在样品中。在1 129 cm-1处,有3种不同Fe/Ti摩尔比的Fe2O3/TiO2样品均出现α-FeOOH的特征吸收峰;在656 cm-1处,只有n(Fe)∶n(Ti)=1∶3的Fe2O3/TiO2出现了与TiO2对应的Ti—O—Ti键特征峰,其他两种Fe2O3/TiO2则在976 cm-1处出现了代表α-Fe2O3结构的Fe—O键特征吸收峰,这是由于α-FeOOH因脱水而发生部分结构演变所致[15]。
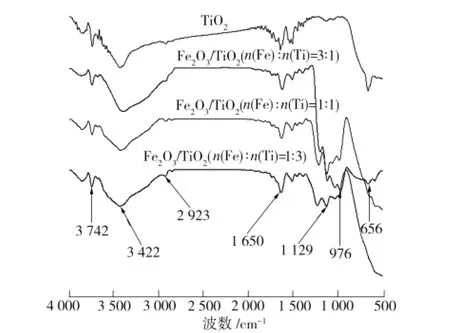
图2 TiO2和不同Fe/Ti摩尔比所制Fe2 O3/TiO2红外光谱Fig.2 FTIR spectra of the TiO2 and Fe2 O3/TiO2 nanoparticles
2.3 Fe2 O3/TiO2颗粒形貌
不同Fe/Ti摩尔比时所制Fe2O3/TiO2样品SEM照片如图3所示。从图3中可看出,Fe/Ti摩尔比为1∶3时所制Fe2O3/TiO2样品疏松多孔、颗粒细小且分散性较好(图3(a));Fe/Ti摩尔比为1∶1时所制Fe2O3/TiO2样品粒径分布虽较均匀,但粒径较大,且存在少量团聚现象,颗粒之间存在明显的界限(图3(b));Fe/Ti摩尔比为3∶1时所制Fe2O3/TiO2样品为无数分布极不均匀的颗粒聚集而成的团聚体(图3(c))。
2.4 Fe2 O3/TiO2比表面积及孔径分布
经500℃×1.5 h煅烧,Fe/Ti摩尔比为1∶3时所制Fe2O3/TiO2样品孔径分布及N2吸附等温曲线如图4所示。由图4孔径分布曲线可以看出,Fe/Ti摩尔比为1∶3时所制Fe2O3/TiO2孔径分布主要聚集于5.45~6.14 nm,平均孔径为5.79 nm。不同Fe/Ti摩尔比所制Fe2O3/TiO2及TiO2和P-25总孔体积和比表面积如表1所示。从表1中可见,n(Fe)∶n(Ti)=1∶3时所制Fe2O3/TiO2样品比表面积为60.282 m2/g,Fe/Ti摩尔比为1∶3时所制Fe2O3/TiO2复合光催化剂比TiO2、P-25光催化剂具有更大的比表面积,是一种孔径细小的多孔材料,这种多孔结构有利于光催化反应物的吸附和产物的快速扩散,提高了光催化反应效率。

图3 不同Fe/Ti摩尔比所制Fe2 O3/TiO2 SEM照片Fig.3 SEM images of Fe2 O3/TiO2
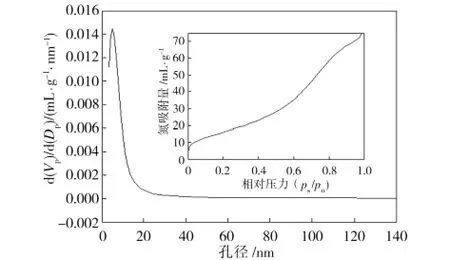
图4 Fe2 O3/TiO2孔径分布及N2吸附曲线Fig.4 Pore size distribution curve and N2 adsorption isotherms curve of Fe2 O3/TiO2

表1 不同光催化剂总孔体积和比表面积Table 1 Total pore volume and specific surface area of different photocatalysts
2.5 Fe2 O3/TiO2对甲基橙降解率
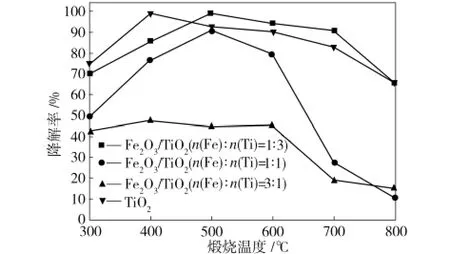
图5 不同煅烧温度下Fe2 O3/TiO2和TiO2对甲基橙的降解率Fig.5 Comparison of photocatalytic degradation of methyl orange over Fe2 O3/TiO2 and TiO2
不同煅烧温度下所制Fe2O3/TiO2和TiO2对甲基橙的降解率如图5所示。由图5中可看出,煅烧温度低于500℃时,除n(Fe)∶n(Ti)=3∶1时所制Fe2O3/TiO2外,其他Fe2O3/TiO2对甲基橙的降解率均随煅烧温度升高而增高,500℃时n(Fe)∶n(Ti)=1∶3所制Fe2O3/TiO2对甲基橙的降解率高达99.7%,优于相同条件下的TiO2光催化剂。
3 结论
铁与钛的摩尔比为1∶3、煅烧温度为500℃和煅烧时间为1.5 h条件下所制Fe2O3/TiO2复合光催化剂样品疏松多孔、颗粒细小且热稳定性高,经紫外光照15 min后对甲基橙的降解率为99.7%,与相同条件下制备的TiO2相比具有更好的光催化活性和更大的比表面积。
[1] Masakazu A,Masato T.The design and development of highly reactive titanium oxide photocatalysts operating under visible light irradiation[J].J Catal,2003,216:05-16.
[2] 陈晓青,杨娟玉,蒋新宇,等.掺铁TiO2纳米微粒的制备及光催化性能[J].应用化学,2003,20(1):73-76.
[3] 付川,祁俊生,潘杰,等.Fe2O3-TiO2光催化降解水中酸性橙Ⅱ研究[J].环境科学与技术,2009,32(9):49-52.
[4] 张廷相,杨芬.TiO2-Fe2O3复合材料降解甲基橙溶液的研究[J].化学工程与装备,2009,11(11):32-36.
[5] 谢立进,马峻峰,赵忠强,等.半导体光催化剂的研究现状及展望[J].硅酸盐通报,2005,24(6):80-84.
[6] Wang C Y,Shang H M,Ying T,et al.Properties and morphology of CdS compounded TiO2visiblelight photocatalytic nanofilms coated on glass surface[J].Separation and Purification Technology,2003,32(1-3):357-362.
[7] Takayuki H,Keiko S,Isao K.Preparation and photocatalytic properties of composite CdS nanoparticles-titanium dioxide particles[J].Colloid Interface Science,2001,244(2):262-265.
[8] Fang J H,Lu X M,Zhang X F,et al.CdSe/TiO2nanocrystalline solar cells[J].Supramolocular Science,2001,5(5-6):709-711.
[9] 李志杰,侯博,徐耀,等.水热法制备氧化硅改性的纳米二氧化钛光催化剂[J].石油化工,2004,33:789-791.
[10]蒲玉英,方建章,彭峰,等.微乳法制备纳米TiO2/SiO2的结构及光催化研究[J].无机化学学报,2007,23(6):1 045-1 049.
[11]Wang M,Liu S W,Xiu Z L.Preparation and photocatalytic properties of silica gel-supported TiO2[J].Materials Letters,2006,60(7):974-978.
[12]K Tennakone,J Bandara.Enhanced rates of photocatalytic degradation of an azo dye using coupled SnO2/TiO2semiconductor thin films[J].Environ Sci Technol,2005(29):841-845.
[13]孙旋,刘红,倪昕.Fe2O3-TiO2光催化剂的制备及其对碱性嫩黄的降解[J].水处理技术,2008,34(4):61-64.
[14]Hong L,H K Shou,Xuan S,et al.Preparation and characterization of visible light responsive Fe2O3-TiO2composites[J].Applied Surface Science,2011(257):5 813-5 819.
[15]龚潇,陈天虎,庆承松,等.TiO2/α-Fe2O3复合光催化剂的制备及表征[J].硅酸盐学报,2008,36(6):838-843.
[16]牛新书,许亚杰,张学治,等.微乳液法制备纳米二氧化钛及其光催化活性[J].功能材料,2003,5(34):548-550.
[17]Yu J G,Zhao X J,Yu J C,et al.The grain size and surface hydroxyl content of super-hydrophilic TiO2/SiO2composite nanometer thin films[J].Journal of Materials Science Letters,2001,20(18):1 745-1 748.
[18]李跃军,曹铁平.静电纺丝法制备Fe2O3/TiO2复合纳米纤维及光催化性能研究[J].河北师范大学学报,2010,34(6):702-706.

