非均相催化氧化合成葡萄糖醛酸及内酯的研究进展
周 红,王怡宁, 潘志权,黄齐茂
(武汉工程大学化工与制药学院,湖北 武汉 430074)
0 引 言
葡糖醛酸(Glucuronic acid),又称葡萄糖醛酸,是葡萄糖的 C-6 羟基被氧化为羧基形成的糖醛酸.D-葡糖醛酸一般不以游离的形式存在,因为该形式不稳定,而是以更稳定的呋喃环的 3,6-内酯形式存在,即葡萄糖醛酸内酯,简称葡醛内酯,制剂名为肝泰乐(俗称肝通),是一种常用的护肝型保健药品,主要用于预防和治疗流行性肝炎、肝硬化、食物及药物中毒等.其化学成分为:D-(+)-呋喃葡萄糖醛-γ-内酯[D-(+)-Glucofuranurono-6,3-lactone][1].在水溶液中不能稳定存在,易开环转变成葡萄糖醛酸.室温下,会以60%(摩尔百分比)和40%(摩尔百分比)的葡萄糖醛酸和内酯比例达到平衡;加热和酸性条件下,更易达到平衡.但在高温且强酸性条件下,葡醛内酯容易脱羧生成二氧化碳、呋喃及其它裂解产品.其作为肝脏调节剂的作用机理是,在肝内能在酶的催化作用下,开环成为葡萄糖醛酸,葡萄糖醛酸再与含有羟基、羧基、巯基等的有毒物质结合成无毒或低毒的物质而由尿排出[2];可降低肝淀粉酶活性,使肝糖原增加,脂肪贮量降低,从而起到保护肝脏及解毒作用[3].另外,葡醛内酯还是关节炎、结缔组织疾病等的辅助治疗药品,功能性食品、减肥药、化妆品等的主要添加剂[1].由于其在医药及保健品的广泛应用,葡醛内酯的市场需求量逐年显著增加.
葡醛内酯生产工艺主要分为三种:生物发酵法、多糖水解法、化学氧化法.其中,生物发酵法是利用特定的生物酶或菌株对能够形成葡萄糖醛酸或其前体的特定物质进行发酵来制备葡萄糖醛酸,由于酶及菌株的筛选与制备过程繁琐、成本高且收率极低,生物发酵法目前仅限于探索研究.多糖水解法是通过水解自然界中存在的多糖醛酸或含糖醛酸的多糖来制备葡萄糖醛酸及其内酯,由于该方法需要很强的酸碱水解条件,会造成产物糖醛酸的分解,且产品收率低,不能满足生产需要[4-5].化学氧化法主要是对醛糖衍生物进行催化氧化反应,分为均相催化氧化和非均相催化氧化.均相催化氧化法是利用特定的催化剂在均相体系中对糖类进行催化氧化来制备葡萄糖醛酸,均相催化氧化法虽然具有较高的选择性、反应时间短,但反应过程控制严格、反应产物分离及催化剂回收利用困难且存在环境污染问题.非均相催化氧化法是气、液、固三相反应,主要以固体催化剂在碱性条件下选择性催化氧化葡萄糖及其衍生物的伯羟基制取葡萄糖酸盐.该方法工艺过程简单、反应条件温和、反应时间短、转化率高、三废少、催化剂易于回收利用[6].氧化过程是制备糖醛酸的重要步骤,其中氧化方法的选择是合成糖醛酸及内酯的关键所在.本研究仅对非均相催化氧化合成葡醛内酯的研究进展进行综述.
1 以铂为催化剂的非均相催化
Van Dam H E等在研究用氧气将糖类氧化成酸的过程中发现:贵金属Pt催化剂对糖上的伯羟基表现出一定的选择性[7],其选择性氧化单糖的顺序是半缩醛>伯羟基>轴向仲羟基>径向仲羟基[8].
Bols M[9]报导了以Pt为催化剂合成1-O-新戊酰-β-D-葡萄糖醛酸的制备工艺(见图1).以2,3,4,6-四-O-苯甲基-D-葡萄糖苷为原料经酰化、加氢和氧化合成1-O-新戊酰β-D-葡萄糖醛酸.当1-O-新戊酰-D-葡萄糖苷和催化剂(铂黑)的质量比为2∶1,温度87~88 ℃,反应pH = 7~8 时,氧化反应收率可达60%,总产率为43%.Lichtenthaler F W等人也曾用这种氧化法将l-O-甲基-α-D-葡萄糖氧化成相应的糖醛酸[10].
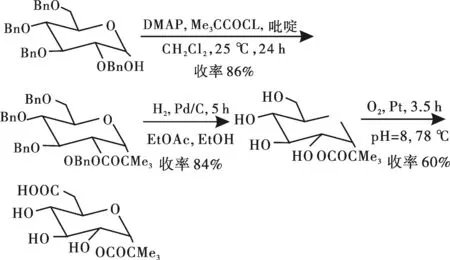
图1 1-O-新戊酰-β-D-葡萄糖醛酸合成路线图Fig.1 Synthesis procedure of 1-O-pivaloyl-β-D-glucopyranuronic acid
Van Dam H E等人[11]报导了用负载在活性炭上的Pt作催化剂,催化氧化葡萄糖-1-磷酸合成葡萄糖醛酸-1-磷酸的方法(图2),研究了Pt/C催化剂的催化活性,结果表明:当Pt的负载量为2%,温度为60 ℃,pH = 9时,得到最高收率约为60%.

图2 葡萄糖醛酸-1-磷酸的合成图Fig.2 Synthesis procedure of glucuronic acid 1-phosphate
Schuurman Y等人[12]用负载在活性炭上的Pt做催化剂,通过控制温度和O2的用量,先将α-D-葡萄糖苷氧化成1-O-甲基α-D-醛基-葡萄糖苷,再得到1-O-甲基-α-D-葡萄糖醛酸. 当Pt的负载量为5%,pH = 10, 温度为60 ℃时,收率可达到56%.

图3 1-O-甲基-α-D-葡萄糖醛酸合成图Fig.3 Synthesis procedure of 1-O-methyl α-D-glucoside
Vleeming J H[13]等人也对用石墨负载Pt的催化剂催化氧化α-D-甲基-葡萄糖苷和α-D-n-辛基葡萄糖苷做了相关报道.认为总的反应速率或催化活性与葡萄糖苷1位烷基R基团密切相关,R烷基链越长,分子尺寸越大,空间位阻大易吸附于催化剂的载体上,使得其催化活性显著下降.在pH = 8, 温度50 ℃下,R为辛基的反应活性较R为甲基的反应活性小10倍,但长的R基能保护与其邻近的仲羟基的氧化与水解,故其催化选择性高.该研究表明在相同实验条件下,选择不同的起始原料催化剂的催化活性存在明显差异性.理论模型研究也表明活性高低与氧化剂氧浓度及催化剂颗粒尺寸相关[14-15].
2 以钯为催化剂不同载体的非均相催化
通过负载贵金属铂作催化剂用分子氧对糖类化合物的伯羟基进行催化氧化方法具有较高活性和选择性.但因铂成本昂贵,使其应用受到限制.以价格相对较低的其它金属活性成份替代金属铂,并通过选择合适的助剂有效提高贵金属的催化活性, 成为化学及材料领域研究热点.在所有贵金属催化剂的研究中,最受关注的就是以Pd为活性中心的催化剂,几乎占据了所有贵金属催化研究报导的30%[8].该方法具有选择性强,效率高的特性.
在催化氧化工业中,可用作负载贵金属的碳共有3种,活性炭、炭黑、石墨及石墨化材料[10].其中,以活性炭的应用性最为广泛.这是因为活性炭具有很稳定的化学和物理性质,能稳定存在于酸和碱中,且对贵金属的回收和重复利用具有非常重要的意义[8, 12].
袁华等以甲基葡萄糖苷为原料, 结合掺杂钙钛矿型复合金属氧化物的助催化作用, 采用钯替代贵金属铂作为主活性成分, 制备了三个系列钯催化剂[16-19]:
2.1 Pd/CuO-Ce0.5Mn0.5O2
该方法是采用溶胶-凝胶法,将按比例称取的含有Ce、Mn、Cu的硝酸盐和柠檬酸反应后,经烘干,研磨,600 ℃焙烧,得到CuO-Ce0.5Mn0.5O2载体,再将Pd用沉淀法负载在该载体上,高温300 ℃焙烧,制得该催化剂[16].其最佳工艺条件及合成路线图见图4.当Pd和CuO的负载量分别为0.5%和9%,葡甲苷和催化剂的质量比为6∶1,温度70 ℃,反应pH = 8~10时,该葡萄糖醛酸及其内酯的总收率可达到70%.

图4 以葡甲苷为原料合成葡萄糖醛酸路线图Fig.4 Synthesis procedure of glucuronic acid by using methyl α-D-glucoside as a starting material
2.2 Pd/La0.5Pb0.5Mn0.9Sn0.1O3
该催化剂的制备方法与上相似,只是载体及催化剂制备的焙烧温度与上不同,均为800 ℃.通过对其催化氧化甲苷合成葡萄糖醛酸及内酯的机理与催化活性的研究发现:当Pd负载量为1%,葡甲苷和催化剂的质量比为6∶1,温度70 ℃,反应pH = 9时, 总收率可达60%,循环使用次数高于5次[17].
2.3 Pd/La0.5 Pb0.5 MnO3
采用以水为溶剂的柠檬酸络合法制备钙钛矿型复合金属氧化物载体,用沉淀法负载活性组分钯得到催化剂Pd/La0.5Pb0.5MnO3,在Pd负载量为1%时,葡甲苷和催化剂的质量比为6∶1,温度70 ℃,反应pH=9时,葡萄糖醛酸收率达29.5%,内酯收率20.5%,葡萄糖醛酸及内酯总收率可达到50%,载体焙烧温度为800 ℃[18-19]. 催化剂稳定性较好,实验表明经5次重复使用,葡萄糖醛酸含量基本保持不变.
以上3种Pd系催化剂合成葡醛酸及内酯总收率分别为50%、60%和70%,表明在Pd负载量相同时,可通过变更掺杂的金属氧化物提高其收率,且当Pd负载量下降时,可通过组份氧化物的调整提高收率,说明以钙钛矿型复合金属氧化物载体,沉淀法负载活性组份钯在葡萄糖醛酸内酯合成中是一个有较好应用前景的方法.
3 以钌为催化剂的非均相催化
硅胶是另一种贵金属的常见载体.Jorna AMJ等人[20]报导了以改性硅胶络合钌离子为催化剂将辛基-α-D-葡萄糖苷催化氧化成辛基-α-D-葡萄糖醛酸的工艺研究.该催化剂的合成方法如下:硅胶活化后,分别与氯丙基三甲氧基硅烷和氯苯基乙基三甲氧基硅烷两种硅胶偶联剂反应,再分别与2-(苯基偶氮)吡啶反应,得到配体,该配体再与钌离子络合得到两种催化剂(如图5).该体系催化氧化辛基-α-D-葡萄糖苷的工艺路线如图5.当辛基葡萄糖苷与次溴酸钠和催化剂的比为500∶2 000∶1时,辛基葡萄糖醛酸的收率具有pH依赖性,当pH = 3,反应时间10 min,温度为60 ℃时,收率达到88%.当pH = 7,反应时间40 min,温度为60 ℃时,收率为69%.相比而言,甲基化的氨基(R = CH3)较含仲氨(R = H)的催化剂的稳定性更好,循环使用4次仍具有较高的氧化活性.但该催化剂较相似的均相催化剂的选择性低.

图5辛基-α-D-葡萄糖醛酸合成路线Fig.5 Synthesis procedure of 5-octyl-α-D-glucuronic acid
4 以氧化铬为催化剂的催化氧化
用CrO3,H2SO4和丙酮体系氧化糖衍生物的方法由来已久,是一种经典的氧化方法[21]. Schell P等人[22]用该方法氧化葡萄糖衍生物,在D-葡萄糖醛和L-艾杜烯糖醛酸的合成与转化报导中涉及到羟甲基的催化氧化.先在3-O-苯基-葡萄糖中引入6-O-三苯甲基,后经乙酰化作用得到中间产物[23],再经CrO3,H2SO4和丙酮的混合液氧化及甲基酯化使中间产物中的6-O-三苯甲基转化为6-O-甲酯[24].最佳反应条件是pH = 9,温度为60 ℃,其收率最高可达到56%.该方法特点是反应过程简单,且氧化剂价格便宜,但选择性较差.CrO3虽为固体,与硫酸作用会生成Cr(III)而溶于液体中,因此,此催化氧化应为固体催化剂的均相催化反应.相比非均相催化反应,其催化剂不能回收利用,并产生有毒废液.
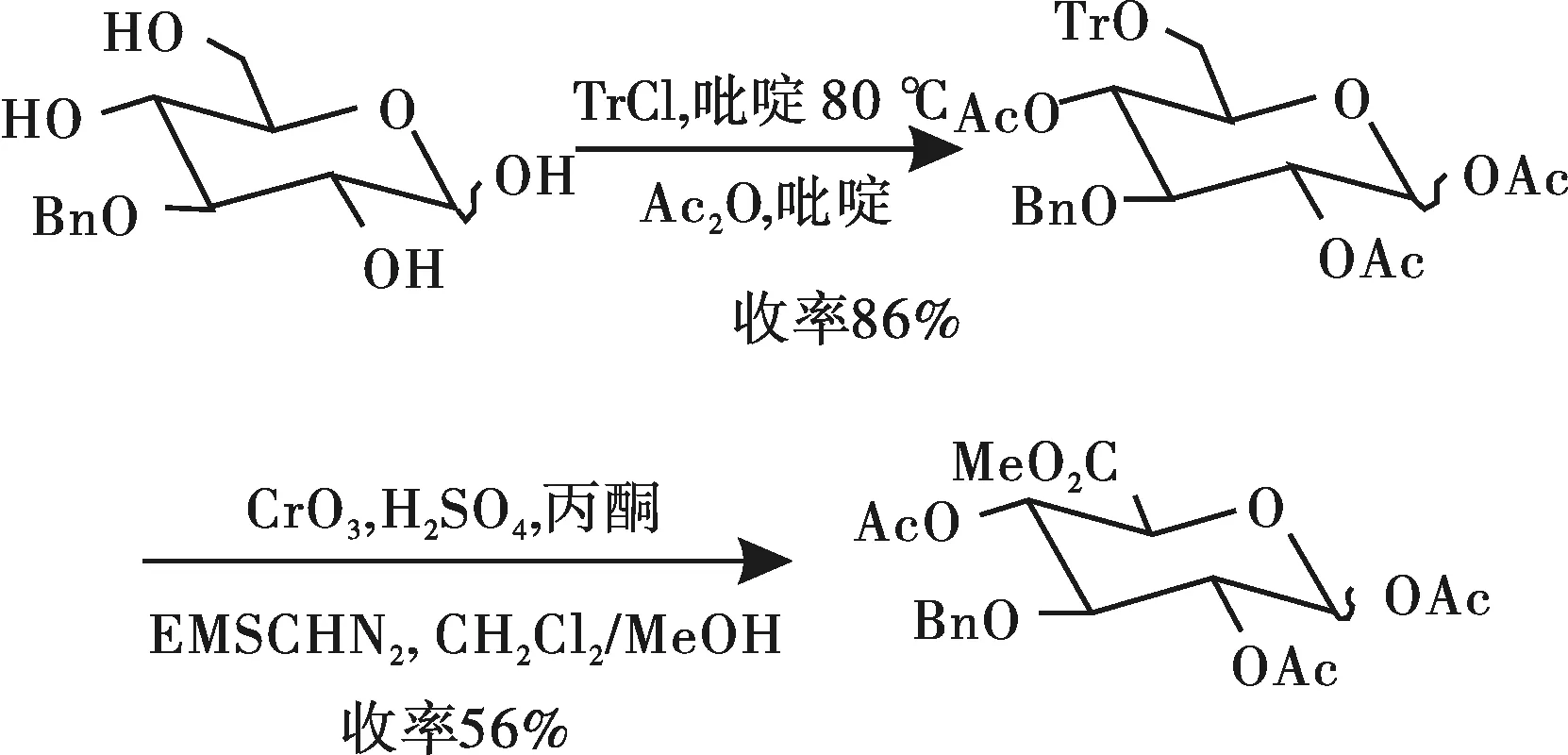
图6 以CrO3为催化剂将伯羟基转化为甲酯的合成路线Fig.6 Synthesis route of the oxidation of primaryhydroxyl to methyl Ester using CrO3 as a catalyst
5 用2,2,6,6-四甲基-1-哌啶作为催化剂的非均相催化
以金属作为催化剂的一个缺点是毒性重金属的浸出.Brunel D等[25]提出用2,2,6,6-四甲基-1-哌啶(2,2,6,6-tetramethyl-1-piperdinyloxy,TEMPO)作为有机自由基选择性将伯羟基氧化成醛.其催化剂的合成方法有两种,一是先用烯丙基溴与4-羟基-TEMPO偶合,经双键氢化硅烷化后衍生成3-(三甲氧基硅烷)丙基TEMPO,并以此为甲硅烷基试剂键合到硅胶上.第2种方法是先将氨基键键合到硅胶上,再通过缩氨酸型偶合将4-羟基TEMPO键合到硅胶上.用次氯酸作为氧化剂,以TEMPO接技的硅胶为催化剂氧化a-甲基-葡萄糖苷,(pH=8, 0 ℃)时,其反应转化率和选择性均大于95%, 环境友好、 重复利用性好.但该法相对于一般的贵金属催化剂的制备过程繁锁.Heeres A等[26]用NaBH3CN还原氨化将4-氧-2,2,6,6-四甲基哌啶-1-氧自由基接技到氨基化的硅胶上作为催化剂, 用NaClO氧化经保护的糖醛酸盐后得到D-葡萄糖醛酸酯.其产率为65%,但3次重复使用后其产率仅为35%.

图7 以TEMPO负载硅为催化剂的D-葡萄糖醛酸酯合成路线Fig.7 Synthesis route of D-glucuronic acid using TEMPO loaded silicon catalyst
6 结 语
在上述各种非均相催化氧化合成葡醛内酯的研究中,以不同载体负载贵金属为催化剂应用的最为广泛.而载体中,又以活性碳应用的最为普遍,因为它具有很强的物理和化学稳定性质,能稳定存在于酸和碱中.硅胶载体可通过硅胶偶联剂的作用引入催化基团,如有机自由基或具有催化功能的配位基团,其催化合成收率较高,重复利用率也较好,但使用硅胶为载体时催化反应不易在碱性介质中进行,因为硅胶在碱性介质中不稳定.除以上提到的几种载体外,还有以氧化铝为载体的催化氧化方法,但使用局限性较大,强酸强碱下稳定性不高.以钙钛矿型复合金属氧化物载体,沉淀法负载活性组份钯作为催化剂,具有稳定性好、重复利用率高的优点,有望通过对载体的组份的改进,进一步提高合成收率.
综上所述,人们开展了多途径的非均相催化合成葡醛内酯的研究,已取得较有成效的研究成果,其循环可再生利用及易分离特性使其具有潜在的研究、开发及工业应用价值.由于催化活性受诸多因素的影响,从实验室的研究成果转化为工业应用仍有较多的问题需要加以解决:重金属负载催化剂中如何防止重金属的浸出和提高其循环次数及降低催化剂成本;以硅胶为载体的催化剂如何提高其在介质中的稳定性及选择性和简化催化剂合成步骤等.寻找选择性好、适用性强,环境友好,价廉的高效非均相催化剂仍是以后研究的重要方向.
参考文献:
[1] 袁华,孙炎彬,闰志国,等. 葡醛内酯的研究与开发[J]. 化学与生物工程,2006, 23(2):53-54.
[2] 陈辉,和娴娴. 葡萄糖醛酸及其内酯制备方法的研究进展[J]. 山东食品发酵,2011(1): 6-8.
[3] 王德法. D-葡萄糖醛酸-γ-内酯的开发和应用[J]. 安徽化工, 2001(4):21-22.
[4] 林培喜,周锡堂,胡智华. 葡醛内酯生产工艺改进研究[J].茂名学院化工学院学报, 2003, 23(1): 23.
[5] 林培喜,周锡堂,胡智华. 一种生产肝泰乐的新工艺研究[J].宜春学院学报,2002, 24(6): 29.
[6] Gootzen J F E, Wonders A H, Cox A P, et al. On the adsorbates formed during the platinum catalyzed (electro) oxidation of ethanol, 1,2-ethanediol and methyl-α-D-glucopyranoside at high pH[J]. J Mol Catal A: Chem,1997, 127: 113-131.
[7] Van D H E, Wisse L J, Van B H. Platinum/carbon oxidation catalysts. VIII. Selecting a metal for liquid-phase alcohol oxidations[J]. Applied Catalysis, 1990, 61(1): 187-97.
[8] Auer E, Freund A, Pietsch J, et al. Carbons as supports for industrial precious metal catalysts[J]. Applied Catalysis, A: General,1998, 173(2): 259-271.
[9] Bols M. Stereoselective Synthesis of 1-O-pivaloyl-β-D-glucopyranuronic Acid[J]. Journal of Organic Chemistry. 1991, 56(20): 5943-5945.
[10] Lichtenthaler F W, Morino T, Winterfeldt W, et al. Nucleosides. XXVI. Alternate synthetic approach to gougerotin[J]. Tetrahedr Lett, 1975(41):3527-3530.
[11] Van D H E, Kieboom A P G, Van B H, et al. Pt/C oxidation catalysts. Part 2. Oxidation of glucose 1-phosphate into glucuronic acid 1-phosphate using diffusion stabilized catalysts[J].Applied Catalysis,1987, 33(2): 373-382.
[12] Schuurman Y, Kuster B F M, Van D W K, et al. Selective oxidation of methyl α-D-glucoside on carbon supported platinum[J]. Applied Catalysis A:General,1992, 89: 31-38.
[13] Vleeming J H, Kuster B F M, Marin G B. Oxidation of methyl and n-octyl α-D-glucopyranoside over graphite-supported platinum catalysts: effect of the alkyl substituent on activity and selectivity[J]. Carbohydrate Research,1997, 303(2): 175-183.
[14] Gangwal V R, Van D Schaaf J, Kuster B F M, et al. Catalyst performance for noble metal catalysed alcohol oxidation: reaction-engineering modelling and experiments[J]. Catalysis Today,2004(96):223-234.
[15] Gangwal V R, Van W B G M, Kuster B F M, et al. Platinum catalysed aqueous alcohol oxidation: model-based investigation of reaction conditions and catalyst design[J]. Chemical Engineering Science,2002(57):5051-5063.
[16] 袁华,马彦,王维华,等. Pd/CuO-Ce0.5Mn0.5O2催化氧化合成葡萄糖醛酸及其内酯[J].合成化学,2010, 18(B09): 106-112.
[17] 袁华,杜治平,闫志国,等. Pd/La0.5Pb0.5Mn0.9Sn0.1O3对甲苷伯羟基的选择催化氧化[J]. 化学学报,2009, 67(4): 345-351.
[18] 袁华,孙炎彬,邬茂,等. Pd/La0.5Pb0.5MnO3催化氧化甲苷合成葡萄糖醛酸[J]. 过程工程学报,2008, 8(3): 572-575.
[19] 袁华, 熊小焱, 邬茂,等. 非均相催化氧化甲苷制备葡萄糖醛酸及其内酯[J]. 精细石油化工, 2009, 26(3): 31-33.
[20] Jorna A M J, Boelrijk A E M, Hoorn H J, et al. Heterogenization of a ruthenium catalyst on silica and its application in alcohol oxidation and stilbene epoxidation[J]. Reactive & Functional Polymers,1996, 29(2):101-114.
[21] 来庚,张军良,郭燕文,等. 糖醛酸合成方法的研究进展[J]. 精细与专用化学品,2006, 14(5):8-10.
[22] Schell P, Orgueira H A, Roehrig S, et al. Synthesis and transformations of D-glucuronic and L-iduronic acid glycals[J]. Tetrahedron Letters, 2001, 42(23): 3811-3814.
[23] Freudenberg K, Plankenhorn E. Synthesis of 2,4,6-trimethylglucose and its relation to yeast glucan[J]. Ann Chem,1938, 536: 257-266.
[24] Jacquinet J C, Petitou M, Duchaussoy P, et al. Synthesis of heparin fragments. A chemical synthesis of the trisaccharide O-(2-deoxy-2-sulfamido-3,6-di-O-sulfo-α-D-glucopyranosyl) -(1→4)-O-(2-O-sulfo-α-L-idopyranosyluronic acid)-(1→4)-2-deoxy-2-sulfamido-6-O-sulfo-D-glu copyranose heptasodium salt[J]. Carbohydr Res,1984, 130: 221-241.
[25] Brunel D, Fajula F, Nagy J B, et al. Comparison of two MCM-41 grafted TEMPO catalysts in selective alcohol oxidation[J]. Applied Catalysis A: General,2001(213): 73-82.
[26] Heeres A, Van D H A, Gotlieb K F, et al. Synthesis of α- and β-D-glucopyranuronate 1-phosphate and α-D-glucopyranuronate 1-fluoride: Intermediates in the synthesis of D-glucuronic acid from starch[J]. Carbohydrate Research,1997(299):221-227.

