LC-MS/MS同时测定四逆汤中11个有效成分
缪 萍,裘福荣,曾 金,李秋月,沈淑娇,贺 敏,王猛猛,蒋 健(上海中医药大学附属曙光医院,上海 201203)
四逆汤为东汉名医张仲景之名方,始载于《伤寒论》,全方由生附子、干姜和炙甘草组成,具有回阳救逆之效,主治少阴病如四肢厥逆、下利清谷、呕吐腹痛、苔白滑、脉沉迟或细微等症。现代药理研究证实,四逆汤具有强心、升压、抗休克、抗心肌缺血、抗动脉粥样硬化和提高免疫功能等作用[1-6],且全方合用效果明显优于各单味药或任意两两组合,维持时间持久。乌头类生物碱、姜酚、甘草皂苷和甘草黄酮是四逆汤中的主要有效成分[7]。乌头类生物碱以C19双酯型二萜类生物碱 (乌头碱、新乌头碱和次乌头碱)毒性最强,易导致严重的心律失常、呼吸抑制和休克。故临床上使用附子需经过炮制,将剧毒性的双酯型二萜生物碱水解为毒性较小的单酯型(苯甲酰乌头原碱、苯甲酰新乌头原碱和苯甲酰次乌头原碱)及毒性更小的醇胺型 (乌头原碱、新乌头原碱和次乌头原碱)生物碱[8]。姜酚是干姜的主要活性成分,具有强心、改善血液循环、降血脂和抗氧化的作用[9]。甘草主要含甘草酸、甘草次酸等三萜皂苷类以及甘草苷、甘草素等黄酮类成分,对心血管疾病有广泛的治疗作用[10]。而《中国药典》2010年版一部仅以甘草酸作为四逆汤的成分定量测定标准[11],未对其他活性成分进行监测。本研究建立了液相-质谱联用 (LC-MS/MS)色谱法同时测定四逆汤中乌头碱、新乌头碱、次乌头碱、苯甲酰乌头原碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、乌头原碱、次乌头原碱、甘草苷、甘草酸和6-姜酚的量的方法,可为其质量控制研究提供依据。
1 仪器与试药
1.1 仪器 ABI 4000Q-Trap质谱仪 (美国ABI/SCIEX公司),配有电喷雾离子化源 (ESI)、三级四极杆质量分析器以及Analyst 1.4.2数据处理软件;日本岛津LC-20A超高速液相色谱仪;Beckman Allegra 64R高速冷冻离心机 (美国Beckman公司);XS-105电子天平 (瑞士Mettler Toledo公司);Millpore纯水机 (美国Millipore公司);Thermo超低温冰箱 (美国Thermo公司)。
1.2 试药 生附子购自安徽亳州药材公司,干姜和炙甘草均购自上海养和堂中药饮片有限公司,经上海中医药大学中药学院魏莉副研究员鉴定分别为毛茛科植物乌头Aconitum carmichaelii Debx.子根的加工品,姜科植物姜Zingiber officinale Rosc.的干燥根茎及豆科植物甘草Glycyrrhiza uralensis Fisch.的干燥根和根茎。新乌头碱 (批号110798-200805)、次乌头碱 (批号110799-201106)和地西泮 (批号115-9302)均购自中国药品生物制品检定所;乌头碱 (批号20120211)、苯甲酰乌头原碱 (批号20130105)、苯甲酰新乌头原碱 (批号20121210)、苯甲酰次乌头原碱 (批号20121210)、乌头原碱 (批号 20121210)和甘草酸 (批号20120910)均购自上海源叶生物科技有限公司;甘草苷 (批号ZL20120219GCG)和6-姜酚 (批号ZL20120422JF)均购自南京泽朗医药科技有限公司。次乌头原碱 (批号MUST-13061403)购自成都曼斯特生物科技有限公司。除次乌头原碱 (纯度≥90%)外,其余对照品纯度均≥98%。甲醇、乙腈 (色谱纯)购自美国TEDIA公司;其他试剂均为分析纯。水为去离子水。
2 方法与结果
2.1 液相条件 Agilent Eclipse XDB-C18色谱柱(4.6 mm ×150 mm,5 μm);流动相 A为含4 mmol/L乙酸铵和0.08%甲酸水溶液,流动相B为乙腈,梯度洗脱 (0~1 min,40%B;1~4 min,40%B~90%B;4~9 min,90%B;9.5~16 min,40%B)。体积流量0.8 mL/min;进样量10 μL;柱温30℃。
2.2 质谱条件 电喷雾离子源 (ESI),正离子扫描,离子源喷雾电压 (IS)3000 V,离子化温度(TEM)500℃,喷雾气压 (GS1)60 psi(1 psi=6.895 kPa),辅助气压 (GS2)60 psi。多反应检测(MRM)模式。11种被测成分的离子对、去簇电压 (DP)、碰撞能量 (CE)和碰撞室射出电压(CXP)见表1。

表1 四逆汤中11种指标成分的离子对和主要质谱参数Tab.1 Optimized structures parameters of eleven components in Sini Decoction
2.3 对照品溶液的制备 分别精密称取乌头碱、新乌头碱、次乌头碱、苯甲酰乌头原碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、乌头原碱和次乌头原碱适量,加入乙腈溶解并定容,摇匀,即得贮备液,-20℃冷藏备用。
精密称取甘草苷、甘草酸和6-姜酚适量,分别置于10 mL量瓶中,用甲醇溶解并稀释至刻度作为标准贮备液,4℃冰箱保存。
用乙腈溶解地西泮,制成质量浓度为0.25 mg/mL的内标贮备液,并用乙腈稀释至2.5 ng/mL。
2.4 四逆汤煎煮液的制备 依照《中国药典》2010年版中四逆汤处方比例,取各味饮片 (生附子30 g,干姜20 g,炙甘草30 g),加8倍量水,浸泡30 min,水沸后再煎30 min,趁热过滤,药渣加入6倍量水,同法煎煮30 min,合并两次滤液,减压浓缩至1 mL含0.2 g生药。平行制备3个批次,批号分别为20130921、20130923、20130925。4℃冰箱冷藏备用。将制得的汤剂至离心机中10000 r/min离心 10 min。
各样品进样分析前,与2.5 ng/mL地西泮内标乙腈溶液按体积比1∶3涡旋混合30 s,离心(10000 r/min)10 min,0.45 μm 的微孔滤膜滤过,按“2.1”项和“2.2”项下条件分析。
2.5 阴性对照溶液的制备 按配伍剂量及供试品溶液制备方法制备同时不含生附子、干姜、炙甘草的阴性对照溶液。
2.6 专属性 在该实验条件下,分别精密吸取混合对照品溶液、四逆汤煎煮液及阴性对照溶液各10 μL进样,结果显示阴性对照溶液未检测到干扰成分,按出峰顺序11种成分乌头原碱、次乌头原碱、甘草苷、苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、甘草酸、乌头碱、次乌头碱、6-姜酚和内标 (地西泮)的保留时 间 分 别 为 1.57、1.59、1.75、2.17、2.53、2.81、 3.68、 3.90、 5.05、 5.27、 7.77、8.14 min。色谱图见图1。
2.7 标准曲线的制备 精密量取各对照品溶液适量,用乙腈稀释成系列混合对照品溶液 (乌头碱、新乌头碱的质量浓度均为0.01、0.025、0.075、0.1、0.3、1、2.5 ng/mL;次乌头碱、苯甲酰次乌头原碱、乌头原碱和次乌头原碱的质量浓度均为0.1、0.25、0.75、1、3、10、25 ng/mL;苯甲酰乌头原碱的质量浓度为 0.05、0.125、0.375、0.5、1.5、5、12.5 ng/mL;苯甲酰新乌头原碱的质 量 浓 度 为 0.2、0.5、1.5、2、6、20、50 ng/mL;甘草苷的质量浓度为 6、15、45、60、180、600、1500 ng/mL;甘草酸的质量浓度为10、25、75、100、300、1000、2500 ng/mL;6-姜酚的质量浓度为 4、10、30、40、120、400、1000 ng/mL),按“2.1”项和“2.2”项下条件分析,以对照品质量浓度 (X)为横坐标,待测物峰面积As与内标峰面积Ais的比值 (Y)为纵坐标,作加权线性回归计算,结果表明各成分在相应的线性范围内线性关系良好 (见表2)。
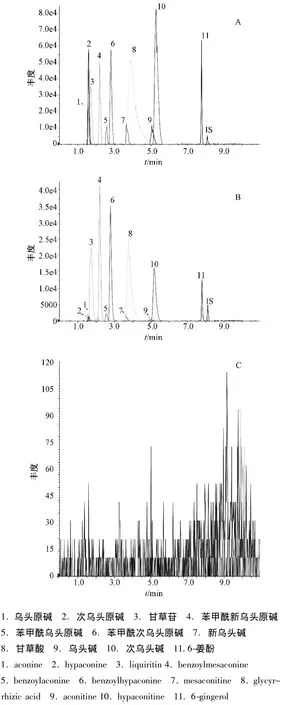
图1 11种混合对照品 (A)、四逆汤样品溶液 (B)和阴性供试品溶液 (C)的LC-MS/MS色谱图Fig.1 LC-MS/MS chromatograms of reference substances(A),Sini Decoction(B)and negative samples(C)

表2 四逆汤中11种化学成分的线性回归方程和相关系数Tab.2 Linear regression equations,correlation coefficients and quantitation limits of eleven components in Sini Decoction
2.8 精密度试验 精密吸取混合对照品溶液 (含乌头碱、新乌头碱均为0.30 ng/mL,次乌头碱、苯甲酰次乌头原碱、乌头原碱和次乌头原碱均为3.0 ng/mL,苯甲酰乌头原碱为1.5 ng/mL,苯甲酰新乌头原碱为6.0 ng/mL,甘草苷180 ng/mL,甘草酸300 ng/mL,6-姜酚120 ng/mL),按“2.1”项和“2.2”项下条件连续进样5次,将峰面积比值代入当天标准曲线计算浓度,求得精密度,结果表明仪器精密度良好,乌头碱、新乌头碱、次乌头碱、苯甲酰乌头原碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、乌头原碱、新乌头原碱、甘草苷、甘草酸和 6-姜酚的 RSD值分别为 2.1%、2.7%、2.8%、4.0%、3.5%、4.1%、3.3%、2.4%、4.0%、3.6%、1.7%。
2.9 重复性试验 同一批四逆汤样品,平行取样6份,按“2.4”项下方法制备供试品溶液,按“2.1”项和“2.2”项下条件分析,测定各化合物的量,结果乌头碱、新乌头碱、次乌头碱、苯甲酰乌头原碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、乌头原碱、新乌头原碱、甘草苷、甘草酸和6-姜酚的 RSD值分别为 1.9%、3.1%、2.8%、4.3%、5.5%、5.0%、3.3%、2.2%、3.0%、2.6%、1.4%,表明方法重复性良好。
2.10 稳定性试验 取四逆汤同一供试品溶液在室温下放置 0、2、4、8、12 h,按 “2.1”项和“2.2”项下条件分别进样分析,根据标准曲线计算,结果乌头碱、新乌头碱、次乌头碱、苯甲酰乌头原碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、乌头原碱、新乌头原碱、甘草苷、甘草酸和6-姜酚的RSD值分别为3.8%、2.2%、2.0%、4.0%、1.9%、1.8%、3.5%、2.0%、1.7%、0.92%、2.0%,表明样品溶液在12 h内稳定。
2.11 回收率试验 精密量取已知11种成分含有量的四逆汤水煎液,平行6份,分别加入上述混合对照品溶液适量 (每1 mL含乌头碱1.25 ng、新乌头碱3.12 ng、次乌头碱46.1 ng、苯甲酰乌头原碱14.9 ng、苯甲酰新乌头原碱110 ng、苯甲酰次乌头原碱52.4 ng、乌头原碱3.32 ng、次乌头原碱5.93 ng、甘草苷2501 ng、甘草酸4252 ng、6-姜酚755 ng),按照“2.4”项下制备供试品溶液,依法测定,结果乌头碱、新乌头碱、次乌头碱、苯甲酰乌头原碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、乌头原碱、次乌头原碱、甘草苷、甘草酸和6-姜酚的平均回收率为 103%、96.2%、101%、95.4%、 97.0%、 98.3%、 96.7%、 95.7%、99.4%、98.3%、100%,RSD分别为 2.1%、1.8%、1.3%、2.4%、3.5%、0.82%、1.5%、2.4%、2.7%、1.9%、2.3%,表明各成分加样回收率良好。
2.12 样品测定 精密吸取3个批次的四逆汤样品,每批样品平行测定 3次,按“2.1”项和“2.2”项下条件分析测定,以内标法计算各成分的量。结果见表3。
3 讨论
四逆汤是一首组方简单、疗效确切的经典方,临床应用广泛。由于中药复方是复杂体系,经多成分多途径协同作用而发挥药效,因此建立多组分同时定量的分析方法,对全面控制四逆汤的质量具有重要的意义。
表3 3个批次四逆汤中11种成分的测定结果(ng·mL -1,,n=3)Tab.3 Contents of eleven components in Sini Decoction(ng·mL-1,,n=3)

表3 3个批次四逆汤中11种成分的测定结果(ng·mL -1,,n=3)Tab.3 Contents of eleven components in Sini Decoction(ng·mL-1,,n=3)
头原碱20130921 0.54±0.02 1.33±0.13 19.2±1.44 6.35批号 乌头碱 新乌头碱 次乌头碱 苯甲酰乌±0.3620130923 0.62±0.01 1.42±0.09 18.0±1.32 5.72±0.2820130925 0.46±0.01 1.24±0.05 18.0±1.15 6.87±0.24批号 苯甲酰新乌头原碱苯甲酰次乌头原碱 乌头原碱 次乌头原碱20130921 45.0±2.54 21.8±0.87 1.33±0.09 2.41±0.2020130923 46.4±1.84 19.6±0.64 1.26±0.07 2.58±0.1620130925 48.4±1.95 20.4±1.05 1.21±0.06 2.64±0.14批号 甘草苷 甘草酸 6-姜酚20130921 1040±4.33 1742±5.26 320±3.2620130923 997±3.12 1800±5.55 324±2.2020130925 1024±3.56 1796±4.67 317±3.32
既往文献对四逆汤的活性成分大多采用高效液相色谱法进行检测,要求各种成分色谱峰完全分离,分析时间较长,多在30 min左右,并且最小检测质量浓度均在5 μg/mL以上[12-15]。而串联质谱法 (MS/MS)专属性强,灵敏度高,不要求各种成分色谱峰完全分离,快速高效。实验采用水提的方法对药材进行处理,而未采用《中国药典》中所述氨水润湿后以异丙醇-二氯甲烷 (1∶1)混合液溶解提取的方法,主要是考虑到此方法只是单纯的针对附子双酯型生物碱而言,而本课题主要应用于四逆汤方剂研究,所以采用煎煮法,保证与传统给药方案的一致性。本实验所建的色谱条件相对温和,梯度洗脱,以乙腈-水为流动相,可以有效降低系统压力。而且由于乌头类生物碱具有弱碱性,所以在水相中加入4 mmol/L乙酸铵和0.08%甲酸,能够明显缓解乌头碱的拖尾现象,实现对各个成分的分离。
本实验采用LC-MS/MS法,对四逆汤中乌头碱、新乌头碱、次乌头碱、苯甲酰乌头原碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、乌头原碱、次乌头原碱、甘草苷、甘草酸和6-姜酚进行同时定量分析,范围涵盖方剂中全部药味。该方法分离效果理想,精密度、重复性、稳定性、回收率均符合测定要求,耗时短,并且最低定量限为0.01 ng/mL,可用于活性成分含有量较低的相关研究,有利于进一步完善四逆汤的质量控制及相关研究。
[1]商李超,郁保生.四逆汤的药理作用研究进展[J].中西医结合脑血管病杂志,2009,7(11):1333-1335.
[2]赵明奇,吴伟康,赵丹洋,等.四逆汤对阿霉素性心衰的治疗作用及其机制探讨[J].中药材,2009,32(12):1860-1863.
[3]裴 卉,张宇忠,吴海燕,等.四逆汤对内毒素性休克大鼠脑组织肿瘤坏死因子-α及超氧化物歧化酶的影响[J].中华中医药杂志,2009,24(6):728-730.
[4]王 钰,马大勇,韩经丹,等.四逆汤不同折算剂量对失血性低血压大鼠缺血缺氧状态的影响[J].中华中医药杂志,2012,27(11):2802-2806.
[5]梁宇峰,杨镒宇,李木胜,等.四逆汤对脓毒症大鼠心肌细胞线粒体损伤的影响[J].中药材,2012,35(5):776-779.
[6]孙慧兰,吴伟康,罗汉川,等.四逆汤有效部位抗心肌缺血/再灌注损伤神经酰胺机制的研究[J].中成药,2005,27(12):1429-1434.
[7]谭光国,朱臻宇,李 翔,等.中药复方四逆汤化学成分的RRLC-TOF/MS分析[J].药学实践杂志,2009,27(4):270-273.
[8]Singhuber J,Zhu M,Prinz S,et al.Aconitum in traditional Chinese medicine—a valuable drug or an unpredictable risk[J].J Ethnopharmacol,2009,126(1):18-30.
[9]Ali B H,Blunden G,Tanira M O,et al.Some phytochemical,pharmacological and toxicological properties of ginger(Zingiber officinale Roscoe):A review of recent research[J].Food Chem Toxicol,2008,46(2):409-420.
[10]Asl M N,Hosseinzadeh H.Review of pharmacological effects of Glycyrrhiza sp.and its bioactive compounds[J].Phytother Res,2008,22(6):709-724.
[11]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:650.
[12]孙婷婷,栾立标.HPLC分离测定四逆汤中3种双酯型生物碱及其6种水解产物[J].中国中药杂志,2006,31(19):1634-1638.
[13]刘 晓,范林乾,蔡 皓,等.HPLC同时测定四逆汤中4种指标性成分的含量[J].中国中药杂志,2012,37(6):803-805.
[14]刘 敏,张 海,蔡亚梅,等.高效液相色谱法同时测定四逆汤中6个指标性成分[J].第二军医大学学报,2013,34(6):682-686.
[15]李 莹,章津铭,傅超美,等.不同方法制备四逆汤中化学成分对比研究[J].中成药,2012,34(4):673-678.

