3,5-二甲基苯酚的合成与应用
方东兵,冯柏成
(青岛科技大学 化工学院,山东 青岛 266042)
3,5-二甲基苯酚又名5-羟基间二甲苯,是一种重要的精细化工原料及有机合成中间体,其主要合成方法:①苯酚烷基化法[1],使用苯酚与甲醇为原料,通过高温烷基化反应得到目的产物。该方法操作简单,仅需一步反应即可完成,但是反应选择性低,只有30%左右,且反应生成的副产物难以分离,因此该方法不能满足实际生产应用的需要;②间二甲苯磺化碱熔法[2-3],这是3,5-二甲基苯酚的传统生产方法。以间二甲苯为原料,经过磺化、碱熔以及酸化,得到最终产品。该方法用于生产3,5-二甲基苯酚收率可达到60%左右并且产品纯度较高,但是工艺过程复杂,并且最大的问题在于反应过程的进行主要依赖强酸强碱的作用,对设备的腐蚀和环境的污染都十分严重,并不符合当前绿色化学的要求;③是异佛尔酮芳构化法[4],以异佛尔酮为原料,在高温(350 ~400 ℃)下反应生成3,5-二甲基苯酚。该方法具有操作简单的优点,但是由于异佛尔酮在高温下会发生酚酮的重排[5],产物中除了3,5-二甲基苯酚和甲烷,还会有异佛尔酮的分解产物,比如均三甲苯、间甲酚、双丙酮醇等。
3,5-二甲基苯酚作为重要的精细化工原料及有机合成中间体,主要有以下几种重要的应用。①制备酚醛树脂粘合剂和酚·脲·醛树脂粘合剂[6-8],这种树脂是不仅对木材同时也对玻璃、陶瓷、纸类、皮革和金属等许多材料都有很好的粘合作用,是一种应用非常广泛的树脂粘合剂。②用于生产杀菌剂,消毒剂等产品[9],其中4-氯-3,5-二甲基苯酚就是较为重要的一种产品。这是一种具有独特的杀菌性和防腐性,并能使两种性能达到良好结合的消毒杀菌剂,被认为是高效、安全、广谱的杀菌剂。③用于合成杀虫剂[10],例如3,5-二甲基苯酚和氨基甲酸反应可以制得灭除威。灭除威是一种高效低毒的杀虫剂,对高等动物毒性中等,对鱼类毒性小,具有触杀作用强,速效性强,残效期短(只需要2 ~3 d)和药效不易受温度变化影响等优点,是当今应用相当广泛的杀虫剂之一。④用于合成维生素E[11]。3,5-二甲基苯酚作为合成保健品维生素E 的原料,近些年已经引起了人们越来越多的关注。用它合成的维生素E,就广泛用于保健品、药品、食品添加剂、化妆品及营养剂中。
本研究采用异丙基间二甲苯氧化分解法合成3,5-二甲基苯酚。该方法以工业上成熟的异丙苯法生产苯酚丙酮工艺为原型,首先通过反应原料间二甲苯与异丙醇的烷基化反应,得到5-异丙基间二甲苯,然后通过氧化酸解工艺得到3,5-二甲基苯酚和丙酮。
1 实验部分
1.1 试剂与仪器
间二甲苯、异丙醇、三氯化铝、偶氮二异丁腈(AIBN)、N-羟基邻苯二甲亚酰胺(NHPI)、乙腈、浓硫酸、丙酮均为分析纯。
精密增力电动搅拌器;恒温油浴;高效液相色谱仪;DAD230 紫外检测器;Varian 3800 气相色谱仪;Bruker500M 型核磁共振仪。
1.2 实验方法
1.2.1 烷基化 向带有温度计、回流冷凝管、滴液漏斗和搅拌装置的250 mL 四口烧瓶中加入74.88 g间二甲苯,搅拌下加入13.34 g 三氯化铝,用冰水降至10 ℃以下,慢慢滴加含异丙醇6.01 g 与间二甲苯10 g 的混合液,不断搅拌,滴完继续反应30 min,然后用恒温油浴升温至70 ℃反应7 h。反应结束后,水解,分液,取油相。将油相减压精馏,得到产品9.83 g,收率为75%。其结构通过NMR 确认,纯度通过气相色谱分析,确定产品纯度为90%。
1.2.2 氧化反应 向带有温度计、回流冷凝管和磁力搅拌装置的250 mL 四口烧瓶中加入蒸馏得到的5-异丙基间二甲苯纯净物30 g,乙腈200 mL,搅拌下加入NHPI 3.26 g,AIBN 1 g,使其全部溶解。然后升温至50 ℃,通入空气,空气流速为600 mL/min,不断搅拌。反应过程中使用液相检测,控制氧化反应深度为15%,反应16 h 后停止。将反应液减压蒸馏,过滤,得反应液23 g。
1.2.3 酸解反应 向带有温度计、回流冷凝管和搅拌装置的250 mL 四口烧瓶中加入氧化反应液20 g,搅拌下加入浓硫酸0.5 g、丙酮49.5 g 的混合溶液。然后将反应液升温至50 ℃,不断搅拌反应2 h。反应产物进行液相色谱分析并与标准品对照确定结构。
2 结果与讨论
2.1 烷基化反应
间二甲苯与异丙醇的反应属于傅-克烷基化反应,间二甲苯芳环上的氢原子被异丙基取代,而在逆向傅-克反应或者称之为傅-克去烷基化反应过程中异丙基同样可以在路易斯酸的存在下去除。本反应中,间二甲苯上甲基的存在提高了苯环的活性,使异丙基的烷基化更容易进行,同时由于甲基的定位效应,异丙基优先进入苯环上的邻位或对位,生成4-异丙基间二甲苯。但是由于异丙基的空间位阻较大,间位产物比起邻对位产物具有较小的空间位阻,因此热力学控制该反应产生热力学上更稳定的间位产物,最终在一系列烷基化与去烷基化共同作用的结果下,反应形成稳定产物5-异丙基间二甲苯。
2.1.1 催化剂对烷基化反应的影响 本实验中分别实验了三氯化铝、三氯化铁、浓硫酸、磷酸的催化效果。实验结果见表1。

表1 催化剂对反应转化率和选择性的影响Table 1 The influence of catalyst on the reaction conversion and selectivity
由表1 可知,三氯化铁以及浓磷酸对反应没有明显的催化效果。三氯化铝以及浓硫酸的催化效果较好,原料的转化率较高。但是浓硫酸作为催化剂,反应的选择性较差,副产物较多,主产物的选择性只有75%左右。而三氯化铝选择性可以达到90%,转化率可达到75%以上。因此,选择三氯化铝作为该反应的催化剂是较为合适的。
2.1.2 反应温度对烷基化反应的影响 反应温度对烷基化反应有明显影响。当温度过高时,反应会生成包括4-异丙基间二甲苯在内的多种副产物。而当反应温度过低时,反应速率较慢,反应所需时间大大延长。本实验在40 ~100 ℃的范围内分别选择40,50,60,70,80 ℃进行考察,结果见图1。

图1 反应温度与收率的关系Fig.1 The relation of reaction temperature and yield
由图1 可知,在相同的反应时间内,40 ℃时产物的收率只有43%,随着温度的提高,产品的收率也在提高。在70 ℃时达到75%以上。继续升高温度,产品收率开始下降。这是由于过高的温度导致了副反应的发生,虽然原料转化率在提高,但是反应的选择性在下降,最终导致了反应收率的下滑。结果表明,70 ℃是较好的反应温度,此时反应的转化率较高、选择性较好。
2.1.3 反应时间对烷基化反应的影响 依前述所选出的最佳条件,在70 ℃下反应8 h,反应4 h 后每隔1 h 取样进行分析,结果见图2。
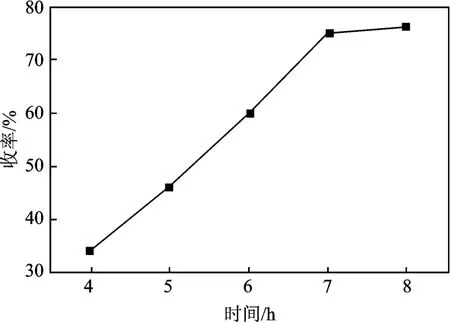
图2 反应时间与收率的关系Fig.2 The relation of reaction time and yield
由图2 可知,随着反应时间的延长,产品收率逐渐提高,5 ~7 h 内收率提高较快,表明此时反应速度较快。反应至7 h 时收率达到75%。随后反应速度开始减慢,收率变化较小。因此从反应效率的角度考虑,7 h 的反应时间是比较合适的。
2.2 氧化反应
5-异丙基间二甲苯的氧化反应是自由基引发的链式反应,其主要根据是该反应存在诱导期,若是存在能够解离成自由基的物质,则氧化反应的反应速度会加快,反应时间会大大缩短;若是存在酚类等杂质,氧化反应的反应速度会减慢,甚至可能停止。此外,对于该氧化反应,当反应温度较高或者反应时间较长时,会有醇类或酮类副产物的出现[12]。因此在反应过程中要严格控制反应时间和反应温度,以此来达到控制氧化反应深度的目的,最终得到选择性较好的目的产物。
2.2.1 引发剂的影响 自由基链式反应大致可分为三步:链的引发、链的增长以及链的终止[13]。其中链引发是控制反应时间的关键,选择合适的引发剂可以大大的缩短链引发的时间,从而减少反应所需的时间。
根据文献报道,选择偶氮二异丁腈(AIBN)作为该反应的引发剂。考察了在50 ℃,空气流量为600 mL/min的反应条件下,引发剂对反应的影响,结果见图3。

图3 引发剂对氧化反应收率的影响Fig.3 The influence of the initiator on the oxidation reaction yield
由图3 可知,当没有引发剂加入时,反应进行20 h 仍无过氧化物产生;而加入引发剂,4 h 后氧化反应就开始发生,过氧化物含量迅速增加,反应时间为12 h 时,反应转化率达到10%。可以看出,引发剂的加入对加快反应速度有重要作用。因为自由基链式反应,其反应速度主要受链引发反应速率的影响,而引发反应的活化能很高,引发剂或催化剂的存在可以降低活化能,加快引发速度。偶氮类引发剂反应稳定,是一级反应[13],容易控制,对加快氧化反应有很好的作用。因此,选择偶氮二异丁腈作为该反应的引发剂。
2.2.2 反应时间的影响 气液两相反应需要经过扩散和反应两个阶段来完成[14],所以需要一定的反应时间,如果反应时间不足,则气液两相没有完全反应,反应物转化率较低,如果反应时间过长,则会促进副反应的发生,虽然反应转化率较高,但选择性较差。

图4 反应时间对氧化反应转化率的影响Fig.4 The influence of reaction time on the oxidation reaction conversion
由图4 可知,5-异丙基间二甲苯的转化率是随着反应时间的增加而增加的,从反应开始至20 h,反应速度较快,在反应时间超过20 h 之后反应速度有所下降,此时原料转化率达20%以上,反应24 h,5-异丙基间二甲苯的转化率达到25%以上;反应时间较短时,5-过氧化氢异丙基间二甲苯的选择性较好,约为90%。随着反应的进一步进行,选择性逐渐下降,副反应增多。因此,为了得到较好的反应选择性,就需要控制反应时间来控制反应的转化率。研究发现,16 h 是原料转化率和产物选择性的较好契合点,是适当的反应时间,此时5-异丙基间二甲苯转化率为15%左右,选择性可以达到85%以上。
2.2.3 反应温度的影响 反应温度是影响氧化反应方向和氧化深度的重要因素。本研究中考察了40,50,60,70 ℃下反应的不同变化,见图5。
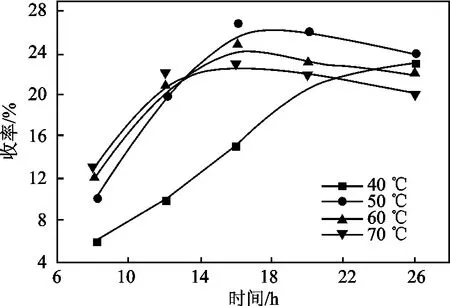
图5 反应温度与氧化反应收率的关系Fig.5 The relation of reaction temperature and yield
由图5 可知,反应时间在12 h 以内,产品的收率随着反应温度的升高而增加,因为反应温度越高,氧化反应越剧烈,氧化速度越快。但是当反应时间达到12 h 时,氧化反应情况出现分化,60,70 ℃下,产品收率开始下降,因为此时发生了氧化产物的热分解反应,生成相应的苄醇和间二甲基苯乙酮等副产物,引起了产品收率的下降。40 ℃和50 ℃下,反应进行至16 h 时,产品收率也出现收率下降的情况。这说明,副反应开始的时间与反应温度有关,温度越高,副反应开始的也越早。另外,在反应过程中,当反应温度较高时,溶剂乙腈会大量挥发,不利于反应溶剂的回收利用。当温度较低时,氧化反应的速度较慢,在较长的反应时间内也无法达到理想状态。因此总体来说,50 ℃是较为理想的反应温度,在此温度下,反应转化率平稳上升,反应选择性可以保持在85%以上。
2.3 酸解反应
过氧化氢物在酸催化条件下生成3,5-二甲基苯酚和丙酮,根据反应条件的变化,也有可能生成醇、烯等副产物。本实验从反应温度,催化剂用量,反应时间三个方面考察了各因素对酸解反应的影响之后得出:当温度为50 ℃,催化剂浓硫酸用量为2.5%,硫酸丙酮溶液浓度为1%,反应时间2 h 时,3,5-二甲基苯酚的收率可达到80%。
3 结论
本论文通过异丙基间二甲苯氧化酸解法,使用间二甲苯与异丙醇为原料,实现3,5-二甲基苯酚的新法合成。其优化的合成工艺条件如下:①烷基化工艺条件:原料摩尔比n(间二甲苯)∶n(异丙醇)∶n(三氯化铝)=8∶1∶1,反应温度为70 ℃,反应时间为7 h,在此工艺下产品收率为75%,纯度为90%;②氧化工艺条件:5-异丙基间二甲苯30 g,NHPI 3.26 g,AIBN 1.0 g,乙腈200 mL,空气流速为600 mL/min,反应温度50℃,反应时间16 h;③酸解工艺条件:氧化反应液20 g,浓硫酸与丙酮混合液50 g(浓硫酸质量分数为5%),反应温度为50 ℃,反应时间为2 h。
3,5-二甲基苯酚作为重要的精细化工原料和有机合成中间体,其用途十分广泛,市场需求量很大。而异丙基间二甲苯氧化分解法生产3,5-二甲基苯酚,是一种绿色安全的新型合成方法,其原料利用率高,对环境污染小,符合当前绿色化学的要求,是对已有合成工艺的有效补充。
[1] 于金刚.异佛尔酮催化芳构化法制备3,5-二甲基苯酚[D].天津:天津大学,2006.
[2] 章思规,章伟.精细化学品及中间体手册(下卷)[M].北京:化学工业出版社,2000:1831.
[3] 徐克勋.精细有机化工原料及中间体手册[M].2 版.北京:化学工业出版社,1999.
[4] Paul H,Berkeley,Seaver A.Production of phenolic compounds:US,2369196[P].1942-07-13.
[5] 金姬.间二异丙苯氧化合成间苯二酚[D].大连:大连理工大学,2010.
[6] Yomoto Masatoshi.Antimicrobial phenolic resin molding materical:JP,11189503[P].1999-07-13.
[7] Miyagl Sachiko,Maeda Toyohiko,Masuda Toru.New trisphenol compound:JP,10218815[P].1998-08-18.
[8] Mcallister L,Dietrich H.Fire retardant polymer resin:US,4471089[P].1984-09-11.
[9] 汤凤,黄洪.3,5-二甲基苯酚的合成与分离[D].广州:华南理工大学,2005:1-75.
[10]姜红宇,张敏,湛雪辉.3,5-二甲基苯酚的新法合成[J].湖南科技学院学报,2009,29(12):42-44.
[11]洪记.维生素E 开发应用现状及发展趋势[J].江苏化工,2000,28(6):7-10.
[12]刘佳.间二异丙苯氧化制备间苯二酚[D].北京:北京化工大学,2009.
[13] Eiichi Yonemitsu,Takeo Igarashi.Process for preparing hydroperoxide:US,4013725[P].1977-03-22.
[14]史福涛,陈标华.仲丁基苯氧化分解生产苯酚丁酮的研究[D].北京:北京化工大学,2011.

