高能叠氮基OS(N3)2的几何结构与稳定性研究
张国华,张影,李晶,刘芳
哈尔滨理工大学应用科学学院
高能叠氮基OS(N3)2的几何结构与稳定性研究
张国华,张影,李晶,刘芳
哈尔滨理工大学应用科学学院
本章利用高斯软件对OC(N3)2分子的合成与分解路径进行研究,计算其几何结构,并通过振动频率分析确定基态结构。通过对各个分子势能曲面的研究确定分解与异构通道,从而确定稳定性。
该项目是由黑龙江省教育厅科技项目(No.12541172)资助
1、简介
高能量的含氮分子因其具有较多的N-N单键和双键,从而具有较高的能量储备,当分子分解时单键和双键变成三键,而放出较高的能量,这种性质叫做高能量密度性质。叠氮基化合物就是其中的一种。通过对含氟或含氯分子进行N3取代,就能够形成叠氮基化合物。
2、计算方法
本章利用密度泛函(DFT-B3LYP)对OS(N3)2分子结构优化和振动频率的计算。谐振频率的计算用来确定稳定结构(全正频)以及过渡结构(有一个负频),并且提供零点振动能修正(0.9806修正)。对势能面的分子内禀反应路径(IRC)计算能够确定合成与分解反应的反应路径和反应产物。所有计算结果都是利用Gaussian 03软件包得到的。
3、结果与讨论
(1)、OS(N3)2的合成
首OS(N3)2的合成是通过用HN3中的N3基团取代OSCl2中的Cl原子来实现的,我们对该合成路径所涉及的物质进行结构优化,各物质的对称性、能量以及相对能列于表1,几何结构列于图1。
OSCl2是Cs对称性的非平面分子,与HN3反应时N3基团与H原子分离,N3基团取代其中一个Cl原子,生成一个OSClN3分子,同时产生一个气态的HCl分子。OSClN3分子中叠氮基N3基团的N-N键长为1.121和1.241Å,介于双键和三键之间,当期N-N键断裂释放氮气过程中将会放出巨大能量。OSClN3分子与HN3进一步反应,另一个Cl原子也将被取代,生成一个OS(N3)2分子和一个气态HCl分子。
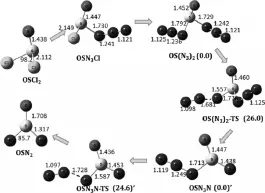
图1 .OS(N3)2分子合成与分解路径上所涉及物质的几何结构及相对能
(2)、OS(N3)2的稳定性分析
为了确定OS(N3)2分子的动力学稳定性,我们对其势能曲面进行系统计算,确定其分解路径,找到其分解过渡态结构,如图1。OS(N3)2中的一个N3基团的一个N-N键长由1.236Å增加到1.681Å(如图1中的OS(N3)2-TS,过渡结构),接下来将会释放一个N2分子。该分解反应势垒为26.0kcal/mol,说明OS(N3)2具有较高的动力学稳定性,在试验中一旦合成,将不易分解。
4、结论
1、OS(N3)2分子可以由OSCl2分子和2个HN3分子的取代反应来合成。
2、OS(N3)2分子可以通过增加N-N键长来释放氮气从而放出巨大能量,分解势垒分别为26.0 kcal/mol和24.6 kcal/mol,说明该叠氮基分子具有较理想的动力学稳定性,在实验室中合成稳定性较理想,不易分解,具有较好的应用价值。
[1]王广厚.物理学的新进展[M].物理学进展,1994,14(2):121~172.
[2]冯端,金国钧.凝聚态物理学新论.上海科学技术出版社. 1992:286~292.
[3]S.Herler,P.Mayer,H.Nöth,A.Schulz,M.Suter,M.Vogt. S2N3+:An Aromatic SN Cation with an N3 Unit.Angew.Chem.Int. Ed.2001,40:3173~3175.
[4]【美】J.A.波普尔,D.L.贝弗里奇,江元生译《分子轨道近似方法理论》.科学出版社,1978.

