2-乙酰基吡啶缩异烟酰腙稀土配合物合成、表征与荧光性能研究
乔秀丽,田军,董艳萍
(绥化学院 食品与制药工程学院,黑龙江 绥化 152061)
Schiff 碱是一类重要的有机配体[1-2],易于制备、结构灵活易变,是配位化学研究的重点内容之一。许多Schiff 碱及其配合物在催化、生物模拟、医药、化学分析、金属防腐、发光材料、传感器中有广泛的应用[3]。发光材料应用较多的为荧光,比如荧光免疫分析[4]等方面都表现出诱人的应用前景,从而吸引了越来越多的研究者的关注[5-7]。
Schiff 碱结构多样,种类繁多,可分为单和双席夫碱、大环席夫碱、对称和不对称席夫碱、含杂环席夫碱、含硫及酰腙类席夫碱等。其中酰腙类席夫碱与金属的配位能力强而且热稳定性高,有些还具有抗癌、抗菌、抗病毒等作用[8-11]。吡啶类化合物具有较好的生理活性[12-13]。利用2-乙酰基吡啶与异烟酰肼反应合成的schiff 碱,含有双吡啶杂环,不仅具有丰富的配位方式,而且其配合物在发光方面可能具有潜在应用价值。
本文合成了Ce(III)、Nd(III)的2-乙酰基吡啶缩异烟酰腙的配合物,并对其进行了结构表征,同时研究了它们热稳定性,为进一步深入研究奠定了基础。
1 实验部分
1.1 试剂与仪器
异烟酰肼、2-乙酰吡啶、无水乙醇、冰醋酸、硝酸铈、硝酸钕等均为分析纯。
Elmentar Vario EL 元素分析仪;DDS-307A 型电导仪;NETZSCH STA 409 PC 型综合热分析仪;Nicolet Avater-360 型FTIR 红外光谱仪;岛津UV-260 型紫外-可见分光光度计;Varian CARY/Eclipse 型荧光分光光度计。
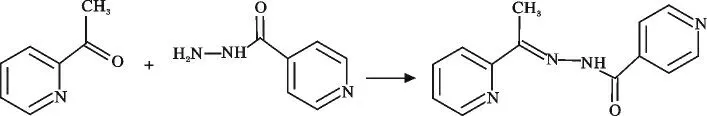
1.2 2-乙酰基吡啶异烟酰腙配体(L)的合成
取2.742 8 g 异烟酰肼溶于50 mL 无水乙醇,在室温下搅拌,滴加2.47 mL 2-乙酰吡啶,以醋酸为催化剂,加热回流2 h。冷却至室温析出白色固体,抽滤,并用无水乙醇重结晶,室温下真空干燥2 d。产率约为37%,m. p. 173. 3 ~175. 2 ℃。元素分析(C13H12N4O),实 测 值/计 算 值(%):C 64. 91/64.99,H 4.98/5.03,N 23.29/23.32。
1.3 Ce(III)、Nd(III)配合物的制备
将0.245 3 g 配体L 溶于40 mL 无水乙醇中,加热搅拌下滴加10 mL 含有1 mmol Ce(NO3)3·6H2O的无水乙醇溶液,在70 ~75 ℃下回流2 h。冷却,过滤。产物用无水乙醇洗涤2 次,真空干燥,配合物记作(1)。
Nd(III)配合物的制备方法同上,得Nd(III)配合物(2)。
配合物(1)的元素分析(C26H24CeN11O11),实测值/计算值(%):C 38. 59/38. 71,H 2. 91/3. 00,N 19.02/19.10。摩尔电导为124.23 s·cm2/mol。
配合物(2)的元素分析(C26H24NdN11O11),实测值/计算值(%):C 38. 40/38. 52,H 2. 96/2. 98,N 18.89/19.00。摩尔电导为129.67 s·cm2/mol。
2 结果与讨论
2.1 红外光谱特征
用KBr 压片,在4 000 ~400 cm-1范围扫描,主要红外光谱数据见表1。
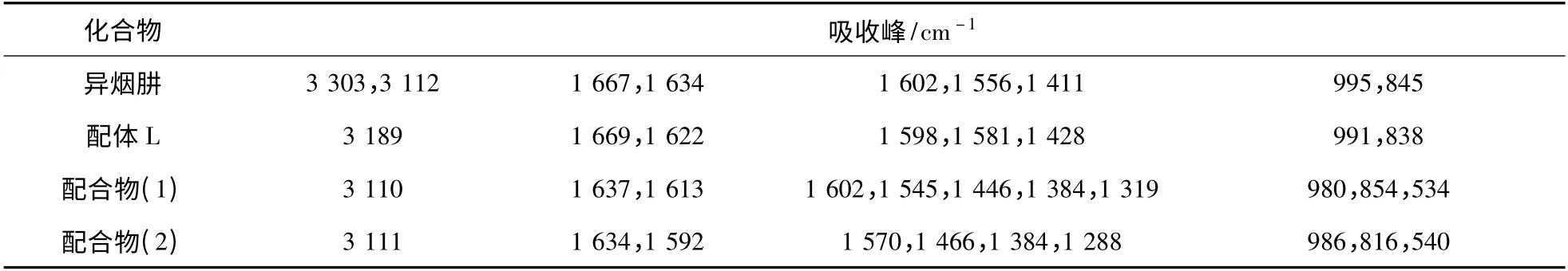
表1 化合物的IR 主要数据Table 1 IR data of the compounds
由表1 可知,L 的IR 谱图3 303 cm-1属于伯胺基(—NH2)的伸缩振动,1 634 cm-1为—NH2面内弯曲振动。3 112 cm-1归属于仲酰胺(—CONH-)的ν(NH)吸收峰,羰基的伸缩振动ν(C O)则出现在1 667 cm-1。在配体的IR 光谱中,—NH2的ν(NH2)和δ(NH2)均消失,说明酰肼的—NH2与乙酰基的吡啶 CO发生了反应,有新键产生。
在两个配合物中,1 634 ~1 637 cm-1属于CO的伸缩振动,与配体1 669 cm-1相比,明显红移了35 ~32 cm-1,说明 CO氧原子参与了配位。所有化合物在3 110 cm-1处都有较强的吸收峰,这是亚胺基(NH)的特征。在配体中,1 622 cm-1属于CN的伸缩振动,形成了配合物后分别红移至1 613,1 592 cm-1,说明亚胺基参与配位。Ce(III)配合物中的1 446,1 319 cm-1以及Nd(III)配合物中的1 466,1 288 cm-1一组吸收峰,说明含有单齿配位的硝酸根。配合物的摩尔电导均大于120 s·cm2/mol,说明配合物属于1∶2 型电解质,因此在IR 光谱中的1 384 cm-1处出现了一个很强的游离的硝酸根的伸缩振动。534 ~540 cm-1处新生产的弱吸收峰是由Ln—O 键产生的,从而进一步证明了 C O与金属配位。
2.2 紫外光谱特征
以DMSO 为溶剂,在190 ~500 nm 扫描范围内测定配体及其配合物的紫外光谱,结果见图1、表2。
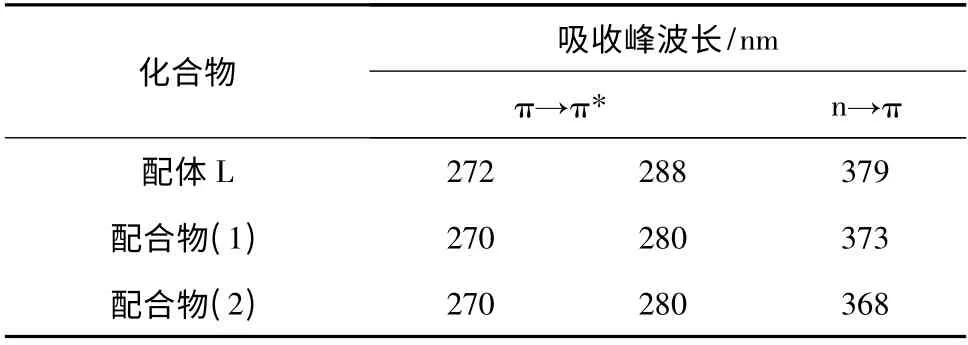
表2 配体和配合物在DMSO 溶剂中的紫外光谱数据Table 2 UV data of the ligand and complexes in DMSO
在电子吸收光谱中未出现稀土离子的特征吸收峰,说明配合物的紫外吸收特性主要取决于配体。
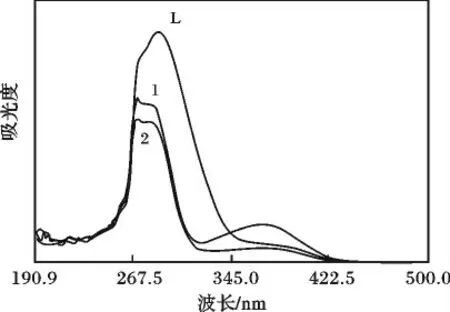
图1 配体及其配合物的紫外光谱Fig.1 UV curve of the ligand and complexes
2.3 荧光光谱
在室温下,以DMF 为溶剂,测定了配体和配合物溶液的荧光光谱,结果表明配体和其稀土配合物都不具有发光性质。原因可能是稀土离子Ce3+、Nd3+都是顺磁性的离子,本身对荧光具有淬灭作用,因此,它们形成的配合物发光性能较弱。
在配体的溶液中加入氯化铝之后,呈现出很强的紫色荧光,激发波长为367 nm 时,最大发射波长为456 nm(图2),属π*→n 的电子跃迁。其原因可能是配体与Al3+形成配合物后,使分子的共平面程度增大、刚性增强,从而提高了荧光量子效率。因此,如果更换其他的金属离子,选择合适的金属离子,可能设计合成新的发光材料。
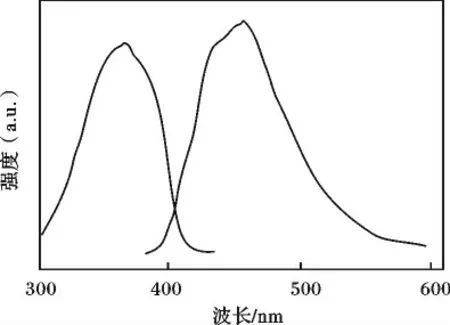
图2 L-AlCl3 体系的激发光谱(λex =367 nm)和发射光谱(λem =456 nm)Fig.2 The excitation and emission spectra of L-AlCl3 in DMF
2.4 配体及配合物的热分析
由图3 可知,Schiff 碱配体L 在180 ℃之前无失重现象,170 ℃左右有一尖锐的吸热效应峰,与配体的熔点相符。在226 ℃开始快速失重,发生有机挥发,部分炭化,324 ℃左右伴随着出现一个最大吸热效应,最终残重为7.9%。

图3 配体L 的热重分析图Fig.3 The curve of ligand

图4 Ce 配合物的热分析图Fig.4 The curve of Ce complex
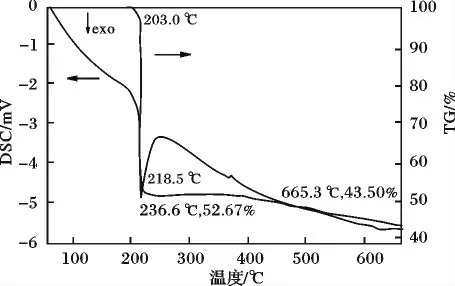
图5 Nd 配合物的热分析图Fig.5 The curve of Nd complex
由图4、图5 可知,两个配合物热分解行为非常相似,Ce(III)配合物从室温~229 ℃前为恒重,Nd(III)配合物从室温~203 ℃前为恒重,而且都没有热效应峰,说明两个配合物中均不含有结晶水或配位水。配合物热失重分解均分为两个阶段,Ce(III)配合物在229.2 ℃时开始放热分解,最大放热峰对应的温度为244.4 ℃,到272.1 ℃时失重51.65%,在272.1 ~667.2 ℃,失重10.98%,667.2 ℃以后恒重,残重为38.37%。Nd(III)配合物在203.0 ℃时开始放热分解,最大放热峰对应的温度为218.5 ℃,到236.6 ℃时失重47.33%,在236.6 ~665.3 ℃,失重9.17%,665.3 ℃以后恒重,残重为43.50%。
由热分析图可知,配合物的热稳定性与配体相比均有所下降,原因主要是硝酸根离子具有一定的氧化性,而从Schiff 碱的结构可以看出,其具有还原性,当温度升高到一定程度时,二者可迅速发生氧化还原反应,二者分解的温度均>200 ℃,说明该类配合物仍有较高的热稳定性。
3 结论
(1)合成了2-乙酰基吡啶酰腙Schiff 碱(C12H12ON4)及两个稀土配合物,分别对其进行元素分析、电导率测定及红外光谱、紫外光谱、荧光、热分析等表征,可以初步确定配合物的组成为[Ln-(L2)(NO3)]·2NO3,Ln=Ce(III)和Nd(III),推测配合物配位结构如下。
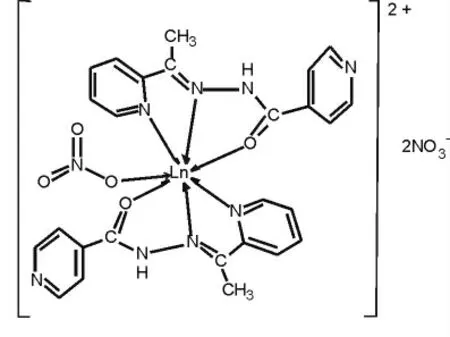
(2)该法合成的Schiff 碱本身不具有发光性能,但是如果选择合适的金属离子,比如Al3+,可以发出强紫色荧光,因此合理的选择金属离子则有可能设计合成出结构新颖、性能优良的发光材料,为发光材料的选择提供了理论指导。
[1] 康信煌,杨志斌.新希夫碱SAAQ 合成及其分析应用的研究——分光光度法测定镓[J]. 化学试剂,1993,15(1):17-18.
[2] Handa S,Gnanadesikan V,Matsunaga S,et al.Syn-selective catalytic asymmetric nitro-mannich reactions using a heterobimetallic Cu-Sm-Schiff base complex[J]. J Am Chem Soc,2007,129:4900-4901.
[3] 蔡红新,叶行培,吴伟娜,等. 两个喹啉氧基乙酰胺的镧系(La、Pr)配合物的合成、表征及荧光性质[J]. 无机化学学报,2014,30(9):2134-2140.
[4] 冯婧,周亮,王卓,等.具有超顺磁和可见/近红外发光性质的双功能介孔磁/光纳米复合材料[J]. 发光学报,2013,9(34):1103-1107.
[5] 杨正银,杨汝栋. 邻羟基苯甲醛苯甲酰腙稀土配合物的合成和抗氧化活性[J]. 中国稀土学报,2007,20(4):366-369.
[6] Occhipinti G,Jensen V R,Bjorsvik H R.Green and efficient synthesis of bidentate Schiff base Ru catalysts for olefin metathesis[J].J Org Chem,2007,72:3561-3564.
[7] 陈凤英,曹文凯,何水样,等.RE(III)与二羰基丙酸水杨酰腙配合物的合成、表征和热化学[J].物理化学学报,2006,22(3):280-285.
[8] Brooker S,Sunatsuki Y,Motoda Y,et al.Copper complexes with multidentate schiff base ligands containing imidazole groups:ligand-complex or self-complementary molecule[J].Coord Chem Rev,2002,226:199-209.
[9] Yang X P,Jones R A,Michael M O,et al. Near infrafed luminesccnce and supramolecular structure of a helical triple-decker Yb (III)Schiff base cluster[J]. Cryst Growth des,2006,6:2122-2125.
[10]Paola V,Matteo I,Irini A D,et al.Synthesis and antiproliferative activity of benzo[d]isothiazole hydrazones[J].Eur J Med Chem,2006,41:624-632.
[11]丁瑜,刘志伟,张忠海,等.席夫碱三核锌(II)配合物的晶体结构及荧光活性研究[J]. 化学学报,2007,65(8):688-692.
[12]丁瑜,张忠海,胡宗球,等. 水杨醛缩水杨酰肼晶体结构电化学性质[J].无机化学学报,2006,22(7):1187-1190.
[13]Patricia M,Virginie L,Christian S,et al.Synthesis and in vitro antimalarial activity of an acylhydrazone library[J].Bioorg Med Chem Let,2006,16:31-35.

