替加环素治疗泛耐药鲍曼不动杆菌医院获得性肺炎的临床疗效及不良反应
王凯歌,谭 芬,彭 红,陈 平
(中南大学湘雅二医院 湖南省呼吸疾病诊疗中心 中南大学呼吸疾病研究所,湖南 长沙 410011)
·论著·
替加环素治疗泛耐药鲍曼不动杆菌医院获得性肺炎的临床疗效及不良反应
王凯歌,谭芬,彭红,陈平
(中南大学湘雅二医院 湖南省呼吸疾病诊疗中心 中南大学呼吸疾病研究所,湖南 长沙410011)
[摘要]目的观察替加环素对泛耐药鲍曼不动杆菌(XDRAB)医院获得性肺炎(HAP)的临床疗效及不良反应。方法对2013年3月—2014年6月某院重症监护病房(ICU)发生XDRAB HAP并使用替加环素治疗的患者临床资料进行回顾性分析。结果31例HAP患者痰分离的XDRAB对替加环素均敏感,对碳青霉烯类及舒巴坦类抗生素,包括头孢哌酮/舒巴坦(SCF),耐药率为100%,其中混合感染患者17例(54.84%)。替加环素联用SCF使用率:呼吸ICU组为85.71%(12/14),中心ICU组为47.06%(8/17)。31例患者,临床痊愈率为29.03%、有效率为45.16%,细菌清除率为61.29%,药物不良反应率为16.13%,无严重药物不良反应发生。呼吸ICU组与中心ICU组痊愈率分别为42.86%、17.65%,有效率分别为71.43%、23.53%,细菌清除率分别为78.57 %、47.06%,两组临床有效率比较,差异具有统计学意义(P<0.05)。替加环素联用SCF组与非联用SCF组痊愈率分别为35.00%、18.18%,有效率为60.00%、18.18%,细菌清除率为65.00%、54.55%,两组临床有效率比较,差异具有统计学意义(P<0.05)。结论替加环素对XDRAB HAP具有良好的临床疗效,药物不良反应少;联合SCF是一个值得推广的选择。
[关键词]替加环素; 泛耐药鲍曼不动杆菌; 医院获得性肺炎; 头孢哌酮/舒巴坦
[Chin J Infect Control,2016,15(2):97-101]
近年来随着广谱抗菌药物大量应用,鲍曼不动杆菌耐药率逐年上升,目前泛耐药鲍曼不动杆菌(extensively drug-resistantAcinetobacterbaumannii,XDRAB)和全耐药鲍曼不动杆菌(pandrug-resistantAcinetobacterbaumannii,PDRAB)感染日益增多,并且缺乏有效治疗措施。替加环素是甘氨酰环素类抗菌药物的首个药品,对多重耐药鲍曼不动杆菌(MDRAB)、XDRAB和PDRAB有一定抗菌活性。为进一步了解替加环素对XDRAB的临床疗效和不良反应,回顾性分析2013年3月—2014年6月本院重症监护病房(ICU)发生XDRAB医院获得性肺炎(HAP)并使用替加环素治疗患者的临床资料。现将结果报告如下。
1对象与方法
1.1研究对象选取2013年3月—2014年6月本院中心ICU及呼吸ICU发生XDRAB HAP并使用替加环素治疗的患者31例。研究对象纳入标准:年龄>18岁,符合HAP诊断标准;痰培养至少连续2次检出XDRAB,并考虑其为致病菌;排除其他部位感染;应用替加环素抗感染治疗。研究对象分组:根据入住科室将患者分为呼吸ICU组和中心ICU组;根据患者应用替加环素是否联用头孢哌酮/舒巴坦(cefoperazone-sulbactam,SCF)将患者分为联用SCF组和非联用SCF组。
1.2诊断标准HAP参考卫生部2001年发布的医院感染诊断标准[1]、美国胸科协会(ATS)和美国感染性疾病协会(IDSA)2005年联合发布关于HAP的诊治指南[2]。入院时不存在、也不处于感染潜伏期,而入院48 h后发生肺部感染;具有咳嗽、咳痰、气急、胸痛、发热及肺部啰音等临床表现;血常规及其他炎性指标升高;胸片或肺部CT显示新发或进展性炎性改变。XDRAB定义为鲍曼不动杆菌对现有(除多粘菌素B及替加环素外)所有抗菌药物均耐药。
1.3细菌鉴定及药敏试验所有患者均在早期进行痰细菌学检查。痰标本来自患者自主咳痰,采用一次性吸痰管或纤维支气管镜经气管插管吸痰,取痰标本后行显微镜检查,如镜下白细胞>25个/低倍视野,而鳞状上皮细胞<10个/低倍视野,为合格痰标本。按照《全国临床检验操作规程》对细菌进行分离、培养、鉴定,采用法国生物梅里埃公司VITEK 2全自动细菌鉴定系统进行菌株鉴定。药敏试验采用纸片琼脂扩散法(K-B),药敏试验结果参考美国临床实验室标准化协会(CLSI)2008年版标准判定,以敏感、中介和耐药报告结果[3]。
1.4治疗方法29例患者给予替加环素常规剂量治疗(50 mg,1次/12 h,静脉滴注,首剂剂量加倍),其中19例患者联用SCF治疗,10例患者单用替加环素或联合其他抗菌药物治疗;2例患者由于替加环素常规剂量联合SCF治疗无效,参考国外相关文献[4],经患者及家属同意并签字后给予替加环素超常规剂量治疗(100 mg,1次/12 h,静脉滴注),治疗期间严密观察肝、肾功能变化及其他不良反应。
1.5临床疗效、细菌学疗效及不良反应评定根据抗菌药物临床研究指导原则,临床疗效按痊愈、显效、进步和无效4级评定,痊愈和显效合计为临床有效。细菌学疗效按病原菌清除、部分清除、未清除、替换和再感染5级评定。不良反应则按与药物关系分为肯定有关、可能有关、可能无关、肯定无关、无法评价5级评定,其中肯定有关和可能有关合计为不良反应,并计算不良反应率。治疗总有效率(%)=(痊愈例数+显效例数)/总例数×100%。
1.6统计分析应用SPSS 19.0软件进行统计分析,计量资料采用独立样本t检验,计数资料采用Fisher精确概率法,P≤0.05为差异有统计学意义。
2结果
2.1一般资料共回顾性分析31例患者,其中男性23例,女性8例;年龄45~90岁,平均(71.2±8.5)岁。31例患者均诊断为HAP,其中呼吸机相关肺炎(VAP)患者28例,非VAP患者3例。31例患者平均住院时间为37.52 d。两对比组(呼吸ICU组和中心ICU组,联用SCF组与非联用SCF组)组间比较,差异均无统计学意义(均P>0.05)。确诊为XDRAB HAP至开始使用替加环素平均间隔时间为8.09 d,两对比组组间比较,差异均无统计学意义(均P>0.05)。应用替加环素平均治疗时间为11.35 d,呼吸ICU组平均治疗时间长于中心ICU组,差异具有统计学意义(P=0.01);联用SCF组与非联用SCF组平均治疗时间比较,差异无统计学意义(P=0.30)。呼吸ICU组替加环素联用SCF率为85.71%(12/14),中心ICU组为47.06%(8/17)。见表1。

表1 两组HAP患者一般情况比较
2.2痰培养及药敏结果31例患者痰培养均为XDRAB,对替加环素均敏感,对碳青霉烯类及舒巴坦类(包括SCF)抗生素耐药率为100%,其中7例患者(22.58%)对多粘菌素B耐药。混合感染(2种或2种以上细菌/真菌生长)患者17例(54.84%),其中4例患者发现3种细菌/真菌生长,培养出铜绿假单胞菌13株,肺炎克雷伯菌4株,白假丝酵母菌2株,金黄色葡萄球菌和洋葱伯克霍尔德菌各1株。见表2。
表2各组XDRAB HAP患者混合感染情况
Table 2Mixed infection in different groups of patients with XDRAB HAP
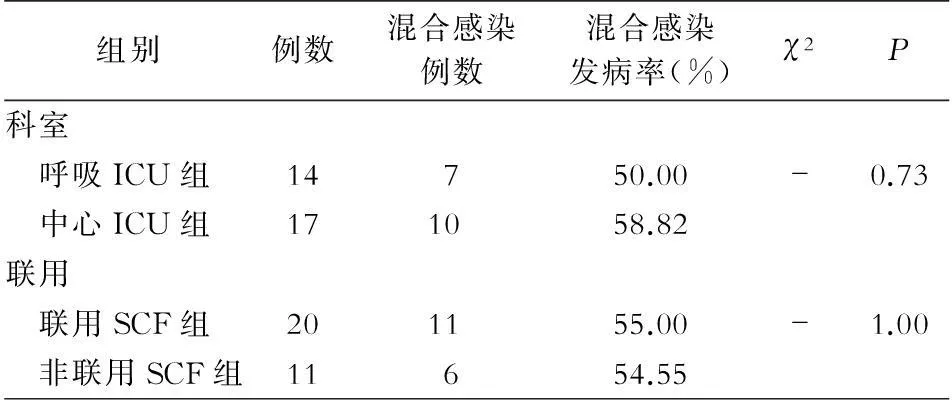
组别例数混合感染例数混合感染发病率(%)χ2P科室 呼吸ICU组14750.00-0.73 中心ICU组171058.82联用 联用SCF组201155.00-1.00 非联用SCF组11654.55
2.3临床及细菌学疗效31例患者中,临床痊愈率为29.03%、有效率为45.16%,细菌清除率为61.29%。中心ICU组痊愈率为17.65%,有效率为23.53%,细菌清除率为47.06%;呼吸ICU组痊愈率为42.86%,有效率为71.43%,细菌清除率为78.57%。中心ICU组和呼吸ICU组临床有效率比较,差异具有统计学意义(P=0.01)。联用SCF组痊愈率为35.00%,有效率为60.00%,细菌清除率为65.00%;非联用SCF组痊愈率为18.18%,有效率为18.18%,细菌清除率为54.55%;两组临床有效率比较,差异具有统计学意义(P=0.03);其余各组比较差异无统计学意义(P>0.05)。详见表3。
表3各组XDRAB HAP患者临床及细菌学疗效
Table 3Therapeutic effectiveness and bacterial clearance rates of different groups of patients with XDRAB HAP

组别总例数痊愈例数率(%)临床有效例数率(%)细菌清除例数率(%)科室 呼吸ICU组14642.861071.431178.57 中心ICU组17317.65423.53847.06联用 联用SCF组20735.001260.001365.00 非联用SCF组11218.18218.18654.55
2.4不良反应31例XDRAB HAP患者应用替加环素发生药物不良反应5例,发生率为16.13%。29例患者常规剂量治疗期间出现恶心、呕吐2例,腹泻1例,对症处理后好转,转氨酶升高1例,予停药后恢复正常,未见其他不良反应及实验室指标异常;2例患者超常规剂量治疗期间出现转氨酶升高1例,未停药,经护肝降酶治疗后降至正常。
2.5临床转归31例患者经治疗后治愈及好转14例,7例因治疗无明显效果放弃治疗,10例因治疗无效死亡。死亡原因:呼吸衰竭6例,心力衰竭2例,脓毒血症和弥散性血管内凝血各1例。
3讨论
鲍曼不动杆菌是一种革兰阴性条件致病菌,其引起的医院感染最常见的为肺部感染,是HAP、尤其是VAP重要的致病菌。由于该菌具有强大的获得耐药性和克隆传播能力,对常用抗菌药物耐药率呈逐年升高趋势。近年来,MDRAB、XDRAB、PDRAB感染逐渐增多,鲍曼不动杆菌已成为医院感染的主要病原菌之一,科室分布以ICU最多[5]。2010年CHINET监测[6]显示,鲍曼不动杆菌占所有呼吸道标本分离革兰阴性菌的19.40%,其中敏感型鲍曼不动杆菌为17.50%,MDRAB和XDRAB分别达55.00%和21.40%,鲍曼不动杆菌对亚胺培南和美罗培南的耐药率分别为62.10%和63.60%,对SCF的耐药率为33.60%,对其他监测抗菌药物的耐药率均≥56.20%。湖南省2011年度细菌耐药检测结果[7]显示,耐亚胺培南和美罗培南鲍曼不动杆菌检出率分别为50.1%、44.8%。ICU内鲍曼不动杆菌主要感染患者呼吸道,对SCF耐药率为36.70%,对其他抗菌药物耐药率均>90.00%[8],XDRAB在国内往往无抗菌药物可选。根据2012年中国鲍曼不动杆菌感染诊治与防控专家共识[9],对鲍曼不动杆菌治疗药物推荐分为以下几类:舒巴坦及含舒巴坦和β-内酰胺类抗生素的复合制剂、碳青霉烯类、多粘菌素类、替加环素、四环素类、氨基糖苷类、喹诺酮类、第三/四代头孢菌素等抗菌药物。目前XDRAB感染常采用二联、甚至三联用药。本研究多数患者采用二联用药方案(替加环素联合SCF)进行治疗。
替加环素为甘氨酰环素类抗菌药物,结构独特,其全新的甘氨酰胺增加了抗菌活性和抗菌谱,不受四环素类两大耐药机制(核糖体保护和外排机制)的影响,通过与核糖体30S亚单位结合,阻止氨酰化tRNA分子进入核糖体A位而抑制细菌蛋白质的合成。目前,也尚未发现替加环素与其他抗菌药物存在交叉耐药。替加环素也不受β-内酰胺酶(包括超广谱β-内酰胺酶)、靶位修饰、大环内酯类抗生素外排泵或酶靶位改变等耐药机制的影响,具有广谱抗菌活性。美国食品药品管理局(FDA)批准该药的适应证为复杂性腹腔和皮肤软组织感染、社区获得性肺炎。国外相关文献[10]报告,替加环素在MDRAB引起的VAP治疗中,临床有效率及微生物清除率分别为84.00%、80.00%。本研究分析了31例使用替加环素治疗的XDRAB HAP患者,临床有效率为45.16%,细菌清除率为61.29%,临床有效率低于国外相关研究结果,其原因可能与本研究患者多为老龄人、基础疾病较多、感染较重、合并多重感染及用药时机偏晚有关。Freire等[11]对替加环素治疗HAP有效性进行研究,将HAP患者分为VAP组和非VAP组,结果发现,VAP组替加环素治愈率为46.50%,而非VAP组治愈率为69.30%,两组比较差异有统计学意义;而本组VAP患者28例,占90.32%,其临床有效率与Freire等[11]研究中VAP组的有效率相近。说明病情较重可能是导致本研究对象治疗有效率低于国外文献报道的重要原因。
本研究结果显示,呼吸ICU组临床有效率高于中心ICU组。从APACHE(III) 评分可知,中心ICU组患者基础情况较差,病情较重;呼吸ICU组应用替加环素平均疗程明显长于中心ICU组。呼吸ICU组与中心ICU组替加环素联用SCF率分别为85.71%、47.06%,前者联用SCF率明显高于后者。呼吸ICU组治疗效果优于中心ICU组,考虑与前者应用替加环素疗程足,患者病情相对较轻且基础情况较好有关,不排除与前者联用SCF较多有关,还需进一步研究。
替加环素是广谱高效抗菌药物,对临床难治性细菌具有较高的敏感性,但单独使用易产生耐药,临床医生应优化抗菌药物的应用方案,降低抗菌药物耐药风险,且替加环素对铜绿假单胞菌无效,所以在临床上建议联合其他药物治疗。相关研究[12]报道,舒巴坦对部分耐碳青霉烯类的鲍曼不动杆菌有效,舒巴坦单独应用对不动杆菌属细菌有一定杀灭作用,SCF对碳青霉烯类耐药菌也部分敏感,被认为是治疗鲍曼不动杆菌感染的优选药物。本研究中替加环素联用SCF治疗组临床有效率高于非联用SCF组,两组治疗效果比较,差异具有统计学意义;两组APACHE(III) 评分、住院时间、确诊后开始使用替加环素平均间隔时间、应用替加环素平均治疗时间比较,差异均无统计学意义,提示两组患者病情、基础情况、用药时机、用药疗程及住院日数相当,且两组混合感染发病率比较,差异也无统计学意义,故疗效差异可能归因于替加环素联用SCF双重抗鲍曼不动杆菌作用。故应用替加环素联合SCF治疗XDRAB HAP不仅可减少鲍曼不动杆菌耐药性的产生,而且可覆盖替加环素不能覆盖的铜绿假单胞菌,对混合感染患者而言,为较好的选择,能提高临床治愈率。Ramirez等[4]在对比较大剂量替加环素组(100 mg,1次/12 h)、较小剂量替加环素组(75 mg,1次/12 h)和亚胺培南/西司他丁组(500~1 000 mg,1次/8 h)治疗HAP的临床效果II期临床试验中,发现较大剂量替加环素组治愈率明显高于较小剂量替加环素组和亚胺培南/西司他丁组,而3组安全性相似。本研究中2例患者接受替加环素超常规剂量 (100 mg,1次/12 h)治疗,其中1例患者常规剂量(50 mg,1次/12 h)治疗13 d后改为超常规剂量治疗,5 d后好转出院,另1例常规剂量治疗17 d后改为超常规剂量治疗,2 d后因原发病加重死亡。由于病例数量少,尚需要增加病例数后评估其临床疗效及不良反应,但在常规剂量治疗无效的XDRAB HAP患者中应用超常规剂量替加环素不失为一种选择。
本组患者对替加环素耐受性较好,主要不良反应为胃肠道症状,但发生率较国外低[13],原因可能为本研究大部分为机械通气及镇静患者,无法表达及无明显主观感觉,影响了对胃肠道症状观察,此外,患者胃肠外营养也影响对胃肠道反应的观察。
本研究提示替加环素对XDRAB HAP具有较好的临床疗效,早期、足疗程用药效果较好,联合SCF是一种值得推广的选择。临床中必要时可考虑选择应用大剂量替加环素。目前本研究仍存在许多不足之处,属于回顾性研究,且样本量较小,尤其是超常规剂量替加环素的应用,因此还需进一步扩大样本量进行分析,但对于替加环素的临床应用仍有一定的指导作用和借鉴价值。
[参 考 文 献]
[1]中华人民共和国卫生部.医院感染诊断标准(试行)[J].中华医学杂志,2001,81(5):314-320.
[2]American Thoracic Society, Infectious Diseases Society of America. Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia[J]. Am J Respir Crit Care Med, 2005, 171(4): 388 -416.
[3]National Committee for Clinical Laboratory Standards. Performance standards for antimicrobial susceptibility testing[J]. Eighteenth informational supplement NCCLS document, M100-S18, Pennsylvania: NCCLS, 2008.
[4]Ramirez J, Dartois N, Gandjini H, et al. Randomized phase 2 trial to evaluate the clinical efficacy of two high-dosage tigecycline regimens versus imipenem-cilastatin for treatment of hospital-acquired pneumonia [J]. Antimicrobial agents and chemotherapy, 2013, 57(4): 1756-1762.
[5]宋志香,薛文英,马冬媛. 鲍氏不动杆菌的流行病学及耐药性研究[J].中华医院感染学杂志,2011,21(4):784-786.
[6]习慧明,徐英春,朱德妹,等.2010年中国CHINET鲍曼不动杆菌耐药性监测[J]. 中国感染与化疗杂志,2012,12(2): 98-104.
[7]黄勋,邓子德,倪语星,等. 多重耐药菌医院感染预防与控制中国专家共识[J].中国感染控制杂志,2015,14(1): 1-9.
[8]张朝晖,钟建华,张蓉,等. 头孢哌酮-舒巴坦治疗泛耐药鲍曼不动杆菌医院获得性肺炎36例[J].中国感染与化疗杂志,2012,12(6): 416-418.
[9]陈佰义,何礼贤,胡必杰,等.中国鲍曼不动杆菌感染诊治与防控专家共识[J].中华医学杂志,2012,92(8):3-8.
[10] Schafer JJ, Goff DA, Stevenson KB, et al. Early experience with tigecycline for ventilator-associated pneumonia and bacteraemia caused by multidrug-resistantAcinetobacterbaumannii[J]. Pharmacotherapy, 2007, 27(7): 980-987.
[11] Freire AT, Melnyk V, Kim MJ, et al. Comparison of tigecycline with imipenem/ cilastatin for the treatment of hospital-acquired pneumonia[J]. Diagn Microbiol Infect Dis, 2010, 68(2):140-151.
[12] Karageorgopoulos DE, Falagas ME. Current control and treatment of multidrug-resistantAcinetobacterbaumanniiinfections[J]. Lancet Infect Dis, 2008, 8(12): 751- 762.
[13] Cai Y, Wang R, Liang B, et al. Systematic review and meta-analysis of the effectiveness and safety of tigecycline for treatment of infectious disease[J]. Antimicrobial agents chemotherapy, 2011, 55(3): 1162-1172.
(本文编辑:刘思娣)
Clinical efficacy and adverse reactions of tigecycline in treatment of healthcare-associated pneumonia caused by extensively drug-resistantAcinetobacterbaumannii
WANGKai-ge,TANFen,PENGHong,CHENPing
(InstituteofRespiratoryDiseaseofCentralSouthUniversity,RespiratoryDiseaseDiagnosisandTreatmentCenterofHunanProvince,TheSecondXiangyaHospitalofCentralSouthUniversity,Changsha410011,China)
[Abstract]ObjectiveTo observe the clinical efficacy and adverse reactions of tigecycline in treatment of healthcare-associated pneumonia (HAP) caused by extensively drug-resistant Acinetobacter baumannii (XDRAB).MethodsClinical data of patients who used tigecycline for the treatment of XDRAB HAP in intensive care units of a hospital from March 2013 to June 2014 were retrospectively analyzed.ResultsXDRAB isolated from 31 patients with HAP were all sensitive to tigecycline, the resistance rates to carbapenems and sulbactams (including cefoperazone-sulbactam, SCF) were all 100%,17 cases (54.84%)were mixed infection. Combined use rates of tigecycline and SCF were 85.71%(12/14)in respiratory intensive care unit(RICU) and 47.06%(8/17) in general intensive care unit(GICU). Of 31 patients, the cure rate, effective rate, bacterial clearance rate, and antimicrobial adverse reaction rate were 29.03%,45.16%, 61.29%, and 16.13% respectively, no serious adverse drug reactions occurred. In RICU group and GICU group, the cure rates were 42.86% and 17.65% respectively, effective rates were 71.43% and 23.53% respectively, and bacterial clearance rates were 78.57 % and 47.06% respectively, difference in effective rate between two groups was significant (P<0.05).Among patients receiving combination of tigecycline and SCF as well as not receiving combined SCF, the cure rates were 35.00% and 18.18% respectively, effective rates were 60.00% and 18.18% respectively, and bacterial clearance rates were 65.00% and 54.55% respectively, difference in effective rate between two groups was significant (P<0.05).ConclusionTigecycline has a good clinical efficacy and little adverse reaction in treating XDRAB HAP; tigecycline combined with SCF is a good choice.
[Key words]tigecycline; extensively drug-resistant Acinetobacter baumannii; healthcare-associated pneumonia; cefoperazone-sulbactam
[中图分类号]R181.3+2
[文献标识码]A
[文章编号]1671-9638(2016)02-0097-05
DOI:10.3969/j.issn.1671-9638.2016.02.006
[作者简介]王凯歌(1987-),男(汉族),河南省平顶山市人,医师,主要从事肺间质疾病研究。[通信作者]彭红E-mail:dianaph6@hotmail.com
[基金项目]国家自然科学基金(81370164);湖南省自然科学基金(2015JJ4087);国家临床重点专科建设项目
[收稿日期]2015-04-12

