HBeAg定量检测对预测阿德福韦酯治疗慢性乙型肝炎疗效的价值*
凌宁,刘毅,彭明利
(重庆医科大学:1附属第二医院感染病科;2病毒性肝炎研究所,中国重庆400010)
HBeAg定量检测对预测阿德福韦酯治疗慢性乙型肝炎疗效的价值*
凌宁1,刘毅1,彭明利2
(重庆医科大学:1附属第二医院感染病科;2病毒性肝炎研究所,中国重庆400010)
目的:探讨外周血HBeAg定量水平的变化与阿德福韦酯治疗HBeAg阳性慢性乙型肝炎(CHB)患者疗效的关系。方法:对57例接受阿德福韦酯治疗的HBeAg阳性CHB患者随访96周,分别在抗病毒治疗的基线、12周、24周、48周、96周收集患者血清,化学发光法定量检测HBeAg水平,实时荧光定量聚合酶链反应(PCR)检测HBV DNA水平,全自动生化分析仪检测血清ALT水平。根据患者治疗96周后是否达到完全应答,分成完全应答组和非完全应答组,对两组患者相关数据进行分析。结果:96周治疗后完全应答组有15例,非完全应答组有42例。①完全应答组基线、24、48、96周HBV DNA水平均较非完全应答组低,P<0.01;②完全应答组12、24、48周、HBeAg定量水平的变化与同时期的HBV DNA定量的变化均有相关性,与96周HBeAg血清转换相关;③完全应答组基线、12、24、48周HBeAg水平可预测96周完全应答,AUC分别是0.977、0.977、0.992、0.953,敏感性均为100%,特异性分别为96.87%、93.75%、96.87%、90.62%。12周、24周、48周HBeAg定量的变化亦可预测96周完全应答,AUC分别是0.969、0.992、0.953,敏感性均为100%,特异性分别为93.75%、96.87%、90.62%。④12、48周HBV DNA水平,12、24周HBeAg水平及HBeAg定量的变化均能预测随访结束时患者发生病毒学突破。结论:①基线HBV DNA和HBeAg水平可以预测96周的完全应答,有助于优化治疗,选择适合的患者;②12周、24周、48周HBeAg的水平及其变化能预测96周的完全应答,其效能优于HBV DNA的水平及其变化;③12周、24周HBeAg定量的变化能预测随访结束时患者发生病毒学突破,其效能优于同时期HBeAg水平。
慢性乙型肝炎;HBeAg定量;预测;阿德福韦酯;
目前慢性乙型肝炎(Chronic hepatitis B,CHB)抗病毒药物包括干扰素和核苷(酸)类药物,其疗效有限,与药物、病毒和宿主多因素有关[1]。《慢性乙型肝炎防治指南》指出:停药标准为达到ALT恢复正常,HBV DNA小于最低检测限和血清HBeAg转换后巩固治疗至少3年,总疗程4年。疗程与疗效是影响患者依从性的重要因素[2]。研究发现,HBeAg定量监测有助于预测持久病毒学应答和HBeAg血清学转换[3-4]。
本研究通过检测使用阿德福韦酯治疗HBeAg阳性慢性乙型肝炎的疗效指标,探索血清HBeAg定量水平及其变化与预测抗病毒疗效之间的关系。
1 对象与方法
1.1 研究对象
选取重庆医科大学附属第二医院感染科门诊确诊的CHB患者,诊断均符合《2010版慢性乙型肝炎防治指南》[5]。共入组57例,男42例,女15例,年龄18~55岁。入组符合:HBsAg、HBeAg阳性,抗-HBe阴性,HBVDNA>105拷贝/mL,ALT>80 U/L。病例均排除HCV、HIV重叠感染以及自身免疫性肝炎、酒精性肝病、代谢性肝病。
1.2 仪器和试剂
HBV血清标志物检测:HBV血清标记物化学发光试剂盒(罗氏公司)。HBeAg检测:AXSYM HBe2.0,Abbott Laboratories,Abbott Park,IL。HBVD NA检测:COBAS AMPLICOR HBV Monitor,Roche Diagnostics,Branchburg,NJ;HBV DNA荧光定量聚合酶链反应(PCR)试剂盒(上海复星长征医学科学有限公司);检测下限为500拷贝/mL。肝功能检测:HITACHI7100全自动生化分析仪,ALT正常上限为40 U/L。
1.3 研究方案
所有CHB患者接受阿德福韦酯(10 mg,qd)治疗,共随访96周。分别检测患者治疗前、治疗12、24、48周及96周的ALT水平、HBV DNA载量、HBV血清标记物及HBeAg定量。根据检测结果分为两组:一组为完全应答,即ALT正常、HBV DNA低于检测值、HBeAg血清转换(HBeAg转阴,HBeAb转阳)。另一组为非完全应答组,即未达到以上标准的患者。
1.4 统计学分析
以SPSS 19.0软件进行分析。所有资料行正态分布检验,计量资料数据采用均数±标准差(x±s),若服从正态分布且方差齐性,差异以t检验(两组)进行比较,相关性分析采用Spearman秩相关检验。诊断性能评价采用受试者工作特征曲线(Receiver operating characteristic curve,ROC)分析,计算曲线下面积、敏感度、特异度、阳性预测值和阴性预测值。P<0.05表示差异有统计学意义。
2 结果
2.1 基础资料
共入组57例,男42例,女15例。随访结束后,15例患者达到完全应答,男11例,女4例,平均年龄(26.0±5.1)岁;42例患者未达到完全应答,其中男31例,女11例,平均年龄(28.6±7.9)岁。
2.2 两组患者HBeAg定量水平与HBVDNA水平在治疗前后的检测结果
两组患者HBV DNA水平和HBeAg定量值在基线时差异即有统计学意义,P<0.01。
完全应答组24、48、96周HBV DNA及HBeAg定量水平均较非完全应答组低,P<0.05,差异有统计学意义,表1。
表1 两组患者治疗前后HBVDNA水平和HBeAg定量值水平(±s)
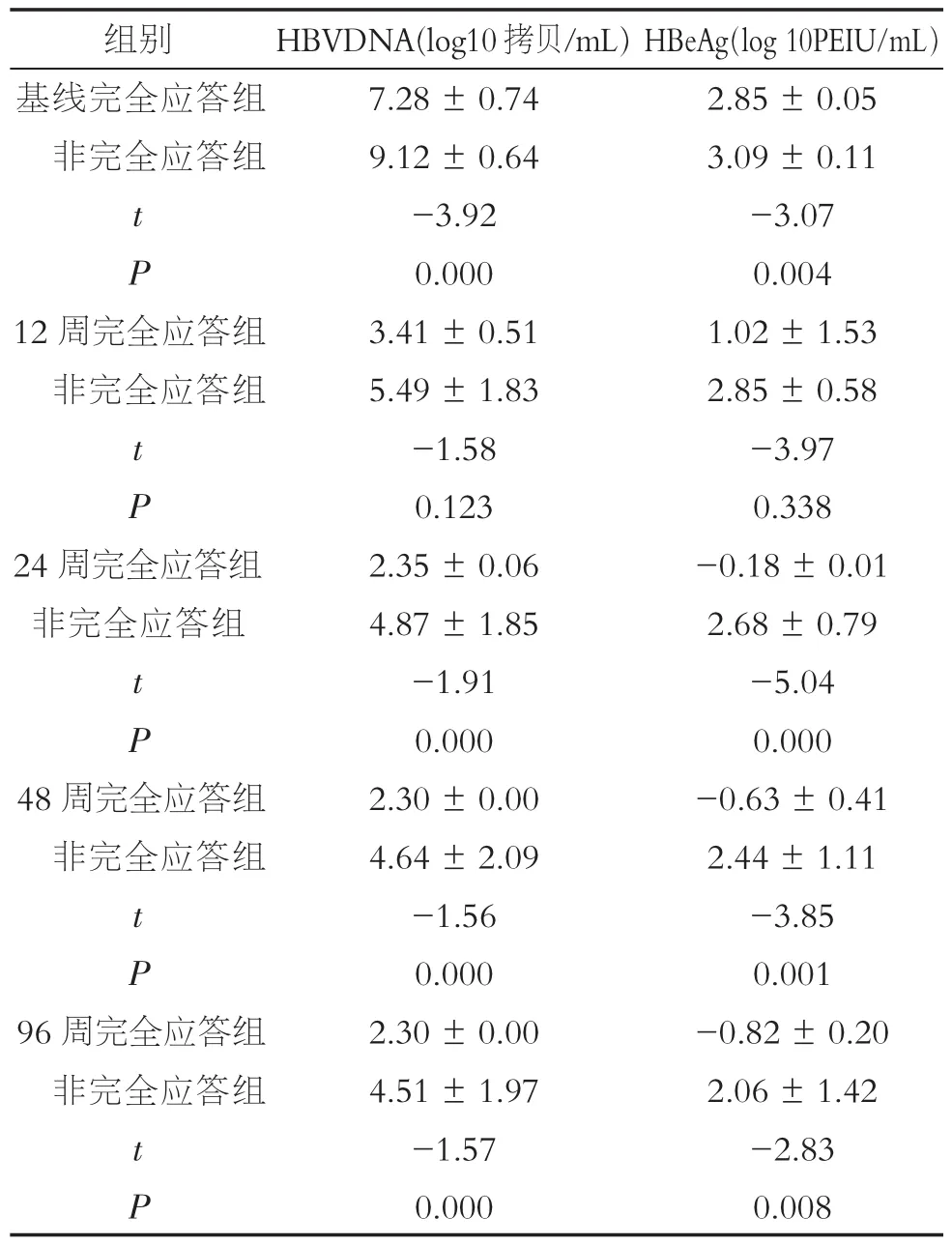
表1 两组患者治疗前后HBVDNA水平和HBeAg定量值水平(±s)
组别基线完全应答组非完全应答组t P 12周完全应答组非完全应答组t P 24周完全应答组非完全应答组t P 48周完全应答组非完全应答组t P 96周完全应答组非完全应答组t P HBVDNA(log10拷贝/mL)7.28±0.74 9.12±0.64 -3.92 0.000 3.41±0.51 5.49±1.83 -1.58 0.123 2.35±0.06 4.87±1.85 -1.91 0.000 2.30±0.00 4.64±2.09 -1.56 0.000 2.30±0.00 4.51±1.97 -1.57 0.000 HBeAg(log 10PEIU/mL)2.85±0.05 3.09±0.11 -3.07 0.004 1.02±1.53 2.85±0.58 -3.97 0.338 -0.18±0.01 2.68±0.79 -5.04 0.000 -0.63±0.41 2.44±1.11 -3.85 0.001 -0.82±0.20 2.06±1.42 -2.83 0.008
2.3 完全应答组,HBeAg定量水平变化与同时期HBV DNA水平变化、96周HBeAg血清学转换之间的相关性
完全应答组12、24、48、96周HBeAg定量水平较基线的变化与同时期的HBV DNA定量的变化均有相关性(r值分别为0.726、0.873、0.839、0.828,P<0.01)。12、24、48周HBeAg定量水平的变化亦与96周HBeAg血清转换相关(P值分别为0.01、0.014、0.028)。
2.4 完全应答组,HBeAg定量水平、HBV DNA水平及其变化对预测96周完全应答的价值
完全应答组,各随访点HBV DNA水平及其变化可预测96周完全应答,各随访点HBeAg水平及其变化亦可预测96周完全应答。HBeAg定量变化的预测效能优于HBV DNA水平的变化,表2。
2.5 治疗早期HBeAg定量水平、HBV DNA水平变化对随访结束时患者发生病毒学突破的预测价值
针对所有患者,12周、48周HBV DNA水平,12、24周HBeAg水平,12、24周HBeAg定量的变化均能预测随访结束时患者发生病毒学突破,但12周HBeAg定量水平的变化的预测效能最强,表3。
3 讨论
HBeAg是由HBV C基因转录生成的可溶性蛋白,引起HBV的持续慢性感染,目前被认为是免疫耐受的指标[6]。HBeAg血清转换常意味着病毒持续抑制,病情由活动性趋于静止[7]。
在干扰素治疗HBeAg阳性慢乙肝的研究中发现,不同时间点HBV DNA、HBeAg及ALT与治疗结束时HBeAg血清转换有不同程度的关系,但基线HBeAg的水平,以及治疗早期HBeAg的下降程度是否获得HBeAg血清转换的最强预测因子[8-14]。Fried的研究认为,在PEG-IFNa-2a治疗HBeAg阳性CHB患者的HBeAg血清转换率预测上,HBeAg水平较HBV DNA的灵敏度及特异度更高。基线HBeAg≤31 PEIU/mL的患者发生HBeAg血清转换的阳性预测值为54%。治疗12周HBeAg水平下降至<10 PEIU/mL时,53%患者可获得血清学转换。治疗24周HBeAg水平下降至<10 PEIU/mL时,52%患者可获得血清学转换。而治疗24周时HBeAg水平≥100 PEIU/mL,则仅4%患者获血清学转换,其阴性预测值达96%[8]。而Tangkijvanich等[9]人的研究提示,与HBsAg及HBV DNA相比,HBeAg水平对HBeAg血清转换有更好的预测作用。12周HBeAg<2.4 s/co及24周HBeAg<2.0 s/co的阳性预测值和阴性预测值分别是65.2%、86.5%和80.9%、92.3%,均高于同期HBsAg、HBV DNA的阳/阴性预测值。
在核苷类似物治疗HBeAg阳性慢乙肝的研究中,发现HBeAg血清转换以及后期可能出现的病毒突破,与HBV DNA、HBeAg及ALT也有类似的关系。Lu H等对48例接受阿德福韦酯治疗的HBeAg阳性CHB患者随访5年的结果显示,基线HBeAg滴度越低(<800 s/co),HBV DNA水平越低(<109 copies/mL),ALT水平越高(>5倍上限),获得HBeAg转换率的几率越大[15]。这也与本文的研究结果一致,完全应答组与非完全应答组的HBV DNA和HBeAg水平在基线时即有统计学差异。提示抗病毒治疗应优化对患者的选择。
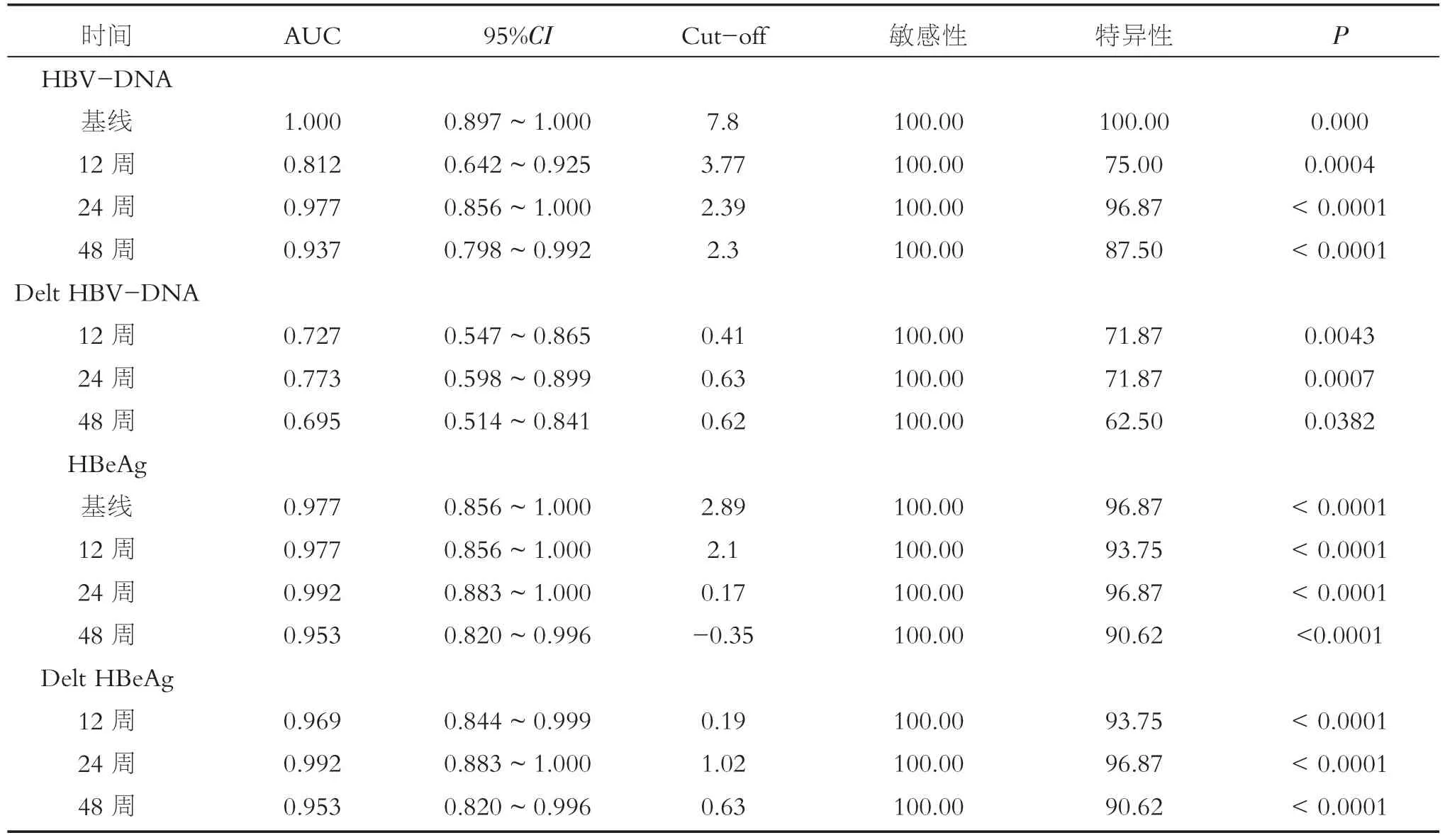
表2 HBV DNA水平、HBeAg定量水平及其变化对预测96周完全应答的价值
本研究中,完全应答组治疗过程中各随访点的HBeAg定量水平的变化与同时期的HBV DNA定量的变化均有相关性。基线、12周、24周、48周HBV DNA及HBeAg水平可预测96周完全应答。12周、24周、48周HBV DNA及HBeAg定量的变化也可预测96周完全应答。抗病毒治疗早期HBeAg的水平及其变化的效能优于HBV DNA的水平及其变化。这与黄晶等多人多项研究的结果相似[16-19]。
Yen等[20]报道,定量HBeAg测定能预测未发生HBeAg血清转换患者病毒突破的出现。本研究也观察了所有患者HBV DNA、HBeAg与随访结束时发生病毒学突破的关系。结果显示:12周、48周HBVDNA和HBeAg水平,12周、24周HBeAg定量水平的变化均能预测96周时患者发生病毒学突破,但12周HBeAg定量水平的变化预测效能最强。
因此,本研究的数据说明:接受抗病毒治疗前,患者的HBeAg定量水平及HBV DNA水平越低,越有利于96周时达到完全应答。提示在抗病毒治疗前,对患者的优化选择,有利于达到满意的治疗效果。而在抗病毒治疗过程中除了检测HBV DNA定量水平的变化,加强对HBeAg水平监测,观察HBeAg水平的动态变化,对预测慢性乙肝患者抗病毒治疗能否获得完全应答,以及后期是否会出现病毒突破也有较大的价值。可以指导慢乙肝抗病毒方案的选择和调整,达到优化治疗的目的。
1.Lok AS,McMahon BJ.Chronic hepatitis B:update 2009 [J].Hepatology,2009,50(3):1-36.
2.徐曼曼,陈煜.慢性乙型肝炎患者抗病毒治疗依从性的研究现状[J].临床肝胆病杂志,2015,31(10):1735-1739.
3.Park NH,Shin SH.Monitoring of HBeAg levels may help to predict the outcomes of lamivudine therapy for HBeAg positive chronic hepatitis B[J].J Viral Hepat,2005,12(2): 216-221.
4.Wang CC,Liu CJ,Lai MY,et al.Dynamics of hepatitis B e antigen index ratio correlate with treatment response in chronic hepatitis B patients[J].Liver International,2007, 27(2):235-239.
5.中华医学会肝病学分会,感染病学分会.慢性乙型肝炎防治指南(2010年版)[J].中华肝脏病杂志,2011,19(1): 13-32.
6.Lang T,Lo C,Skinner N,et al.The hepatitis B e antigen (HBeAg)targets and suppresses activation of the toll-like signaling pathway[J].J Hepatol,2011,55(4):762-769.
7.Lau G,Marcellin P,Peters M.Chronic hepatitis B:a global health problem requiring coherent worldwide treatment strategies[J].Hepatol Int,2007,1(2):316-325.
8.Fried MW,Piratvisuth T,Lau GK,et al.HBeAg and hepatitis B virus DNA as outcome predictors during therapy with peginterferon Alfa-2a for HBeAg-positive chronic hepatitis B[J].Hepatology,2008,47(2):428-434.
9.Tangkijvanich P,Komolmit P,MahachaiV,et al.Comparison between quantitative hepatitis B surface antigen, hepatitis B e-antigen and hepatitis B virus DNA levels for predicting virological response to pegylated interferon-a-2b therapy in hepatitis B e-antigen-positive chronic hepatitis B[J].Hepatol Res,2010,40(4):269-77.
10.Van Der Eijk AA,Niesters HGM,Hansen BE.et al. Quantitative HBV DNA levels as an early predictor of nonresponse in chronic HBe-antigen positive hepatitis B patients treated with interferon-alpha[J].Journal of Viral Hepatitis,2006,13(2):96-103.
11.李明慧,谢尧.干扰素治疗慢性乙型肝炎时e抗原血清学转换的相关因素[J].中华肝脏病杂志,2007,15(7): 481-484.
12.朱月永,董菁,陈攸涛,等.e抗原定量对聚乙二醇干扰素治疗HBeAg阳性慢性乙型肝炎e抗原血清学转换的预测[J].胃肠病学和肝病学杂志,2010,19(10):883-885.
13.高国生,颜华东,徐晓珍,等.HBeAg定量对聚乙二醇干扰素α治疗慢性乙型肝炎疗效的预测价值[J].中华临床感染杂志,2013,6(6):351-354.
14.肖灿辉,张春兰,刘新华,等.聚乙二醇干扰素α-2a与替比夫定治疗HBeAg阳性慢性乙型肝炎的疗效比较及HBeAg血清学转换的预测因素[J].实用临床医药杂志, 2014,18(7):20-23.
15.Lu H,Geng DY,Shen F,et al.Optimization of adefovir therapy in chronic hepatitis B according to baseline predictors and on-treatment HBVDNA:a 5-year prospective study[J].Virol J,2011,21(8):444.
16.黄晶,陈小平,陈学福,等.替比夫定和恩替卡韦治疗HBeAg阳性慢性乙型肝炎的疗效及HBeAg血清学转换的预测因素[J].中华肝脏病杂志,2011,13(3):178-181.
17.苏智军,林琪,柯邵鹏,等.HBeAg下降幅度早期预测恩替卡韦治疗HBeAg阳性慢性乙型肝炎的疗效[J].福建医科大学学报,2008,42(5):441-443.
18.俎燕会,刘志荣,董格峰,等.慢性乙型肝炎患者HBeAg水平与恩替卡韦长期疗效的相关性[J].中华传染病杂志,2012,30(10):598-602.
19.Park NH,Shin JW,Park JH,et al.Monitoring of HBeAg levels may help to predict the outcomes of lamivudine therapy for HBeAg positive chronic hepatitis B[J].Journal of Viral Hepatitis,2005,12(2):216–221.
20.Yen YH,Lu SN,Chen CH,et al.Changes in serum hepatitis B e antigen(HBeAg)levels associated with the emergence of YMDD mutants in HBeAg non-seroconverted patients during lamivudine therapy[J].Liver Int, 2007,27(10):1349-1355.
(2016-07-31收稿)
Evaluation of the therapeutic effect of Adefovir using quantitative analysis of HBeAg on chronic hepatitis B
Ling Ning1,Liu Yi1,Peng Mingli21Department of Infectious Disease of the 2ndAffiliated Hospital;2Institute for Viral Hepatitis,the Chongqing Medical University,Chongqing,400010,China
Objective:To investigate the value of using quantitative serum HBeAg(hepatitis B e antigen)for evaluating the antivirus efficacy in HBeAg positive CHB(chronic hepatitis B)patients treated with adefovir dipivoxil.Methods:Fifty seven HBeAg-positive chronic hepatitis B patients treated with adefovir dipivoxil were enrolled and followed up for 96 weeks.Serum HBV DNA load,quantitative HBeAg and ALT levels were detected at baseline,week 12,24,48 and 96 respectively.Results:After 96 weeks,patients were divided into either complete response group when their ALT level was normal,HBV DNA load was less than the detective values, and HBeAg was converted,or incomplete response group otherwise.Fifteen cases were complete response while 42 cases were incomplete response.①There was statistically significant difference between the two groups at baseline level of HBV DNA and HBeAg(P<0.01).Compared to the incomplete response group,HBV DNA and quantitative HBeAg levels were significantly lower in complete response group at 24,48 weeks and 96 weeksrespectively(P<0.05),②In complete response group,at 12 weeks,24 weeks and 48 weeks,the changes of HBeAg were associated with the changes of HBV DNA and HBeAg seroconversion at 96 weeks in the same period (P<0.05),③In complete response group,HBeAg levels at baseline,12 weeks,24 weeks and 48 weeks could be used to predict whether a patient would have a complete response at 96 weeks,AUC were 0.977,0.977,0.992, 0.953 respectively(P<0.01),the sensitivity were 100%in all time points and specificity were 96.87%,93.75%, 96.87%,90.62%respectively.Tha changes of HBeAg at 12 weeks,24 weeks and 48 weeks could be used to predict complete response at 96 weeks,with AUC were 0.969,0.992,0.953 respectively(P<0.01),sensitivity were all 100%in each time point,and specificity of 93.75%,96.87%,90.62%respectively.④HBV DNA levels, HBeAg levels,and changes of HBeAg at 12 weeks and 24 weeks could be used to predict whether a patient would have a viral breakthrough at the end of the follow-up.Conclusion:①HBV DNA and HBeAg levels at baseline can be used to predict the complete response at 96 weeks,which helps to optimize the antivirus treatment and choose suitable patients.②HBeAg levels at 12,24 and 48 weeks and their changes can be used to predict the complete response at 96 weeks.The level of HBeAg level is a better predictor than that of HBV DNA.③The changes of HBeAg at 12 and 24 weeks can be used to predict whether a patient will have virological breakthrough at the end of the follow-up and are better predictors than the absolute values of HBeAg at the same period.
Chronic hepatitis B;Therapy;Hepatitis B antigen quantitative detection;Prognosis;Adefovir dipivoxil
R512.62
A
10.3969/j.issn.1000-2669.2016.05.010
*重庆市卫计委医学科研项目(2008-2-193)
凌宁(1973-),女,博士。E-mail:zjlovelning@sina.com

