华法林抗凝、肉眼血尿、血清肌酐进行性升高
涂远茂 周 云 谢红浪 刘志红
·临床集锦·
华法林抗凝、肉眼血尿、血清肌酐进行性升高
涂远茂 周 云 谢红浪 刘志红
老年女性患者,生物瓣膜置换术后长期使用华法林抗凝。肾脏疾病病程4月,表现为持续镜下血尿、发作性肉眼血尿,血清肌酐进行性升高,查MPO-ANCA阳性,肾活检符合ANCA相关性肾炎合并IgA肾病。患者发作肉眼血尿期间存在抗凝过度,停用抗凝剂后尿色转清、肾功能明显改善,考虑同时合并华法林相关肾病。
华法林 急性肾损伤 华法林相关肾病 ANCA相关性血管炎
病史摘要
现病史 66岁老年女性, 因“尿检异常4月,肉眼血尿1月”于2015-09-06入院。
患者2015-04-13体检查尿常规隐血++,蛋白阴性,血清肌酐(SCr)73 μmol/L,血红蛋白(Hb)131 g/L;无肉眼血尿,因长期服用华法林4.375 mg/d抗凝,故未重视镜下血尿。8月初出现洗肉水样肉眼血尿,无血丝血块,多次查尿常规隐血持续+++、蛋白偶有+;14日查凝血功能异常:凝血酶原时间(PT)54.1s、活化部分凝血活酶时间(APTT)78.7s,国际标准化比值(INR)4.51,华法林减至3.75 mg/d;16日INR 2.68,华法林减至2.5 mg/d;22日INR 1.8,加至3.125 mg/d;持续肉眼血尿,不伴鼻出血、皮肤瘀斑等;无药物合并使用,饮食如常。24日外院查Hb 88 g/L,SCr 187 μmol/L、血清尿素氮(BUN)14.8 mmol/L,血清白蛋白36.4 g/L、球蛋白35.3 g/L,INR 2.0;PET-CT示“右肺上叶后段厚壁空洞影,考虑良性病变可能;副鼻窦未见明显异常,肝脾无明显肿大”,心电图示心房颤动,心室率72 次/min。26日因肉眼血尿加重停用华法林。9月1日行膀胱镜发现双侧输尿管均引流出血尿;逆行尿路造影提示左肾下盏小结石可能。次日出现排尿困难,查Hb 74 g/L,BUN 13 mmol/L、SCr 247 μmol/L;予悬浮红细胞2U输注,维生素K1及血凝酶止血治疗;9月3日SCr升至320 μmol/L,泌尿超声示“肾脏结构正常、集合系统光带分离13 mm,双侧输尿管扩张,未见明显结石影”,放置双J管后引流通畅,可见血块,尿色逐渐转清,肾功能明显改善(9月5日查BUN 12.3 mmol/L、SCr 178 μmol/L),为进一步诊治来我院就诊。病程中偶感腰酸、腰痛,夜尿1次/晚,无尿频、尿急、尿痛;无发热、皮疹、关节痛等不适。精神食欲一般,大便正常,尿量无明显减少,体重稳定。
既往史 “风湿性心脏病”史28年,2005年行“二尖瓣扩瓣术”,2012年行“心脏瓣膜置换术”,长期服用华法林抗凝。血压升高8年,最高150/90 mmHg,口服厄贝沙坦150 mg/d口服,血压控制尚可。个人史及婚育史无特殊。
体格检查 体温36.6℃,脉搏109 次/min,律不齐,呼吸 16次/min,血压 125/87 mmHg,身高158 cm,体重56.6 kg,体质量指数22.67 kg/m2;神志清楚,精神可,皮肤黏膜未见皮疹及瘀点瘀斑,咽不红,扁桃体不大,心率121次/min,律不齐,听诊心音强弱不等,心尖区可闻及2/6级收缩期吹风样杂音,肺、腹部未及明显异常,双下肢无水肿。
实验室检查
尿液 尿蛋白定量0.62 g/24h,尿沉渣红细胞计数1 000万/ml(多形型);C3 2.47 mg/L、α2巨球蛋白(α2-MG)2.37 mg/L;NAG 15.9 U/(g·cr)、视黄醇结合蛋白 1.2 mg/L、溶菌酶<0.5 mg/L、胱抑素C 0.13 mg/L;白细胞介素18(IL-18)18.23 ng/L、NGAL 37 μg/L。Rous试验阴性。
血液 白细胞计数5.7×109/L、血小板174×109/L、Hb 91 g/L、MCV 87.5 fL、MCH 29.8 pg、Ret 0.71%,C反应蛋白 1.5 mg/L、ESR 60 mm/h;血清白蛋白36.6 g/L、球蛋白25.2 g/L、谷草转氨酶9 U/L、谷丙转氨酶9 U/L、乳酸脱氢酶229 U/L,BUN 7.7 mmol/L、SCr 123.8 μmol/L、UA 304 μmol/L、胱抑素C 1.73 mg/L, 钠141.3 mmol/L、钾4.21 mmol/L、氯103.8 mmol/L、TCO224.9 mmol/L,铁8 μmol/L、TIBC 27 μmol/L,空腹血糖4.59 mmol/L。pro-BNP 304 pmol/L,甲状腺功能正常。
免疫学检查 MPO-ANCA 140.33 RU/ml,pANCA 1:80,PR3-ANCA、cANCA阴性;ANA、抗ds-DNA抗体、抗核抗体谱、抗GBM抗体阴性。免疫球蛋白:IgG 13.9 g/L、IgA 2.95 g/L、IgE<20 IU/ml、IgM 1.27 g/L、RF<20、ASO 78.1 IU/ml;补体C3 0.724 g/L、C4 0.19 g/L。外周血淋巴细胞计数: CD3+1 063 个/μl、CD4+592 个/μl、CD8+145 个/μl、CD4+/CD8+1.9,CD19+234 个/μl、CD20+240 个/μl,Treg 23 个/μl。
内皮损伤指标 E选择素51.7 ng/ml、血栓调节蛋白7.5 ng/ml、血管细胞黏附分子879.98 ng/ml、循环内皮细胞10 个/ml、抗内皮细胞抗体1∶ 20。
病原学检查 血真菌G、真菌GM均阴性。血培养(需氧+厌氧)阴性。
影像学检查
胸部CT(2015-9-8) 右肺上叶空洞样病变(图1),考虑炎性改变;两肺散在机化性炎症;心脏瓣膜置换术后改变,心脏普遍性增大。
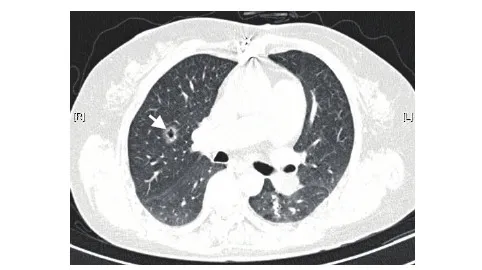
图1 右肺上叶空洞性病变(↑)
心脏超声 房颤心律;符合二尖瓣生物瓣置换术超声心动图改变;符合三尖瓣修补术后声像图改变;轻-中度三尖瓣反流;双心房扩大;主动脉瓣钙化并轻度反流。
双肾B超 LK 110 mm×47 mm×55 mm,RK: 106 mm×38 mm×53 mm,形态:皮质厚度不清,回声正常,皮髓界限清晰,集合系统正常。双肾轮廓规则,包膜连续完整,双肾内未见肾盂肾盏扩张。
心电图 心房纤颤(快速型),心率119次/min。
诊疗分析 患者病史特点:(1)老年女性患者,有“风湿性心脏病”,生物瓣膜置换术后长期华法林抗凝,近期有抗凝过度的情况;(2)肾脏损害起病隐匿,进展迅速;表现为急进性肾小球肾炎(RPGN),持续镜下血尿,发作肉眼血尿,伴少量蛋白尿,血白蛋白轻度下降,肾功能急骤恶化,肌酐最高320 μmol/L(图2);肾脏大小形态正常;(3)肾外有肺部病变,右上肺厚壁空洞;(4)血液系统受累,轻~中度贫血,正细胞正色素、低增生性贫血;(5)免疫指标异常:MPO-ANCA 140.33 RU/ml,pANCA 1:80,补体C3轻度下降。
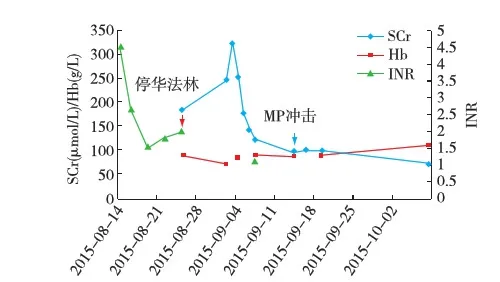
图2 患者INR与SCr、Hb变化INR:国际标准化比值;SCr:血清肌酐;Hb:血红蛋白
根据上述特点,患者应考虑以下疾病:(1)华法林相关肾病(WRN)。患者心脏瓣膜置换术后长期华法林抗凝,发作肉眼血尿以及发现AKI前INR显著升高(最高4.51),而停用华法林后尿色转清、肌酐下降,支持WRN诊断。但是停用华法林后尿色并未立即转清,结合血清MPO-ANCA阳性、补体下降,考虑合并其他疾病可能。(2)抗中性粒细胞胞质抗体相关性血管炎(AAV)。肾脏损害表现为RPGN伴肺部炎性病变,血清MPO-ANCA高滴度阳性,临床诊断AAV成立。但未使用免疫抑制剂后肾功能明显改善,不符合该类疾病病情变化特点。
此外,尚不除外合并其他原发或继发性肾脏疾病可能,故在全面评估出血风险后行肾活检术。
肾活检病理
光镜 30个肾小球中3个球性废弃,2个细胞性、3个纤维细胞性新月体(图3A)。余肾小球系膜区偶见增宽,毛细血管袢开放好,袢腔内见单个核细胞及中性粒细胞浸润,见节段袢坏死(图3B)。PASM-Masson:肾小球系膜区偶见嗜复红物沉积。肾小管间质病变中度,慢性病变基础上合并急性病变,灶性小管萎缩、基膜增厚,多灶性小管扁平、上皮细胞刷状缘脱落,管腔内见较多蛋白管型及红细胞管型(图3C),小灶性肾小管上皮细胞内见棕黄色颗粒,间质浸润细胞灶性分布,以单个核细胞为主,少量浆细胞,小灶性中性粒细胞,散在嗜酸性粒细胞。普鲁士蓝染色肾小管上皮细胞内见含铁血黄素颗粒(图3D)。动脉未见明确病变。
免疫荧光 IgA++,C3++,呈颗粒状弥漫分布于肾小球系膜区(图3E、F)。IgG、IgM、C1q阴性。
电镜 节段肾小球系膜区增宽,系膜细胞及基质增多,数处见高密度电子致密物分布(图3G),毛细血管袢开放好,内皮细胞吞饮,袢腔内见单核细胞,毛细血管袢基膜内皮下及上皮侧未见电子致密物分布。近端肾小管上皮细胞刷状缘脱落,胞质内见较多溶酶体,部分上皮细胞内见含铁小体(图3H)。
此患者肾活检病理具有以下特点:(1)肾小球节段坏死性病变伴新月体形成;(2)肾小管间质慢性病变基础上合并中度急性病变,管腔内见较多红细胞管型,小管上皮细胞内见含铁血黄素颗粒;(3)免疫荧光IgA、C3弥漫颗粒状沉积于肾小球系膜区;(4)电镜肾小球系膜区见高电子致密物沉积,肾小管上皮细胞内见含铁小体。结合临床病史及病理特点:
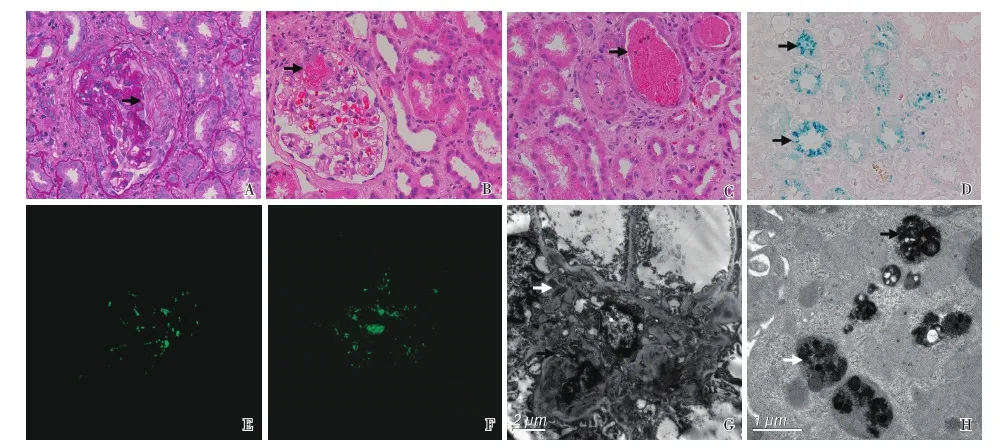
图3 A:肾小球细胞性新月体(↑)(PAS,×400);B:肾小球节段袢坏死(↑)(HE,×400);C:肾小管管腔内红细胞管型(↑)(HE,×400);D:肾小管上皮细胞内含铁血黄素沉积(↑)(普鲁士蓝,×400);E、F:IgA++(E),C3++(F),呈颗粒状弥漫分布于肾小球系膜区(IF,×400);G:肾小球系膜区高密度电子致密物(↑)(EM);H:肾小管上皮细胞内含铁小体(↑)(EM)
最后诊断 (1)AAV、ANC相关性肾炎;(2)WRN;(3)IgA肾病(IgAN);(4)急性肾损伤(AKI)3期;(5)高血压病1级(极高危);(6)心脏瓣膜置换术后;(7)心房纤颤(快速型)。
治疗及随访 诊断明确并排除活动性感染后自9月14日起予甲泼尼龙注射剂250 mg/d冲击治疗4d,继予泼尼松30 mg/d口服,利伐沙班10 mg/d抗凝;复查尿沉渣红细胞计数260 万/ml、多形型,MPO-ANCA 115.52 RU/ml,SCr降至正常(图2)。出院(再度抗凝5d)后诉尿色加深,停用利伐沙班尿色转清。10月8日门诊复查尿沉渣红细胞计数245 万/ml(多形型),尿蛋白阴性;SCr 72 μmol/L,Hb 110 g/L。改用阿司匹林抗血小板。
讨 论
该例老年患者心脏瓣膜置换术后长期接受华法林治疗,合并持续性房颤,基础疾病多,病情复杂;起病早期表现隐匿未重视,出现肉眼血尿及AKI时未及时停用华法林,对华法林引起肾损害的意识不足。该病例最后经肾活检病理检查确诊为ANCA相关肾损害、IgAN合并华法林相关肾病。
患者肾小球病变同时具有AAV肾损害和IgAN的特征,是AAV合并IgA沉积,还是IgAN合并ANCA阳性,或AAV合并IgAN?有报道126例AAV患者中肾组织有免疫复合物(IC)沉积者68例(54.0%);其中以IgM和C3肾小球系膜区沉积居多,荧光染色强度一般≤++; IgA沉积15例,但染色强度>++仅1例[1]。有报道40例AAV患者中有8例肾组织有IC沉积(≥++),其中IgM沉积5例,IgA沉积2例(++者1例,+++者1例),IgG沉积1例[2]。可见,AAV肾损害合并IgA沉积并不少见。另一研究显示,34例新月体型IgAN(新月体比例>10%)中8例伴ANCA阳性;伴ANCA阳性者年龄更大、全身症状更常见,其中6例有咯血和肺部浸润;新月体的比例更多,系膜增生较少,但IgA沉积强度类似;强化免疫抑制治疗反应更好[3]。合并ANCA阳性的IgAN患者病理和临床及治疗反应上更类似于AAV,可认为是AAV合并IgAN。该患者伴明显系统性血管炎的表现(肺部损害),IgA、C3肾小球系膜区沉积,因此原发肾脏疾病考虑AAV肾损害合并IgAN,治疗以控制AAV肾损害活动性病变为主。
患者病程中出现AKI(图2),结合病史及病理特点有以下可能:(1)血管袢坏死及新月体形成,导致滤过屏障破坏、红细胞漏出,出现血尿、肾功能损害,如无治疗干预,多慢性进展。患者病程中未经免疫抑制治疗即尿色转清、肾功能恢复,与此特点不符,考虑合并其他原因。(2)输尿管完全性梗阻加重肾功能损伤,但无法解释之前SCr为何进行性升高。(3)红细胞管型阻塞肾小管会导致AKI;而肉眼血尿和含铁血黄素沉积也是导致肾小管间质损害的重要因素[4-5]。肾小管上皮含铁血黄素沉积可能与红细胞尿、溶血(血红蛋白)及横纹肌溶解(肌红蛋白)相关,临床证据支持血尿所致。患者尿色转清后SCr随之下降也进一步支持肉眼血尿导致AKI的推断。此外,不能忽视患者肉眼血尿发作时有抗凝过度,而停药后尿色自行转清,高度提示肉眼血尿与抗凝过度相关。推断华法林抗凝过度是AKI的发生的重要诱因,患者在原发肾脏疾病基础上考虑合并WRN。
WRN的概念由Brodsky[9]团队于2009年首次提出。该作者回顾9例接受华法林治疗出现血尿及AKI患者的资料后发现,发生AKI时均有INR异常升高,病理可见急性肾小管损伤和肾小球出血,肾小管中见大量红细胞管型。研究发现慢性肾脏病患者发生WRN的风险更大,出现WRN者1年死亡率明显升高[7]。该研究将WRN定义为“使用华法林的情况下,在出现过度抗凝(INR>3)1周以内,SCr升高0.3 mg/dl以上,且不伴活动性出血”。利用小鼠疾病模型观察到的肾脏病理改变与人群肾活检病理类似,且使用维生素K可阻止其血清肌酐升高、减轻肾小球内出血[8]。本例肾脏病理未见肾小球出血,但在肾小管上皮细胞观察到含铁血黄素沉积,可能与肾活检时机偏晚有关。文献报道病例及WRN动物模型肾脏病理检查均于疾病发生后短期进行,而此病例肾活检时距起病已1个月,且临床症状均已缓解,早期的活动出血病变已经转化为红细胞管型及含铁血红素沉积等出血后的病理改变。
肾小球毛细血管袢断裂、红细胞管型阻塞肾小管以及急性肾小管损伤被认为是WRN的主要病理机制[6,8],但细胞及分子生物发病机制尚不明确,可能的机制有:氧化应激损伤[4-5,9],华法林抑制维生素K依赖蛋白激活导致的肾小球损伤[10]及肾小球内皮细胞和小管上皮细胞凋亡增加[11]。另外,肾功能也对华法林的抗凝效果产生影响,GFR越低所需华法林剂量更小,INR更难控制,出血事件发生率更高[12]。该患者此前长期服用华法林没有发生WRN,此次发病可能与血管炎活动的推波助澜有关。
除WRN外,华法林的其他肾脏不良反应也屡见报道,包括白细胞破碎性血管炎[13]和过敏性间质性肾炎[14]、自发性胆固醇栓塞[15]、双侧肾盂输尿管出血导致AKI[16]。但未见华法林导致ANCA阳性的报道,此病例肾脏血管炎表现及肾脏间质炎性是否与华法林相关目前尚无法明确。
此外,亦有其他抗凝剂引起的类似于WRN的肾脏损伤报道,如达比加群[17],其机制与华法林类似;因而有学者将此类病变统称为“抗凝剂相关肾病”[18]。患者服用利伐沙班后再次出现肉眼血尿,是否“抗凝剂相关肾病”再发值得深思。
本例患者经肾活检病理检查明确了复杂的肾脏疾病诊断,通过调整抗凝方案和免疫抑制治疗,肾脏疾病明显缓解。目前对WRN尚缺乏有效的诊断和评估体系,发病机制仍有诸多疑问亟待解答。对长期华法林抗凝治疗的患者,临床医师应密切监测INR,及时调整药物剂量,积极处理合并危险因素(表1),定期监测肾功能变化,完善华法林代谢基因检测以利于个体化用药。疑诊WRN时应及时停药,如病情仍无明显改善,应争取行肾活检明确是否合并其他肾脏疾病。

表1 WRN发生的危险因素
WRN:华法林相关肾病;INR:国际标准化比值;ACEI:血管紧张素转换酶抑制剂;CCB:钙离子拮抗剂;AST:谷草转氨酶
小结:WRN在临床上并不少见,可与其他原发或继发性肾脏疾病合并存在,对于疾病高危患者应完善相关检查,必要时行肾活检明确诊断。
1 Haas M,Eustace JA.Immune complex deposits in ANCA-associated crescentic glomerulonephritis:a study of 126 cases.Kidney Int,2004,65(6):2145-2152.
2 于峰,赵明辉,邹万忠,等.肾脏有免疫复合物沉积的小血管炎的临床病理特点.中华肾脏病杂志,2003,19(4):219-222.
3 Bantis C,Stangou M,Schlaugat C,et al.Is presence of ANCA in crescentic IgA nephropathy a coincidence or novel clinical entity? A case series.Am J Kidney Dis,2010,55(2):259-268.
4 Moreno JA,Martín-Cleary C,Gutiérrez E,et al.AKI associated with macroscopic glomerular hematuria:clinical and pathophysiologic consequences.Clin J Am Soc Nephrol,2012,7(1):175-184.
5 Martines AM,Masereeuw R,Tjalsma H,et al.Iron metabolism in the pathogenesis of iron-induced kidney injury.Nat Rev Nephrol,2013,9(7):385-398.
6 Brodsky SV,Satoskar A,Chen J,et al.Acute kidney injury during warfarin therapy associated with obstructive tubular red blood cell casts:a report of 9 cases.Am J Kidney Dis,2009,54(6):1121-1126.
7 Brodsky SV,Nadasdy T,Rovin BH,et al.Warfarin-related nephropathy occurs in patients with and without chronic kidney disease and is associated with an increased mortality rate.Kidney Int,2011,80(2):181-189.
8 Ozcan A,Ware K,Calomeni E,et al.5/6 nephrectomy as a validated rat model mimicking human warfarin-related nephropathy.Am J Nephrol,2012,35(4):356-364.
9 Tracz MJ,Alam J,Nath KA.Physiology and pathophysiology of heme:implications for kidney disease.J Am Soc Nephrol,2007,18(2):414-420.
10 Yanagita M,Ishii K,Ozaki H,et al.Mechanism of inhibitory effect of warfarin on mesangial cell proliferation.J Am Soc Nephrol,1999,10(12):2503-2509.
11 Ware K,Brodsky P,Satoskar AA,et al.Warfarin-related nephropathy modeled by nephron reduction and excessive anticoagulation.J Am Soc Nephrol.2011.22(10):1856-62.
12 Limdi NA,Beasley TM,Baird MF,et al.Kidney function influences warfarin responsiveness and hemorrhagic complications.J Am Soc Nephrol,2009,20(4):912-921.
13 Hsu CY,Chen WS,Sung SH.Warfarin-induced leukocytoclastic vasculitis:a case report and review of literature.Intern Med,2012,51(6):601-606.
14 Kapoor KG,Bekaii-Saab T.Warfarin-induced allergic interstitial nephritis and leucocytoclastic vasculitis.Intern Med J,2008,38(4):281-283.
15 Moll S,Huffman J.Cholesterol emboli associated with warfarin treatment.Am J Hematol,2004,77(2):194-195.
16 Gültekin N,Akn F,KüçükateE.Warfarin-induced bilateral renal hematoma causing acute renal failure.Turk Kardiyol Dern Ars,2011,39(3):228-230.
17 Ryan M,Ware K,Qamri Z,et al.Warfarin-related nephropathy is the tip of the iceberg:direct thrombin inhibitor dabigatran induces glomerular hemorrhage with acute kidney injury in rats.Nephrol Dial Transplant,2014,29(12):2228-2234.
18 Wheeler DS,Giugliano RP,Rangaswami J.Anticoagulation-related nephropathy.J Thromb Haemost,2016,14(3):461-467.
(本文编辑 莫 非 凡 心)
Warfarin anticoagulation, gross haematuria and progressive renal dysfunction
TUYuanmao,ZHOUYun,XIEHonglang,LIUZhihong
NationalClinicalResearchCenterofKidneyDiseases,JinlingHospital,NanjingUniversitySchoolofMedicine,Nanjing210016,China
A 66 year old woman underwent long-term anticoagulation therapy with warfarin due to bioprosthetic heart valve replacement. The renal involvement was noticed 4 months ago, manifesting persistent microscopic hematuria and paroxysmal gross hematuria with simultaneously serum creatinine increasing, in the case of excessive anticoagulation. Blood examination found positive MPO-ANCA and renal biopsy conformed the renal damage of ANCA associated vasculitis, combined with IgA nephropathy. Gross hematuria dissovled after anticoagulant withdrawal and renal function recovered spontaneously. So warfarin associated nephropathy was also considered..
warfarin acute kidney injury Warfarin-related Nephropathy ANCA associated vasculitis
10.3969/cndt.j.issn.1006-298X.2016.05.020
南京军区南京总医院肾脏科 国家肾脏疾病临床医学研究中心 全军肾脏病研究所(南京,210016)
2016-06-23

