利妥昔单抗联合甲氨蝶呤在中重度类风湿关节炎中的临床应用
李 威
·短篇论著·
利妥昔单抗联合甲氨蝶呤在中重度类风湿关节炎中的临床应用
李威
本溪市中心医院急诊科,辽宁 本溪 117000
[摘要]目的评价利妥昔单抗(RTX)及甲氨蝶呤(MTX)在中重度类风湿性关节炎中联合应用的临床效果。方法将68例中重度类风湿性关节炎患者随机分为试验组及对照组,每组34例,分别给予RTX+MTX及安慰剂+MTX治疗,观察两组间类风湿性关节炎的临床及化验指标变化。结果治疗后1个月,试验组触痛关节数、晨僵时间、Barthel指数与对照组比较,差异有统计学意义(P<0.05)。治疗后3个月,试验组的肿胀关节数、触痛关节数、晨僵时间、DAS28评分及Barthel指数与对照组比较,差异有统计学意义(P<0.05或P<0.01)。治疗后1个月,试验组CRP、ESR、RF、IL-6低于对照组(P<0.05或P<0.01);治疗后3个月,试验组CRP、ESR、RF、IL-6低于对照组(P<0.01)。随访期内,试验组的并发症、过敏反应发生率高于对照组(P<0.05)。结论MTX联合应用RTX治疗中重度类风湿性关节炎可达到安全满意的临床效果。
[关键词]类风湿性关节炎;利妥昔单抗;甲氨蝶呤
0引言
类风湿性关节炎是一种免疫性疾病,具有病情迁延、病程长及致残率高的特点[1]。患者由于长期反复的病情发作导致关节功能受损,生活质量降低,甚至由长期发展导致抑郁倾向[2]。类风湿关节炎治疗的药物主要包括激素、非甾体抗炎药及慢作用抗风湿药物(Disease modifying anti-rheumatic drugs,DMARDs)[3]。利妥普单抗(Rituximab,RTX)2006被美国FDA批准应用治疗中重度类风湿性关节炎。甲氨蝶呤(Methotrexate,MTX)是叶酸拮抗剂,是DMARD中常用的一种药物,属抗代谢类药物。本研究应用甲氨蝶呤联合利妥昔单抗(RTX)治疗类风湿性关节炎,评估其效果及临床反应,探讨其临床应用价值。
1资料与方法
1.1研究对象以2013年2月至2014年11月在我院风湿免疫科住院治疗的68例类风湿关节炎患者为研究对象,男31例,女37例,年龄(53.7±21.9)岁,病程(73.62±47.19)个月。以ACR(American College of Rheumatology,美国风湿病学会)2010年修订的类风湿诊断标准进行诊断。满足下列活动条件:肿胀关节数≥4个,触痛关节数≥4个,红细胞沉降率(ESR)>28 mm/h,血清C反应蛋白(CRP)>5 mg/L,病情活动度为中重度,类风湿活动指数DAS28≥3.2,采用Barthel指数进行患者的日常生活质量评分。计算机随机数法随机分为对照组及试验组,每组34例。RTX注射液(美罗华)购自上海罗氏制药有限公司,MTX片购自通化茂祥制药有限公司。排除标准:伴有心、脑、肺、肝、肾等重要器官疾病或功能不全;有上消化道溃疡病史者;有炎性关节病或伴有其他结缔组织病者;严重感染、结核、HIV感染、活动肝炎、肿瘤、血液病患者,曾经接受过单克隆抗体治疗的患者;白细胞计数<4×109/L,血红蛋白<85 g/L,血小板计数<100×109/L;妊娠期、2年内计划生育女性及哺乳期女性;用药依从性差者。在应用RTX前,两组患者的年龄、性别、病程、关节功能分级、肿胀关节数、触痛关节数、晨僵时间、DAS28评分、Barthel指数、ESR、CRP、RF、IL-6等比较差异均无统计学意义(P>0.05),可进行病例对照研究,无伦理学争议。
1.2研究方法所有纳入研究病例治疗前均使用过1种或几种改善病情抗风湿药(激素、非甾体抗炎药或DMARDs)且效果不满意。1个月内停用激素、非甾体抗炎药及DMARDs。试验组:MTX 10 mg/周,口服,维持稳定剂量6周,RTX 1 000 mg加入500 mL生理盐水静脉滴注给药2次,两次间隔15 d。对照组:给予MTX 10 mg/周口服,维持稳定剂量6周,安慰剂(生理盐水500 mL)静脉滴注给药2次,两次间隔15 d。

2结果
2.1两组临床资料比较随访至治疗后3个月,两组患者治疗后肿胀关节数少于对照组,触痛关节数、晨僵时间较短,DAS28评分及Barthel指数均有改善,在治疗后1个月,试验组的触痛关节数目少于对照组,晨僵时间较对照组缩短,差异有统计学意义(P<0.05),Barthel指数高于对照组(P<0.05)。治疗后3个月,试验组的肿胀关节数、触痛关节数、晨僵时间及DAS28评分低于对照组,差异有统计学意义(P<0.05或P<0.01),Barthel指数高于对照组(P<0.01)。见表1。
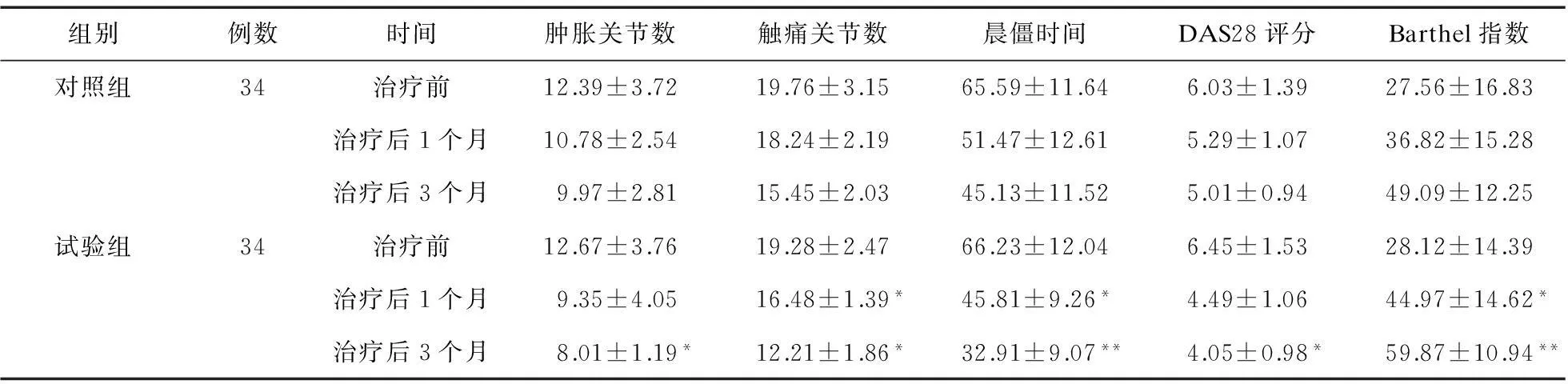
表1 两组临床指标比较
注:与对照组比较,*P<0.05,**P<0.01
2.2两组化验指标比较随访至治疗后3个月,两组CRP、ESR、RF、IL-6均改善。治疗后1个月,试验组CRP、ESR、RF、IL-6低于对照组(P<0.05或P<0.01);治疗后3个月,两组比较差异有统计学意义(P<0.01),见表2。

表2 两组化验指标比较
注:与对照组比较,*P<0.05,**P<0.01
2.3两组药物不良反应比较随访期间,两组患者均无肝坏死、心肌毒性及过敏休克等严重不良反应事件发生,两组胃肠道反应、血糖异常、神经症状、肝功能变化、白细胞减少、黏膜溃疡及感染等并发症比较差异无统计学意义(P>0.05),试验组过敏反应率高于对照组(P<0.05)。见表3。

表3 患者药物不良反应发生情况(例,%)
注:与对照组比较,*P<0.05
3讨论
类风湿性关节炎病情迁延,患者痛苦,生活质量下降[4]。药物治疗无论是激素、非甾体抗炎药还是DARMDs均需要长期应用,不良反应较大,对于一部分中重度患者治疗效果并不满意[5]。MTX是DMARDs中的一种,属于抗代谢类药,能通过抑制二氢叶酸还原酶及甲酰基转移酶生物活性,从而抑制IL、TNF等细胞因子释放,发挥抗炎效果,减轻关节肿胀及疼痛[7]。RTX用于治疗中重度类风湿性关节炎患者,与DMARDs类药物联合使用,或应用于1种及多种抗TNF-α抗体效果不显著时[8]。RTX是嵌合鼠/人单克隆抗体,该抗体可与B淋巴细胞膜上的CD20结合,引发B细胞进入溶解免疫反应,细胞溶解机制包括抗体依赖性细胞毒性和补体依赖性细胞毒性[9]。有研究认为,RTX可用于MTX联合其他的抗风湿药或其他非生物抗风湿药物治疗效果不满意的类风湿性关节炎病例[10]。本研究联合应用RTX及MTX治疗中重度类风湿性关节炎,结果显示,随访至治疗后3个月,两组治疗后肿胀关节数目、触痛关节数目、晨僵时间、DAS28评分及Barthel指数均有改善,且CRP、ESR、RF、IL-6均得到改善,但RTX组的临床指标及化验指标改善更为明显,Van Vollenhoven等[11]研究显示,其临床症状、体征及化验指标在应用RTX 8~16周明显改善。本研究显示,用药4周后症状开始出现改善,3个月后明显改善。Genovese等[12]研究显示,RTX联合MTX达到ACR50缓解的比例达51%,RTX组在ACR缓解指标上有明显优势,在影像学表现、关节功能改善、生活质量提高等方面都有良好的效果。而且,RTX单独应用也可达到临床缓解的目的。MTX的不良反应包括恶心、呕吐、饱胀及腹泻等消化道症状,血糖异常,肝肾功能损伤,致畸及精神症状等[13],RTX不良反应除了消化道症状、肝肾毒性外,变态反应的发生率也较高[14]。本研究结果显示,在药物不良反应方面,RTX增加了患者过敏反应的发生几率。RTX可能并发难以控制的感染,但本研究纳入患者中没有出现严重感染病例,所发生感染病例为泌尿系感染及疖肿等,经抗炎治疗均治愈。
本研究通过联合应用MTX及RTX对中重度类风湿性关节炎进行治疗,结果显示,联合应用RTX可明显改善患者临床症状,对常规抗风湿治疗效果不明显的患者,可以考虑给予RTX治疗。
参考文献:
[1]Gashi AA,Rexhepi S,Berisha I,et al.Treatment of rheumatoid arthritis with biologic DMARDS (Rituximab and Etanercept) [J].Med Arch,2014,68(1):51-53.
[2]Roshique KK,Ravindran V.Efficacy and safety of a biosimilar rituximab in biologic naïve patients with active rheumatoid arthritis[J].Clin Rheumatol,2015,34(7):1289-1292.
[3]Harrold LR,Reed GW,Shewade A,et al.Effectiveness of rituximab for the treatment of rheumatoid arthritis in patients with prior exposure to anti-TNF:results from the CORRONA registry[J].J Rheumatol,2015,42(7):1090-1098.
[4]Reddy V,Cambridge G,Isenberg DA,et al.Internalization of rituximab and the efficiency of B cell depletion in rheumatoid arthritis and systemic lupus erythematosus[J].Arthritis Rheumatol,2015,67(8):2046-2055.
[5]Wu B,Song Y,Leng L,et al.Treatment of moderate rheumatoid arthritis with different strategies in a health resource-limited setting:a cost-effectiveness analysis in the era of biosimilars[J].Clin Exp Rheumatol,2015,33(1):20-26.
[6]Yamada K,Oshiro Y,Okamura S,et al.Clinicopathological characteristics and rituximab addition to cytotoxic therapies in patients with rheumatoid arthritis and methotrexate-associated large B lymphoproliferative disorders[J].Histopathology,2015,67(1):70-80.
[7]Bazzichi L,Biasi D,Tinazzi E,et al.Safety of rituximab in the routine treatment of rheumatoid arthritis in Italy in patients refractory to anti-TNFa drugs:results from the observational retrospective-prospective RUBINO study[J].Reumatismo,2014,66(3):224-232.
[8]Valleala H,Korpela M,Hienonen-Kempas T,et al.Long-term real-life experience with rituximab in adult finnish patients with rheumatoid arthritis refractory or with contraindication to anti-tumor necrosis factor drugs[J].J Clin Rheumatol,2015,21(1):24-30.
[9]Gamonet C,Deschamps M,Marion S,et al.The alternative CD20 transcript variant is not a surrogate marker for resistance to rituximab in patients with rheumatoid arthritis[J].Rheumatology (Oxford),2015,54(9):1744-1745.
[10]Schattner A.ACP Journal Club.Review:In rheumatoid arthritis,adding rituximab to methotrexate improves clinical outcomes[J].Ann Intern Med,2015,162(12):JC9.
[11]Van Vollenhoven RF,Emery P,Bingham CO,et al.Long-term safety of rituximab in rheumatoid arthritis:9.5-year follow-up of the global clinical trial programme with a focus on adverse events of interest in RA patients[J].Ann Rheum Dis,2013,72(9):1496-1502.

[13]Kudo-Tanaka E,Shimizu T,Nii T,et al.Early therapeutic intervention with methotrexate prevents the development of rheumatoid arthritis in patients with recent-onset undifferentiated arthritis:A prospective cohort study[J].Mod Rheumatol,2015,30(4):1-6.
[14]Isvy A,Meunier M,Gobeaux-Chenevier C,et al.Safety of rituximab in rheumatoid arthritis:a long-term prospective single-center study of gammaglobulin concentrations and infections[J].Joint Bone Spine,2012,79(4):365-369.
Clinical application of rituximab combined with methotrexate in the treatment of rheumatoid arthritis
LI Wei
(Emergency Department,Benxi Central Hospital,Benxi 117000,China)
[Abstract]ObjectiveTo evaluate the clinical efficacy of rituximab combined with methotrexate in the treatment of rheumatoid arthritis.MethodsSixty-eight patients diagnosed with moderate or severe rheumatoid arthritis were divided into experiment group (n=34) and control group (n=34) who accepted RTX+MTX and placebo+MTX respectively.The clinical and laboratory indexes were observed.ResultsCompared with control group,the number of tender joint and time of morning stiffness in experiment group were lower at 1 month after treatment (P<0.05),and the Barthel index was higher (P<0.05).The number of swollen joint and tender joint,the time of morning stiffness and DAS28 score in experiment group were lower than those of control group at 3 months after treatment (P<0.05 or P<0.01) with higher Barthel index (P<0.05).The levels of CRP (C-reactive protein),ESR (erythrocyte sedimentation),RF (rheumatoid factor) and IL-6 (Interleukin 6) in experiment group were lower than those of control group at 1 month (P<0.05 or P<0.01) and 3 months (P<0.01) after treatment.The allergic rate in experiment group was higher than that of control group during follow-up period (P<0.05).ConclusionRituximab combined with methotrexate is effective and safe with satisfactory result in the treatment of rheumatoid arthritis.
Key words:Rheumatoid arthritis;Rituximab;Methotrexate
收稿日期:2015-09-09
DOI:10.14053/j.cnki.ppcr.201605032

