胰高血糖素样肽1受体激动剂类降糖药致2型糖尿病患者鼻咽炎和上呼吸道感染的网状meta分析
李志霞,武珊珊,杨智荣,詹思延△,孙 凤△
(1. 北京大学公共卫生学院流行病与卫生统计学系, 北京 100191; 2. 首都医科大学附属北京友谊医院国家消化系统疾病临床研究中心, 北京 100050; 3. Primary Care Unit, University of Cambridge, Cambridge CB21TN, UK)
·论著·
胰高血糖素样肽1受体激动剂类降糖药致2型糖尿病患者鼻咽炎和上呼吸道感染的网状meta分析
李志霞1,武珊珊2,杨智荣3,詹思延1△,孙凤1△
(1. 北京大学公共卫生学院流行病与卫生统计学系, 北京100191; 2. 首都医科大学附属北京友谊医院国家消化系统疾病临床研究中心, 北京100050; 3.PrimaryCareUnit,UniversityofCambridge,CambridgeCB21TN,UK)
[摘要]目的:使用网状meta分析系统评价胰高血糖素样肽1受体激动剂(glucagon-like peptide-1 receptor agonists,GLP-1 RAs)类降糖药对两种常见的呼吸系统不良事件(respiratory system adverse event,RSAE,包括鼻咽炎和上呼吸道感染)的影响。方法:系统检索Medline、Embase、Clinical trials和Cochrane数据库中(截止2015年5月)比较GLP-1 RAs与传统降糖药或安慰剂对鼻咽炎和上呼吸道感染发生风险影响的随机对照研究,采用网状meta分析方法对纳入的研究结果进行加权合并。结果: 共纳入50个研究,包括13种干预措施:7种GLP-1 RAs类药(艾塞那肽、艾塞那肽缓释剂、利拉鲁肽、利西拉来、他司鲁肽、阿必鲁肽、杜拉鲁肽)、5种传统降糖药(胰岛素、二甲双胍、磺脲类、西格列汀、噻唑烷二酮类)和安慰剂。网状meta分析结果显示,与胰岛素相比,他司鲁肽显著降低了鼻咽炎(OR=0.67,95%CI:0.46~0.96)和上呼吸道感染(OR=0.39,95%CI:0.23~0.73)的发生风险;与安慰剂相比,他司鲁肽显著降低了上呼吸道感染(OR=0.57,95%CI:0.34~0.99)的发生风险。此外,基于贝叶斯理论的网状meta分析显示,鼻咽炎和上呼吸道感染发生风险排最末位的均为他司鲁肽。结论: 他司鲁肽显著降低了鼻咽炎和上呼吸道感染的发生风险,但仍有待专门针对RSAE设计的大型前瞻性研究加以验证。
[关键词]胰高血糖素样肽1受体;糖尿病,2型;鼻咽炎;上呼吸道感染;Meta分析
许多研究表明,炎症反应在糖尿病的发生、发展中扮演着至关重要的作用[1-3],血液循环中炎性反应标志物的升高可加剧2型糖尿病(type2diabetesmellitus,T2DM)患者常见并发症的发生风险,如心血管疾病[4-6],其中,鼻咽炎和上呼吸道感染作为临床常见的炎症性疾病,其发病率较高,而且二者往往并存且相互影响[7]。目前关于胰高血糖素样肽1受体激动剂(glucagon-likepeptide-1receptoragonists,GLP-1RAs)类降糖药、传统降糖药或安慰剂致T2DM患者发生鼻咽炎和上呼吸道感染等呼吸系统不良反应(respiratorysystemadverseevent,RSAE)风险的研究结论不一[8-9]。Kadowaki等[10]2009年的一项研究指出,艾塞那肽致T2DM患者发生鼻咽炎和上呼吸道感染的发生率低于安慰剂(OR=0.88),然而,Buse等[11]2011年的一项研究则报道艾塞那肽致T2DM患者发生鼻咽炎(OR=1.2)和上呼吸道感染(OR=1.1)的发生率高于安慰剂。导致不一致结果产生的原因可能是由于现有研究多为小样本的探索性分析,并非主要研究结局。为此,本文拟采用网状meta分析[12-13]综合直接和间接比较结果,对比不同GLP-1RAs与传统降糖药或安慰剂对RSAE发生风险的影响,为T2DM的临床安全用药提供更多参考。
1资料与方法
1.1检索策略
以“GLP-1receptoragonists”为关键词或主题词检索Medline、Embase、Clinicaltrials和Cochrane数据库中相关文献,文献限定为“随机对照试验(randomizedclinicaltrial,RCT)”及“呼吸系统不良事件”,各数据库检索时间范围均为从该数据库最早收录的文献到2015年5月1日。
1.2纳入、排除标准
纳入标准:(1)文献语言限定为英文;(2)研究类型为RCT;(3)研究对象为T2DM患者;(4)干预措施为GLP-1RAs与传统降糖药或安慰剂等的比较;(5)疗程≥4周;(6)研究结局为鼻咽炎和上呼吸道感染。排除标准:不符合上述标准的、正在进行的或者Clinicaltrials网站上已完成但尚未发布研究结果的试验。
呼吸系统不良事件定义:鼻咽炎和上呼吸道感染两个结局事件均摘自文献报告的次要结局。
1.3文献信息摘录及质量评价
摘录信息包括作者、发表年份、对照类型、背景用药、结局事件、样本量、疗程、平均年龄、平均病程等。对每篇纳入的文献按照JADAD改良量表[14]进行质量评分。以上过程均由两人独立平行完成,意见经讨论不一致时由第3人裁决。
1.4统计学分析
网状meta分析主要是借助间接比较技术对处于同一个证据体的所有干预措施同时进行综合评价并排序[12]。间接比较的思想为:想要评价两种不同干预措施的效果,但又找不到它们之间直接比较的临床研究证据,此时就必须借助一个中间桥梁(通常是安慰剂或者某个公认的处理措施)对两种干预的效能进行间接评价。
利用WinBUGS(版本1.4)软件选择Bayes随机效应模型进行网状meta分析,并用R(版本3.1.2)软件绘制各干预措施的网状关系图,分析中遇到两组均为0发生事件的研究则以0.5校正发生数[15]。
2结果
2.1纳入研究基本特征
共检索到相关文献1 106篇和33个临床试验,根据纳入排除标准最终纳入50篇,筛选过程见图1。
2.2网状meta分析证据网络图
网状meta分析干预措施之间关系见图2,图中的线段越粗表示相连接的可进行直接比较的两种干预措施的研究数目越多,反之越少,无连接线的两种干预措施可采用网状meta分析进行间接比较(如他司鲁肽和利拉鲁肽目前无相关RCT研究,可借助安慰剂这个中间桥梁进行间接比较以评价二者的RSAE效应),圆点大小表示该干预措施的合计样本量。共涉及13种干预措施:7种GLP-1RAs类药(艾塞那肽、艾塞那肽缓释剂、利拉鲁肽、利西拉来、他司鲁肽、阿必鲁肽、杜拉鲁肽)、安慰剂和5种传统降糖药(胰岛素、二甲双胍、磺脲类、西格列汀、噻唑烷二酮类),其中艾塞那肽和安慰剂比较的研究数目最多,纳入研究对象数目最多的干预措施为他司鲁肽。纳入研究的发表年代的范围为2005年至2014年,背景用药多为传统降糖药、吡格列酮、饮食、运动等的组合,疗程范围为12~156周,T2DM患者平均年龄范围为50.31~63.30岁,病程范围为1.3~13.9年。

RCT, randomized clinical trial; T2DM, type 2 diabetes mellitus; GLP-1, glucagon-like peptide-1.图1 文献纳入排除流程图Figure 1 Flow chart of studies considered for inclusion
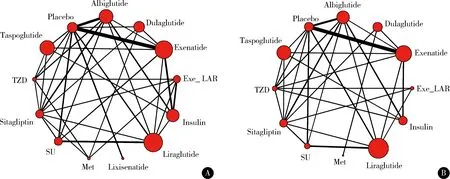
A,nasopharyngitis (43 RCTs, 93 arms, n=23 029);B,upper respiratory tract infection (35 RCTs,76 arms, n=20 499). SU, sulphanylureas; Met, metformin; TZD, thiazolidinedione; Exe_LAR, exenatide long-acting release. Lines connect the interventions that have been studied in head-to-head (direct) comparisons in the eligible RCTs. The width of the lines represents the cumulative number of RCTs for each pairwise comparison and the size of every node is proportional to the number of randomized participants (sample size).图2 网状meta分析中各干预措施的关系图Figure 2 Evidence structure of eligible comparisons for network meta-analysis
按照JADAD改良量表对文献进行质量评价,纳入的文献总体质量较好,有82%、64%、60%和88%的文献分别报告了随机化、分配隐藏、盲法和失访情况,86%的文献使用了意向治疗分析。
2.3GLP-1RAs对T2DM患者发生两种RSAE结局影响的网状meta分析
图3展示了GLP-1RAs致T2DM患者发生鼻咽炎(左下角)和上呼吸道感染(右上角)风险的网状meta分析结果。最终,对于鼻咽炎事件,本研究纳入了全部7种GLP-1RAs类药物,对于上呼吸道感染事件,由于未有关于利西拉来的相关文献符合纳入标准,只纳入了其余6种GLP-1RAs药物进行分析。
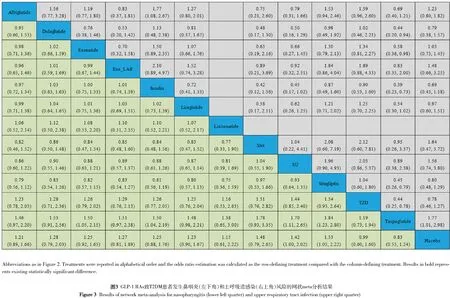
对于鼻咽炎事件,与胰岛素相比,他司鲁肽显著降低了鼻咽炎发生的风险(OR=0.67,95%CI:0.46~0.96);与西格列汀和噻唑烷二酮相比,他司鲁肽降低T2DM患者发生鼻咽炎效果显著(OR=0.59,95%CI:0.38~0.90;OR=0.54,95%CI:0.36~0.81);GLP-1RAs两两比较的结果显示,与艾塞那肽相比,他司鲁肽显著降低了鼻咽炎发生的风险(OR=0.67,95%CI:0.47~0.95)。此外,对于鼻咽炎事件,网状meta分析的结果还提示:与安慰剂相比,他司鲁肽致T2DM患者发生鼻咽炎的风险降低(OR<1),其余6种GLP-1RAs类药均致T2DM患者发生鼻咽炎的风险增加(OR>1);与胰岛素相比,阿必鲁肽、利拉鲁肽和利西拉来致T2DM患者发生鼻咽炎的风险降低(OR<1),而杜拉鲁肽和艾塞那肽缓释剂则增加了该风险(OR>1);与二甲双胍、磺脲类、西格列汀相比,7种GLP-1RAs均能降低T2DM患者发生鼻咽炎的风险(OR<1),但以上结果差异均无统计学意义。
对于上呼吸道感染事件,与安慰剂相比,他司鲁肽降低上呼吸道感染风险的效果显著(OR=0.56,95%CI:0.34~0.99);与胰岛素相比,阿必鲁肽和他司鲁肽降低风险效果显著(OR=0.56,95%CI:0.37~0.93;OR=0.39,95%CI:0.23~0.73);与噻唑烷二酮和西格列汀相比,他司鲁肽降低风险效果显著(OR=0.44,95%CI:0.25~0.78;OR=0.45,95%CI:0.26~0.79);GLP-1RAs两两比较的结果显示,与杜拉鲁肽和艾塞那肽相比,他司鲁肽显著降低了T2DM患者发生上呼吸道感染的风险(OR=0.44,95%CI:0.20~0.94;OR=0.58,95%CI:0.36~0.98)。此外,对于上呼吸道感染事件,网状meta分析的结果还提示:与安慰剂相比,除杜拉鲁肽和利拉鲁肽增加了T2DM患者发生上呼吸道感染的风险之外(OR>1),其余4种GLP-1RAs(阿必鲁肽、艾塞那肽、艾塞那肽缓释剂、他司鲁肽)均降低了该风险(OR<1);与胰岛素和噻唑烷二酮相比,6种GLP-1RAs均能降低T2DM患者发生上呼吸道感染的风险(OR<1);与西格列汀相比,杜拉鲁肽增加了T2DM患者发生上呼吸道感染的风险(OR>1),其余5种GLP-1RAs降低了该风险(OR<1);与二甲双胍和磺脲类相比,除他司鲁肽外,其余5种GLP-1RAs均增加了T2DM患者发生上呼吸道感染的风险(OR>1),但以上结果差异均无统计学意义。
2.4呼吸系统不良事件风险排序
13种干预措施的两种RSAE风险排序见表1,其中,鼻咽炎和上呼吸道感染发生风险排第末位的均为他司鲁肽。

表1 GLP-1 RAs 致 T2DM 患者发生鼻咽炎和上呼吸道感染风险排序结果
SUCRA,surfaceunderthecumulativerankingcurve.OtherabbreviationsasinFigure2.
3讨论
本研究结果显示,与传统降糖药及其他种类的GLP-1RAs相比,他司鲁肽显著降低了鼻咽炎和上呼吸道感染事件发生的风险,这一结果与Pratley等[16]2013年的结论相一致,Pratley等的结果表明,他司鲁肽每星期10mg和20mg致T2DM患者鼻咽炎的发生率分别为4.5%和5.6%,均低于传统降糖药(5.8%),且他司鲁肽致T2DM患者上呼吸道感染发生率为2.1%~2.4%,远低于对照组吡格列酮的发生率(5.1%)。
此外,本研究结果还提示,对于鼻咽炎事件,与二甲双胍、磺脲类、西格列汀相比,7种GLP-1RAs均能降低T2DM患者发生鼻咽炎的风险(OR<1)。对于上呼吸道感染事件,与胰岛素相比,GLP-1RAs类药物均能降低上呼吸道感染的发生风险(OR<1),但以上差异均无统计学意义,可能是由于本研究的样本量较小所致。Lee等[17]2012年的一项基础研究表明,在糖尿病小鼠模型中,GLP-1确实可以通过减少巨噬细胞浸润和直接抑制炎症通路来改善胰岛素的敏感性。Kodera等[18]2011年的一项基础研究也表明,GLP-1能改善糖尿病小鼠的炎性反应状态。Bergenstal等[19]2010年在Lancet发表的研究表明,与西格列汀相比,艾塞那肽显著降低了T2DM患者上呼吸道感染发生的风险(OR=0.44)。王兴纯等[20]2014年的一项综述也表明,GLP-1降糖类药物可以通过减少炎性因子的释放、减少巨噬细胞浸润及改善炎性反应相关的信号通路等机制降低机体C反应蛋白水平,改善机体炎性反应状态。
虽然本研究收集了目前所有有关GLP-1RAs类药物安全性问题的RCT研究,并且使用了网状meta分析方法对GLP-1RAs与传统降糖药或安慰剂进行了比较分析,有效弥补了传统meta分析的不足,能给出证据体中的任意两者之间的效应关系,分析结果更细致。但仍有很多临床试验表明,不同剂量的GLP-1RAs致T2DM患者发生鼻咽炎和上呼吸道感染的风险不一,而且其结论并不一致[21-22]。本研究中,除了阿必鲁肽和他司鲁肽外,其余GLP-1RAs类药的相关结局研究数目非常有限,对于GLP-1两两比较的研究更少之又少,因此本研究未按照剂量进行亚组分析,得出的结果也仅是一个探索性结果,要得到稳定的明确的结论,还需等待纳入更多GLP-1之间头对头直接比较的研究对系统综述进行更新。此外,由于本研究的分析仍然是基于研究水平,不同的研究对结局事件的判断标准可能不一,因此存在一些不可避免的偏倚,研究结果仍需要进一步探讨和补充。
本研究的结果提示,与传统降糖药相比,大部分的GLP-1RAs类降糖药导致T2DM患者发生鼻咽炎和上呼吸道感染的风险较低,但由于鼻咽炎和上呼吸道感染是鼻咽癌的危险因素,而且T2DM患者自身的免疫力较健康人群低,因此为了预防不良反应的进一步发展,早期的对症处理尤其重要。
综上所述,本研究表明,他司鲁肽可显著降低两种RSAE的发生风险,但仍有待专门针对RSAE设计的大型前瞻性研究加以验证。
参考文献
[1]程会兰, 翁雅婧, 王利芳, 等.康复运动与糖尿病炎症、胰岛素抵抗和氧化应激的相关性研究 [J]. 中国康复, 2014, 29(4): 287-289.
[2]葛进. 肥胖与糖尿病的炎症机制及治疗的研究进展[J]. 医学综述, 2013, 19(16): 2964-2966.
[3]李秀钧, 邬云红. 糖尿病是一种炎症性疾病?[J]. 中华内分泌代谢杂志, 2003, 19(4): 251-253.
[4]JinQH,LouYF,LiTL,etal.Serumgalectin-3:ariskfactorforvascularcomplicationsintype2diabetesmellitus[J].ChinMedJ(Engl), 2013, 126(11): 2109-2115.
[5]吴伟华, 孙丽芳, 刘晓民. 炎症与冠心病和糖尿病的关系[J]. 临床内科杂志, 2007, 24(12): 800-802.
[6]叶翎, 孙国燕, 孙玉瑶, 等. 慢性低度炎症与糖尿病关系的研究进展 [J]. 医学综述, 2014, 20(21): 3846-3848.
[7]江志超. 鼻咽炎及相关问题研究现状[J]. 中国中西医结合耳鼻咽喉科杂志, 2005, 13(5): 297-300.
[8]MathieuC,RodbardHW,CariouB,etal.Acomparisonofaddingliraglutideversusasingledailydoseofinsulinasparttoinsulindegludecinsubjectswithtype2diabetes(BEGIN:VICTOZAADD-ON)[J].DiabetesObesMetab, 2014, 16(7): 636-644.
[9]BuseJB,RosenstockJ,SestiG,etal.Liraglutideonceadayversusexenatidetwiceadayfortype2diabetes:a26-weekrandomised,parallel-group,multinational,open-labeltrial(LEAD-6)[J].Lancet, 2009, 374(9683): 39-47.
[10]KadowakiT,NambaM,YamamuraA,etal.Exenatideexhibitsdose-dependenteffectsonglycemiccontrolover12weeksinJapanesepatientswithsuboptimallycontrolledtype2diabetes[J].EndocrJ, 2009, 56(3): 415-424.
[11]BuseJB,BergenstalRM,GlassLC,etal.Useoftwice-dailyexenatideinBasalinsulin-treatedpatientswithtype2diabetes:arandomized,controlledtrial[J].AnnInternMed, 2011, 154(2): 103-112.
[12]AdesAE,SculpherM,SuttonA,etal.Bayesianmethodsforevidencesynthesisincost-effectivenessanalysis[J].Pharmacoeconomics, 2006, 24(1): 1-19.
[13]LuG,AdesAE.Combinationofdirectandindirectevidenceinmixedtreatmentcomparisons[J].StatMed, 2004, 23(20): 3105-3124.
[14]JadadAR,MooreRA,CarrollD,etal.Assessingthequalityofreportsofrandomizedclinicaltrials:isblindingnecessary?[J].ControlClinTrials, 1996, 17(1): 1-12.
[15]KeusF,WetterslevJ,GluudC,etal.Robustnessassessmentsareneededtoreducebiasinmeta-analysesthatincludezero-eventrandomizedtrials[J].AmJGastroenterol, 2009, 104(3): 546-551.
[16]PratleyRE,UrosevicD,BoldrinM,etal.Efficacyandtolerabilityoftaspoglutideversuspioglitazoneinsubjectswithtype2diabetesuncontrolledwithsulphonylureaorsulphonylurea-metformintherapy:Arandomized,double-blindstudy(T-emerge6)[J].DiabetesObesMetab, 2013, 15(3): 234-240.
[17]LeeYS,ParkMS,ChoungJS,etal.Glucagon-likepeptide-1inhibitsadiposetissuemacrophageinfiltrationandinflammationinanobesemousemodelofdiabetes[J].Diabetologia, 2012, 55(9): 2456-2468.
[18]KoderaR,ShikataK,KataokaHU,etal.Glucagon-likepeptide-1receptoragonistamelioratesrenalinjurythroughitsanti-inflammatoryactionwithoutloweringbloodglucoselevelinaratmodeloftype1diabetes[J].Diabetologia, 2011, 54(4): 965-978.
[19]BergenstalRM,WyshamC,MacconellL,etal.Efficacyandsafetyofexenatideonceweeklyversussitagliptinorpioglitazoneasanadjuncttometforminfortreatmentoftype2diabetes(DURATION-2):arandomisedtrial[J].Lancet, 2010, 376(9739): 431-439.
[20]王兴纯, 曲伸.GLP-1及其受体激动剂与炎性反应及氧化应激[J]. 国际内分泌代谢杂志, 2014, 34(4): 263-266.
[21]KendallDM,RiddleMC,RosenstockJ,etal.Effectsofexenatide(exendin-4)onglycemiccontrolover30weeksinpatientswithtype2diabetestreatedwithmetforminandasulfonylurea[J].DiabetesCare, 2005, 28(5): 1083-1091.
[22]MorettoTJ,MiltonD,RidgeTD,etal.Efficacyandtolerabilityofexenatidemonotherapyover24weeksinantidiabeticdrug-naivepatientswithtype2diabetes:arandomized,double-blind,placebo-controlled,parallel-groupstudy[J].ClinTher, 2008, 30(8): 1448-1460.
(2016-02-23收稿)
(本文编辑:赵波)
Impact of glucagon-like peptide-1 receptor agonists on nasopharyngitis and upper respiratory tract infection among patients with type 2 diabetes: a network meta-analysis
LI Zhi-xia1, WU Shan-shan2, YANG Zhi-rong3, ZHAN Si-yan1△, SUN Feng1△
(1.DepartmentofEpidemiologyandBiostatistics,PekingUniversitySchoolofPublicHealth,Beijing100191,China; 2.NationalClinicalResearchCenterforDigestiveDiseases,BeijingFriendshipHospital,CapitalMedicalUniversity,Beijing100050,China; 3.PrimaryCareUnit,UniversityofCambridge,CambridgeCB21TN,UK)
ABSTRACTObjective:To systematically review the effects of glucagon-like peptide-1 receptor agonists (GLP-1RAs) on two common respiratory system adverse events (RSAE: nasopharyngitis and upper respiratory tract infection) among type 2 diabetes (T2DM).Methods: Medline, Embase, Clinical trials and Cochrane library were searched from inception through May 2015 to identify randomized clinical trials(RCTs) assessed safety of GLP-1RAs versus placebo or other anti-diabetic drugs in T2DM. Network meta-analysis within a Bayesian framework was performed to calculate odds ratios for the incidence of RSAE. Results: In the study, 50 RCTs were included, including 13 treatments: 7 GLP-1RAs (exenatide, exenatide-long-release-agent, liraglutide, lixisenatide, taspoglutide, albiglutide and dulaglutide), placebo and 5 traditional anti-diabetic drugs(insulin, metformin, sulfonylureas, sitagliptin and thiazolidinediones ketones). Compared with insulin, taspoglutide significantly decreased the incidence of nasopharyngitis (OR=0.67, 95%CI: 0.46-0.96). Significant lowering effects on upper respiratory tract infection were found when taspoglutide versus placebo (OR=0.57, 95%CI: 0.34-0.99) and insulin (OR=0.39, 95%CI: 0.23-0.73). The result from the network meta-analysis based on Bayesian theory could be used to rank all the treatments included, which showed that taspoglutide ranked last with mi-nimum risk on nasopharyngitis and upper respiratory tract infection.Conclusion: Taspoglutide was associated with significantly lowering effect on RSAE.
KEY WORDSGlucagon-like peptide-1 receptor; Diabetes mellitus, type 2; Nasopharyngitis; Respiratory tract infections; Meta-analysis
基金项目:国家自然科学基金(81302508)资助Supported by National Natural Science Foundation of China (81302508)
Corresponding author△’s e-mail, siyan-zhan@bjmu.edu.cn, sunfeng@bjmu.edu.cn
[中图分类号]R587.1
[文献标志码]A
[文章编号]1671-167X(2016)03-0454-06
doi:10.3969/j.issn.1671-167X.2016.03.014
网络出版时间:2016-5-2710:36:47网络出版地址:http://www.cnki.net/kcms/detail/11.4691.R.20160527.1036.012.html

