葡萄糖醛酸制备工艺中的糖化及发酵条件研究
王丽萍,李 祥,师春兰,彭西峰(.陕西科技大学化学与化工学院,陕西西安700;.九江学院,江西九江33005)
葡萄糖醛酸制备工艺中的糖化及发酵条件研究
王丽萍1,李 祥1,师春兰1,彭西峰2
(1.陕西科技大学化学与化工学院,陕西西安710021;2.九江学院,江西九江332005)
以氧化淀粉为原料,采用酶解和发酵工艺来制备葡萄糖醛酸,以糖化液和发酵液中葡萄糖醛酸含量为评价指标,研究了葡萄糖醛酸制备工艺中的糖化条件、发酵条件。结果表明:糖化的最佳条件为:75 g氧化淀粉中加入2 mL糖化酶,在温度为55℃下反应12 h时,糖化液中的葡萄糖醛酸最高达7.79%;发酵的最佳条件为:25 mL糖化液中加2.0 g酵母粉,在35℃的水浴中发酵4 d时发酵液中的葡萄糖醛酸含量最高达28.03%。该研究为高含量葡萄糖醛酸的制备及其变性淀粉的应用提供了理论指导。
氧化淀粉,糖化,发酵,葡萄糖醛酸
1 材料与方法
1.1 材料与仪器
氧化淀粉 自制;氢氧化钠、盐酸、浓硫酸、四硼酸钠、3,5-二硝基水杨酸、丙三醇、葡萄糖、间羟基联苯、葡萄糖醛酸标准品 均为分析纯,购于西安化学试剂公司;安琪酿酒活性干酵母 购于安琪酵母股份有限公司;淀粉酶(20000 U·mL-1)、糖化酶(10000 U·mL-1) 均购于开封东大化工有限责任公司。
D60-2F型电动搅拌机 杭州仪表电机厂;HH-2型数显恒温水浴锅 国华电器有限公司;PB-10型酸度计 北京赛多利斯仪器系统有限公司;7230 G型分光光度计 上海科技仪器有限公司制造;NDJ-5S型数字旋转粘度计 上海地学仪器研究所。
1.2 实验方法
1.2.1 葡萄糖醛酸的测定
1.2.1.1 葡萄糖醛酸标准曲线的绘制 称取0.1 g葡萄糖醛酸标准品置于100 mL容量瓶中,加水定容,配制1.00 mg/mL的葡萄糖醛酸标准液。取上述标准液0.1、0.2、0.3、0.4、0.5、0.6、0.7 mL分别置于10 mL的具塞试管中,在冰水浴中加入5 mL四硼酸钠/硫酸溶液,摇匀,在沸水浴中加热5 min后冷却,将试管置于冰水浴中,用微量移液器加入1.5 mg/mL的间羟基联苯100 μL,盖上塞子摇匀,以1 mL蒸馏水做空白,在520 nm处测定吸光度,以标准葡萄糖醛酸的质量浓度c(mg/mL)为横坐标,吸光度为纵坐标,绘制标准曲线。
1.2.1.2 糖化液、发酵液中葡萄糖醛酸含量的测定取糖化液、发酵液各0.5 mL,稀释500倍,吸取1 mL置于10 mL具塞试管中,按上述方法处理,在520 nm处测定糖化液、发酵液的吸光度,再根据葡萄糖醛酸标准曲线得出糖化液、发酵液中葡萄糖醛酸的含量。
1.2.2 时间因素:疾病从开始到进展恶化或缓解是一个动态的过程,每一阶段有不同的表现。而医务人员可能在疾病的某个阶段接触患者,因此并没有机会了解疾病的全过程。在某个时间节点,有些重要的有诊断意义的证据可能尚未出现或已经消失。例如哮喘的病情有明显的可逆性和可变性,1例青年学生患哮喘,急性发作时气急明显且有惊恐烦躁等精神症状。在发作后到医院检查,两肺未闻罗音,肺功能检查正常。一度误诊为“神经官能症”。
1.2.2 糖化阶段实验条件的确定
1.2.2.1 糖化温度对葡萄糖醛酸含量的影响 分别称取75.0 g的氧化淀粉五份,加150 mL水调制成淀粉乳,置于250 mL三口瓶中,用NaOH调节体系pH6.5,分别加入12 mL α-淀粉酶,在85℃下水解1 h后,各加入糖化酶2 mL,再调节pH4.5,按编号依次在40、45、50、55、60℃下糖化12 h,研究糖化温度对葡萄糖醛酸含量的影响。
1.2.2.2 糖化酶添加量对葡萄糖醛酸含量的影响分别称取75.0 g的氧化淀粉五份,加150 mL水调制成淀粉乳,置于250 mL三口瓶中,用NaOH调节体系pH6.5,分别加入12 mL α-淀粉酶,在85℃下水解1 h后,调节pH4.5,按编号分别加入0.5、1.0、1.5、2.0、2.5 mL的糖化酶,置于55℃水浴中反应12 h,研究糖化酶加量对葡萄糖醛酸含量的影响。
1.2.2.3 糖化时间对葡萄糖醛酸含量的影响 称取75.0 g的氧化淀粉8份,加150 mL水调制成淀粉乳,置于250 mL三口瓶中,用NaOH调节体系pH6.5,分别加入12 mL α-淀粉酶,在85℃下水解1 h后,调节体系pH4.5,加入2.0 mL糖化酶,在55℃下按编号依次糖化6、7、8、9、10、11、12、13 h,研究糖化时间对葡萄糖醛酸含量的影响。
1.2.3 发酵阶段实验条件的确定
1.2.3.1 酵母粉的添加量对葡萄糖醛酸含量的影响称取氧化淀粉150 g,加300 mL蒸馏水调制成淀粉乳,在85℃下加入24 mL α-淀粉酶,水解1 h后,调节体系pH4.5,加入4.0 mL糖化酶,在55℃下糖化12 h,取25 mL糖化液五份分别置于5个100 mL锥形瓶中,调节体系pH4.3,按编号依次加入酵母粉0.5、1.0、1.5、2.0、2.5 g,用棉花塞紧瓶口,在35℃水浴温度下静置发酵4 d,考察酵母粉加量对葡萄糖醛酸含量的影响。
1.2.3.2 发酵温度对葡萄糖醛酸含量的影响 称取氧化淀粉150 g加水调制成淀粉乳,在85℃下加入24 mL α-淀粉酶水解1 h后,调节体系pH4.5,加入4.0 mL糖化酶,在55℃下糖化12 h,取25 mL糖化液七份分别置于7个100 mL锥形瓶中,调节体系pH4.3,分别加入2.0 g的酵母粉,按编号在20、25、30、32、35、40、45℃的水浴中发酵4 d,研究发酵温度与葡萄糖醛酸含量的关系。
1.2.3.3 发酵时间对葡萄糖醛酸含量的影响 称取氧化淀粉150 g加水调制成淀粉乳,在85℃下加入24 mL α-淀粉酶水解1 h后,调节体系pH4.5,加入4.0 mL糖化酶,在55℃下糖化12 h,取25 mL糖化液六份分别置于6个100 mL锥形瓶中,调节体系pH4.3,分别加入2.0 g的酵母粉,在35℃的水浴中按编号发酵2、2.5、3、3.5、4、4.5 d,研究发酵时间对葡萄糖醛酸含量的影响。
1.2.4 红外谱图表征 分别配制质量浓度为1×10-2mg/mL的葡萄糖醛酸标准溶液、糖化液和发酵液,采用傅里叶变换红外光谱仪进行红外检测。
2 结果与讨论
2.1 葡萄糖醛酸标准曲线的制作
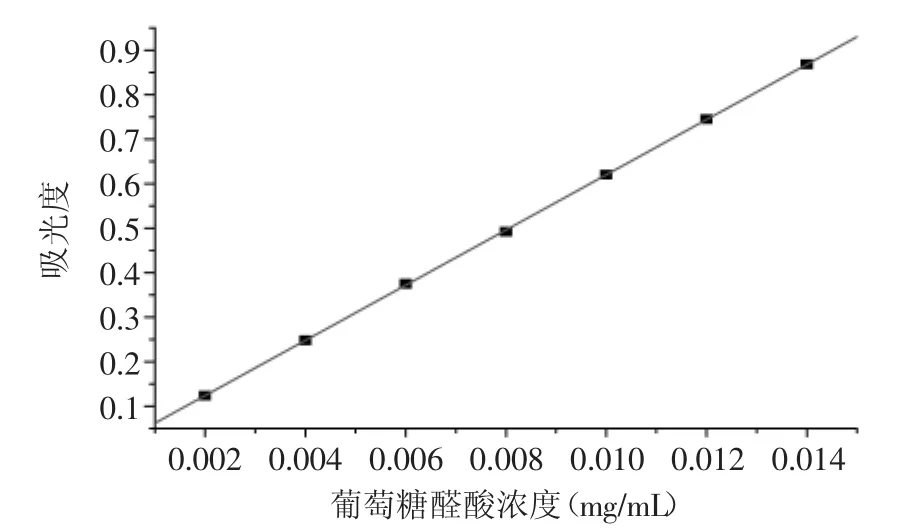
图1 葡萄糖醛酸标准曲线Fig.1 Standard curve of glucuronic acid
以葡萄糖醛酸浓度(mg/mL)为横坐标,吸光度为纵坐标绘制葡萄糖醛酸标准曲线,见图1,回归方程为:y=6.08929x+0.11286,R2=0.99966,线性关系良好。据此推导得到糖化液、发酵液中葡萄糖醛酸含量计算公式ω(%)=(y-0.11286)/6.08929×6.1×250/m,式中:m为所取的糖化液或者发酵液的质量。
2.2 糖化条件的确定
2.2.1 糖化温度对葡萄糖醛酸含量的影响 从图2可以看出,当低于55℃时,随着温度的增加,葡萄糖醛酸含量也增加,而当温度超过55℃时葡萄糖醛酸含量急剧下降。糖化酶是一种外切型淀粉酶,系统名称为α-1,4葡聚糖葡萄糖水解酶,除了能从淀粉分子的非还原性末端切开α-1,4糖苷键之外,也能切开α-1,6糖苷键[6]。一般来说,糖化酶最适作用是50~60℃,低温下酶的活性比较低,温度过高酶也会因为蛋白变性而失活,所以该实验选择55℃为糖化酶的最适温度。

图2 糖化温度对葡萄糖醛酸含量的影响Fig.2 The effect of saccharifying temperature on content of glucuronic acid
2.2.2 糖化酶添加量对葡萄糖醛酸含量的影响 由图3可以看出,在糖化酶较少时,糖化酶加量对葡萄糖醛酸的影响较大,而超过2.0 mL时葡萄糖醛酸的增加不太明显。酶的添加量直接影响到酶促反应的效率,但在底物一定的情况下,过量的糖化酶并不会加快糖化速率,综合考虑糖化酶的最佳量为2.0 mL。
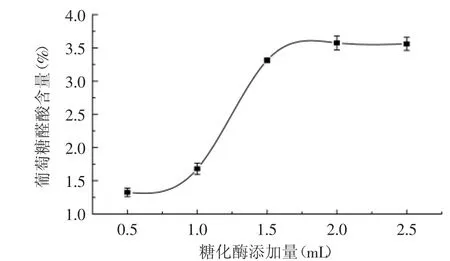
图3 糖化酶添加量对葡萄糖醛酸含量的影响Fig.3 The effect of glucoamylase dose on content of glucuronic acid
2.2.3 糖化时间对葡萄糖醛酸含量的影响 从图4可以看出,糖化酶在作用12 h时葡萄糖醛酸含量基本保持不变,糖化酶水解淀粉和较大分子的低聚糖时属于单链式水解,即完成一个分子的水解以后,再水解另一个分子,但水解较小分子的低聚糖时属于多链式,即水解一个分子几次后脱离,再水解另一个分子。本实验是先将氧化淀粉用α-淀粉酶作用一定的时间再用糖化酶水解,理论上,糖化酶会将淀粉单链试水解至完全,但实际上糖化酶水解α-1,4糖苷键的速度随底物相对分子质量的下降而降低,从图4中可得出选择糖化12 h为最佳时间。
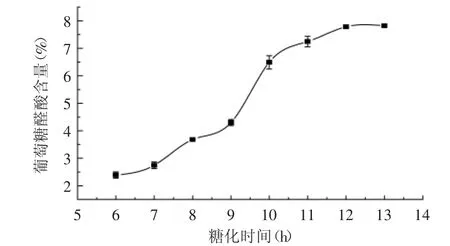
图4 糖化时间对葡萄糖醛酸的影响Fig.4 The effect of saccharifying time on content of glucuronic acid
2.3 发酵条件的确定
2.3.1 酵母粉的加量对葡萄糖醛酸含量的影响 从图5可以看出,随着酵母粉的增加,葡萄糖醛酸含量也急剧增加,当酵母粉的加量超过2.0 g后,葡醛酸的增加量就不太明显。酵母粉是酵母细胞没有经过自溶而直接压滤干燥粉碎后的产物,含有大量的完整的酵母细胞[7]。糖化液中的葡萄糖经EMP途径形成了丙酮酸,在无氧条件下,酵母细胞中的丙酮酸脱羧酶氧化丙酮酸脱羧形成乙醛和二氧化碳,乙醛在乙醇脱氢酶的作用下又可以被NADH还原成乙醇[8],酵母粉的添加量直接影响发酵除糖的效果。酵母粉增加,发酵液中葡萄糖量减少,而葡萄糖醛酸量相对增加,由图5可以得出,酵母粉的最佳添加量为2.0 g。

图5 酵母粉量对葡萄糖醛酸的影响Fig.5 The effect of yeast dosage on content of glucuronic acid
2.3.2 温度对发酵过程的影响 从图6可以看出,发酵液中的葡萄糖醛酸含量随着发酵温度的增加呈先增加后下降的趋势,在35℃时含量最高,所以选择酵母粉最佳发酵温度为35℃。

图6 发酵温度对葡萄糖醛酸含量的影响Fig.6 The effect of fermentation temperature on glucuronic acid content
2.3.3 发酵时间对葡萄糖醛酸含量的影响 从图7可以看出,随着发酵天数的增加,葡萄糖醛酸含量逐渐增加,到超过4 d的时候,葡醛酸含量基本保持不变。这是因为在酵母粉存在的条件下,发酵液中的葡萄糖逐渐发酵形成乙醇,在发酵液一定量的情况下,随着葡萄糖含量的减少,葡萄糖醛酸的含量相对逐渐增加,在发酵4 d之后,葡萄糖醛酸含量变化不明显,说明葡萄糖基本发酵除去。所以最佳发酵时间为4 d。
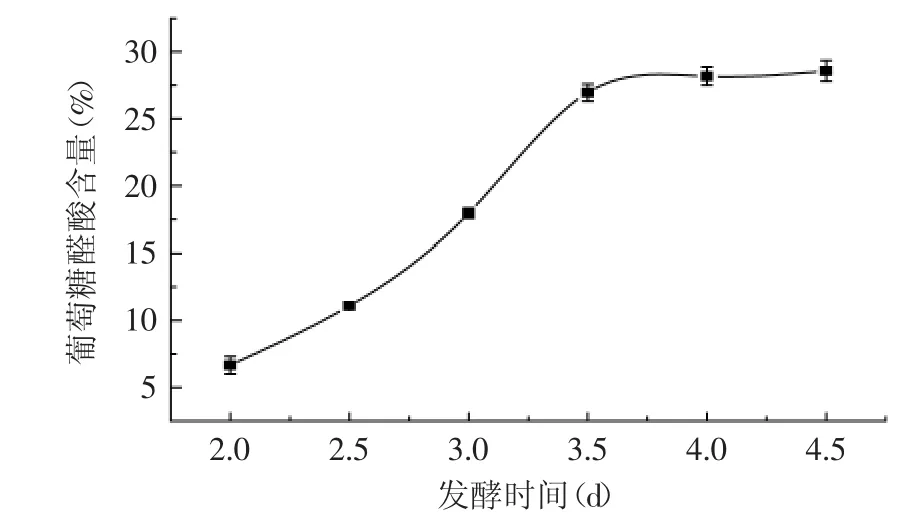
图7 发酵时间对葡萄糖醛酸含量的影响Fig.7 The effect of fermentation time on content of glucuronic acid
2.3 发酵液的红外谱图表征及分析
图8为葡萄糖醛酸标准品、糖化液、发酵液的红外谱图,从图8中可以看出,糖化液、发酵液和葡萄糖醛酸标准品在3400、1700、1100 cm-1处有明显的吸收峰,3400 cm-1为O-H的伸缩振动峰,1700 cm-1为醛类中的C=O伸缩振动峰,说明糖化液和发酵液中均含有葡萄糖醛酸。
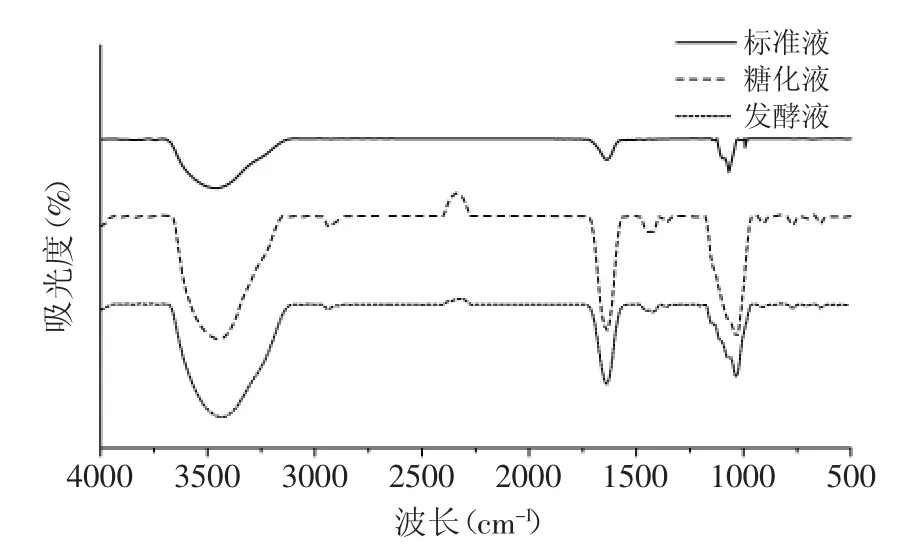
图8 红外谱图Fig.8 FT-IR spectra
3 结论
实验结果表明:在葡萄糖醛酸前期制备工艺一定的情况下,糖化酶作用的最佳条件是:75 g氧化淀粉中加入2 mL糖化酶,在温度为55℃时反应12 h,得到水解液的葡萄糖醛酸含量为7.79%。最佳发酵条件为:25 mL糖化液中加2.0 g酵母粉,在35℃的水浴中发酵4 d,得到的发酵液的葡萄糖醛酸含量为28.03%。本实验在糖化酶和酵母粉的条件下,通过研究水解和发酵阶段中各个单因素的影响,得到葡萄糖醛酸含量较高的水解液及其发酵液,为后续葡萄糖醛酸的制备提供了一定的理论指导。
[1]马彦,赵林,刘华庆,等.淀粉及其衍生物催氧化制备葡萄糖醛酸研究进展[J].应用化工,2011,40(7):1244-1247.
[2]周红,王怡宁,潘志权,等.非均相催化氧化合成葡萄糖醛酸及内酯的研究进展[J].武汉工程大学学报,2012,34(4):1-5.
[3]Ruud ter Haar,Johan W Timmermans,Ted M Slaghek.TEMPO Oxidation of Gelatinized Potato Starch Results in Acid Resistant Blocks of Glucuronic Acid Moieties[J].Carbohydr Polym,2010,81:830-838.
[4]范艳群,许建中,徐询,等.离子排斥色谱法同时测定葡萄糖醛酸和内酯及葡萄糖醛酸稳定性[J].应用化学,2014,31(4):450-453.
[5]李祥,赵倩,张青,等.葡萄糖醛酸内酯清洁生产关键技术[J].中国酿造,2011(12):151-154.
[6]李娜.玉米淀粉糖生产工艺改进研究[D].济南:齐鲁工业大学,2014.
[7]司马迎春.酵母粉的作用及氮源对bacillus subtilis 24/PMX45核黄素发酵的影响[D].天津:天津大学,2004.
[8]房媛.葡萄糖醛酸内酯清洁生产[D].西安:陕西科技大学,2013.
Study of saccharification and fermentation conditions in the process of glucuronic acid preparation
WANG Li-ping1,LI Xiang1,SHI Chun-lan1,PENG Xi-feng2
(1.College of Chemistry and Chemical Engineering,Shaanxi University of Science and Technology,Xi'an 710021,China;2.Jiujiang College,Jiujiang 332005,China)
Using the oxidation starch as raw material,the glucuronic acid was obtained by the processes of saccharification and fermentation.The conditions of saccharifying enzyme reaction and the yeast fermentation was studied,and the glucuronic acid of saccharification liquid and fermented liquid was regarded as evaluation standard.The results showed that the optimal conditions of saccharifing were as follows:reaction at 55℃ for 12 h and amount of saccharifying enzyme was 1 mL in the 75 g of oxidation starch.The optimal conditions of fermentation were 25 mL saccharification liquid with 2.0 g yeast,temperature of 35℃ for 4 d.The research provided the theoretical guidance for the preparation of high content of glucuronic acid and the application of oxidized starch.
oxidation starch;saccharification;fermentation;glucuronic acid
TS236.9
B
1002-0306(2016)06-0260-04
10.13386/j.issn1002-0306.2016.06.045
2015-06-10
王丽萍(1989-),女,硕士研究生,研究方向:天然产物化学,E-mail:389173363@qq.com。
西安市科技局项目(CXY1434(2));未央区科技局项目(201411);江西省自然科学基金(ZBBF60011)。
——α-葡萄糖醛酸酶的研究进展*

