不对称Strecker反应催化剂的研究进展
纵朝阳, 孙雅泉
(1. 南京工业大学,江苏 南京 210000; 2. 盐城师范学院 药学院,江苏 盐城 224051;3. 大丰盐师院海洋生物制药科技有限公司,江苏 大丰 224100)
·综合评述·
不对称Strecker反应催化剂的研究进展
纵朝阳1, 孙雅泉2,3*
(1. 南京工业大学,江苏 南京 210000; 2. 盐城师范学院 药学院,江苏 盐城 224051;3. 大丰盐师院海洋生物制药科技有限公司,江苏 大丰 224100)
综述了不对称Strecker反应催化剂的研究进展,重点介绍了金属配合物催化剂、固体酸催化剂、有机小分子手性催化剂、路易斯酸和Brønsted酸催化剂在不对称Strecker反应中的应用。并对其未来发展进行了展望。参考文献44篇。
不对称Strecker反应; 催化剂;α-氨基氰; 综述
α-氨基酸是组成蛋白质、多肽及药物的重要模块,而不对称Strecker反应是合成手性α-氨基酸衍生物的主要途径之一。1998年以前,不对称Strecker反应几乎无人问津[1],但是最近几年却成为研究热点,许多新的催化体系被探索出来,成为发展较快的不对称催化反应之一。研究更加高效、绿色及立体选择性催化剂已成为近年的研究热点,近年来报道的催化不对称Strecker反应的催化剂主要有五类:金属配合物催化剂、固体酸催化剂和有机小分子手性催化剂、路易斯酸和Brønsted酸催化剂。
本文重点综述了近五年不对称Strecker反应催化剂的新进展,主要对该类反应中新出现的高效催化剂进行介绍,并对其未来发展进行了展望。
1 金属配合物催化剂
金属配合物在不对称氢化、不对称环丙烷化、不对称环氧化等不对称合成中都可作为催化剂[2],其对于不对称Strecker反应的催化近几年也成为化学家探索的一个方向。
Salen金属配合物已被成功用于众多不对称反应,取得了极大的成功。Saravanan等[3]合成了一种具有手性的双核大环Salan金属聚合物催化剂催化醛亚胺和KCN的Strecker反应。在-20 ℃条件下,对不同的N-苄基亚胺和KCN或TMSCN的不对称加成反应具有较高收率(91%)。实验表明,它还具有较高的对映选择性(ee>99%),并且对于有机和无机氰化物均具有良好的催化活性。2014年,Hou等[4]通过溶剂热反应合成了一种Cu(I)/Cu(II)-salan配位高聚物(CP1),该催化剂对于三组分Strecker反应具有突出的双金属催化活性而且可以在可见光照明下可以降解有机染料。
Esteves等[5]以钒或铝共价键连接Salan配合物固定在不同树脂上,合成了四个新的Salen型金属配合物催化剂,并将其催化Strecker反应(Scheme 1)。结果表明:钒(V)异构催化剂比铝异构催化剂更有效;钒(V)的异构催化剂类似于未异构配合物(催化剂10 mol%,于-40 ℃反应4 h),而其对映体与相应均相催化剂相比活性却下降。
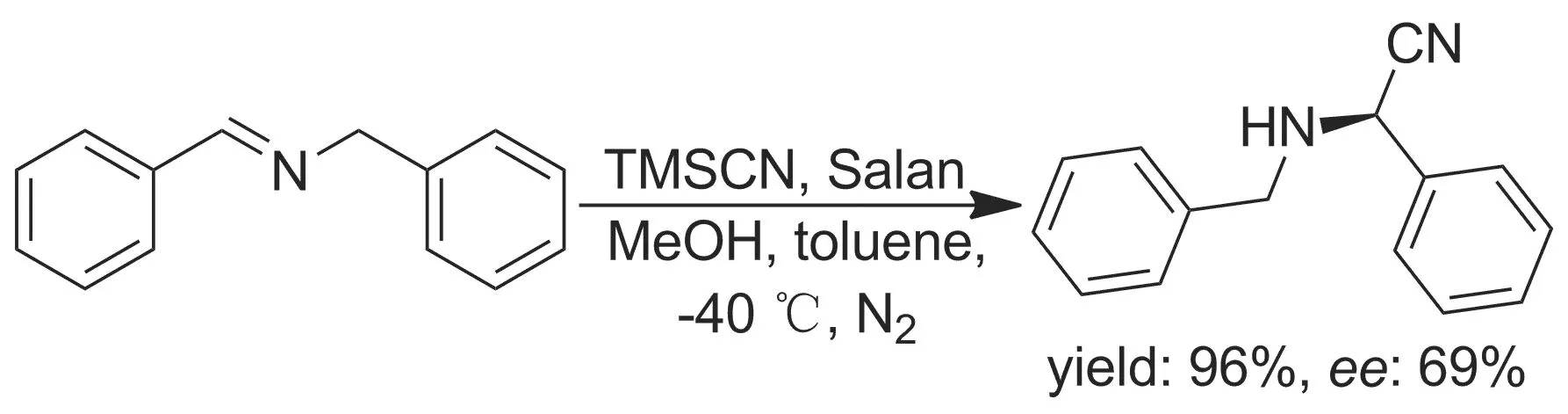
Scheme 1
2 固体酸催化剂
近期,固体酸催化剂以其廉价易得、无毒及对水和空气比较稳定等特点而受到重视,并应用于多种有机合成反应中,获得了良好的效果。
陈巍等[6]采用一种含有磺酸基团的高度交联的多酚类聚合物-木质素磺酸,其主要来源于造纸工业的副产物(造纸黑液)。近年来,木质素磺酸已经成为生物质领域研究的热点,它作为一种绿色可回收的固体酸催化剂在无溶剂条件下可以催化Strecker反应。实验表明,该催化剂能够多次循环使用并且催化活性没有明显降低,具有很好的工业应用前景。
固体催化剂钨磺酸已被应用于多种反应,且效果良好。2013年,陆军等[7]以固体酸催化剂钨磺酸为催化剂,以醛、胺(伯胺、仲胺) 和三甲基氰硅烷(TMSCN)顺利地进行了Strecker反应(Scheme 2),高收率地获得了相应的α-氰基化合物,收率高达91%。该合成方法原料易得,反应条件温和,反应迅速,后处理简单方便,易于操作,且催化剂钨磺酸能够高活性地循环使用。
Mobaraki等[8]制备了一种固体磺酸催化剂S-3CR,该催化剂以Fe3O4为核心、SiO2为外壳的磁性纳米技术相结合制备。在Strecker反应中具有疏水性、高效的传质性和催化活性等优点。该催化剂很容易地被一个外部磁铁分离,回收的催化剂可以循环使用6次以上,并且没有活性损失。催化剂的回收方法:混合液用乙酸乙酯稀释之后,利用磁倾析的方法分离催化剂。
Derikvand等[9]采用一种高效且可重复使用的固体酸催化剂纳米Zr-MCM-41催化Strecker反应合成一种新的氨基腈。实验结果证明,此催化剂具有高收率(84%~95%)和绿色环保等优点,并介绍了一种简单方便的方法合成与表征Zr-MCM-41催化剂,并且比较了不同种类的胺醛在此催化剂的催化作用下的反应时间、收率,发现作用时间4.5 h,效率最高可达98%。
Dekamin等[10]采用一种固体酸催化剂纳米体系的有序介孔硅硼(B-MCM-41)催化Strecker反应得到α-氨基腈。此催化剂的优点是作用条件温和(室温)、收率高、反应时间短。B-MCM-41表现出比Fe(III)改性的MCM-41(Fe-MCM-41)较高的催化活性。实验表明使用B-MCM-41催化剂可以回收至少4次,且无明显催化活性丧失。
2014年,Wang等[11]发现一种以八面体分子筛铝PKU-1作为固体酸催化剂催化Strecker反应(Scheme 3)。PKU-1是一种高效快捷、在温和的反应条件下合成亚胺和TMSCN氨基腈的固体酸催化剂。
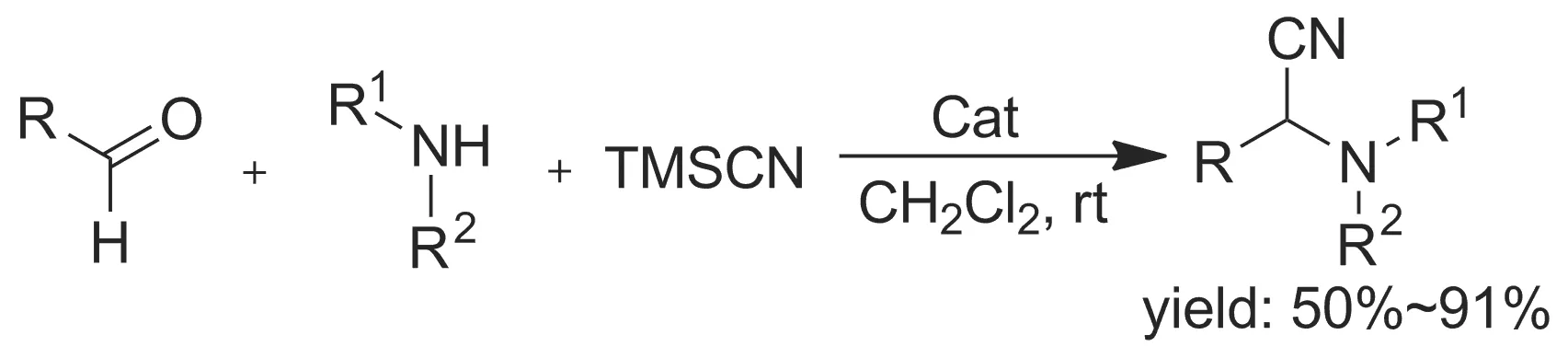
Scheme 2
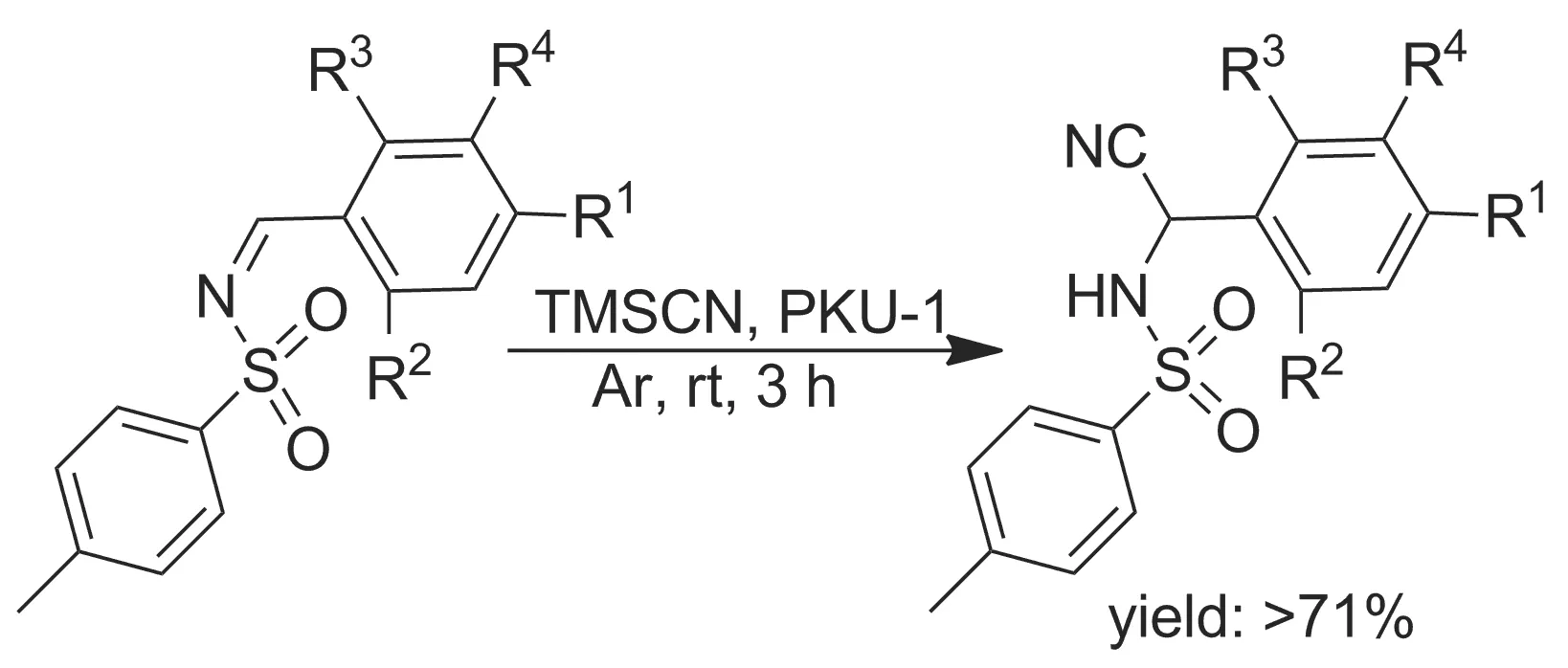
Scheme 3
该催化剂中催化活性位点与18环结构通道中的羟基基团有关。实验发现PKU-1中既有布朗酸的位点也有路易斯酸位点,因此是一种高效的固体酸催化剂。
2015年,Chen等[12]发现了一种新的多微孔分子筛硼铝酸盐催化剂PKU-3,由酸性硼酸通量的方法制得。PKU-3的结构是混合同步旋转电子衍射和X-射线粉末衍射得出的,其组成和晶体结构分析表明,PKU-3有两个质子和氯离子通道,这些质子和氯离子可以通过基本的方法被清洗掉从而可以活化这些打开的孔道。实验结果表明其收率高于90%,为一种高效的固体酸催化剂。
Fatemeh等[13]使用不同介孔材料上负载高活性与稳定性的钴(II)配合物,制得Co/SBA-15, Co/HMS, Co/silica和Co/MCM-41。在无溶剂中,使用1 mol%Co/SBA-15催化剂催化三组分Strecker反应,反应时间1~5 h,收率大于90%。而且他们分别比较了室温与低温微波条件下,催化剂的活性。最后得出结论,催化剂可重复使用至少10次以上而不损失催化剂的活性;微波加热比室温下反应得到的收率更高;Co/silica比其他的催化剂作用效果更突出。
Mohammad等[14]使用介孔材料MCM-41负载在磺酸上,制备了一种在温和条件下使用的环保、高效,可重复使用的催化剂MCM-41-SO3H催化Strecker反应。反应时间50~250 min,收率85%~98%,并比较了在不同溶剂下以及无溶剂下催化剂的催化效果,得出在乙醇溶剂下反应效果最好并说明了原因。
3 手性有机小分子催化剂
最近不含金属的低分子量手性有机小分子催化的不对称合成反应得到了突飞猛进的发展。有机小分子催化剂与过渡金属催化剂相比,具有无毒无害、价廉易得、反应体系无重金属残留、易于修饰与负载等特点,符合当前大力提倡的绿色化学的要求。目前已发展成为继酶和手性过渡金属催化剂之外的又一类重要的手性催化剂,有机催化的不对称合成反应已成为国内外研究最为活跃的领域之一[15]。催化不对称Strecker 反应的有机催化剂主要有金鸡钠碱类衍生物、手性(硫)脲衍生物、氮-氧偶极化合物等取得了良好的催化活性和对映选择性。
金鸡纳碱及其部分衍生物作为手性相转移催化剂和手性非相转移催化剂在不对称合成中的应用已取得了重大成就[16]。何海晓等[17]在方酰胺催化亚胺与三甲基硅氰的不对称Strecker反应研究中利用金鸡纳碱基的芳酰胺催化剂含苯并噻唑结构单元的亚胺与三甲基硅氰的不对称Strecker反应(Scheme 4),以较高收率(99%)和对映选择性(98%)获得含有该类含噻唑杂环的手性α-氨基氰化合物。所合成的该类化合物可高收率高对映选择性地转化为咪唑烷酮类化合物。
李乃凯[18]以金鸡纳碱奎宁衍生的硫脲为活化剂兼催化剂(Chart 1),以吡唑烷酮与醛缩合而成的内盐式环状腙为底物,合成了一系列多功能催化剂,并将其用于不对称Strecker反应中,分别考察了催化剂种类、催化剂用量、反应溶剂、反应温度及添加剂对反应收率的影响,最后以几乎定量的收率(>87%)和最高为97%的对映选择性获得了目标化合物,成功实现了环状腙的不对称Strecker反应。
刘运林[19]利用奎宁衍生的新型手性叔胺-次磷酸胺双功能催化剂(Chart 1),首次尝试了N-芳基取代靛红亚胺与TMSCN的Strecker不对称反应,最高取得71%的对映选择性。他们还利用辛可宁定衍生的硫脲180为催化剂,实现了首例TMSCN与N-Boc靛红亚胺的氰化反应,极大地改善了反应收率及对映选择性。该方法条件温和、底物普适性广,并且产物可以方便地转化成光学活性的α-季碳氨基酸。
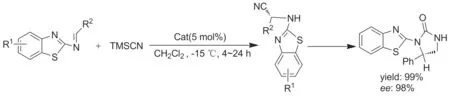
Scheme 4
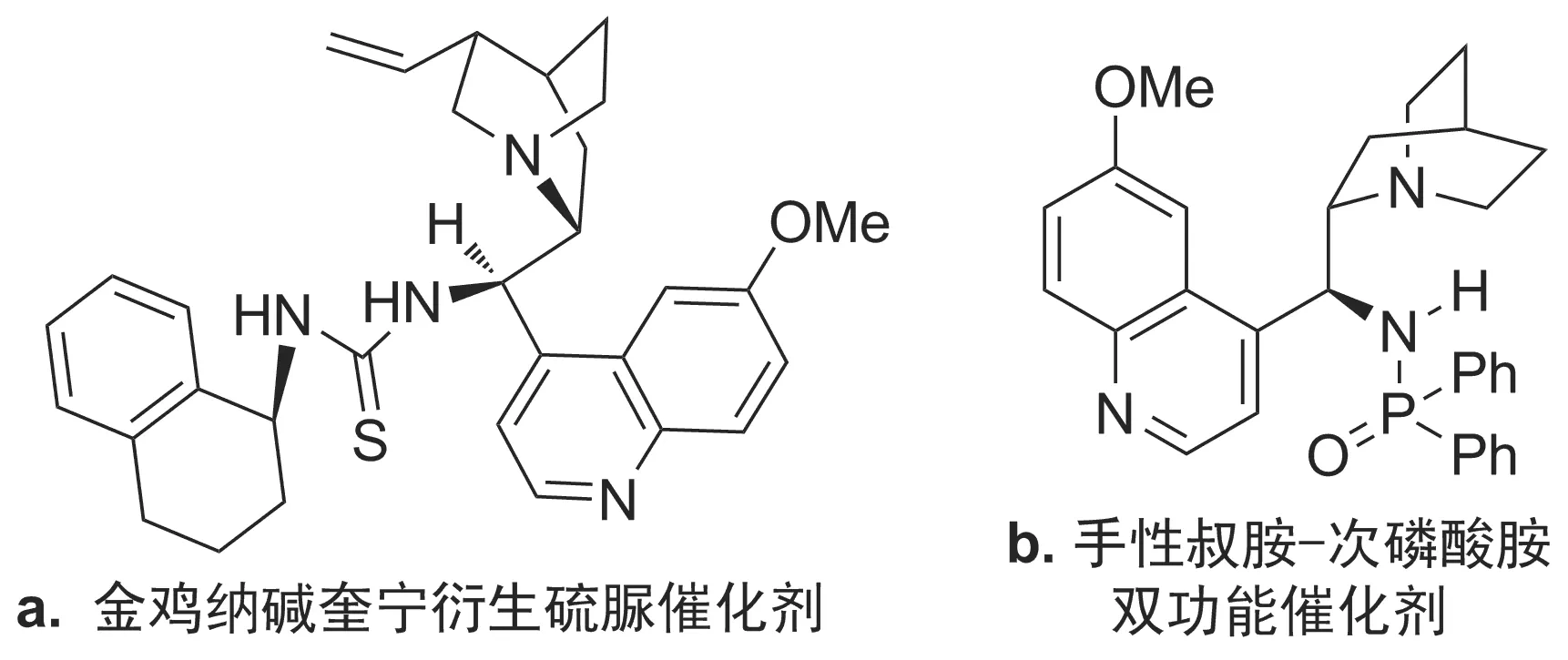
Chart 1
Scheme 5
Xie等[20]研究了一种有机小分子催化剂金鸡纳碱及环己二胺衍生的手性硫脲叔胺催化剂催化环酮亚胺类的不对称Strecker反应。反应温度为-78 ℃,二氯甲烷作溶剂,使用10 mol%的催化剂,收率最高达到98%,对映选择性最高为97%。他们考察了当三氟甲基被苯基、4-三氟甲基苯基及甲基分别取代后的四类环酮亚胺,并且比较了它们在相同条件下催化所得到的α-氨基腈收率及ee值,结果表明手性三氟甲基酮具有高收率与高选择性。
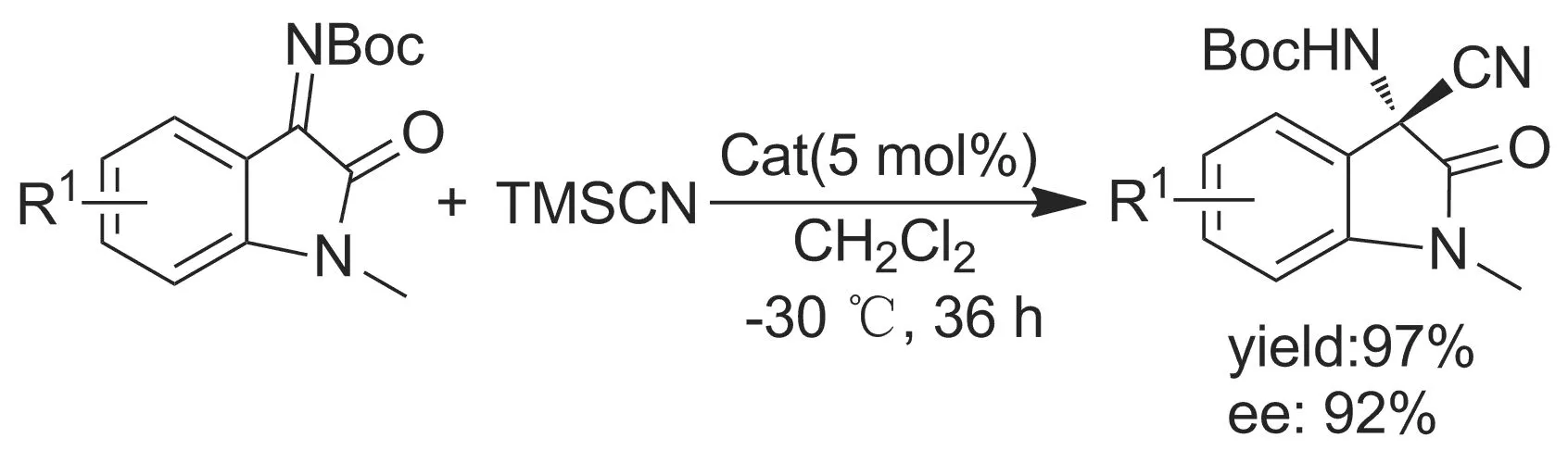
Chauhan等[21]论述了具有光学活性的有机小分子催化剂催化合成手性的3-氨基2-氧化吲哚类催化Strecker反应。该反应使用10 mol%催化剂,以二氯甲烷为溶剂,于-70 ℃反应48~96 h,收率81%~95%,对映选择性90%~99%。
2012年,Wang等[22]报道了靛红亚胺类有机小分子催化剂催化Strecker反应。2013年他们[21]又研究了金鸡纳碱硫脲II介导的多吲哚醌亚胺化催化Strecker反应,首次使用含有叔丁氧基的酮亚胺和三甲基氰化硅的不对称加成合成了高选择性的α-氨基氰,并取得了很高的收率(81%~97%)(Scheme 5);作者也采用辛可宁衍生的硫脲为催化剂也具有很好的对映选择性(ee>90%)。
Dariush等[24]研究出一种高效环保的脱氢抗坏血酸酸DHAA覆盖的磁性纳米颗Fe3O4(DHAA-Fe3O4)催化不对称Strecker反应。在乙醇中反应,当DHAA-Fe3O4用量为0.9 mol%时,反应在15 min后完成且收率为90%,并且可以重复使用6次以上而活性稍微减弱。
Kiasat等[25]发现了一种高效可回收的纳米结构催化剂Al2O3催化Strecker反应。在无溶剂存在下,该催化剂所需反应时间25 min,收率可达94%,符合绿色化学的要求。
4 路易斯酸催化剂
路易斯酸催化剂有极高的耐热性和耐氧化还原性,水相有机相均可催化,因温和、环境友好、可循环使用等特点而受到广泛关注。近年来利用路易斯酸催化多组分化学反应已经成为绿色化学的重要手段之一。
Dhanasekaran等[26]采用一种修饰后的路易斯酸催化剂Zn(OTf)2和In(OTf)3催化Strecker-内酰胺化反应合成了异吲哚酮、异喹啉酮等药物(Scheme 6)。该反应具有反应条件温和且收率高等优点。
郑勤[27]研究了无溶剂条件下碘化镁能有效催化醛或酮、胺与三甲基氰化硅(TMSCN)之间的硅腈化反应,取得了很好的反应收率。考察了影响该催化反应的各种因素,对比不同卤化镁催化剂的活性差异,各种醛(酮)底物的催化活性,包括具有不同取代电子效应的芳香醛(酮)、脂肪醛(酮)、不饱和醛(酮)等。
Bruina等[28]通过不对称Strecker反应对映选择性地合成了两个药物,比较了几种路易斯酸催化剂Sc(OTf)3, TBA-Ac和CsF用以降低这两种药物的非对映异构体的比例。结果发现,在-50 ℃, DMF为溶剂、CsF作催化剂时,收率98%且非对映异构体的比例最低为48%。
杨璐[29]论证了化合物Zn-MOF在其内表面拥有高浓度的路易斯酸Zn(II)位点,可以催化芳香醛亚胺的Strecker反应并且具有较高的收率。与此同时,作为路易斯碱位点的甲氧基中氧原子的存在有效激活了TMSCN。动力学结果显示,加入26 mol%该催化剂,2-苄胺-2-苯乙腈的Strecker反应在48 h后转化率即可达到100%。
Liu等[30]采用多孔和强大的镧系金属有机硼框架作为耐水路易斯酸催化剂(Ln-MOFs)催化Strecker反应。比较了在不同溶剂中用Ln-MOFs催化的收率以及NdCl3和H3L催化与Ln-MOFs催化的差距。结果表明:在水溶剂下,Ln-MOFs催化效率最高,且收率最高可达99%。

Scheme 6
Scheme 7
Aguirre-Díaz等[31]通过特定选择的金属离子的比例来建立有机金属框架催化剂(MOFs)在Strecker反应中的催化活性。他们制备了一种Ga和In结合的催化剂[InxGa1-x(O2C2H4)0.5(hfipbb)],该催化剂催化收率99%。并且解释了这种非均相催化剂在Strecker反应中不同反应阶段的反应机理。2014年,Xia[32]采用铟金属有机框架(MOFs)的路易斯酸高性能异构催化剂催化醛亚胺与TMSCN的反应得到一系列氨基酸衍生物。此外,经核磁共振证实,暴露的醚基(路易斯酸中的结构)对MOF可激活硅腈的孔壁,形成高价硅酸盐中间体。
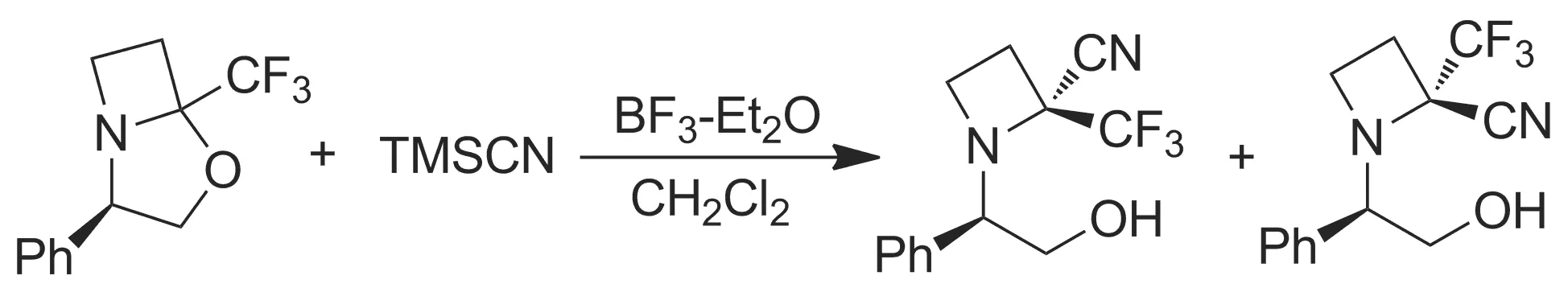
Meyer[33]在研究三氟甲基氮杂环化合物的生物活性时,采用Strecker反应在BF3-Et2O做催化剂,二氯甲烷为溶剂合成了一种具有手性的α-氨基氰(Scheme 7)。
2012年,Prakash等[34]研究了一种对于酮Strecker反应新的有效的“绿色”路易斯酸催化剂全氟磺酸-铁(Nafion-Fe)。该催化剂分别用于苯甲醛与苯胺、酮与苯胺、2-丁酮与苯胺以及微波促进下的Strecker反应。当催化剂催化苯甲醛与苯胺的反应时,溶剂为二氯甲烷,温度60 ℃,反应时间4 h,收率最高达到95%。催化剂重复利用7次以上而活性丝毫没有降低。实验表明微波无溶剂条件下,Strecker反应在常见的脂肪胺中顺利进行且该方法缩短了反应时间,提高产量和减少形成副产品。
2015年,Bigler等[35]采用手性的路易斯酸催化剂[Fe(MeCN)2](BF4)2催化不对称Strecker反应,在CH2Cl2溶剂中于-25 ℃反应1.5 h,收率90%。作者还比较了几种配体的活性和解释了甲亚胺在不对称Strecker反应中的低选择性。
Shen等[36]采用铁盐催化一锅法合成α-氨基氰:使用仲胺、伯醇、三甲基氰硅烷与叔丁基过氧化氢在温和的反应条件下反应。该反应使用草酸亚铁作为催化剂(0.05 mmol),以甲苯为溶剂,反应时间4 h,反应温度90 ℃合成系列α-氨基腈。
Safa等[37]采用不同的路易斯酸或离子液体作为催化剂催化4-[(双三甲基硅基)乙烯基]苯甲醛、芳香胺和三甲基氰(TMSCN)的反应,成功合成了带有双(三甲基硅基)乙烯基α-氨基腈,并分别比较了室温下在不同溶剂中不同反应物的Strecker反应,采用薄层色谱法对醛的消失和产物的形成进行了监测。实验发现:带有供电子的芳香胺参加反应收率可达95%,而带有吸电子基团的芳香胺则不发生反应;离子液体BF4比PF6催化的收率更高;路易斯酸如LiClO4催化剂在四氢呋喃中反应2 h,催化收率可达92%。
Wang等[38]制得2,20-吡啶-4,40-羧酸稀土配位聚合物[Ln2(bpdc)3(DMF)2](I:Ln=Tb, II:Ln=Eu),I与II作为路易斯酸催化剂催化Strecker反应。I在CDCl3溶剂中于室温催化反应,收率高达82.8%。
Mohsen等[39]采用磁性Fe3O4纳米颗粒负载在BF3上作为一种新型的可分离的路易斯酸催化剂催化合成α-氨基氰。该反应在室温下进行,产物易分离,并且反应在很短的时间(5~30 min)内即可完成,收率90%以上。反应完成后,催化剂通过磁铁回收重复利用。
5 Brønsted催化剂
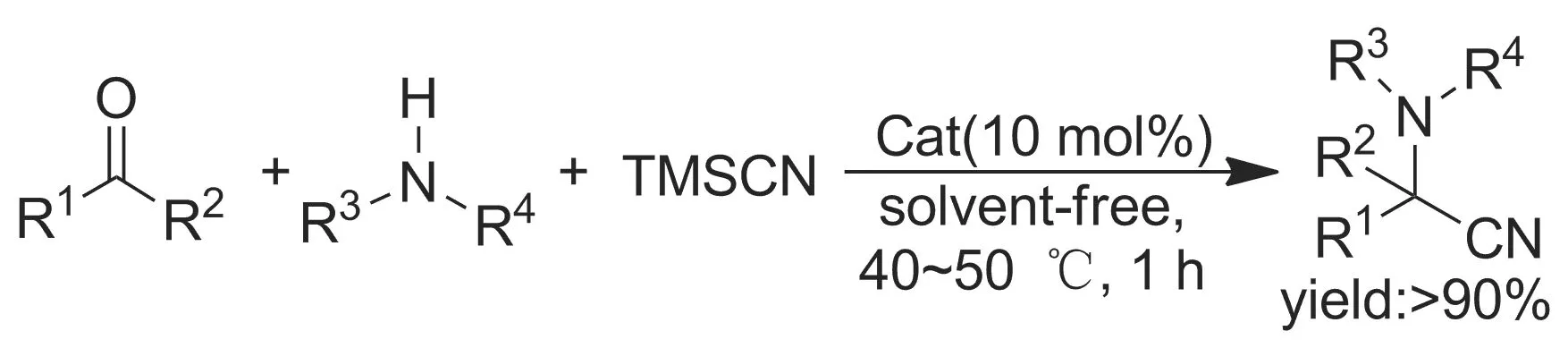
Vahdat等[40]使用一种有机Brønsted酸催化剂草酸催化TMSCN与不同的胺加成生成α-氨基氰(Scheme 8)。该反应催化剂用量0.2 mmol,无溶剂条件下,于50~60 ℃反应1 h即可完成,收率大于90%。因为使用的是Brønsted酸催化剂,从而避免了价格昂贵且对环境有害的路易斯酸催化剂的使用,是一种环境友好型催化剂。
Scheme 8
2012年,Barbero等[41]采用苯磺酰胺及其手性衍生物作为Brønsted酸催化剂催化一锅三组分醛、酮、芳香胺的Strecker反应,催化剂用量5 mol%,在无溶剂条件下升温至40 ℃,平均收率85%。作者还比较了5种Brønsted酸催化剂的催化活性。结果表明2,4-二硝基苯磺酸的催化活性与苯磺酰胺的相当。
由于自然界中存在大量的炭,碳材料作为一种环境友好的催化剂目前得到了迅速发展。其中作为石墨单质的衍生物氧化石墨烯(GO),因为其多孔和良好的水溶性,改性后对有机合成具有良好的催化活性[42]。Su等[43]将Pd纳米颗粒嵌入到氧化石墨烯内,对于胺和亚胺中间体加氢连续氧化为仲胺的偶联产物的协同催化体系具有良好的催化活性。2014年,Sengupta等[44]合成了一种经过修饰的碳催化剂氧化石墨烯衍生物(GO)催化多组分Strecker反应:催化剂用量12wt%,室温条件下,收率82~97%。实验发现,催化活性是由于位于GO上的Brønsted酸活性位点,而且可以在无溶剂条件下在空气中进行多次催化且没有副产品的生成,并且随着使用次数的增加,催化活性基本不变。
6 总结与展望
近年来,有关不对称Strecker反应的催化已取得了很大的进展,催化剂不仅在结构和功能上更加多样化,而且对环境更加绿色环保、适应条件更加温和。但是目前报道的催化剂在使用范围以及通用性等方面还存在一定的局限,因此,设计并合成出结构新颖、催化效能更好、应用范围更广泛的催化剂成为今后发展的趋势。这对于合成具有重要生物活性的α-氨基酸具有重要意义。
[1] Ben L F, Richard A V D. Absolute asymmetric synthesis:The origin,control,and amplification of chirality[J].Angew Chem Int Ed,1999,38:3418-3438.
[2] 黄秋封,林深,许美羡. 过渡金属配合物在不对称合成中的催化应用[J].合成化学,2004,12:245-250.
[3] Saravanan S, Noorul H K, Sayed H R,etal. Enantioselective Strecker reaction of aldimines using potassium cyanide catalyzed by a recyclable macrocyclic V(V) salen complex[J].RSC Adv,2015,121(5):99951-99958.
[4] Hou Y L, Sun R W, Zhou X P,etal. A copper(I)/copper(Ii)-salen coordination polymer as a bimetallic catalyst for three-component Strecker reactions and degradation of organic dyes[J].Chem Commun(Camb),2014,18(50):2295-2297.
[5] Esteves M A, Gigante B, Santos C,etal. New heterogeneous catalysts for the synthesis of chiral amino acids:Functionalization of organic resins with chiral salen complexes[J].Catal Today,2013,218-219:65-69.
[6] 陈巍,吴昌艳,钟林新,等. 木质素磺酸催化的多组分反应[C].北京,中国化学会,2014.
[7] 陆军,李新生. 钨磺酸催化一锅法合成α-胺基腈化合物[J].浙江师范大学学报,2013,36(1):96-100.
[8] Mobaraki A, Movassagh B, Karimi B. Magnetic solid sulfonic acid decorated with hydrophobic regulators:A combinatorial and magnetically separable catalyst for the synthesis of alpha-aminonitriles[J].ACS Comb Sci,2014,16(7):352-358.
[9] Derikvand Z, Derikvand F. Zr-MCM-41 nanoreactors as efficient and reusable catalysts in the synthesis of new aminonitriles by the Strecker reaction[J].Chinese Journal of Catalysis,2011, 32 (3-4):532-535.
[10] Dekamin M G, Mokhtari Z, Karimi Z. Nano-ordered B-MCM-41:An efficient and recoverable solid acid catalyst for three-component Strecker reaction of carbonyl compounds,amines and TMSCN[J].Scientia Iranica,2011,18(6):1356-1364.
[11] Wang W, Wang Y, Wu B,etal. Octahedra-based molecular sieve aluminoborate (PKU-1) as solid acid for heterogeneously catalyzed Strecker reaction[J].Catal Commun,2015,58:174-178.
[12] Chen H, Ju J, Meng Q,etal. PKU-3:An HCl-inclusive aluminoborate for Strecker reaction solved by combining RED and PXRD[J].J Am Chem Soc,2015,137(22):7047-7050.
[13] Rajabi F, Nourian S, Ghiassian S,etal. Heterogeneously catalysed Strecker-type reactions using supported Co(ii) catalysts:Microwave vs. conventional heating[J].Green Chemistry,2011,13(11):3282.
[14] Dekamin M, Mokhtari Z. Highly efficient and convenient Strecker reaction of carbonyl compounds and amines with TMSCN catalyzed by MCM-41 anchored sulfonic acid as a recoverable catalyst[J].Tetrahedron,2012,68(3):922-930.
[15] 杜曦,王钦. 氢键诱导的不对称催化反应研究进展[J].化学试剂,2012,34(2):129-136.
[16] 袁奇学,史福强. 金鸡纳碱类化合物在不对称合成中的应用[J].合成化学,2008,16:371-377.
[17] 何海晓,杜大明. 方酰胺催化亚胺与三甲基硅氰的不对称Strecker反应研究[C].中国化学会第29届学术年会摘要集——第07分会:有机化学,中国北京,2014.
[18] 李乃凯. 金鸡纳碱衍生的硫脲的不对称Strecker反应[D].苏州:苏州大学,2013.
[19] 刘运林. 叔胺亲核催化在一些不对称构建四取代碳手性中心中的应用研究[D].上海:华东师范大学,2015.
[20] Xie H X, Song A G, Song X X,etal. Organocatalytic enantioselective Strecker reaction of cyclic trifluoromethyl-ketoimines[J].Tetrahedron Lett,2013,54(11):1409-1411.
[21] Pankaj C, Swapandeep S C. Organocatalytic asymmetric synthesis of 3-amino-2-oxindole derivatives bearing a tetra-substituted stereocenter[J].Tetrahedron:Asymmetry,2013,24(7):343-356.
[22] Wang D, Liang J Y, Feng J C,etal. The quinine thiourea-catalyzed asymmetric Strecker reaction:An approach for the synthesis of 3-aminooxindoles[J].Advanced Synthesis & Catalysis,2013,355:548-558.
[23] Liu Y L, Zhou J. Organocatalytic asymmetric cyanation of isatin derivedN-Boc ketoimines[J].Chem Commun(Camb),2013,49(39):4421-4423.
[24] Dariush S, Samaneh C, Samaneh M,etal. Dehydroascorbic acid(DHAA) capped magnetite nanoparticles as an efficient magnetic organocatalyst for the one-pot synthesis ofα-aminonitriles andα-aminophosphonates[J].Tetrahedron Lett,2013,54 (48):6403-6406.
[25] Ali R K, Lida H A, Seyyed J S. Nano Al2O3:An efficient and recyclable nanocatalyst for the one-pot preparation of 1-amidoalkyl-2-naphthols under solvent-free conditions[J].Research on Chemical Intermediates,2016,42:915-922.
[26] Dhanasekaran S, Suneja A, Bisai V,etal. Approach to isoindolinones,isoquinolinones,and thiqsviaLewis acid-catalyzed domino Strecker-lactamization/alkylations[J].Org Lett,2016,18(4):634-637.
[27] 郑勤,赵铭,吴冉然,等. 无溶剂条件下MgI2催化的硅腈化反应研究[C].浙江,长三角药物研讨会,2012.
[28] Gerjan D B, Sascha H, Gijsbert A,etal. Enantioselective synthesis of adamantylalanine andcarboranylalanine and their incorporation into the proteasome inhibitor bortezomib[J].Chem Commun,2016,52:4064-4067.
[29] 杨璐. 基于含N双羧酸配体构筑的配位聚合物的合成/结构及性质[D].长春:吉林大学,2015.
[30] Liu Y, Mo K, Cui Y. Porous and robust lanthanide metal-organoboron frameworks as water tolerant Lewis acid catalysts[J].Inorg Chem,2013,52(18):10286-10291.
[31] Lina M A D, Felipe G, Marta I,etal. Tunable catalytic activity of solid solution metal-organic frameworks in one-pot multicomponent reactions[J].J Am Chem Soc,2015,137(19):6132-6135.
[32] Xia J, Xu J N, Fan Y,etal. Indium metal-organic frameworks as high-performance heterogeneous catalysts for the synthesis of amino acid derivatives[J].Inorg Chem,2014,53(19):10024-10026.
[33] Meyer F. Trifluoromethyl nitrogen heterocycles:Synthetic aspects and potential biological targets[J].Chem Commun(Camb),2016,52:3077-3094.
[34] Surya P, Bychinskaya I, Marinez E,etal. Nafion-Fe:A new efficient “Green” Lewis acid catalyst for the ketonic Strecker reaction[J].Catal Lett,2013,143(4):303-312.
[35] Raphael B, Raffael H, Antonio M,etal. Iron chemistry made easy:Chiral N2P2ligands for asymmetric catalysis[J].Synlett,2016,27:831-847.
[36] Shen H, Hu L Z, Liu Q,etal. Iron-catalysed sequential reaction towards alpha-aminonitriles from secondary amines,primary alcohols and trimethylsilyl cyanide[J].Chem Commun(Camb),2016,52:2776-2779.
[37] Kazem D S, Afsaneh Z, Hassan A,etal. Synthesis of newα-aminonitriles containing organosilicon groupsviathree component Strecker reactions[J].J Iran Chem Soc,2013,10(3):447-452.
[38] Wang S Y, Xu J N, Zheng J F,etal. Lanthanide coordination polymer constructed from 2,2′-bipyridyl-4,4′-dicarboxylic acid:Structure, catalysis and fluorescence[J].Inorg Chim Acta,2015,437:81-86.
[39] Mohsen S, Ali M, Ali K N. Magnetic Fe3O4-BF3:Highly efficient Lewis acid catalyst for the synthesis ofα-aminonitriles[J].Research on Chemical Intermediates,2016,4:3805-3827.
[40] Vahdat S M, Khaksar S, Khavarpourb M,etal. Oxalic acid as a simple and efficient organocatalyst for three-component synthesis of Α-amino nitriles[J].Chinese Chemical Lett,2011,22:543-546.
[41] Margherita B, Silvano C, Stefano D,etal.O-Benzenedisulfonimide and its chiral derivative as Brφnsted acids catalysts for one-pot three-component Strecker reaction.Synthetic and mechanistic aspects[J].Org Biomol Chem,2012,10:4058-4068.
[42] Babli R, Debasish S, Basudeb B,etal. Graphene oxide(Go)-catalyzed chemoselective thioacetalization of aldehydes under solvent-free conditions[J].Tetrahedron Lett,2014,55:6596-6600.
[43] Su C L, Rika T, Janardhan B,etal. Tandem catalysis of amines using porous graphene oxide[J].J Am Chem Soc,2015,137:685-690.
[44] Sengupta A, Su C L, Bao C L,etal. Graphene oxide and its functionalized derivatives as carbocatalysts in the multicomponent Strecker reaction of ketones[J].Chem Cat Chem,2014,6:2507-2511.
Research Progress on Catalysts of Asymmetric Strecker Reaction
ZONG Chao-yang1, SUN Ya-quan2,3*
(1. Nanjing University of Technology, Nanjing 210000, China2. College of Pharmacy, Yancheng Teachers University, Yancheng 224051, China;3. Dafeng Marine Organisms Pharmaceutical Limited Company, Yancheng Teachers College, Dafeng 22410, China)
The research progress on catalysts of asymmetric Strecker reaction was reviewed with 44
. Five kinds of catalysts for catalytic asymmetric Strecker reaction: metal complex catalyst, solid acid catalyst and organic small molecule chiral catalyst, lewis acid and Brønsted acid catalyst were discussed in detail. Suggestions on future development of this method were proposed.
asymmetric strecker reaction; catalyst; alpha amino cyanide; review
2016-06-07
江苏省前瞻性研究项目(72121632202A)
纵朝阳(1989-),男,汉族,安徽宿州人,硕士研究生,主要从事有机合成研究。 E-mail: 18940688746@163.com
孙雅泉,博士,硕士生导师, E-mail: suyaquan@hotmail.com
O621.3; O643.3
A
10.15952/j.cnki.cjsc.1005-1511.2016.10.16147

