中国梦:没有乙型肝炎的未来
樊 蓉, 尹雪如, 侯金林, 刘志华
(南方医科大学南方医院 肝病中心和感染内科, 广州 510515)
中国梦:没有乙型肝炎的未来
樊 蓉, 尹雪如, 侯金林, 刘志华
(南方医科大学南方医院 肝病中心和感染内科, 广州 510515)
HBV感染是我国最重要的公共卫生问题之一。阻断HBV母婴传播是消灭病毒性肝炎对我国人群危害的主要手段之一。最新研究结果证实了妊娠晚期使用替诺福韦酯抗病毒治疗可进一步减少HBV母婴传播。同时,中国肝炎防治基金会于2015年7月25日启动了“乙型肝炎母婴零传播工程”(“小贝壳”项目),旨在通过移动医疗工具对乙型肝炎孕妇进行规范化管理,以达到进一步减少甚至消除HBV母婴传播的目的。目前我国抗击乙型肝炎已经取得了举世瞩目的成就,相信随着这项最新研究的发现以及“小贝壳”项目的启动,终将会实现没有乙型肝炎的未来。
肝炎病毒, 乙型; 疾病传播, 垂直; 述评
在中国,HBV感染是最重要的公共卫生问题之一。据估算,全国约有7000余万慢性HBV感染者,其中包括需要抗病毒治疗的慢性乙型肝炎(CHB)患者约2800万、乙型肝炎肝硬化患者约100万和肝癌患者约30万。如果不给予有效治疗,约有25%~40%的CHB患者可进展为肝硬化或原发性肝癌并最终导致死亡[1]。CHB及其相关疾病对我国造成的负担相当严重,每年直接经济损失约为9000亿人民币。为了减轻CHB对我国公共卫生的严重危害,一方面需对已感染HBV的患者增强疾病监控力度,提高乙型肝炎抗病毒治疗的知晓率和可及率,减缓或阻止HBV感染者的疾病进展;另一方面需要采取措施,最大程度地预防HBV感染,力争实现“HBV零传播”。
自1992年我国政府全面实施新生儿乙型肝炎疫苗接种免疫预防措施以来,我国人群HBV感染率已显著降低,中国疾病预防控制中心调查显示2014年1~4岁人群HBsAg检出率已下降至0.32%[2]。即便如此,目前每年仍有超过50 000名新生儿感染HBV,并且未来很有可能进一步发展成为慢性HBV携带者[3]。对于高病毒载量的母亲而言,其新生儿的免疫预防失败率高达15%[4]。因此,切断HBV的主要传播途径,阻断母婴传播,是消灭乙型肝炎的重要举措。
随着妊娠B级抗病毒药物的上市,孕妇在妊娠晚期短期使用抗病毒药物,可以降低围产期或因生产过程中直接接触被污染的分泌物或母血而导致的HBV母婴传播。有研究[5]表明,孕妇的HBV水平与HBV母婴传播率呈正相关,当母亲生产期血清病毒载量低于6 log10拷贝/ml时,几乎不发生母婴传播。然而,由于在过去的十几年中关于使用抗病毒药物阻断HBV母婴传播的研究尚未取得一致结果[6-11],因此,至今世界卫生组织(WHO)指南仍没有明确推荐孕期使用抗病毒药物阻断母婴传播。
近期Pan等[12]通过开展一项随机对照临床研究发现,高病毒载量(HBV DNA>200 000 IU/ml)的孕妇在妊娠晚期使用低耐药率的替诺福韦酯(TDF)可以显著降低HBV的母婴传播率(由18%降至5%)。在符合方案分析中,所有完成治疗和随访的母亲所生的92名新生儿均未发生HBV母婴传播。此外,服用TDF的母亲及其新生儿的安全性数据(包括先天畸形率)与未服药组间差异无统计学意义,这与早期Han等[11]使用替比夫定(LdT)阻断母婴传播的研究结果一致。
Pan等[12]进行的这项研究首次通过严格的随机对照试验证实了妊娠晚期使用TDF抗病毒治疗对于HBV母婴阻断的有效性和安全性,为妊娠期使用抗病毒药物阻断母婴传播提供了高等级的循证医学证据,对实现乙型肝炎母婴阻断具有重要意义。这项重要发现极大程度地鼓励了我国医护工作者将抗病毒药物预防阻断措施应用于临床实践,从而使乙型肝炎孕妇获益,并大大降低新生儿的HBV感染率。WHO全球HIV/AIDS和肝炎部门负责人指出:“这项新的研究表明,抗病毒治疗将在未来阻断HBV母婴传播中发挥重要作用,特别是对于高病毒载量的孕妇。WHO将会根据目前日益完善的循证医学证据更新HBV指南”[3]。随着这项重要研究的发布,相信各大国际指南都会进一步更新HBV母婴阻断的推荐意见。今后需针对HBV母婴阻断个体化抗病毒治疗进行更多研究,以期完善HBV母婴阻断策略,造福更多乙型肝炎孕妇和新生儿[13]。
然而,在这个振奋人心的时刻必须要清醒地认识到,从科学研究成果转化到临床实践仍有很长的路要走,尤其对于我国这样卫生保健条件分布不均衡的乙型肝炎大国,大多数乙型肝炎孕妇很少有机会接受正规的抗病毒治疗,同时,由于不完善的转诊机制和广泛存在的乙型肝炎歧视导致HBV母婴阻断的理念很难推广。因此,采取行动已刻不容缓。
非常可喜的是,2015年7月25日,中国肝炎防治基金会在北京人民大会堂启动了“乙型肝炎母婴零传播工程”,即“小贝壳”项目。该项目兼具学术性和公益性,目标人群为乙型肝炎孕妇及其婴儿,目的是通过建立妊娠乙型肝炎规范管理的示范基地,按照标准流程对乙型肝炎孕妇及其婴儿进行规范的随访管理,进而最大限度地减少甚至完全阻断母婴传播。该项目也可在很大程度上促进各相关学科间的协作,在肝病医生、全科医生、妇产科医生以及乙型肝炎孕妇之间搭建沟通的桥梁,并向公众普及乙型肝炎母婴阻断的相关知识。
目前,乙型肝炎母婴零传播工程已在全国89家医院启动,并形成了统一的乙型肝炎母婴阻断临床管理标准流程(图1)。该流程对孕妇筛查、评估、妊娠期管理、分娩管理、停药时机和婴儿免疫等各个方面进行了标准化的规定,现已在所有项目医院推广应用。该流程的推广将有力促进乙型肝炎母婴阻断项目的开展,以规范乙型肝炎母婴阻断临床实践,提高防治水平和能力。
同时,该项目还创新性地搭建了一个无处不在、随处可及的智能移动医疗工具“小贝壳”,将其作为乙型肝炎孕产妇妊娠期随访管理工具。该移动医疗工具分为医生端和患者端,医生端是一款专为感染科、妇产科、新生儿科医生打造的应用程序,可协助医生管理患者。患者端是一款为乙型肝炎孕产妇打造的专属软件,两者均借力于移动医疗来阻断乙型肝炎母婴传播。项目组计划首先在10家重点示范基地中推广,并计划在未来应用到全国100家项目医院。此外,该项目还利用“小贝壳”开展了一项关于妊娠期慢性HBV感染的临床特征及HBV母婴传播的流行病学研究,旨在应用移动医疗工具调查妊娠期慢性HBV感染的临床特征和母婴传播发生情况。截至2016年9月29日,共纳入995例CHB孕妇,包括HBeAg阳性595例,HBeAg阴性349例,其中,HBV DNA≥106拷贝/ml的476例孕妇接受抗病毒治疗的比例为61.97%,HBV DNA<106拷贝/ml的467例孕妇接受抗病毒治疗的比例为29.55%。相信该项目结果必将会对政府在公共卫生领域的决策产生深远影响,未来政府也将为全社会实施乙型肝炎母婴阻断工程提供更多资源,包括为乙型肝炎孕妇提供免费孕期病毒定量监测以及抗病毒治疗等。
2016年4月14日,在巴塞罗那召开的第51届欧洲肝病学会年会期间,全球四大肝病学会(亚太肝病学会、美国肝病学会、欧洲肝病学会和拉丁美洲肝病学会)主席在WHO代表的见证下共同签署了消灭病毒性肝炎联合声明[14]。同时,WHO也将敦促各国建立国家层面的预防体系,以期最终消灭病毒性肝炎这一公共卫生问题。我国专家和政府也积极响应号召,呼吁在全国范围内推广HBV母婴阻断策略[15]。在过去的25年中,我国在抗击乙型肝炎方面已经取得了举世瞩目的成就,坚信随着抗病毒治疗重要研究的发现以及“乙型肝炎母婴零传播工程”的启动,终将会实现一直以来孜孜追求的中国梦——没有乙型肝炎的未来。
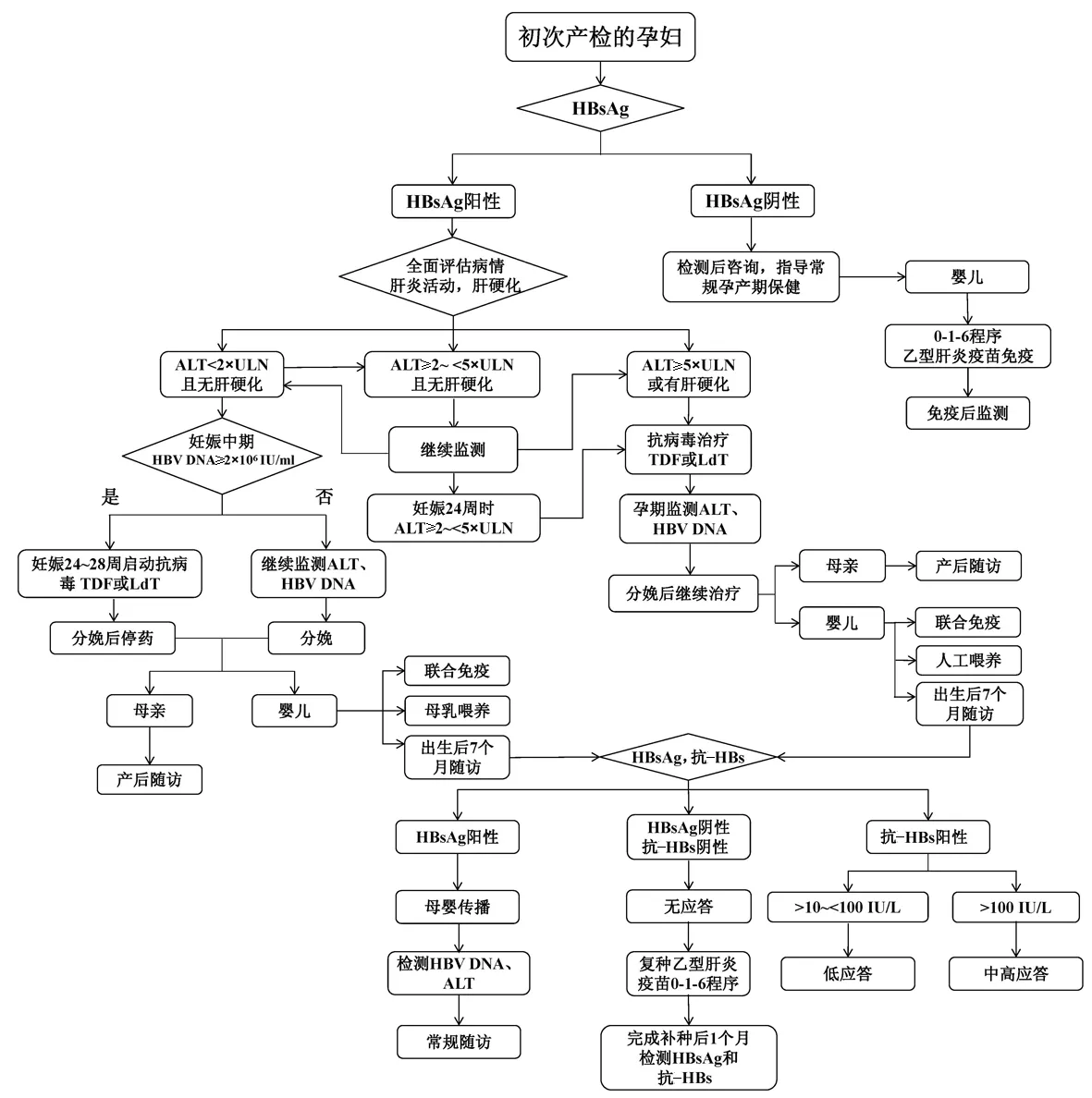
图1 乙型肝炎母婴阻断临床管理流程
注:ULN,正常值上限; 0-1-6程序,分别在出生后当天、1个月以及6个月进行乙型肝炎疫苗的接种
[1] WANG FS, FAN JG, ZHANG Z, et al. The global burden of liver disease: the major impact of China[J]. Hepatology, 2014, 60(6): 2099-2108.
[2] Chinese Society of Hepatology and Chinese Society of Infectious Diseases, Chinese Medical Association. The guideline of prevention and treatment for chronic hepatitis B: a 2015 update[J]. J Clin Hepatol, 2015, 31(12): 1941-1960. (in Chinese) 中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2015年更新版)[J]. 临床肝胆病杂志, 2015, 31(12): 1941-1960.
[3] World Health Organization. Tenofovir reduces mother-to-child transmission of hepatitis B: new study[EB/OL]. [2016-06-16]. http://www.who.int/hepatitis/news-events/hbv-mtct-tenofovir/en/
[4] VISVANATHAN K, DUSHEIKO G, GILES M, et al. Managing HBV in pregnancy. Prevention, prophylaxis, treatment and follow-up: position paper produced by Australian, UK and New Zealand key opinion leaders[J]. Gut, 2016, 65(2): 340-350.
[5] ZOU H, CHEN Y, DUAN Z, et al. Virologic factors associated with failure to passive-active immunoprophylaxis in infants born to HBsAg-positive mothers[J]. J Viral Hepat, 2012, 19(2): e18-e25.
[6] PAN CQ, HAN GR, JIANG HX, et al. Telbivudine prevents vertical transmission from HBeAg-positive women with chronic hepatitis B[J]. Clin Gastroenterol Hepatol, 2012, 10(5): 520-526.
[7] CHEN HL, LEE CN, CHANG CH, et al. Efficacy of maternal tenofovir disoproxil fumarate in interrupting mother-to-infant transmission of hepatitis B virus[J]. Hepatology, 2015, 62(2): 375-386.
[8] ZHANG H, PAN CQ, PANG Q, et al. Telbivudine or lamivudine use in late pregnancy safely reduces perinatal transmission of hepatitis B virus in real-life practice[J]. Hepatology, 2014, 60(2): 468-476.
[9] XU WM, CUI YT, WANG L, et al. Lamivudine in late pregnancy to prevent perinatal transmission of hepatitis B virus infection: a multicentre, randomized, double-blind, placebo-controlled study[J]. J Viral Hepat, 2009, 16(2): 94-103.
[10] GREENUP AJ, TAN PK, NGUYEN V, et al. Efficacy and safety of tenofovir disoproxil fumarate in pregnancy to prevent perinatal transmission of hepatitis B virus[J]. J Hepatol, 2014, 61(3): 502-507.
[11] HAN GR, CAO MK, ZHAO W, et al. A prospective and open-label study for the efficacy and safety of telbivudine in pregnancy for the prevention of perinatal transmission of hepatitis B virus infection[J]. J Hepatol, 2011, 55(6): 1215-1221.
[12] PAN CQ, DUAN Z, DAI E, et al. Tenofovir to prevent hepatitis B transmission in mothers with high viral load[J]. N Engl J Med, 2016, 374(24): 2324-2334.
[13] FAN R, YIN X, HOU J. Prevention of peripartum hepatitis B transmission[J]. N Engl J Med, 2016, 375(15): 1496-1498.
[14] World Health Organization. Combating hepatitis B and C to reach elimination by 2030[EB/OL].[2016-05]. http://apps.who.int/iris/bitstream/10665/206453/1/WHO_HIV_2016.04_eng.pdf
[15] FAN R, YIN X, LIU Z, et al. A hepatitis B-free generation in China: from dream to reality[J]. Lancet Infect Dis, 2016, 16(10): 1103-1105.
引证本文:FAN R, YIN XR, HOU JL, et al. The Chinese dream: hepatitis B-free generation[J]. J Clin Hepatol, 2017, 33(1): 17-20. (in Chinese) 樊蓉, 尹雪如, 侯金林, 等. 中国梦:没有乙型肝炎的未来[J]. 临床肝胆病杂志, 2017, 33(1): 17-20.
(本文编辑:葛 俊)
·国外期刊精品文章简介·
The Chinese dream: hepatitis B-free generation
FANRong,YINXueru,HOUJinlin,etal.
(HepatologyUnitandDepartmentofInfectiousDiseases,NanfangHospital,SouthernMedicalUniversity,Guangzhou510515,China)
In China, hepatitis B virus (HBV) infection remains a great threat to public health. Preventing the mother-to-child transmission (MTCT) of HBV is the main method to reduce the harm and disease burden caused by viral hepatitis in China. Recent studies have demonstrated that antiviral therapy with tenofovir disoproxil fumarate (TDF) during late pregnancy for mothers can further reduce MTCT of HBV. Meanwhile, Chinese Foundation for Hepatitis Prevention and Control launched the Hepatitis B Shield Project on July 25, 2015. This project aims to further reduce or even eliminate MTCT of HBV by means of standard management of pregnant women with HBV via a mobile-health application. At present, China has made great achievements in fighting against HBV. We believe that the remarkable findings of such studies and the launch of the Chinese Shield Project will make the Chinese dream-HBV-free generation come true in the near future.Key words:hepatitis B virus; disease transmission, vertical; editorial
10.3969/j.issn.1001-5256.2017.01.002
2016-11-29;
2016-12-09。
樊蓉(1986-),女,副主任医师,博士,主要从事慢性乙型肝炎临床和转化医学研究。
侯金林,电子信箱:jlhousmu@163.com。
R512.62
A
1001-5256(2017)01-0017-04

