耳聋易感基因患儿人工耳蜗植入术后听觉言语能力评估
戴溪 马静 林垦 高映勤 陈泉东 张铁松
人工耳蜗植入(cochlear implantation,CI)是解决重度或极重度感音神经性耳聋的方法。绝大部分耳聋是由遗传因素造成的,在耳聋人群中70%的遗传性耳聋患者除耳聋外不伴有其他症状,称为非综合征型耳聋(non-syndromic hearing loss,NSHL)[1]。NSHL是临床常见的遗传性疾病,随着基因诊断技术的普及,许多先天性听力障碍儿童通过该技术检测出致聋基因[2],通过人工耳蜗植入NSHL患儿听力水平可显著提高。全国性聋病分子流行病学调查结果显示:中国聋病人群的常见且致病基因比较明确的主要遗传性基因是GJB2基因、SLC26A4基因和线粒体12S rRNA突变。随着临床技术的不断进步,植入术后的康复效果研究也在同步发展。国内研究者曾就人工耳蜗植入术后康复效果进行过一系列研究[3],发现听觉言语康复训练、耳聋基因等是造成人工耳蜗术后康复差异的重要因素。本文对192例重度和极重度感音神经性耳聋患儿人工耳蜗植入后的听觉言语康复效果进行随访评估,比较不同基因改变致聋患儿的术后疗效,探讨CI术后疗效与不同耳聋基因病因的相关性,为通过聋病基因诊断来预测CI的效果提供依据。
1 资料与方法
1.1研究对象
评估对象为2014年1月~2015年5月间在我院接受人工耳蜗植入手术的重度、极重度感音神经性耳聋患儿192例,其中男112例,女80例;植入手术时年龄2岁~10岁,其中<3岁患儿54例,3~6岁(含3岁)94例,6~10岁(含6岁)44例,平均植入年龄4.6±1.4岁,以3~6岁聋儿为多。统计学分析显示组间性别、年龄、术前残余听力等差异无统计学意义(P<0.05);192例患儿中,母亲孕期病毒感染者6例(风疹病毒感染3例、麻疹病毒感染3例),药物中毒3例,大前庭导水管综合征16例,有家族耳聋病史29例(父母或同胞为聋哑人),不明原因的先天性聋138例,所有患儿未发现其他部位明显畸形。均为语前聋患者,5岁以上儿童均有助听器佩戴史,患儿配戴助听器3~6个月无效或者效果不理想,入选条件[4]:①术前听力检查提示双耳重度、极重度感音神经性耳聋;②术前患儿均采外周静脉血进行基因检测诊断;所有参与跟踪随访的患儿家属签署知情同意书;③无手术禁忌证;④对人工耳蜗植入有正确的认识和适当的期望值;⑤具备听觉言语康复教育的条件。
1.2术前诊断及听力学检查
192例患儿术前均进行相关听力学检查。其中82例为重度感音神经性聋,双侧ABR反应阈>95 dB nHL,110例为极重度感音神经性聋,双侧ABR反应阈>100 dB nHL;40 Hz听觉事件相关电位1 kHz以下反应阈值>90 dB nHL;听性稳态反应2 kHz及以上频率阈值>90 dB nHL;耳声发射双耳均未引出。5岁以上患儿行为测听裸耳平均阈值>80 dB HL;助听听阈2 kHz以上频率>50 dB HL。
1.3患儿耳聋基因检测结果
192例耳聋患儿中GJB2基因突变患儿50例、SLC26A4基因突变患儿32例、线粒体12S rRNA基因突变患儿2例、未发现GJB2、SLC26A4及线粒体基因突变患儿108例,与国内聋病患儿耳聋易感基因遗传学基本一致[5]。其中GBJ2基因突变率以235 delC和109G最高,SLC26A4基因突变以IVS7-2A>G为主。
1.4研究方法 将患者分成GJB2基因突变组、SLC26A4基因突变组、线粒体12S rRNA基因突变组、未检出耳聋基因突变对照组,所有患者在我院行单侧面隐窝入路人工耳蜗植入术,手术顺利,术中检测正常,术后未见特殊并发症。术后一周行耳蜗位X摄片,均显示电极植入位置良好,手术后1月开机调试,使用声场扬声器得到的助听听阈3FA(即0.5、1、2 kHz平均听阈)为39.6±7.4 dB HL,4FA(即0.5、1、2、4 kHz平均听阈)为38.5±7.5 dB HL。开机后转入昆明市聋儿康复中心进行系统的听力及言语训练,语训时间长短不等,定期门诊复诊调机。
1.5康复效果评估方法
在术前和术后进行康复训练的第3、6、9、12个月时段,采用国内应用广泛且可操作性强的三种问卷对患儿进行听觉言语能力评估。通过采访密切接触行CI儿童的家长、康复专业人员等,获得儿童在自然环境中的听觉言语康复效果信息。
1.5.1听觉意义整合量表(Meaningful Auditory IntegrationScale,MAIS) Zheng等[6]2009年将MAIS测试进行了汉语的改编。此量表用于评估2岁以上患儿在实际交流环境中对声音的自发性反应。共10个问题,问题1~2对耳蜗装置的接纳程度;问题3~6对声音的察知;问题7~10了解声音的意义。每一个问题得分为0~4分,5个级别,10个问题满分为40分,主要评价患儿的发声情况、对声音的觉察能力和对声音的理解能力等。
1.5.2听觉行为分级(Categories of Auditory Performance,CAP)[7]反映受试者日常生活环境中的听觉水平;是评估听觉感知的分级标准;反映了患儿在日常生活环境中的听觉水平,根据受试者对外界声音的行为反应程度分为0~7分,由家长或老师根据患儿对所有外界声音的行为反应程度对其进行直观的分级评价[8]。
1.5.3言语可懂度分级(Speech Intelligibility Rating,SIR)[9]SIR用于评估语前聋患儿的言语产生能力,根据患儿自发言语可以被倾听者理解的程度将患儿言语可懂度分为1~5分。用于评估受试者的言语产生能力,已广泛用于听觉干预后康复效果的评估[8]。
1.6统计学方法 采用统计学软件SPSS 17.0多元回归分析各基因突变类型与康复效果的相关性,自变量为不同基因突变类型,因变量为CI患儿MAIS、CAP、SIR术后1年的问卷评估得分。分析三种不同基因突变类型对儿童听觉言语康复效果的影响。各组和对照组间相同月份间相互比较、组内术后月份与术前单独比较均采用单因素方差分析,以P<0.05为差异有统计学意义。
2 结果
2.1听觉言语能力发展效果进行评估比较
术后不同康复阶段语言能力康复效果评估与结果分析,分别在术前和术后开机后3、6、9、12个月时对各组患儿进行评估。术后不同康复阶段听觉能力康复效果评估结果,四组听患儿不同时间MAIS问卷评估结果得分由表1可见。四组听患儿不同时间CAP问卷评估结果得分由表2可见。四组听患儿不同时间SIR问卷评估结果得分结果由表3可见。
术前MAIS、CAP、SIR分级得分结果方差为齐性,采用参数检验方法,ANOVA方差分析显示四组得分率差异无统计学意义(P>0.05),不同耳聋基因因素与MAIS、CAP、SIR分级得分的相关性,比较4组术后3、6、9、12个月不同阶段效果结果显示:各组均具有非常好的听觉言语康复效果。
①MAIS得分随患儿康复时间的延长得分呈阶梯式增长,组间样本t检验比较发现,GJB2基因突变组的患儿与对照组术后康复12月得分增长量,其差异有统计学意义(P=0.034<0.05),但SLC26A4组、线粒体12S rRNA组与对照组术后康复12月得分增长量,差异无统计学意义(P=0.47和0.54,P>0.05),说明在MAIS项目评估GJB2基因突变组中优于对照组,其他各组患儿人工耳蜗植入术后听觉康复效果基本一致。②CAP和SIR分级得分,CAP和SIR等级各组术后康复12月得分增长量相似,统计学分析分别显示三组基因突变组与对照组之间差异无显著性(三组均P>0.05)。③四组患儿术后MAIS、CAP、SIR得分较术前均明显改善(四组均P<0.05),各组患儿听觉言语能力得分随开机时间的增加而增加。

表1 不同阶段听觉意义整合量表(MAIS)评估结果得分均值(分)
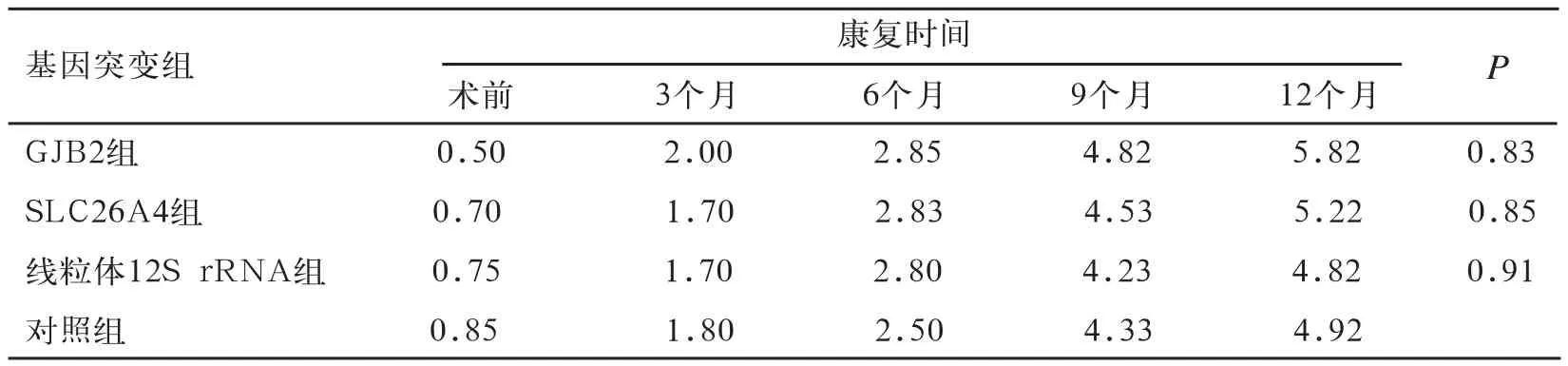
表2 不同阶段听觉行为分级标准(CAP)评估结果得分均值(分)

表3 不同阶段言语可懂度分级标准(SIR)评估结果得分均值(分)
3 讨论
本研究对192例患儿进行了为期1年的纵向跟踪评估,不同阶段的评估结果显示了此类患者听觉言语识别能力的发展规律和趋势,术后患儿整体听觉言语能力有提高,其中GJB2基因突变组各项随访结果显示出了较好的长期听觉性能,最有可能因为致病性的影响GJB2突变是局限于耳蜗,通常不伴随着宏观内耳畸形,受益于完整的听觉通路,GJB2突变患者的颞骨病理切片显示外毛细胞退化,血管纹发育不全,但对螺旋神经节神经元的完整性的影响微乎其微,导致耳蜗植入后的快速恢复听力。而对照组相关性耳聋者的毛细胞数量相对较少[10],理论上推断GJB2组术后可以获得较好的听觉康复效果,尽管统计学分析显示GJB2组与对照组之间除MAIS得分外差异无显著性,对言语的再认知能力相同,前者并无明显优势。国内学者均为GJB2基因突变的患者在术后可以取得良好的康复效果[11],这与目前国际上认可的观点一致[12]。
本研究中,SLC26A4组随访结果统计学分析显示各项评估结果未显现出明显优势,SLC26A4基因突变导致内淋巴的系统异常,导致前庭导水管扩张(见Pendred综合征)。虽然也是神经完整性,在术后的结果似乎并没有发挥重要作用,随着术后年数的增加SLC26A4组是否能逐渐体现出优势将在后续随访中得到验证。首先,本研究中线粒体12S rRNA基因突变组与对照组也没有显著差异,可能由于病例样本量少,不能显示两组数据的差异,对照组在不明病因的情况下更有可能退化螺旋神经节神经元,其康复效果较差,后继研究需要进一步积累和扩大样本量,横向与纵向随访相结合。其次,本研究随访时间仅为1年,从理论上讲,在不同的耳聋基因突变导致不同的病态可能对CI的结果产生影响。再次,本研究采用了国内应用广泛且可操作性强的MAIS、SIR、CAP等评估方法,相对国外研究方法主观性较强,也可能造成组间差异无法显现。最后,术后康复训练、家长的关注程度、患儿是否存在注意力不集中等学习问题,这些因素也可导致随访结果存在偏差。另一方面,也有一些研究表明耳聋因素可能不是一个可靠的预测CI的结果,CI对重度、极重度感音神经性语前聋患儿的言语康复疗效已无争议[13]。CI植入术后患儿虽然能够听到了声音,但需要各类积极配合配套的康复训练,越早尽快的接受康复训练,能使患儿听懂声音,学会与人交流,使其融入有声社会[14]。
参考文献:
[1]Hilgert N,Smith RJ,Van Camp G.Function and expression pattern of nonsyndromic deafness genes[J].Curr Mol Med,2009,9(5):546-564.
[2]高儒真,陈晓巍,历东东,等.新生儿聋病基因筛查及咨询的临床意义[J].中国听力语言康复科学杂志,2015(3):166-171.
[3]Yuan H,Zhang H,Liang W,et al.The study of external factors affecting auditory ability of infants and toddlers after cochlear implantation[J]. Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi,2015,29(19):1671-1676.
[4]中国人工耳蜗植入指南修订大会暨第十届亚太人工耳蜗植入大筹备会在三亚隆重召开[J].中华耳科学杂志,2012(04).
[5]Ma Y,Xiao Y,Bai X,et al.GJB2,SLC26A4,and mitochondrial DNA12S rRNA hot-spots in 156 subjects with non-syndromic hearing loss in Tengzhou,China[J].Acta Otolaryngol,2016,136(8):800-805.
[6]Zheng Y,Soli SD,Wang K,et al.A normative study of early prelingual auditory development[J].Audiol Neurootol,2009,14(4):214-222.
[7]Nikolopoulos TP,Archbold SM,Gregory S.Young deaf children with hearing aids or cochlear implants:early assessment package for monitoring progress[J].Int J Pediatr Otorhinolaryngol,2005,69(2):175-186.
[8]张斯斯,林有辉,张榕,等.语前聋患者人工耳蜗植入术后听觉言语康复相关影响因素的研究[J].中国听力语言康复科学杂志,2013(5):335-338.
[9]O'Neill C,Archbold SM,O'Donoghue GM,et al.Indirect costs,cost-utility variations and the funding of paediatric cochlear implantation[J].Int J Pediatr Otorhinolaryngol,200 1,58(1):53-57.
[10]Zhu Y,Chen J,Liang C.et al.Connexin26[GJB2] deficiency reduces active cochlear amplification leading to late-onset hearing loss[J].Neuroscience,2015,284:719-729.
[11]陈杰,杨烨,史陆森,等.GJB2相关聋儿人工耳蜗植入后听觉康复效果评估[J].中国耳鼻咽喉颅底外科杂志,2015,10(5):393-395.
[12]Kong Y,Liang S,Ren C,et al.The research of rehabilitation effect of cochlear implantation for deaf children with gene mutation[J].Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi,2015,29(13):1172-1174.
[13]Bond M,Mealing S,Anderson R,et al.The effectiveness and cost-effectiveness of cochlear implants for severe to profound deafness in children and adults:a systematic review and economic model[J].Health Technol Assess,2009,13(44):1-330.
[14]刘青,周慧芳,张静,等.语前聋患儿人工耳蜗植入术后康复效果分析[J]. 临床耳鼻咽喉头颈外科杂志,2011(13):582-584.

