甘露醇辛酸二酯的酶法合成、鉴定及其应用研究
张晓慧 孟庆然 张连富,2
(食品科学与技术国家重点实验室;江南大学食品学院1,无锡 214122) (国家功能食品工程技术研究中心2,无锡 214122)
甘露醇辛酸二酯的酶法合成、鉴定及其应用研究
张晓慧1孟庆然1张连富1,2
(食品科学与技术国家重点实验室;江南大学食品学院1,无锡 214122) (国家功能食品工程技术研究中心2,无锡 214122)
脂肪酶催化合成甘露醇辛酸二酯,利用HPLC-MS确定产物,使用混合介质正己烷:乙醚(7∶3)对目标产物进行萃取纯化,产物纯度达到90%以上。采用HPLC-MS、NMR确定目标产物为1,6-二辛酸甘露醇酯。将甘露醇辛酸二酯添加到不同植物油中,探讨在不同植物油中的最低添加量以及在不同加工条件下所制备凝胶油的加工特性。添加量达到0.8%~1.0% (m/m) 时,植物油即可呈现较好的凝胶态。在添加量为10%,搅拌速率为500 r/min,加热温度为125 ℃条件下所制备的凝胶油具有稳定的加工特性。
甘露醇辛酸二酯 酶法合成 分离纯化 凝胶油 流变
随着人们饮食结构的改变,焙烤类、涂抹类等食品所占的比重越来越大,这就使得食品专用油脂的消耗量快速增加[1]。目前,国内市场上常见的专用油脂(人造奶油或涂抹脂产品等)大多数以氢化油为主要成分,其中反式脂肪酸和饱和脂肪酸含量(质量分数在10%左右)超标问题比较严重[2]。研究表明,食用大量含反式/饱和脂肪酸的食物会加速动脉硬化,容易诱发心脑血管疾病、冠心病、糖尿病和老年痴呆等疾病[3-4],故积极研究开发低/零反式脂肪酸和低饱和脂肪酸类型的专用油脂产品具有重大意义[5]。基于这一认识,液态植物油有机结构化所制备的凝胶化油脂越来越受到重视。
常见的凝胶油制备方法是通过添加小分子凝胶剂到液态植物油中,在一定的加工条件下,使液态油成为固态或半固态的胶状物。此种方法制备的凝胶油通常具备可加工的黏弹性,且满足低反式脂肪酸和低饱和脂肪酸等要求[6-7]。目前,用于制备凝胶油的凝胶因子主要有脂肪酸、脂肪醇、植物蜡及植物素等[8]。这些凝胶剂大多是长碳链脂肪酸及其衍生物,不易消化且对人体无额外的营养的价值,故研究开发中碳链的脂肪酸酯备受青睐[9]。本研究通过酶法合成一种新型的中碳链脂肪酸糖醇酯,通过分离纯化得到目标产品。将纯化产物添加到液态植物油中,研究产物的凝胶效果。本研究不仅丰富了凝胶因子的种类,也为开发新的凝胶剂提供借鉴。
1 材料与方法
1.1 试验材料
Novozym 435固定化脂肪酶(10 000 PLU/g):诺维信中国生物技术有限公司;4Å分子筛:上海环球分子筛有限公司;精炼一级大豆油:上海益海嘉里公司;色谱级甲醇、AR级甘露醇、辛酸、丙酮、正己烷、乙醚等:中国医药集团上海化学试剂公司。
1.2 试验仪器
Agilent 1200高效液相色谱仪:美国Agilent公司;ELSD 3300蒸发光散射检测器:美国Alltech公司;ZMD 4000 Mass检测器:美国Waters公司;Physica MCR301型流变仪:奥地利Anton Par公司;DF-101S集热式磁力加热搅拌器:常州迈科诺仪器有限公司;ADVANCE Digital 400MHz核磁共振谱仪:德国Bruker公司。
1.3 试验方法
1.3.1 甘露醇辛酸酯的合成
甘露醇(0.364 g)、辛酸(0.864 g)称量至25 mL圆底烧瓶中,加入15 mL丙酮,于磁力搅拌上平衡1 h后加入0.1 g酶催化剂、2 g 4Å分子筛,混匀后于(50±1)℃、200 r/min 的磁力加热搅拌器中回流反应72 h。目标产物合成过程如图1所示。
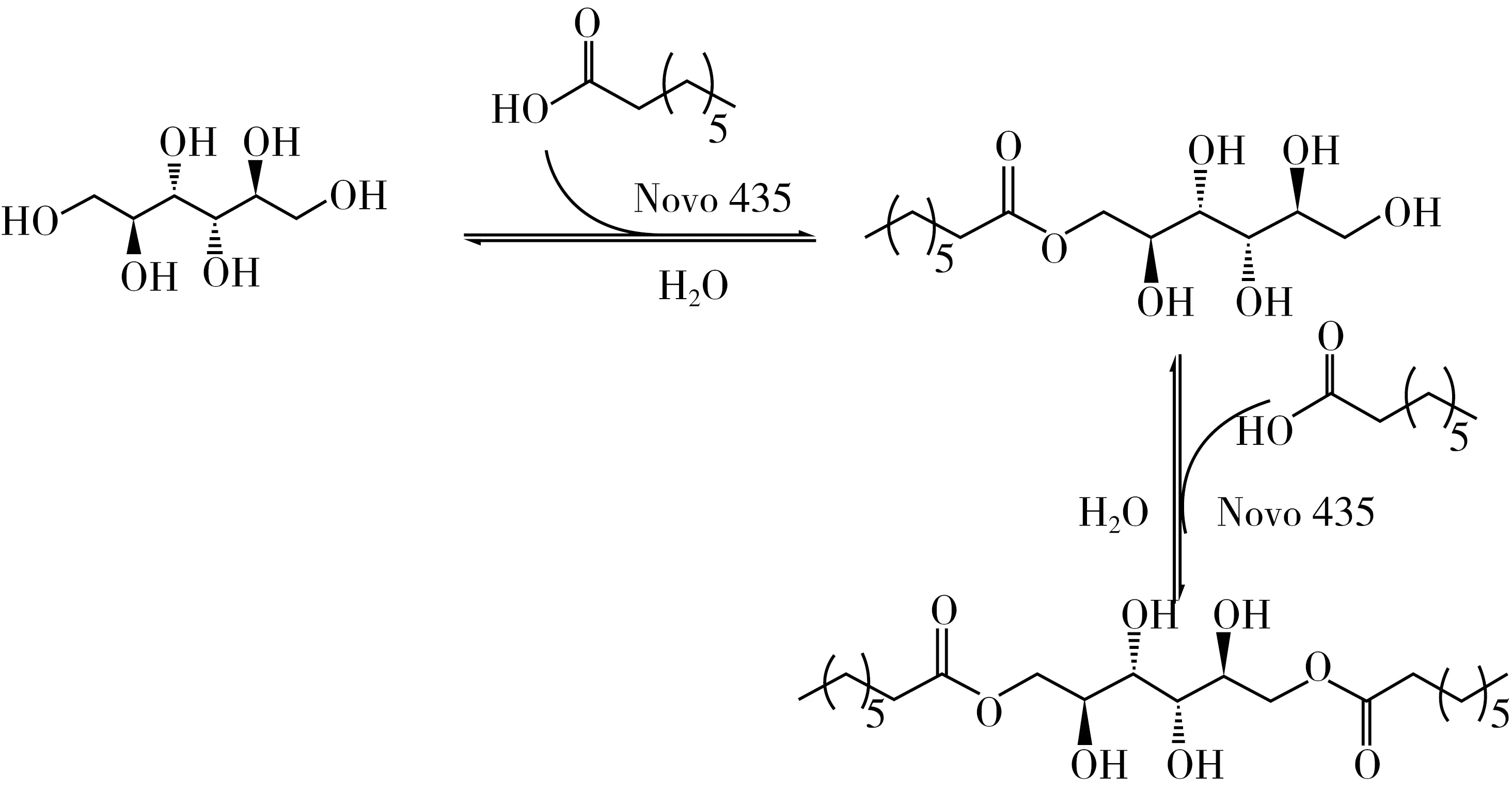
图1 酶催化合成甘露醇酯流程图
1.3.2 产物HPLC分析
取2 mL反应混合液,经0.22 μm微孔滤膜过滤后进行HPLC检测,色谱柱为C18柱(5 μm, 3.9 mm×150 mm Agilent, UAS),流动相条件:A-甲醇,B-0.1%甲酸溶液,梯度洗脱30 min(A:65%~85%,B:35%~15%),流速为1.0mL/min,柱温30 ℃,进样量10 μL,ELSD漂移管温度40 ℃,载气流1.5 L/min。按面积归一法计算产物纯度。
1.3.3 产物纯化及结构鉴定
将反应混合物过滤去除分子筛和固定化酶(回收),滤液减压浓缩去除溶剂。向浓缩物中加入10 mL蒸馏水,于分液漏斗中充分振荡混合,静置10 min,保留上层油相,用适量正己烷与乙醚混合物(7∶3)多次洗涤油相混合物,5 000 r/min离心10 min,沉淀物真空干燥后即得到产物。称取10 mg产物,溶于2 mL的甲醇,经0.22 μm微孔滤膜过滤后进行HPLC-MS、NMR[10-11]检测,确定其结构。
1.3.4 凝胶油的制备
将得到的产品按一定的比例与液态植物油混合,以不同的搅拌速率,在不同的温度下分别加热搅拌10 min,制得不同样品,样品冷却至室温后转移至20 ℃恒温培养箱中,静置1 d后进行检测(时间参数研究除外)。
1.3.5 凝胶油熔点测定
采用GB 24892—2010方法测定所制备凝胶油的滑动熔点(SMP)。
1.3.6 凝胶油流变学性质测定
采用Physical MCR301型流变仪测定振荡频率对上述不同条件下制得的凝胶油流变学性质的影响。分别取适量样品(约2 g),于25 ℃下测定其流变性,测定条件:2 cm椎板(1°58′47″,截距为54 μm);屈服应变0.1%(在线性黏弹区间),扫描频率0.1~10 Hz。
2 结果与讨论
2.1 合成产物检测
试验分别对反应底物和反应产物进行了HPLC分析,结果如图2所示。从图2中可以看出,底物甘露醇和辛酸的保留时间分别为(0.45±0.05)、(4.35±0.03) min;反应后多出的响应峰即为产物峰,产物的保留时间分别(3.30±0.04)、(5.60±0.06)min。由保留时间可以看出,产物2的极性相对较小,由此推测产物1为单酯,产物2为二酯。

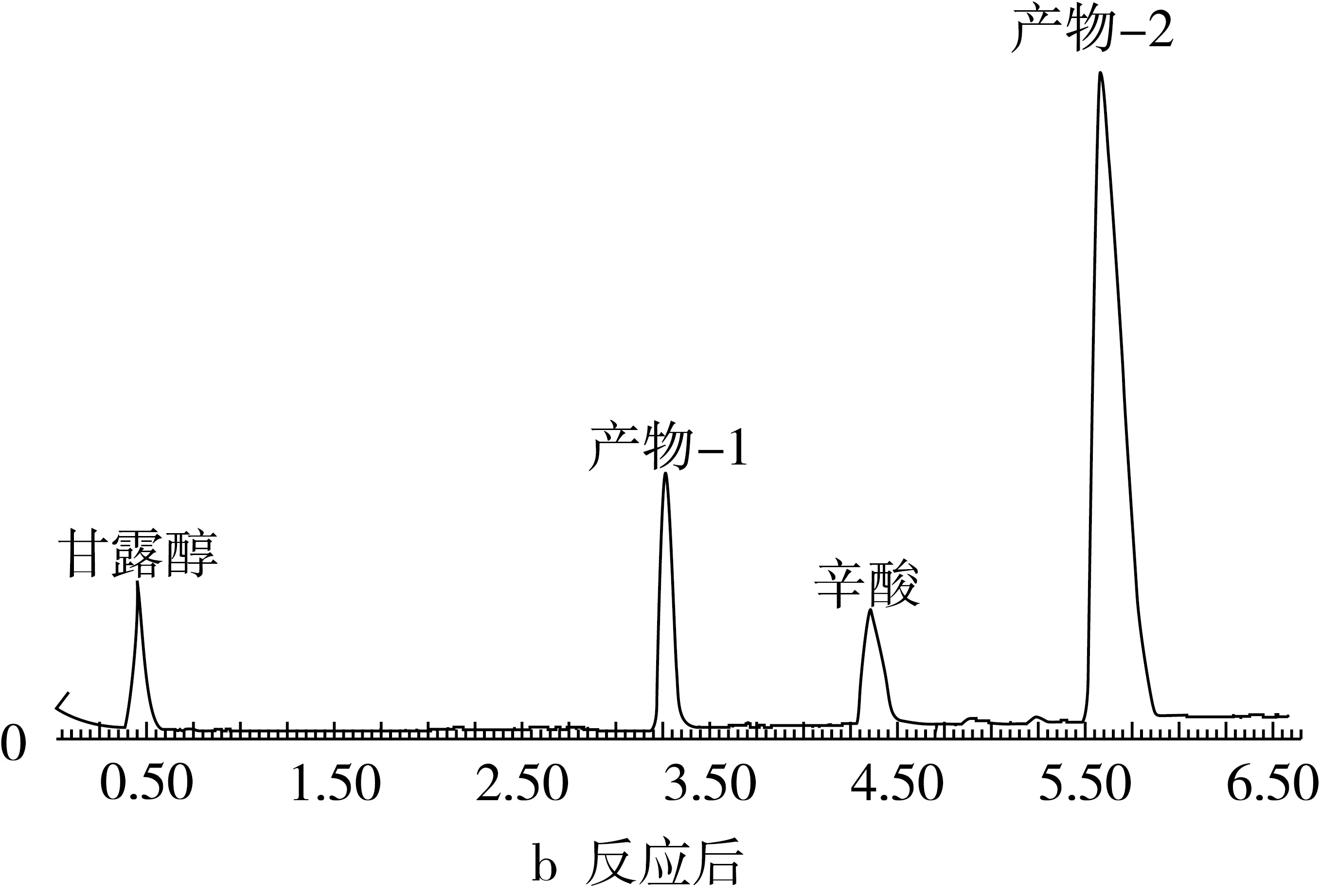
图2 合成反应前后HPLC分析图谱
2.2 产物的分离及鉴定
分离产物HPLC-MS检测结果如图3所示。液相图上只有1个峰,质谱结果显示产物离子峰m/z=433[M-H]-,而甘露醇二酯的分子质量为434,故判定质谱上的离子峰为甘露醇二酯的离子并结合1个H-。
为了进一步鉴定产物的结构,本研究对其进行NMR检测,1H、13C NMR结果为:
1H (75 MHz, CD3OD):σ0.86(t,2×3,J=6.8 Hz), σ1.32(m,2×8H), σ1.62(m,2×2H), σ2.37 (t,2×2H,J=7.3 Hz), σ3.58-4.45(m,8H);
13C NMR (75 MHz, CD3OD):σ175.87(C-8, 8’), 70.61(C-10, 10’), 70.41(C-11, 11’), 67.77(C-9, 9’), 35.02(C-7, 7’),32.86(C-6, 6’), 30.21(C-5, 5’), 30.11(C-4, 4’), 26.01(C-3, 3’), 23.67(C-2, 2’), 14.40(1, 1’)。
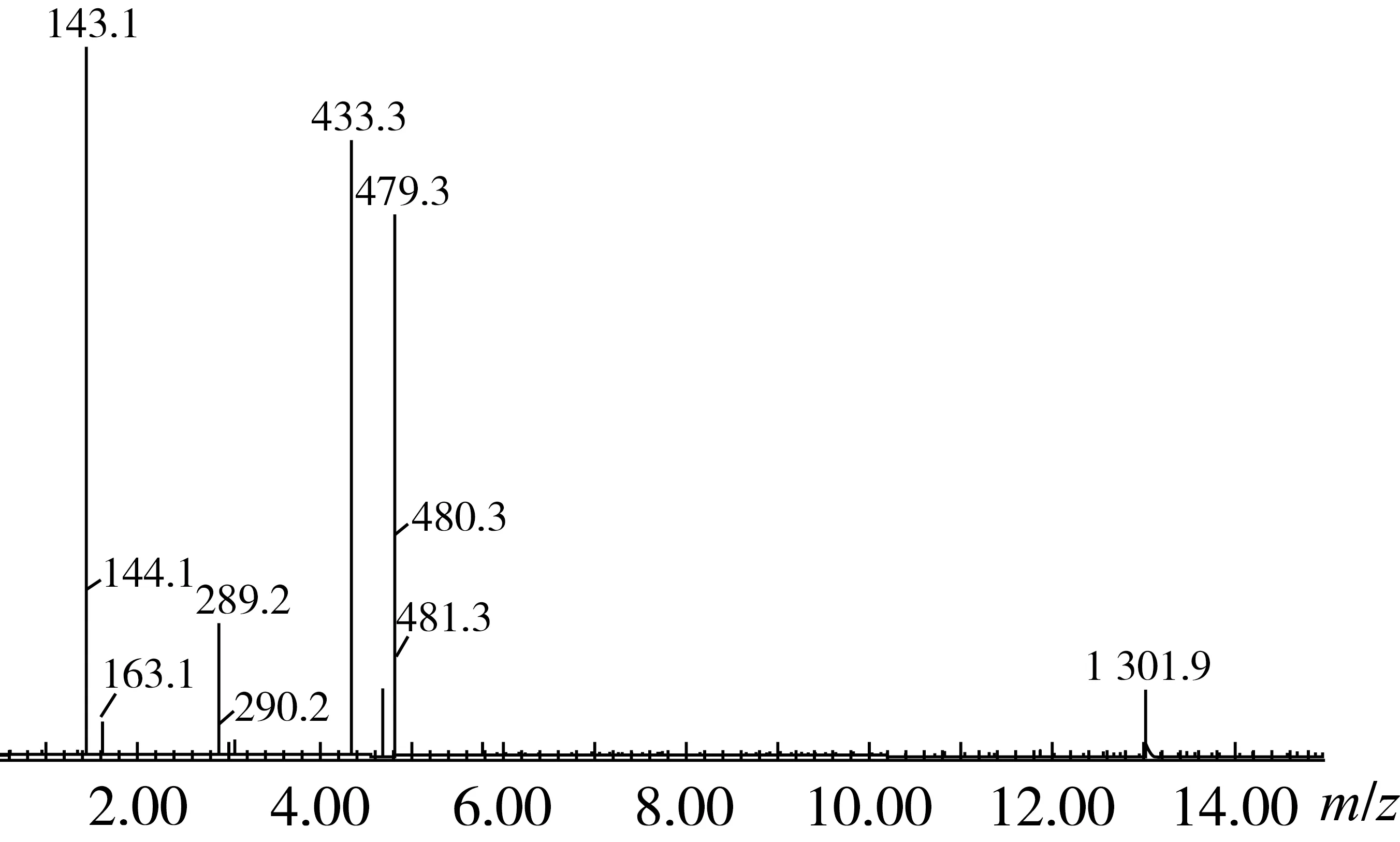
图3 甘露醇辛酸二酯的HPLC-MS图谱
由此确定产物为1,6-二辛酸甘露醇酯。甘露醇的结构为立体结构,由于空间阻力的存在,在参与酯化的过程中,其优势构象位置1,6位置参与反应的机率更大,这与Jia等[12]研究报道一致。
2.3 凝胶油的性质表征
2.3.1 甘露醇辛酸二酯最小添加量
在制备凝胶油时,凝胶剂的最小添加量常作为衡量凝胶效果的指标之一[13]。将本研究合成的甘露醇辛酸二酯添加到下列不同植物油中,最小添加量如表1所示。

表1 甘露醇辛酸二酯最小添加量
从结果可看出,所制备凝胶剂的最小添加量在不同植物油中差别较小。在橄榄油的最少添加量为0.8%,在葵花籽油的添加量达到1.0%。
2.3.2 不同加工方式对凝胶型油脂黏弹性影响
凝胶的物理强度主要体现在硬度、均匀性以及凝胶油的加工特性等方面。动态振荡流变学在一定程度上可以反映凝胶油的物理属性,其中储能模量(G′)是硬度的体现,损耗模量(G″)衡量流动性,屈服应变σy表示凝胶的韧性。在屈服应变σy处,G′急剧下降,两模量相交[14]。
2.3.2.1 不同加热温度对凝胶油流变特性的影响
本试验分析了5%凝胶剂添加量时,不同加热温度对凝胶油流变特性的影响,频率扫描结果如图4所示。从图4可知,在线性黏弹区间内,凝胶型油脂的储能模量G′以及损耗模量G″随着制备温度的升高呈现上升趋势。这说明温度的升高有助于凝胶分子的分散,从而形成更好的三维网络结构[15]。此外,不同温度下,储能模量G′占据主导地位,明显高于损耗模量G″,表明凝胶体系的固体弹性高于其黏性[16]。
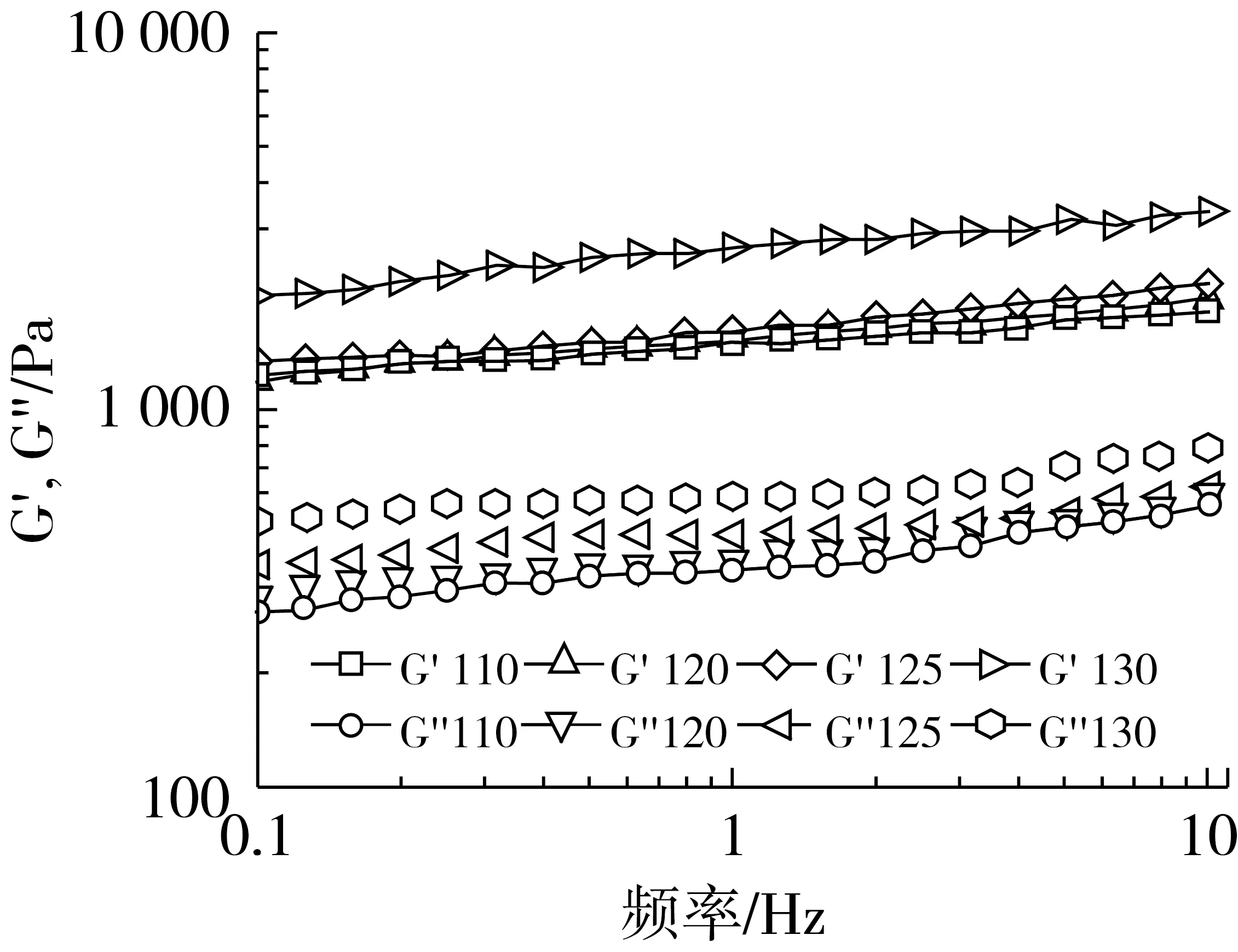
图4 加热温度对凝胶油流变特性的影响
2.3.2.2 搅拌速率对凝胶油流变特性的影响
本试验研究了5%凝胶剂添加量、130 ℃加热温度条件下,不同搅拌速率对凝胶油流变特性的影响,结果如图5所示。从图5中可看出,转速在0~500 r/min范围内,随着搅拌速率的增大,G′、G″逐渐增大;转速在500~600 r/min范围内时,G′、G″的变化不明显;而当转速大于600 r/min时,G′、G″则随着转速的增大而减小。较高的转速使得凝胶结构的定向排列受到一定限制,体系中网络结构不断破碎,这阻碍了体系形成稳定的凝胶结构。表明在一定范围内,剪切速率增加会促进凝胶的形成,然而较高的剪切作用会限制相邻结构的交联作用[17]。
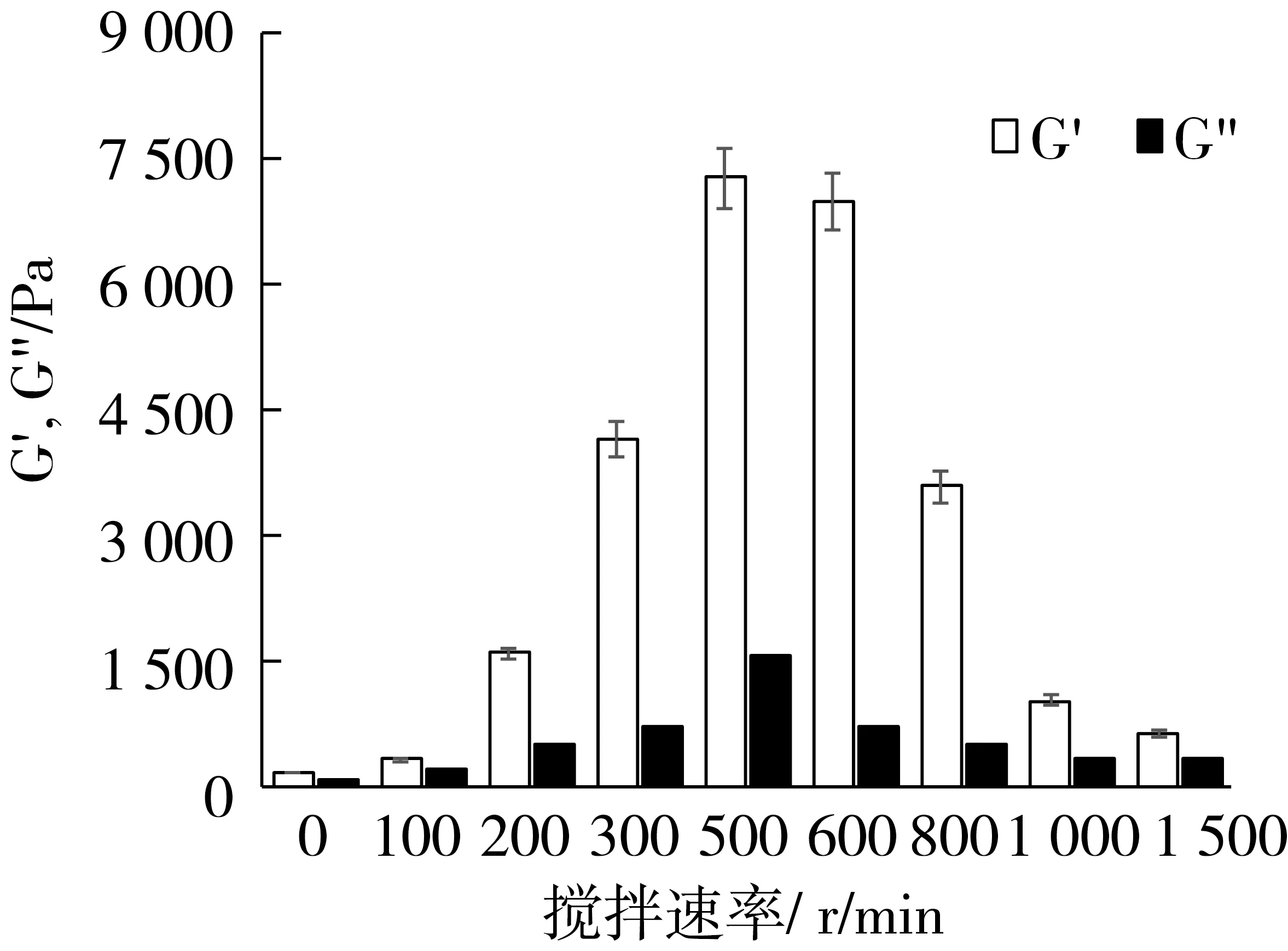
图5 搅拌速率对凝胶油流变特性的影响
2.3.2.3 不同凝胶剂添加量对凝胶型油脂流变特性的影响
由图6可知,随着凝胶剂的增加,凝胶油的黏弹性逐渐增加,且当添加量≥5%时,G′、G″均呈较好的线性增加,说明添加量在5%及以上时,凝胶体系均匀性较好,而低于5%时,体系的凝胶状态较弱。
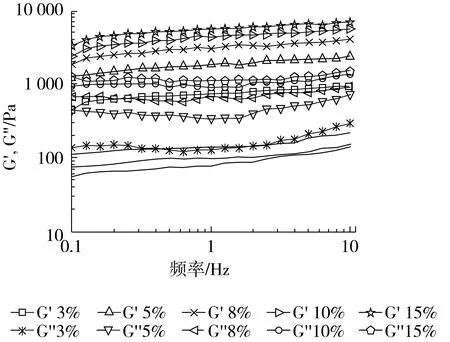
图6 不同凝胶剂浓度对凝胶油流变特性影响
此外,不同添加量对凝胶的屈服应力也有影响,结果见表2。凝胶剂添加量为3%时,屈服应变σy只有2.92,而为5%时,σ增加到4.02,随着添加量的进一步增加,屈服应力也在增加,添加量为10%时,屈服应力σy达到7.84。综合考虑,选择10%为宜。由此亦可看出,随着凝胶剂含量的增加,凝胶油的机械强度也在逐渐增加,此研究与Jadhav等[9]较为一致。
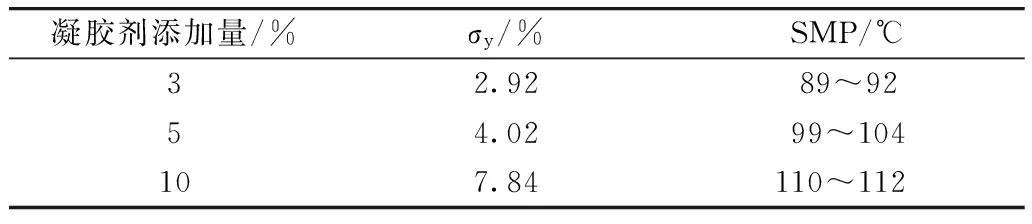
表2 不同浓度的凝胶型油脂特性
由表2可知,凝胶型油脂的滑动熔点(SMP)与凝胶剂的添加量亦呈现一定的关系:当添加量达到10%时,其SMP值达到110 ℃;添加量较低时(3%),其对应的SMP值也较低。故可以通过控制凝胶剂添加量来制备不同熔点的凝胶型油脂。Blake等[18]的研究也证实了这一点。
2.3.2.4 储藏时间对凝胶油流变特性影响
凝胶型油脂广泛应用于即食或者有一定货架期的产品中,这就要求凝胶型油脂性状在存储和运输过程中应保持其应有的理化特性。然而,很多凝胶体系,如聚合凝胶,在放置一段时间后很容易发生形态变化——老化一段时间的凝胶与新制备的凝胶表现出不同的流变特性。
表3显示了老化时间对凝胶油制备效果的影响。结果表明在2周内,凝胶油样品的黏弹性有所增加,老化2周以后的凝胶油的G′、G″基本不再变化,屈服应变也有类似的变化趋势,这表明其硬度和韧性不再发生改变。此外,2周以后的凝胶油样品的物理特性趋于平稳,这表明其凝胶体系均一、稳定性较好。
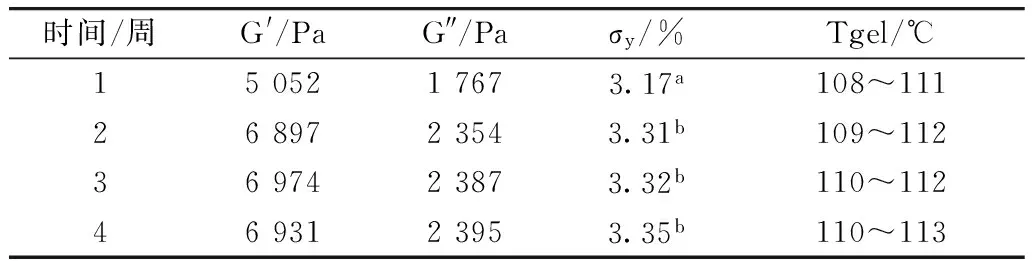
表3 不同老化时间对凝胶型油脂性状影响
3 结论
本研究使用混合溶剂正己烷、乙醚作为萃取介质,有效地去除了反应副产物及残留的底物,得到较高纯度的甘露醇辛酸酯(>90%)。采用HPLC-MS、NMR确定目标产物为1,6-二辛酸甘露醇酯。将甘露醇辛酸二酯添加到不同植物油中,当添加量为0.8%~1.0%时植物即可呈现较好的凝胶状态。不同添加量、不同加工条件对凝胶油的机械特性有显著影响,且在一定的储藏时间内,凝胶油的加工性能趋于稳定。
[1]钟金锋, 覃小丽, 刘雄. 凝胶油及其在食品工业中的应用研究进展 [J]. 食品科学, 2015(3): 272-279 Zhong Jinfeng, Qin Xiaoli, Liu Xiong. Advances in oleogels and its applications in food industry[J]. Food Sciences, 2015(3): 272-279
[2]孟宗, 孟祥永, 徐子剑,等. 零反式脂肪酸涂抹脂的制备研究 [J]. 中国油脂, 2013(10): 39-44 Meng Zong,Meng Xiangyong,Xu Zijian, et al,Preparation of zero trans fatty acid spreads[J]. China Oils and Fats, 2013(10): 39-44
[3]Filip S, Fink R, Hribar J, et al. Trans fatty acids in food and their influence on human health [J]. Food Technology and Biotechnology, 2010, 48(2): 135-42
[4]Wang Y, Proctor S D. Current issues surrounding the definition of trans-fatty acids: implications for health, industry and food labels [J]. British Journal of Nutrition, 2013, 110(8): 1369-1383
[5]Dassanayake L S K, Kodali D R, Ueno S. Formation of oleogels based on edible lipid materials [J]. Current Opinion in Colloid & Interface Science, 2011, 16(5): 432-439
[6]Hughes N E, Marangoni A G, Wright A J, et al. Potential food applications of edible oil organogels [J]. Trends in Food Science & Technology, 2009, 20(10): 470-480
[7]Hwang H S, Singh M, Winkler-Moser J K, et al. Preparation of margarines from organogels of sunflower wax and vegetable oils [J]. Journal of Food Science, 2014, 79(10):1926-1932
[8]朱小勇, 孟宗, 李进伟,等. 凝胶剂种类对凝胶油物性及结晶形态的影响 [J]. 中国粮油学报, 2013, (10): 37-43 Zhu Xiaoyong, Meng Zong, Li Jinwei, et al. Effect of gels on physical properties crystal morphologies of organogel oils[J]. Journal of the Chinese Cereals and Oils Association, 2013, (10): 37-43
[9]Jadhav S R, Hwang H, Huang Q, et al. Medium-chain sugar amphiphiles: a new family of healthy vegetable oil structuring agents [J]. Journal of Agricultural and Food Chemistry, 2013, 61(49): 12005-12011
[10]Beltrani T, Chiavarini S, Cicero D O, et al. Chemical characterization and surface properties of a new bioemulsifier produced by Pedobacter sp strain MCC-Z [J]. International Journal of Biological Macromolecules, 2015, 72,1090-1096
[11]张文斌. 甘露糖月桂酸酯的酶法选择性合成 [D]. 无锡: 江南大学, 2009 Zhang Wenbin. Enzymatically regioselective synthesis of lauryl mannoses[D]. Wuxi: Jiangnan University, 2009
[12]Jia C, Zhao J, Feng B, et al. A simple approach for the selective enzymatic synthesis of dilauroyl maltose in organic media [J]. Journal of Molecular Catalysis B-Enzymatic, 2010, 62(3-4): 265-269
[13]Hwang H S, Kim S, Singh M, et al. Organogel formation of soybean oil with waxes [J]. Journal of the American Oil Chemists Society, 2012, 89(4): 639-47
[14]Bot A, Agterof W G M. Structuring of edible oils by mixtures of gamma-oryzanol with beta-sitosterol or related phytosterols [J]. Journal of the American Oil Chemists Society, 2006, 83(6): 513-21
[15]Vintiloiu A, Leroux J-C. Organogels and their use in drug delivery-A review [J]. Journal of Controlled Release, 2008, 125(3): 179-192
[16]Rogers M A, Wright A J, Marangoni A G. Oil organogels: the fat of the future [J]. Soft Matter, 2009, 5(8):1594-1596
[17]Rogers M A, Wright A J, Marangoni A G. Nanostructuring fiber morphology and solvent inclusions in 12-hydroxystearic acid/canola oil organogels [J]. Current Opinion in Colloid & Interface Science, 2009, 14(1): 33-42
[18]Blake A I, Co E D, Marangoni A G. Structure and physical properties of plant wax crystal networks and their relationship to oil binding capacity [J]. Journal of the American Oil Chemists Society, 2014, 91(6): 885-903.
The Enzymatic Synthesis and Determination of Mannitol Dioctanoate and Its Application
Zhang Xiaohui1Meng Qingran1Zhang Lianfu1,2
(State Key Laboratory of Food Science and Technology;School of Food Sci. & Tech.,Jiangnan University1, Wuxi 214122)(National Engineering Research Center for Functional Food2, Wuxi 214122)
Lipases were catalyzed to synthesize mannitol dioctanoate, HPLC-MS was used to determine products, and mixed medium n-hexane: diethyl ether (7∶3) to extract and purify targeted products to reach the purity of over 90%. The product was identified as 1, 6-di-O-octanomannitol by HPLC-MS, and NMR analysis. Also, we tried to add it into vegetable oil to investigate processing features of gel oil with the minimum addition in different vegetable oil under different processing conditions. In structured vegetable oil preparation, 0.8%~1.8%(m/m) addition of product can form gelation. The prepared gel oil had the stable machining features under the conditions: 10%(m/m)addition of product, the stirring speed of 500 r/min, the heating temperature of 125 ℃.
mannitol dioctanoate, enzymatic synthesis, purification, structured oil, rheological measurements
教育部博士点基金(SRFDP 20130093110008)
2015-11-08
张晓慧,女,1990年出生,硕士,食品科学与工程
张连富,男,1967年出生,教授,功能性食品研究
TS22
A
1003-0174(2017)05-0057-05

