碟脉灵苦碟子注射液上市后安全性监测:一项30 233例真实世界注册登记研究
廖星 于丹丹 谢雁鸣 +张允岭 何燕 张寅 刘艳 易丹辉 王永炎


[摘要]旨在獲得碟脉灵苦碟子注射液(DML)不良反应(adverse drug reaction,ADR)发生率及其特征和影响因素以及DML真实世界中的使用情况。采用前瞻性单队列研究,历时4年在25家医院(包括中医院和西医院)观察使用该药的住院患者。通过采用频数描述方法分析病例的一般信息,用关联规则方法分析合并疾病之间以及合并用药之间的相关性,用交叉列联方法、卡方检验初步筛选不良反应的影响因素,再用Group LASSAO方法做进一步分析。结果显示,一共观察到30 233例患者,发生54例ADE,其中30例ADR。总体不良反应发生率为0099%[95%CI(006%,013%)]。ADR发生为“一般”的27例,“严重”的1例(过敏性休克),“新发”2例。ADR在用药30 min以内发生较多,共计16例。ADR多表现为心悸11例次,呕吐7例次,寒战、皮肤瘙痒、皮疹均为6例次。碟脉灵苦碟子注射液总体不良反应发生率属罕见不良反应,其安全性较好。该研究仍可能低估ADR的真实发生率,且未获取ADR患者血样,需进一步开展机制研究。
[关键词]医院集中监测; 碟脉灵苦碟子注射液; 上市后监测; 不良反应; 真实世界
Postmarketing safety surveillance of Diemailing Kudiezi injection:
real world study in 30 233 cases
LIAO Xing1, YU Dandan1, XIE Yanming1*, ZHANG Yunling2, HE Yan3, ZHANG Yin1, LIU Yan4, YI Danhui4, WANG Yongyan1
(1Institute of Basic Research in Clinical Medicine, China Academy of Chinese Medical Sciences, Beijing 100700, China;
2 Dongfang Hospital, Beijing University of Chinese Medicine, Beijing 100078, China;
3Affiliated Hospital of Chengdu University of Taditional Chinese Medicine, Chengdu 610072, China;
4 School of Statistics, Renmin University of China, Beijing 100872, China)
[Abstract]This study was aimed to obtain the incidence of adverse drug reaction (ADR) of Diemailing Kudiezi injection, explore its characteristics, related risk factors and application in real world A prospective single cohort study was conducted from 25 hospitals (including Chinese medicine hospitals and Western medicine hospitals) for 4 years 30 233 consecutive inpatients using Diemailing Kudiezi injection were observed Their general information was analyzed by using statistic frequency description Association rules were used to analyze the correlation between comorbidities or drug combinations; the influential factors for ADRs were initially screened by using cross contingency method and Chisquare test, and then Group LASSAO method was used for further analysis 54 patients with adverse drug events and 30 patients with ADRs were reported among 30 233 patients, with a total ADR incidence of 0099%[95%CI (006%, 013%)] There were 27 patients identified as the "general" ADR, one patients with "severe" ADR (anaphylactic shock) and two patients with new ADRs ADR occurred most in 30 min after using Diemailing Kudiezi injection, in a total of 16 patients The most ADRs were palpitation, vomiting, chills, pruritus and rash, 6 times for each symptom Diemailing Kudiezi injection was well tolerated in the general population The overall incidence of adverse reactions was rare, with high safety However, the real incidence of ADRs may be underestimated in this study, and the blood samples were not obtained for the patients, so further mechanism studies shall be conducted
[Key words]hospital based intensive monitoring; Diemailing Kudiezi injection; postmarketing safety surveillance; ADR; real world
苦碟子為菊科二年苦荬菜属植物,学名抱茎苦荬菜Ixeris sonchifolia(Bge)Hance,收录于《内蒙古中草药》。蝶脉灵苦碟子注射液为抱茎苦荬菜提取物加工制备而成,其说明书显示该药具有活血止痛,清热祛瘀的功效,使用方式为静脉滴注,每次10~40 mL,用5%葡萄糖或09%氯化钠注射液稀释至250~500 mL后应用。该药1998 年上市,属于我国医保乙类药物。广泛运用于治疗冠心病、心绞痛、脑梗死等。目前国内有 2 家公司生产苦碟子注射液,均有国药准字号。蝶脉灵苦碟子注射液虽为单味药制剂,但其成分也较为复杂。已有研究显示,苦碟子中主要有核苷、有机酸、黄酮和倍半萜内酯 4 大类成分[1]。早在1977—1984年期间,由中国人民解放军第二○四医院和辽宁省药物研究所药理研究室开展了一系列该药在冠心病(缺血型)治疗方面的机制和临床研究,发现该药扩张冠状血管,改善心肌血氧供应,增加纤维蛋白溶解酶活性,抑制血栓形成,并且在临床观察中对缺血型冠心病和脑梗死(脑血栓)也有积极治疗作用[212]。长期以来有关该药的机制和临床研究一直未有间断,主要用于冠心病心绞痛的治疗[13],脑梗死的治疗[14]。近年来,针对该药治疗脑血管的机制研究逐渐增多,发现蝶脉灵苦碟子注射液可能通过抑制PKCδ/MARCKS通路,保护血管内皮细胞的缺氧损伤[15] ;可有效改善急性脑梗死患者血清VEGF,S100β,MMP9水平,促进神经功能恢复,提高生活质量[16];可降低急性脑梗死患者的血清炎症因子(hsCRP,IL18)的含量[17]。相关系统评价也显示蝶脉灵苦碟子注射液对于冠心病心绞痛[1819]和急性脑梗死[2021]有较好疗效。然而,近年来,有关蝶脉灵苦碟子注射液所导致的不良反应时有报告,近期1项“苦碟子注射液用药安全性的系统评价”[22]分析发现:25 个ADR病例报告的25名患者中有11例严重不良反应,14例中轻度不良反应;另外还有297个不同研究类型17 140例苦碟子注射液患者中305例发生ADR/AE,以中枢及外周神经系统损害报告最多,表现主要是头晕、头昏、头胀及头痛。既往也有在真实世界中针对该药疑似不良反应的探索性研究,比如对用药后肝肾功能的改变[2324]以及疑似过敏反应[25]等,还有来自国家自发呈报系统的相关分析性研究[26]。但这些研究报告,均是事后分析,其中ADR发生的因果关系的确定性有待商榷。既往并无有关以获得蝶脉灵苦碟子注射液ADR发生率的前瞻性研究。为此,开展一项针对碟脉灵苦碟子注射液不良反应发生情况的大样本长期随访医院集中监测研究非常有必要[27]。现将本研究团队前期开展的一项旨在明确碟脉灵苦碟子注射液不良反应发生率,明确其不良反应临床特征,探讨其不良反应发生影响因素,掌握其真实世界临床用药情况的大样本长期医院集中监测研究结果报告如下。由于有关该研究的方案已发表[27],故重复内容不再在此赘述。
1基本概况分析
11监测研究过程总结本监测研究严格按照研究设计方案,经历严格的三级质量控制,对监测期间所有使用碟脉灵苦碟子注射液的住院患者进行资料的收集。所有患者均在使用碟脉灵注射液的第1天填写《碟脉灵注射液监测A表》,在用药期间如果发生疑似不良反应/不良事件,在经临床一线医生判断后,填写《碟脉灵注射液监测B表》,如果发生了过敏反应,则尚需匹配4例阴性患者,并抽取血样。具体流程见图1。
12监测人群基本特征分析2012年10月1日监测第1例病例,到2015年6月30日监测第30 233例病例,并于2015年8月1日结束监测。全国10 个省市,25家医院加入本研究,其中西医院14家,中医院11家;三级(或甲等)医院17家,二级(或甲等)医院8家。医院所在地域以西南和华北为主,分别为15 031例(4972%)和9 471例(3133%)。
基于A表分析所监测的30 233例患者,其中男性14 949例,女性15 284例;西医医院患者数量(19 463例,占6438%)多于中医医院(10 770例,占3562%);三级医院患者数量(25 288例,占8364%)多于二级医院(4 945例,占1636%);2 553例(844%)有过敏史,其中药物过敏史占大多数(2 413例,占9452%),其中药物又以西药过敏为主(2 264例,9383%);4例(001%)有家族过敏史。使用碟脉灵注射液的患者主要是老年人群,年龄中位数为62岁。该药的使用人群主要以46~65岁(4292%)、66~80岁(3002%)人群为主,即以中老年为主。
30 233例患者为监测医院中监测期内所有处方使用碟脉灵苦碟子注射液的住院患者和部分门诊患者。总的来说,西医诊断以碟脉灵苦蝶子注射液说明书适应症为主,如冠心病8 780例(2904%)、脑梗死7 407例(2450%),也有用于说明书以外疾病者,如特发性(原发性)高血压、其他椎间盘疾患、下肢静脉曲张等;中医诊断以缺血性中风(2 797例,占925%)、胸痹(2 662例,占880%)为主;说明书中规定,碟脉灵苦蝶子注射液可活血止痛,清热祛瘀,适用于瘀血闭阻证。因此将带含“瘀”和“热(火)”的证候进行统计发现:仅含“瘀”4 767例次(4307%)、含“热”或“火”1 747例次(1578%)。
13监测人群用药情况分析碟脉灵苦蝶子注射液的用法以静滴为主(30 218例,占9995%),单次用量以31~40 mL居多(20 569例,占6803%);注射持续时间以05~2 h居多(26 856例,占8885%);溶媒类型以09%氯化钠注射液(21 927例,占7253%)为主;溶媒用量不少于250 mL(29 830例,占9868%);注射室温平均在2186 ℃;配液放置时间平均在2488 min;滴速平均在4746滴/分;用药天数中位数为8 d。
以每个個体患者为单位,将其住院期间所有的其他药物使用情况进行合并来看,合并用药西药(25 841例次,占8547%)多于中药(9 351例次,占3093%)。从药理作用来看,西药的合并用药主要是神经细胞活化剂及营养药物、β受体阻滞剂、血小板聚集抑制药,占比高达6124%。
由于该药是静脉注射用药,因此本研究在设计之初特别关注了和其合并使用的其他注射剂的分析。注射前使用其他注射剂17 653例,其中以西药居多14 170例次,占7907%,如神经细胞活化剂及营养药物、抑制胃酸分泌药、β受体阻滞剂等,而中药则以祛瘀剂居多;注射中(2种或2种以上药物不同通路同时使用)使用其他注射剂194例,其中以西药居多177例次,占8985%,如主要为扩张血管、钙离子通道阻滞、β受体阻滞剂、降低血中纤维蛋白原等,而中药则以祛瘀剂居多;注射后使用其他注射剂15 113例,其中以西药居多12 345例次,占8056%,如主要为神经细胞活化剂及营养药、抗血小板聚集、抑制胃酸分泌药等,而中药则以祛瘀剂居多;另外还特别分析了注射期间配置使用(与其他药物配置在1个输液袋/瓶里)其他注射剂的情况,577例患者与其他药物配置使用,以西药居多579例次,占9797%,以降糖药、脑功能改善药、水电解质酸碱平衡调节药等为主,而中药则以祛痰药居多。
2ADR/ADE发生情况分析
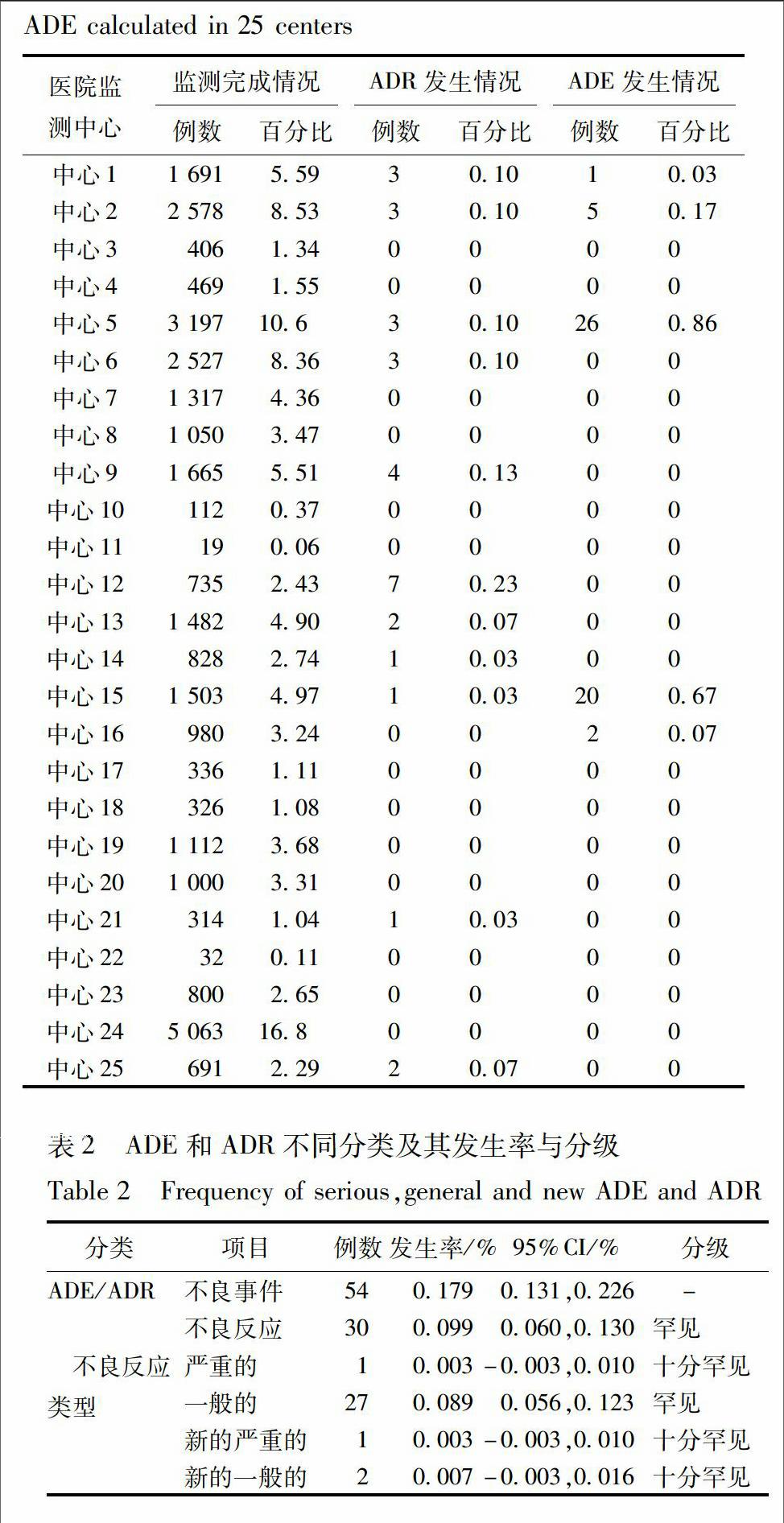
2125个中心监测完成及ADR/ADE发生情况中心24监测样本量最大,却无ADR或ADE报告,而中心12监测数为735,监测到7例ADR,见表1。
2284例ADR/ADE的分析本监测中所发现的84例ADR/ADE,经过三级临床专家判读,按照国家食品药品监督管理总局药品安全监管司、国家药品不良反应监测中心2005年9月发布的《药品不良反应报告和监测工作手册》推荐的关联性评价,来确定不良事件与药品之间的关系,最终确定ADR 30例,54例ADE中,有25例为死亡病例。ADR和ADE发生率的计算以及ADR不同分类后发生率,见表2。从表2可知,本监测研究总体不良反应发生率为0099%,按泊松分布估计碟脉灵苦蝶子注射液ADR发生率的95%CI(006%,013%),按照
“国际医学科学组织委员会”(CIOMS)有关ADR发生频率分级,属于罕见[28];总的不良事件发生率为0179%[95%CI(0131%,0226%)]。
ADR表现涉及系统主要是全身性损害,有17例次,占5667%。ADR发生类型为一般的共27例,严重ADR 1例(过敏性休克),新发2例。ADR以用药30 min以内发生较多,共16例,占5333%。30个ADR病例中,共有70例次的ADR表现,其中多见的为:心悸11例次,呕吐7例次,寒战、皮肤瘙痒、皮疹均为6例次;所累及系统以全身性损害17例次,皮肤及其附件损害13例次,心率及心律紊乱11例次,交感和副交感神经系统损害10例次较多。新发一般ADR主要有:上消化道出血、大便潜血阳性、腹部烧灼不适、腹泻、肝功能异常、巩膜黄染、黑便、皮肤紫斑、双眼发干,均为1例次。30例ADR患者的具体表现及其发生率见表3。
本监测研究中所发现的碟脉灵苦碟子注射液ADR表现主要是心悸、呕吐、寒战、皮肤瘙痒、皮疹,见表4。
另外,从ADR的发生来看,中医院ADR发生率(0066%)比西医院(0033%)高,三级医院(0076%)明显高于二级医院(0023%),女性ADR发生率(0069%)比男性(0030%)高,65~80岁人群ADR发生较多,共计16例,占5333%。30例ADR患者中,17例证候中含有“瘀”或“热”,属于符合说明书辨证用药。30例ADR患者均有合并用药,且均合并有西药。ADR人群在使用碟脉灵苦蝶子注射液的同时,氨溴索与头孢美唑的相互联合用药较常见,或以血小板聚集抑制药与抗血栓形成药的相互联合用药较常见。
23对ADR发生的影响因素探索性分析
列联分析的结果提示,以下因素两两组合容易导致使用碟脉灵苦蝶子注射液时发生ADR:用药疗程1~2 d且剂量为31~40 mL的人群;高浓度且滴速在0~60滴/min的人群;较高浓度且滴速在0~60 滴/min的人群;高浓度且剂量为21~30 mL
人群;滴速为0~60 滴/min且合并用药药理为β内酰胺类抗生素的人群;女性且不辨证的人群。
基于SMOTE+Group LASSO的影响因素筛选分析结果提示:①主效应分析显示:年龄≤18岁患者、性别为女、有过敏史、疗程短(1~2 d)、合并用药为氨溴索、小牛血去蛋白提取物、其他溶媒(除去10%葡萄糖、09%氯化钠注射液、5%葡萄糖注射液外的溶媒)、溶媒为10%葡萄糖的患者发生ADR倾向较其他可能的影响因素大。②交互效应显示:有过敏史、不冲管、不符合适应症、10%葡萄糖、溶媒为其他(为木糖醇注射液)、合并用药为天麻素注射剂、合并用药为泮托拉唑钠注射剂、合并氨溴索、合并小牛血去蛋白提取物、合并前列地尔、疗程为1~2 d、高剂量>40 mL;用药浓度较高和高的且不冲管的人群、用药浓度较高且不符合适应症、用药浓度高且合并用药为其他、注射前不冲管且合并使用天麻素注射剂;注射前不冲管且合并使用泮托拉唑钠注射剂、非适应症且使用其他溶媒、非适应症且合并使用天麻素注射剂可能更容易导致ADR发生。
3讨论
31医院集中监测研究符合国家当下重点监测需求我国已建立起上市后药品不良反应监测和上市后药品安全性研究的体系,目前,重点监测是我国药品上市后监测中的一项重要的工作,旨在加强我国上市后药品的监管力度[29]。2013 年3月,CFDA 药品安全监管司发布了《关于推动生产企业开展药品重点监测工作的通知(征求意见稿)》,并制定了《生产企业药品重点监测工作指南》(以下简称《指南》),以指导企业开展药品重点监测工作。《指南》中提及“药品重点监测”,是指为进一步了解药品的临床使用和不良反应发生情况,研究不良反应的发生特征、严重程度、发生率等,开展的药品安全性监测活动。同时,《指南》又提出“药品重点监测主要是观察上市后药品在广泛人群使用情况下的不良反应”。 鉴于常规监测存在的局限性,药品重点监测在现有安全性监测领域中具有重要作用,如能弥补上市前研究的空白,也是真实世界研究的具体体现[30]。据此,本研究团队结合5年的中药上市后再评价研究经验,于2016年12月发布了1项中华中医药学会团体标准《中成药上市后安全性医院集中监测技术规范》(T/CACM0112016),并重点提出了隶属“药品重点监测”的“医院集中监测”。而碟脉灵苦碟子注射液医院集中监测研究是践行该技术规范的首批品种之一。该监测研究历时4年多,样本量达到30 233例,且涉及地域范围较广,通过主动监测模式,以研究机构为主导,医院为研究主体,药品生产企业积极参与配合,对于该药品的安全性评价以及临床安全用药,起到了良好的促进作用。
32对于监测结果的解读碟脉灵苦碟子注射液总体不良反应发生率为0099%,属罕见不良反应。对ADR发生的影响因素开展了层层递进的探索性分析:首先单独对比了各可能的影响因素之间ADR发生率的区别,寻找差异较大的因素;其次开展了交叉列联分析,探索了各可能的影响因素在不同的前提条件下ADR发生率的差异;最后基于SMOTE+ Group LASSO筛选影响因素,分析主效应及交互效应。结果提示性别、有过敏史、合并氨溴索、前列地尔可能是碟脉灵苦蝶子注射液发生ADR的影响因素或保护因素。需要说明的是,由于监测数据属于不平衡数据,以上的分析方法并不能得到确定性结论。另外,虽然本研究为主动监测模式,且在监测过程中,对参与监测的一线人员进行了ADR/ADE判断和上报程序的培训,但仍然不能排除漏报等问题,因此可能低估ADR实际发生率。再有,本研究未能获得ADR患者血样,进一步开展机制研究,故不能从机制层面进行更加明确因果关系判定。
本监测研究在一定程度和范围上,进行了比较全面且长周期的药品使用情况和安全性信息的收集,对于观测对象的纳入条件并未做过多限定,因此可能存在难以控制的偏倚和混杂。本监测数据来自单队列,未设立对照,且分析多以描述性分析为主,因此结果的实用性有一定局限性,其验证性的结论需要通过进一步设计专门的安全性研究来获得。
4结论
通過本次监测研究,在一定时间和范围内明确了碟脉灵苦蝶子注射液总体ADR发生率、发生特征以及各ADR症状的发生率,对为完善碟脉灵注射液药品说明书、制定ADR处理预案,以及促进临床合理用药具有明确的意义。但由于ADR例数较少,虽然基于数据特点采取了针对性的分析方法,但是对于ADR影响因素的分析仍无法得到确定性结论,临床应用应谨慎。
本次监测虽然获得30例有关碟脉灵苦蝶子注射液的ADR病例,并计算ADR发生率,但是考虑到大量不可控混杂因素的存在,有关该品种的安全性评价研究结果具有一定的局限性,应继续开展全生命周期的安全性监测,并重点分析观测到的严重不良反应和超说明书后的ADE情况。未来临床医生在临床使用中应注意符合说明书用药,如辨证使用。对于可疑的ADR影响因素应该在临床实践中加以关注,尽量在最大程度上避免发生ADR。
[参考文献]
[1]刘颖,卢建秋,张加余,等 苦碟子药材及其注射液中化学成分的HPLCESIMSn分析[J]中国中药杂志,2013,38(16):2675
[2]冯玉书,桂绿荷,徐暑民,等 苦碟子治疗冠心病的研究—9苦碟子及其有效成分腺苷对狗急性心肌梗塞和心肌代谢作用[J] 沈阳药学院学报,1984(1):21
[3]胥玉绂 苦碟子治疗冠心病的研究—10碟脉灵治疗脑血栓形成30例疗效观察[J]沈阳药学院学报,1984(1):28
[4]桂绿荷,冯玉书,李萍,等 苦碟子治疗冠心病的研究—11苦碟子对微循环作用的影响[J] 沈阳药学院学报,1984(1):33
[5]冯玉书,栗砚芬,葛众,等 苦碟子治疗冠心病的研究—7苦碟子及其有效成分腺苷对实验性心肌梗塞和心肌代谢作用的研究[J]沈阳药学院学报,1982(16):30
[6]冯玉书,桂绿荷,林国云 苦碟子治疗冠心病的研究—8苦碟子对小鼠氧代谢和家兔脑循环的影响[J]沈阳药学院学报,1982(16):40
[7]孟宪贞,倪素芳,索鸿勋 苦碟子治疗冠心病的研究—6苦碟子扩冠有效成分的分离与鉴定[J]沈阳药学院学报,1981(14):32
[8]桂绿荷,冯玉书,徐署民,等 苦碟子治疗冠心病的研究—4苦碟子对血小板聚集作用的影响[J]沈阳药学院学报,1981(13):18
[9]冯玉书,桂绿荷,徐署民,等 苦碟子治疗冠心病的研究—5苦碟子对纤维蛋白酶活性影响和毒性研究[J]沈阳药学院学报,1981(13):23
[10]冯玉书,桂绿荷,商晓华,等 苦碟子治疗冠心病的研究—2苦碟子注射液对心血管系统的某些药理作用[J] 沈阳药学院学报,1978(9):1
[11]张彬文 苦碟子治疗冠心病的研究—3苦碟子注射液(碟脉灵)治疗冠心病107例临床观察[J]沈阳药学院学报,1978(9):12
[12]中国人民解放军第二0四医院,辽宁省药物研究所药理研究室 苦碟子注射液对狗冠脉流量及心肌耗氧量的影响[J] 沈阳药学院学报,1977(8):22
[13]李连广,董瑞祥,仲苏媛,等 应用随机双盲法观察苦碟子注射液治疗冠心病心绞痛的疗效[J] 解放军医学杂志,1989,14(1):30
[14]叶晓勤,魏戌,谢雁鸣,等 苦碟子注射液治疗缺血性中风急性期上市后再评价[J] 中国中药杂志,2011,36(20):2793
[15]杨嘉颐,于佳澜,戴中,等 苦碟子注射液对缺氧损伤血管内皮细胞PKC δ/MARCKS通路的调节[J] 北京中医药大学学报,2017,40(3):214
[16]李增攀,周挺,蒋黎 苦碟子注射液用于急性脑梗死的临床评价及对患者血清VEGF、S100β、MMP9水平的影响[J] 中国生化药物杂志,2017,37(3):141
[17]周芸,刘德军 苦碟子注射液对急性脑梗死患者血清炎症因子、疗效及生活质量的影响[J] 中华中医药学刊,2016(4):900
[18]韩燕鸿,张荷 苦碟子注射液治疗不稳定型心绞痛的系统评价[J] 中国实验方剂学杂志,2016,22(11):189
[19]何志超,严惠明,李国成,等 苦碟子注射液治疗冠心病心绞痛的Meta分析[J] 中成药,2014,36(2):253
[20]薛斐然,华国栋,张彦丽,等 苦碟子注射液联合奥扎格雷钠注射液治疗脑梗死有效性的系统评价[J] 中华中医药杂志,2014(6):1797
[21]刘姣,夏芸,路遥,等 苦碟子注射液治疗急性脑梗死的系统评价[J] 北京中医药,2013(7):497
[22]崔瑞昭,谢雁鸣,廖星,等 苦碟子注射液用药安全性的系统评价[J] 中国中药杂志,2017,42(12):2380
[23]廖星,唐浩,谢雁鸣,等 真实世界中苦碟子注射液不同使用剂量对肝肾功能指标变化影响的分析[J] 中国中药杂志,2014,39(18):3585
[24]廖星,张辉,谢雁鸣,等 真实世界中苦碟子注射液不同疗程对肝肾功能指标变化影响的分析[J] 中国中药杂志,2013,38(18):3084
[25]廖星,曾宪斌,谢雁鸣,等 基于巢式病例对照研究苦碟子注射液疑似类过敏反应病例相关影响因素分析[J] 中国中药杂志,2014,39(18):3559
[26]阎博华,成彭,谢雁鸣,等 基于SRS的苦碟子注射液(碟脉灵) ADR信号分析决策树和神经网络模型比较研究[J] 时珍国医国药,2016,27(2):455
[27]廖星,谢雁鸣,王桂倩 一项大样本长期随访医院集中监测研究实施方案的解析—碟脉灵苦碟子注射液为例[J] 中国中药杂志,2016,41(24):4494
[28]CIOMS Working Group V Current challenges in pharmacovigilance: pragmatic approaches 2001[EB/OL]. [20170624]. http://clinicalsafetygeekcom/wpcontent/uploads/2013/08/Group5_Pharmacovigilancepdf
[29]蔡婷,闫磊,刘述森,等 我国药品上市后重点监测相关问题的探讨[J] 药物流行病学杂志,2017,26(5):297
[30]王丹,董铎 我国开展药品重点监测工作的探讨[J] 中国药物警戒,2015,12(9):534
[31]李志强,詹君,常艳鹏,等 苦碟子注射液安全性再评价中的急毒及长毒研究[J] 中国中药杂志,2012,37(18):2828
[责任编辑张燕]

