聚三聚氰胺修饰玻碳电极测定食品中叔丁基对苯二酚
马心英, 朱琪, 张和平
(菏泽学院 化学化工系,山东 菏泽,274015)
分析与检测
聚三聚氰胺修饰玻碳电极测定食品中叔丁基对苯二酚
马心英*, 朱琪, 张和平
(菏泽学院 化学化工系,山东 菏泽,274015)
采用电化学聚合方法制备了聚三聚氰胺膜修饰玻碳电极(poly melamine film modified glassy carbon electrode,PMel/GCE),并采用循环伏安法研究了抗氧化剂叔丁基对苯二酚(tert-butylhydroquinone,TBHQ)在修饰电极上的电化学行为,发现其氧化还原峰电流较在玻碳电极(glassy carbon electrode,GCE)上明显增强,提高了检测的灵敏度。对三聚氰胺电化学聚合时间、扫描速率、电压、段数以及测定TBHQ溶液的pH值等实验条件进行了优化。在最佳的条件下,TBHQ在4.00×10-7~1.00×10-4mol/L内与其氧化峰电流呈线性关系,相关系数:R=0.997 5,检出限为2.00×10-9mol/L。将修饰电极用于食品中TBHQ的检测,回收率在96.9%~102.2%之间。
三聚氰胺;玻碳电极;叔丁基对苯二酚
叔丁基对苯二酚(tert-butylhydroquinone, TBHQ)是一种合成酚类强抗氧化剂化合物[1],常作为防腐剂用于食用油、油炸面制品、熟制坚果与籽类、腌腊肉制品,风干、压干、烘干等水产品和膨化食品中[2]。美国食品药品管理局(U.S. Food and Drug Administration,FDA)和欧洲食品安全局(European Food Safety Authority, EFSA)已对TBHQ进行评估,认为在规定的限量内使用TBHQ作为食品添加剂是安全的。中国于1991年批准使用TBHQ[3]。在GB2760—2014《食品安全国家标准食品添加剂使用标准》中规定,TBHQ在油炸面制品中的最大使用限量为0.2 g/kg,油炸肉制品中禁止检出[4]。但TBHQ的安全性近年来引起人们关注,并存在争议[5-6]。研究表明, 化学合成抗氧化剂如果不按规定使用,会对人体产生潜在的危害[7],动物实验表明,食用过量的TBHQ会对健康产生负面影响,存在患胃肿瘤风险或对脱氧核糖核酸(deoxyribonucleic acid,DNA)造成损伤[8]。因此,有必要建立简单、准确、灵敏的分析方法对TBHQ进行检测。
目前,检测TBHQ分析方法主要有傅里叶变换红外法[9]、气相色谱法(gas chromatography,GC)[10-11]、高效液相色谱法(high performance liquid chromatography, HPLC)[12],以及电化学方法[13-15]。HPLC和 GC过程繁琐,耗费试剂,检测成本高,检测时间长。而电化学分析方法快速、灵敏、选择性好、预处理程序简单、样品分析所需时间短、成本低等优点。抗氧化剂通过电子转移来清除氧自由基的过程类似于在电极上发生了氧化还原反应,可通过电化学方法对其进行检测。
聚三聚氰胺具有良好的电催化特性和较大的比表面积,是一种良好的电极表面修饰材料,在电化学领域的具有较好的应用前景,但少有文献报道将其用于玻碳电极的电化学修饰[16]。本实验通过电化学聚合的方法将聚三聚氰胺薄膜(poly melamine film,PMel)修饰在玻碳电极(glassy carbon electrode,GCE)的表面,制备成具有高导电性能的聚三聚氰胺膜修饰玻碳电极(poly melamine film modified glassy carbon electrode,PMel/GCE)电极,并研究了TBHQ在修饰电极上的电化学行为。该方法具有操作简单、灵敏度高、线性范围宽和选择性好等优点,已用于食品中TBHQ检测,结果满意。
1 材料与方法
1.1仪器与试剂
电化学工作站(CHI660D),上海辰华仪器有限公司);三电极体系:饱和 Ag/AgCl电极为参比电极,铂丝电极为对电极,GCE或PMel/GCE为工作电极;KQ-100型超声波清洗器,昆山市超声仪器有限公司;石英亚沸高纯水蒸馏器(SYZ-550),金坛市江南仪器厂);微量进样器;循环水式三抽头多用真空泵(SHZ-CB),河南省豫章实业有限公司;定量滤纸(Φ12.5 cm),杭州特种纸业有限公司。
1.0 mmol/L的三聚氰胺溶液(0.1 mol/L H2SO4新配),Sigma-Aldrich;1.0×10-3mol/L的TBHQ标准溶液(aladdin),阿拉丁试剂有限公司;无水乙醇,莱阳经济技术开发区精细化工厂;不同pH的磷酸盐缓冲溶液(sodium hydrogen phosphate-citric acid buffer solution, PBS)均用0.2 mol/L Na2HPO4和0.1 mol/L 柠檬酸配制;食用油、手指饼和锅巴,购自超市。所用试剂均为分析纯,实验用水均为二次石英亚沸蒸馏水。
1.2样品处理
锅巴样品: 称取10.00 g食品样品锅巴,粉碎,用10 mL无水乙醇将样品溶解,超声5 min后,用真空泵抽滤,得滤渣,在滤渣中再加10 mL无水乙醇,重复处理,合并2次的滤液,于25 mL容量瓶中配制成锅巴样品溶液。
手指饼样品处理方法同锅巴。
食用油样品: 称取5.00 g样品置于离心管中,加入10 mL乙腈,涡旋振摇1 min,离心5 min,吸取上层乙腈溶液,转移到50 mL离心管中。按同样方法重复处理两次,合并上层乙腈溶液,用乙腈定容至刻度。
1.3聚三聚氰胺修饰电极的制备
将玻碳电极用氧化铝悬浮液在麂皮上抛光,在硝酸(1∶1)、无水乙醇和二次蒸馏水中分别超声清洗30 s,再用蒸馏水冲洗干净。然后对电极进行清洗和活化:在0.1 mol/L KCl的5.0 mmol/L K3[Fe(CN)]6溶液中将电极进行循环扫描,当峰电流基本稳定,电流差小于80 mV时,取出电极清洗吹干。将电极置于含1.0 mmol/L的三聚氰胺的硫酸溶液中,扫描速度为40 mV/s,在-2.3~2.1 V电位范围内,用循环伏安法(cyclic voltammetry,CV)循环扫描24段,取出电极清洗待用。
1.4实验方法
取一定体积的TBHQ 标溶液(pH=5.0的PBS配制),将三电极体系置于标准液中进行循环伏安或差分脉冲伏安法进行扫描,研究TBHQ在PMel/GCE修饰电极上的电化学行为并优化实验条件,记录伏安曲线。
2 结果与讨论
2.1TBHQ的电化学行为
图1所示分别为PMel/GCE测定空白溶液(a)、TBHQ在玻碳电极(b)和在PMel/GCE (c)上的循环伏安曲线,由图1中的b可见,TBHQ在裸电极上的氧化峰、还原峰电流较小,ipa=-1.77 μA,ipc=1.38 μA,而在PMel/GCE上的氧化峰、还原峰电流增大较为明显(图1中的c),ipa=-9.38 μA,ipc=11.0 μA,TBHQ在PMel/GCE上氧化峰电流、还原峰电流分别是在玻碳电极上的5.3倍、7.8倍,一定程度上提高了测定的灵敏度。说明三聚氰胺修饰膜对TBHQ电化学氧化还原具有一定的催化作用,使其电子传递速率加快。TBHQ在PMel/GCE上氧化还原峰电位分别为Epa=0.26 V,Epc=0.15 V,比较其ipa/ipc及ΔE值得出:ipa/ipc=0.85,ΔE=0.11 V,因此该反应为准可逆反应,由此推断TBHQ在电极上可能的氧化还原过程[8],(见图2)。

图1 三聚氰胺修饰玻碳电极测定空白溶液(a)、TBHQ在玻碳电极(b)和在三聚氰胺修饰玻碳电极(c)上的循环伏安曲线Fig.1 Cyclicvoltammograms of PMel/GCE in PBS (pH=5.0) (a), TBHQ at bare GCE (b) and PMel/GCE (c)
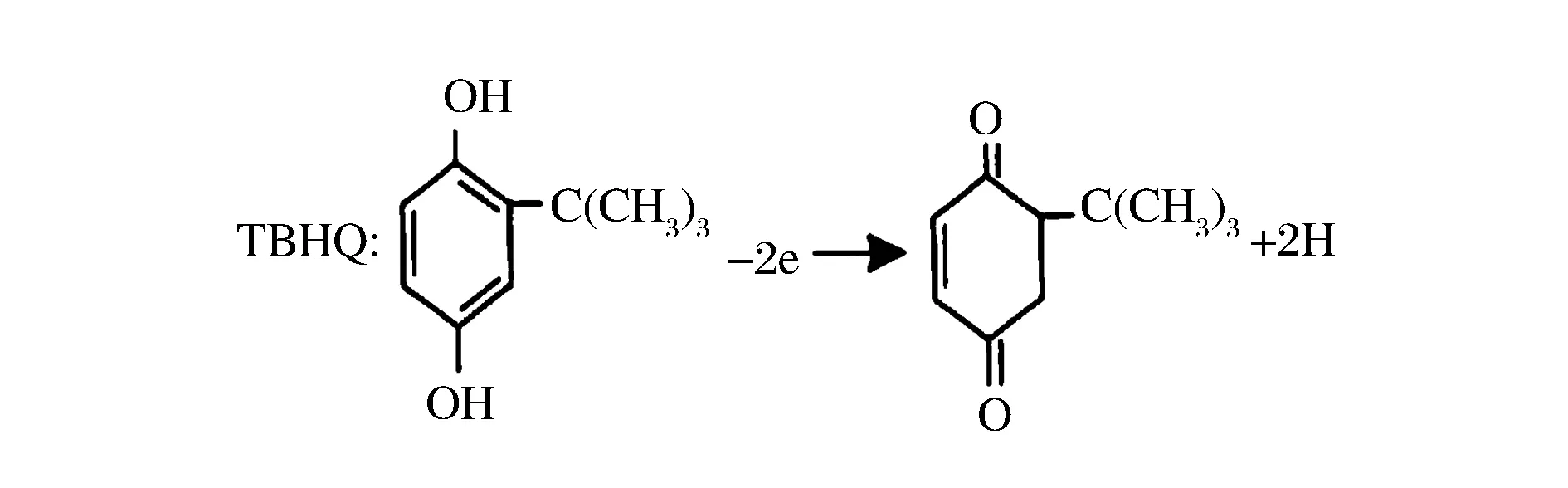
图2 TBHQ在修饰电极上的氧化机理Fig.2 The oxidation mechanism of TBHQ at the modified electrode
2.2修饰电极最佳电化学聚合条件
实验结果表明,修饰电极的制备条件影响着修饰电极的性能及灵敏度。讨论了电极制备过程中扫描段数、聚合电位范围、扫描速度对PMel/GCE测定TBHQ的影响。结果表明,固定三聚氰胺溶液浓度为1.0 mmol/L,当扫描段数为24段,聚合电位范围为-2.3~2.1 V,扫描速度为40 mV/s时,所制备的PMel/GCE测定TBHQ的电流最大。
2.3聚三聚氰胺修饰电极的聚合循环伏安曲线
图3为三聚氰胺在最佳聚合条件下聚合过程的循环伏安图。由图3可知,随扫描段数的增加,峰电流增加,但增加幅度逐渐减小,最后氧化峰和还原峰都达到了稳定,表明三聚氰胺在电极表面发生了聚合反应,三聚氰胺的分子单体不具有电子转移特性,但在电化学作用下发生聚合后,氨基发生变化,其可能的电子转移机理[17]见图4。
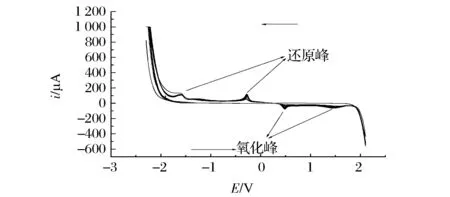
图3 三聚氰胺聚合过程中的循环伏安图Fig.3 Cyclicvoltammetric curves of melamine in polymerization process
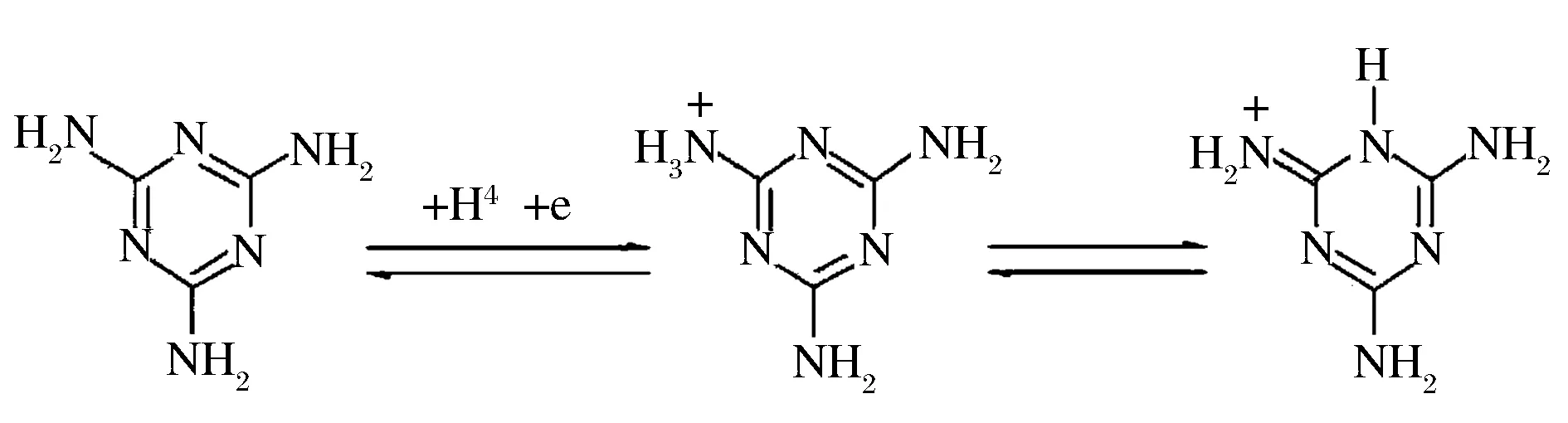
图4 三聚氰胺在玻碳电极上电子转移机理Fig.4 The electron transfer mechanism of melamine at theglasscarbon electrode
2.4测定TBHQ的最佳实验条件
2.4.1 测定底液pH的影响
测定底液pH对电极反应的影响较大。讨论了一定实验条件下测定底液pH对电极反应的影响。固定测定高电位为1.0 V,低电位为-0.7 V,扫描速率为100 mV/s,测定液的浓度为1.00×10-4mol/L,只改变测定底液的pH进行实验,结果表明pH为2.2~8.0时,TBHQ在修饰电极上的响应电流先增大,后减小,当pH等于4.0时,响应电流达到最大值(图5),故本实验选pH=4.0的PBS缓冲溶液为测定底液。实验还表明,TBHQ氧化峰电位随着pH值的升高,氧化峰电位负移,在pH 2.2~8.0,当pH值增加时,氧化峰电位(Epa)呈线性下降,其线性回归方程为Epa=0.47-0.062pH,相关系数R=0.995 8,如图5(内插图)所示,其线性方程的斜率为0.062 V,接近0.059 V,说明TBHQ在氧化过程中涉及质子的参与,而且质子转移数等于电子转移数。
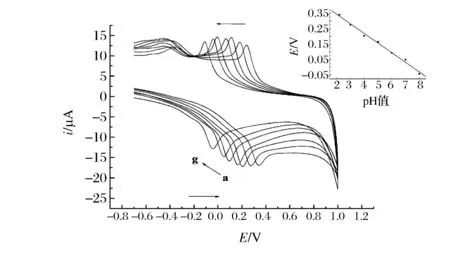
图5 1.00×10-4 mol/L TBHQ在三聚氰胺修饰电极上的随pH值变化的CV曲线Fig. 5 Cyclic voltammograms of 1.0×10-4 mol/L TBHQ at different pH values on the PMel/GCE.注:扫描速率:100 mV/s,从a 到 g的 pH 为:2.2、3.0、4.0、5.0、6.0、7.0、8.0;内插图为氧化峰电位与测定底液pH的关系曲线。
2.4.2 扫描速率的影响
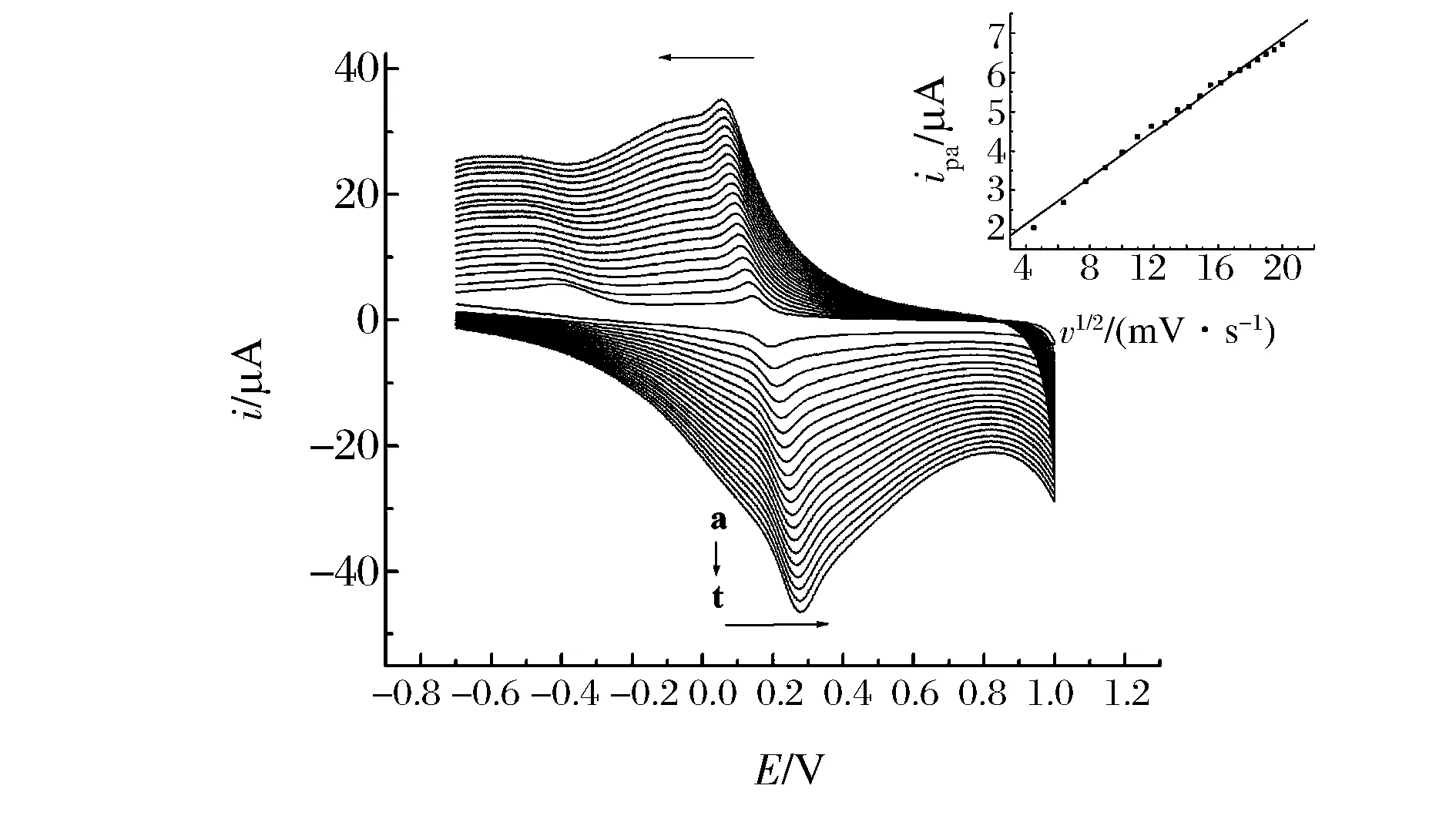
图6 1.00×10-4 mol/L TBHQ在三聚氰胺修饰电极上随扫速变化的CV曲线Fig. 6 Cyclicvoltammograms of 1.00×10-4 mol/L TBHQ at PMel/GCE. Inset is the plot of oxidation peak currents of TBHQ versus the square root of scan rates. 注:从a到t的扫速为:20、40、60、80、100、120、140、160、180、200、220、240、260、280、300、320、340、360、380、400 mV/s; 内插图为 TBHQ在聚三聚氰胺修饰电极上的氧化峰电流值随ν1/2的变化曲线。
固定测定高电位为1.0 V,低电位为-0.7 V,测定液的浓度为1.00×10-4mol/L,缓冲液pH=4.0,只改变扫描速率进行实验,结果表明,随扫描速率的不断增加,氧化峰值也随之增大,从图6中可以看出,扫描速率太低,峰电流较小,不利于检测,在扫描速率为100 mV/s时,峰形较好,此外如果扫描速率太大,会使样品的检出限降低,影响实验结果,故本实验选用的扫描速率为100 mV/s。从图6(内插图)可知氧化峰电流值与扫描速率ν1/2呈线性关系:ipa=9.56×10-7+3.95×10-7v1/2(mV/s)1/2,R=0.996 5,说明TBHQ在聚三聚氰胺修饰电极上的电极过程为扩散过程。
图7是TBHQ在三聚氰胺修饰电极上的氧化峰电位和还原峰电位分别与扫描速率的对数lgv的变化关系曲线,根据可逆薄层电化学的Laviron理论可知氧化峰电位与扫描速率对数的线性关系:Epa=a+(2.303RT/(1-α)nαF)lgv(mV/s) (1),还原峰电位与扫描速率对数的线性关系:Epc=b+(2.303RT/αnαF)lgv(mV/s) (2),两式中a、b均为常数,由图可得出,在pH值为4.0的PBS缓冲溶液条件下,对于TBHQ的氧化还原过程,扫描速率在140~400 mV/s内,得出Epa=0.03+0.096lgv(mV/s),R=0.996 8 (1);Epc=0.33-0.11lgv(mV/s),R=0.993 1 (2)。由(1)(2)两式求得电子传递系数α=0.47,电子转移数nα=1.19,这可能是由于随着扫描速率增大,电极反应可逆性变差,反应不完全,因此计算电子转移数结果偏低。根据文献[8,18],以及测定底液pH值与TBHQ在修饰电极上氧化峰电位(Epa)的线性回归方程为Epa=0.47-0.062pH(2.4.1)的斜率,可知TBHQ氧化反应电子转移数应该为2,质子转移数也等于2;α=0.47,接近理论值0.5,符合准可逆反应特征。

图7 1.00×10-4 mol/L TBHQ在三聚氰胺修饰电极上氧化还原峰电位与lgv变化关系曲线Fig.7 Plots of the peak potentials of 1.00×10-4 mol/L TBHQ versus the logarithms of the scan rates
2.5工作曲线、重现性和稳定性
在最佳实验条件下,分别采用循环伏安法、差分脉冲伏安法和线性扫描伏安法测定了工作曲线,结果表明差分脉冲伏安法所测定工作曲线范围最宽,灵敏度较高,而且避免了线性范围分段现象,因此选择差分脉冲伏安法进行测定。TBHQ氧化峰电流与其浓度在4.00×10-7~1.00×10-4mol/L内呈良好线性关系(如图8所示),其线性方程为:ipa=1.21×10-6+0.04c(mol/L),相关系数:R=0.997 5,检出限为2.00×10-9mol/L。
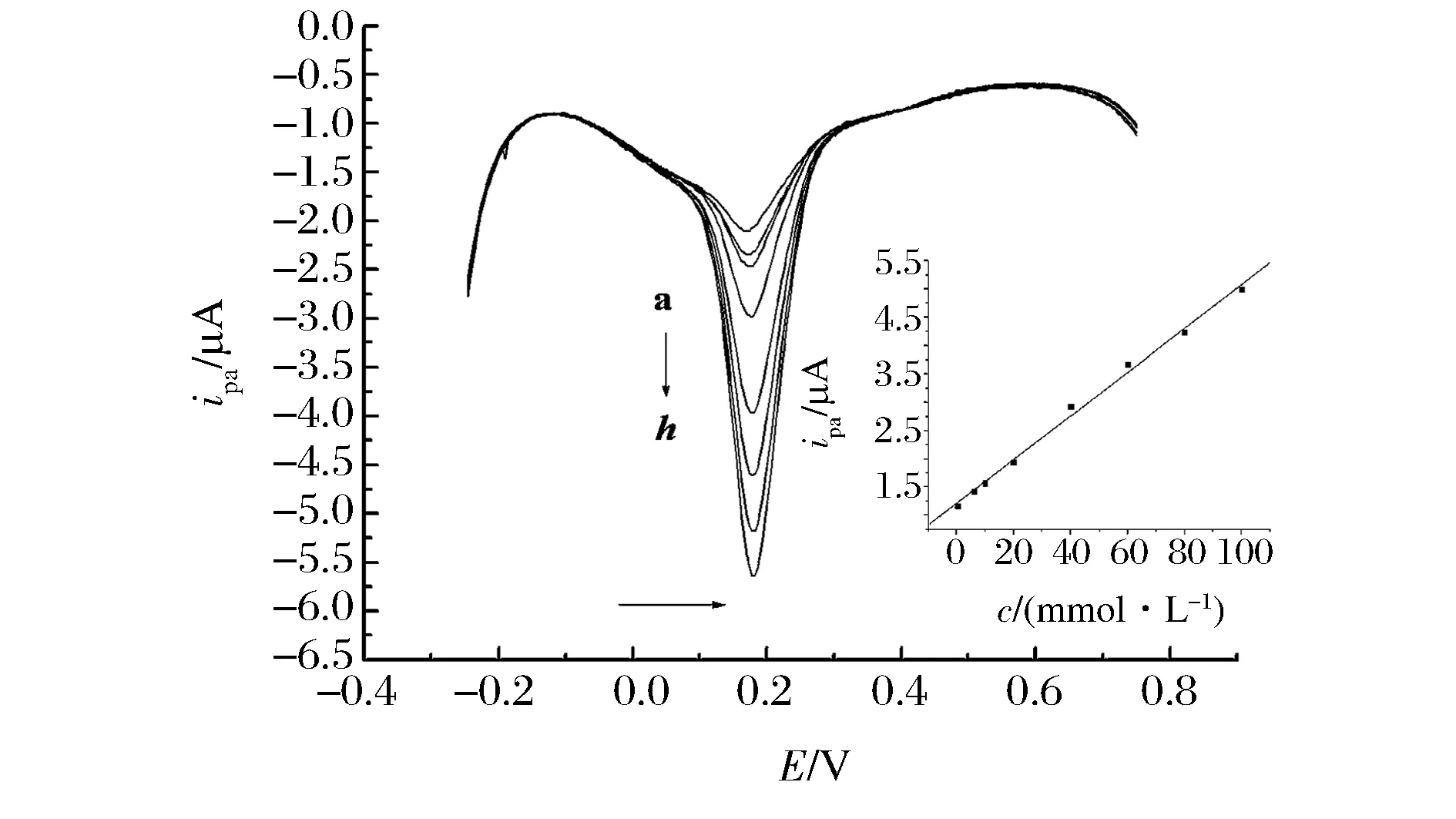
图8 最佳实验条件下不同浓度的TBHQ在三聚氰胺修饰电极上的差分脉冲伏安图Fig.8 Differential pulse voltammetrys of TBHQ at PMel/GCE at different concentrations注:从a到h的浓度分别为: 0.4、6.0、10、20、40、60、80、100 μmol/L;内插图为TBHQ的浓度与氧化峰响应电流的关系曲线。
2.6电极的重现性、稳定性
在最佳的实验条件下,利用聚三聚氰胺修饰电极用差分脉冲伏安法(图9)对TBHQ进行平行测定6次,得出该实验方法的相对标准偏差RSD=2.4%(n=6)。用同一支修饰电极对8.00×10-5mol/LTBHQ进行当天、隔5、10、20 d进行测定,其氧化峰电流分别保持98.2%、97.9%、96.5%初始电流响应,说明修饰电极稳定性较好。
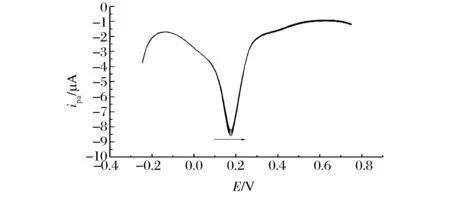
图9 最佳实验条件下8.00×10-5 mol/L的TBHQ在聚三聚氰胺修饰电极上平行测定6次的差分脉冲伏安曲线Fig.9 Differential pulsevoltammetrys of 8.00×10-5 mol/L TBHQ at PMel/GCE by parallel six times
2.7干扰实验
在最佳实验条件下,对浓度为4.0×10-5mol/L的TBHQ做干扰实验。结果表明,允许相对误差在±5%,100倍的蔗糖、KCl、NaCl,50倍的Cu2+、Cd2+,20倍的柠檬黄、日落黄,50倍的叔丁基羟基茴香醚(butylated hydroxyanisole,BHA)、二丁基羟基甲苯(dibutyl hydroxy toluene,BHT)不干扰测定。
2.8样品的测定
在最佳实验条件下对样品进行回收率的测定,结果见表1。

表1 食品样品中TBHQ的回收率测定结果(n=6)
由此计算锅巴中叔丁基对苯二酚含量0.004 6 g/kg;手指饼中TBHQ含量0.004 1 g/kg;食用油中TBHQ含量0.001 2 g/L。
3 结论
制备了三聚氰胺修饰电极,该电极对TBHQ电化学氧化具有明显催化作用,与裸电极相比能够显著增大其氧化峰电流,从而提高了测定方法的灵敏度。TBHQ氧化峰电流与其浓度在4.00×10-7~1.00×10-4mol/L范围内呈良好线性关系,检出限为2.00×10-9mol/L,建立了用三聚氰胺修饰电极测定食品中TBHQ新方法。将修饰电极用于实际食品样品中TBHQ的检测,回收率为96.9%~102.2%,结果满意。
[1] 赵职卫, 毕勇毅, 潘伯群, 等. TBHQ对苯诱导的大鼠骨髓细胞毒性的保护作用[J]. 中华劳动卫生职业病杂志, 2006, 24(3):143-146.
[2] 郝鹏鹏. 食品中TBHQ的检测方法[J]. 粮食食品科技, 2012, 20(3): 33-35.
[3] 李家林, 张雪飞, 李昊力. 特丁基对苯二酚的研究现状[J]. 广东化工, 2014, 41(22): 92-93.
[4] 高延伟. 液相色谱法检测市售油炸食品中的TBHQ残留量[J]. 食品安全导刊, 2015(21): 142-143.
[5] 郝鹏鹏, 倪晋仁, 孙卫玲. 血清药理学方法评价TBHQ的安全性[J]. 食品研究与开发, 2011, 32(12): 175-17.
[6] 岳振峰, 谢丽琪, 吉彩霓. 油脂及其制品中BHA、BHT、PG和TBHQ快速测定方法研究[J]. 食品与发酵工业, 2002, 28(10): 49-52.
[7] 李涛, 余旭亚. 抗氧化剂的研究与应用现状[J]. 食品研究与开发, 2003, 24(2): 23-26.
[8] WANG L, YANG R, LI J J, et al. A selective and sensitive tert-butylhydroquinone sensor based on synergy of CTAB and AuNPs-PVP-graphene nanohybrids[J]. Ionics, 2016, 22: 415-423.
[9] AMMAWATH W, MAN Y B C, BAHARIN B S, et al. A new method for determination of tert-butylhydroquinone (TBHQ) in RBD palm olein with FTIR spectroscopy[J]. Food Lipids, 2004, 11(4):266-277.
[10] GUO L, XIE M Y, YAN A P, et al. Simultaneous determination of five synthetic antioxidants in edible vegetable oil by GC-MS[J]. Anal Bioanal Chem, 2006, 386(6):1 881-1 887.
[11] YANG M H, LIN H J, CHOONG Y M. A rapid gas chromatograph-ic method for direct determination of BHA, BHT and TBHQ in edible oils and fats[J]. Food Res Int, 2002, 35(7):627-633.
[12] SAAD B, SING Y Y, NAWI M A, et al. Determination of syn-thetic phenolic antioxidants in food items using reversed-phase HPLC[J]. Food Chem,2007, 105(1):389-394.
[13] GOULART L A, TEIXEIRA A R L, RAMALHO D A, et al. Development of an analytical method for the determination of tert-butylhydroquinone in soybean biodiesel[J]. Fuel, 2014, 115:126-131.
[14] DE ARAUJO T A, JACQUES BARBOSA A M, VIANA L H, et al. Electroanalytical determination of TBHQ, a synthetic antioxidant,in soybean biodiesel samples[J]. Fuel, 2011, 90(2):707-712.
[15] LIN X Y, NI Y N, KOKOT S. Glassy carbon electrodes modified with gold nanoparticles for the simultaneous determination of three food antioxidants[J]. Anal Chim Acta, 2013, 765:54-62.
[16] 冯利彬, 齐崴, 苏荣欣, 等. 聚(三聚氰胺)与金纳米粒共修饰玻碳电极用于芦丁的电化学测定[J]. 分析测试学报, 2014, 33(9):1 019-1 025.
[17] LIU X, LUO L Q, DING Y P, et al. A highly sensitive method for determination of guanine, adenine and epinephrine using poly-melamine film modified glassy carbon electrode[J]. Journal of Electroanalytical Chemistry, 2012, 675(12):47-53.
[18] LAVIRON E. General expression of the linear potential sweep voltammogram in the case of diffusionless electrochemical systems[J]. Electroanal Chem Interfacial Electrochem, 1979, 101:19-28.
Determinationoftert-butylhydroquinoneinfoodbyapoly-(melamine)modifiedglassycarbonelectrode
MA Xin-ying*,ZHU Qi,ZHANG He-ping
(Department of Chemistry and Chemical Engineering,Heze University,Heze 274015, China)
Poly melamine film modified glassy carbon electrode (PMel/GCE) was fabricated by electroplymerization of melamine. The electrochemical behavior of antioxidants tert-butylhydroquinone (TBHQ) was investigated by cyclic voltammetry (CV), a couple of sensitive redox peaks obtained. It was found that the oxidation peak current (ipa) and the reductive peak (ipc) current at PMel/GCE were obviously stronger than those at the bare glassy carbon electrode(GCE), which indicated that the sensitivity for detection of TBHQ was improved. Experimental parameters, including electro-polymerized time of Mel, scan rate, voltage, cycles and pH value of buffer solution were optimized. Under the optimal conditions, good liner relationships between current intensities and TBHQ concentrations were obtained in the ranges of 4.00×10-7-1.00×10-4mol/L, with correlation coefficients (R) of 0.997 5. The detection limit was 2.0×10-9mol/L. The modified electrode can be applied to the analysis of TBHQ in food with recoveries of 96.9%-102.2%.
melamine; glassy carbon electrode; tert-butylhydroquinone
10.13995/j.cnki.11-1802/ts.013574
硕士,副教授(本文通讯作者,E-mail: maxinying5966@163.com)。
山东省自然科学基金(No. ZR2014BL020);山东省高校科技计划项目(No. J14LC55)
2016-12-08,改回日期:2017-01-04

