DBU骨架含N杂环的合成及产物的核磁共振分析
,
(1.浙江工业大学 分析测试中心,浙江 杭州 310014;2.浙江工业大学 化学工程学院,浙江 杭州 310014)
1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)是上世纪60年代开发出来的一类强碱性有机试剂.自开发以来已成为一种非常有用的结构比较稳定的有机强碱试剂,在消除、环合[1]、缩合[2]和异构[3]等反应中有着广泛的应用.它们在有机溶剂中具有较好的溶解性能,特别适用于原料官能团反应活性较高或生成物不稳定的反应.其参与的反应具有条件温和、副反应较少、产率较高和产物选择性专一等特点[4-5].由于DBU结构的稳定性,文献报道其主要是作为有机位阻强碱试剂或催化剂促进反应的进行[6-8],在有机反应中更多地充当Reagent的角色,而关于DBU作为Reactant参与反应的报道较少.2006年,Gryko等[9]意外发现了DBU与活泼1,2-二氯化合物的成环缩合反应,最终获得产率为35%的2-氨基吡咯衍生物.2014年,Poronik等[10]发现了DBU与烷基香豆素-3-羧基化合物的缩合成环反应.反应过程中形成了新的C—N和C—C键的中间体,随后该中间体被香豆素-3-羧酸酯氧化.该反应对环状脒的结构有较高要求.2015年,Chen等[11]以DBU为氮源,金属Pd催化,合成了一系列由己内酰胺、丁内酰胺衍生而来的邻苯二甲酰亚胺和酰胺化合物.亲核试剂DBU先参与羰基化反应,再发生水解开环.
在研究DBU促进的N-苯基-N-苄基苯丙炔酰胺的分子内环合反应中,意外发现DBU能与苯丙炔酰胺发生反应.经质谱、核磁共振分析,确证反应产物为一种DBU为骨架的多环并环杂环化合物.本文以该反应为研究对象,并针对性地提出可能的反应机理.
1 实验部分
1.1 仪器与试剂
AVANCE III 500 MHz型核磁共振谱仪,Bruker;Agilent 1200-6210型TOF LC/MS, Agilent;R-210型旋转蒸发仪,BUCHI;ZF-I型紫外分析灯,上海宝山顾村电光仪器厂;SM-3型磁力搅拌器,上海智成电器有限公司;SHZ-DIII型循环水式多用真空泵,河南予华仪器有限公司;EL204型电子天平,梅特勒-托利多仪器(上海)有限公司.
N-苯基-N-苄基苯丙炔酰胺,≥98%,自制品;N-甲基-N-甲氧基苯丙炔酰胺,≥98%,自制品;苯丙炔酸乙酯,≥98%,自制品;乙腈(除水处理);无水硫酸钠(AR,上海凌峰化学试剂有限公司);盐酸(AR,杭州双林化工试剂厂);二氯甲烷(AR,上海凌峰化学试剂有限公司);乙酸乙酯(CP,杭州方平化工有限公司);氮气(99.999%,今工气体有限公司).
1.2 实验过程及方法
以N-苯基-N-苄基苯丙炔酰胺为例与DBU反应:氮气下,向25 mL干燥的两口烧瓶依次加入0.093 3 g(0.3 mmol)N-苯基-N-苄基苯丙炔酰胺,0.091 4 g(0.6 mol)DBU,5 mL乙腈溶剂,磁力搅拌,油浴加热至80 ℃,薄板层析(TLC)跟踪监测,展开剂为乙酸乙酯.反应结束,冷却,减压蒸馏除去乙腈溶剂,加10 mL的当量盐酸,二氯甲烷(3×10 mL)萃取,水洗3次,合并有机相并用无水硫酸钠干燥,浓缩,产物用硅胶柱层析,洗脱剂乙酸乙酯,产率24.1%.
2 结果与讨论
2.1 杂环产物合成
N-苯基-N-苄基苯丙炔酰胺与DBU的反应式为
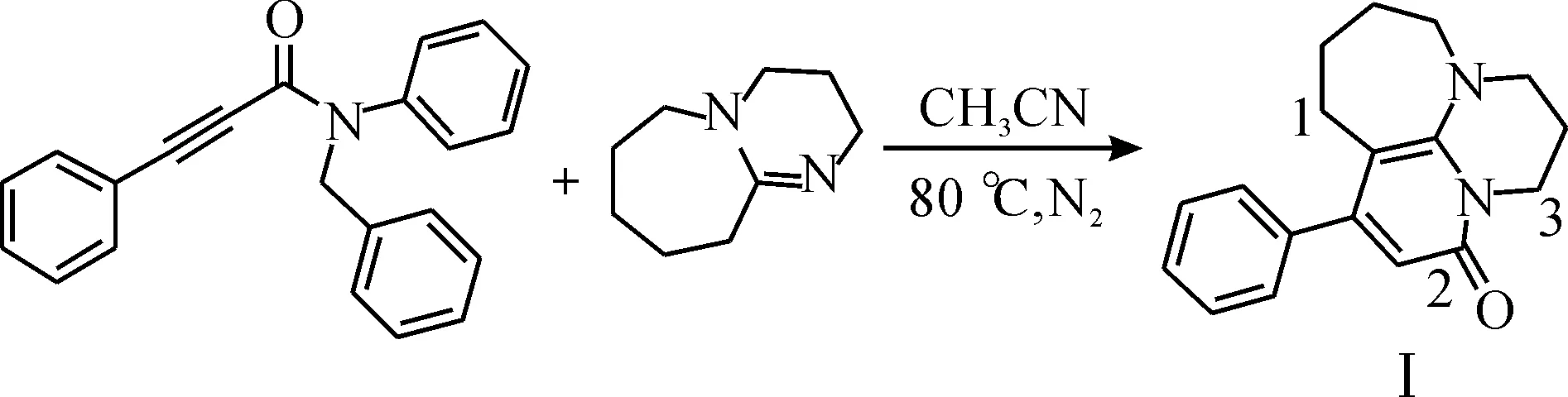
(1)
选择N-苯基-N-苄基苯丙炔酰胺和DBU建立模型反应,考察溶剂、温度和DBU用量对反应的影响.最后得到目标产物I.
解析质谱图,核磁谱图(1H-NMR,13C-NMR,H-H COSY,HSQC,HMBC)确定了产物的结构.值得一提的是在确定含羰基环的结构上,可以从式(1)中产物I的HMBC谱图分析,羰基碳(C-2)与H-1没有HMBC远程相关信号,与H-3有3JC—H的HMBC相关信号,由此确定羰基碳是与氮相连的.
在后续的底物拓展中,只有苯基和对甲苯基的苯丙炔酰胺可获得预期产物,且产率较低.这可能与该类酰胺的空间位阻较大,N-苯基-N-苄基的离去性较差有关.查阅文献发现weinreb酰胺[12]是一种具有更好反应活性的酰胺类化合物,故进一步以该化合物为底物考察其反应性.N-甲氧基-N-甲基苯丙炔酰胺与DBU的反应式为
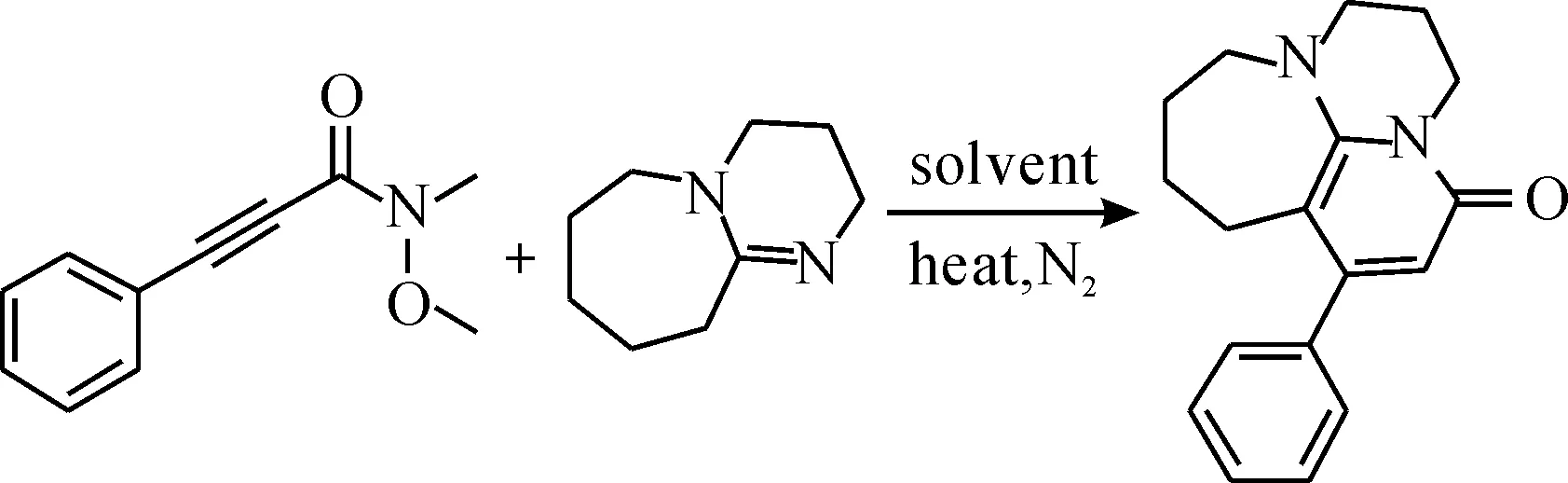
与预期相同,这类weinreb酰胺可与DBU发生反应,并获得了产物I,考察了溶剂、温度和DBU用量对反应的影响.最后确定了相对最优条件为在氮气下,3当量DBU,80 ℃油浴,反应6 h.
2.2 底物拓展
如表1所示,与N-苯基-N-苄基苯丙炔酰胺和DBU反应相比,weinreb酰胺类化合物与DBU的反应活性较好,Ar为对氯苯基和间氯苯基的酰胺能与DBU反应,得到相应的杂环化合物;而Ar为邻氯苯基时,不能得到闭环产物,可能是由该底物的位阻较大造成的.在反应中,分离获得闭环产物的同时,发现存在一些DBU开环的化合物,可能是造成产率不高的原因.weinreb酰胺与DBU的反应式为
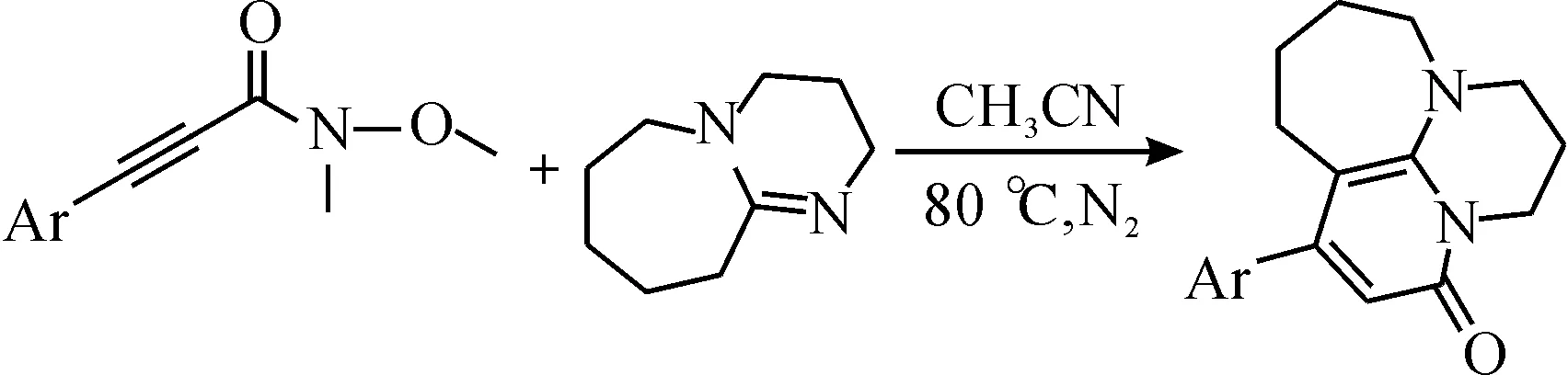
表1 成环反应底物拓展Table 1 The substrate expansion of cyclization
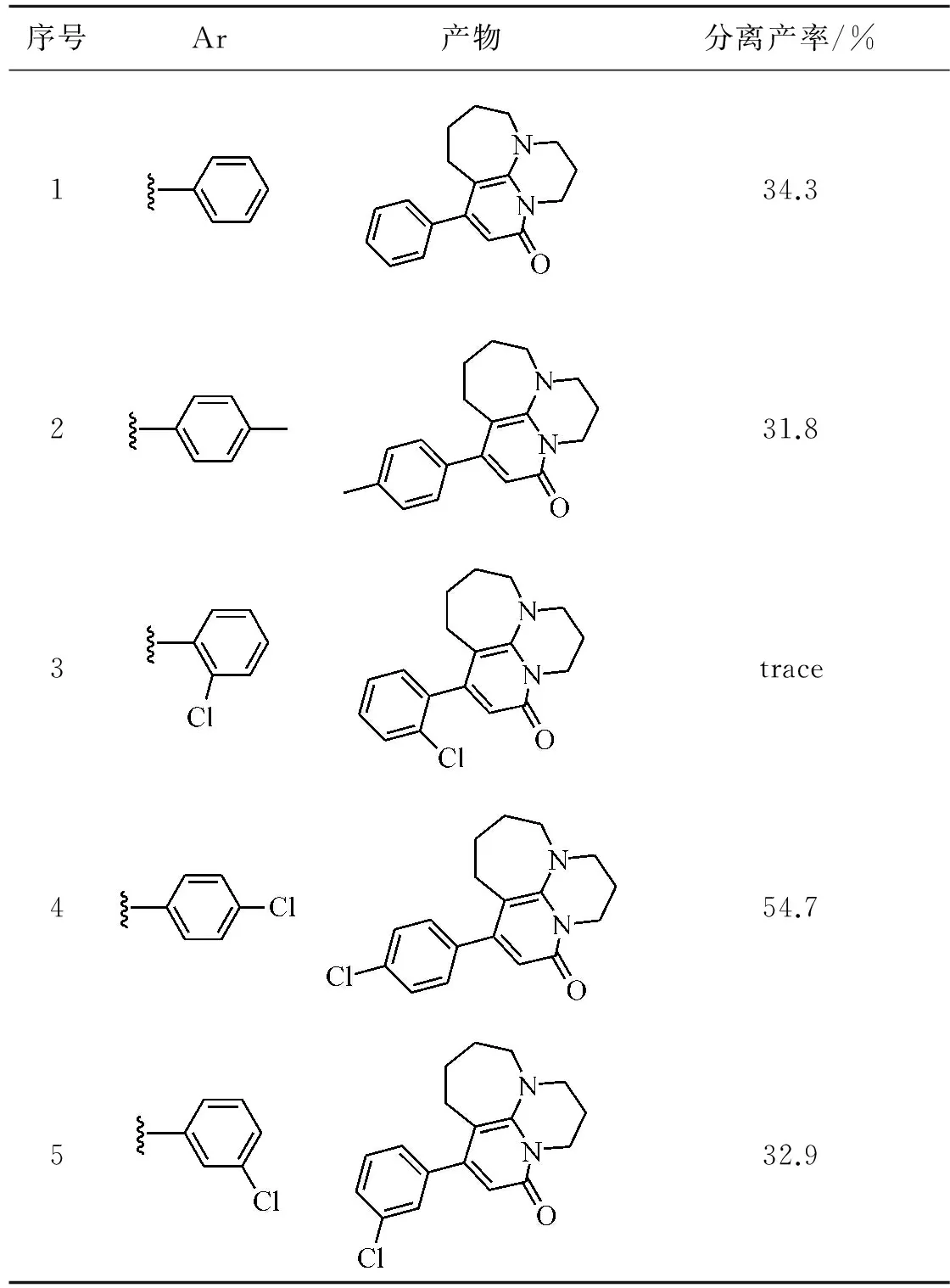
序号Ar产物分离产率/%134.3231.83trace454.7532.9
2.3 苯丙炔酸乙酯与DBU反应
进一步考察了苯丙炔酸乙酯与DBU的反应.按照预想反应可能与酰胺类似,可得到环合产物.实验发现,除了得到预想的产物II外,我们还得到了另一种与产物II分子量相同且核磁共振谱图非常相似的产物III.苯丙炔酸乙酯与DBU的反应式为
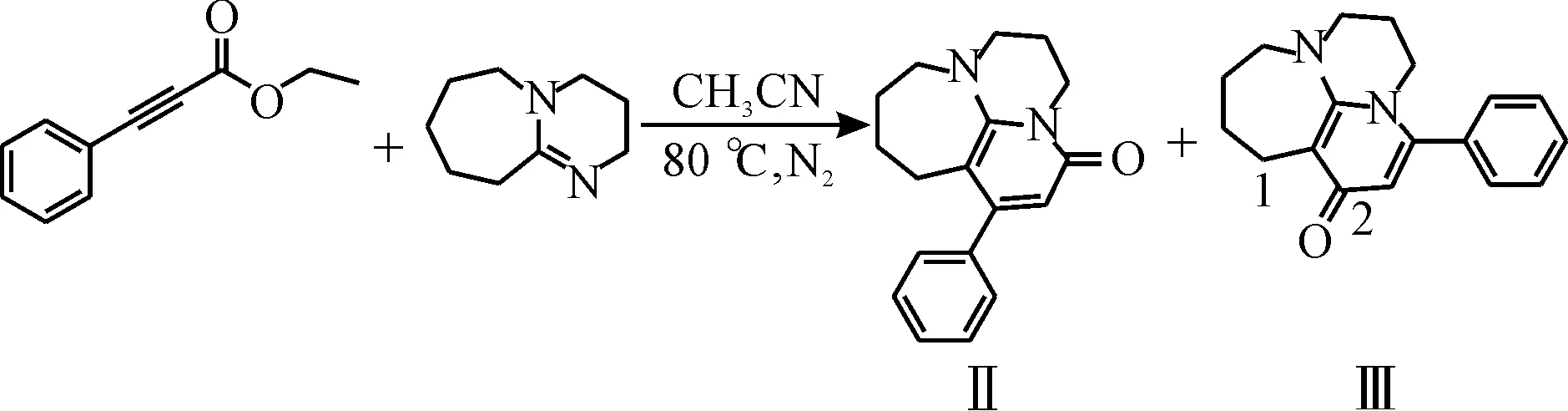
(2)
我们发现产物II(分离产率32.7%)与产物III(分离产率19.2%)除化学位移有所差别,一维谱图上氢谱的质子峰数目、积分值和裂分情况,碳谱的信号个数、强度及DEPT 135的信号都基本相同,仅依靠一维核磁无法区分这两类化合物.通过分析式(2)中的III化合物的HMBC谱图,发现其羰基碳(C-2)和H-1有3JC-H的HMBC远程信号,表明其羰基碳的位置是与I化合物不同的,同时进一步证明化合物I结构的准确性.
2.4 反应机理讨论
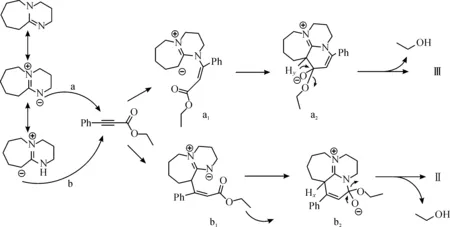
对产物Ⅱ,产物Ⅲ的形成,我们提出了其可能的机理[13-15].产物Ⅲ的形成为机理图中的路线a所示,DBU共振式氮负部分首先进攻苯丙炔酸乙酯三键,生成季铵盐中间体,然后碳负离子夺取七元环上的氢,形成中间体a1;碳负离子进攻羰基,得到中间体a2;乙氧基负离子夺取Hy形成乙醇小分子离去,经异构最终得到产物Ⅲ.这种转变过程中,DBU先后表现出氮负及碳负亲核性.
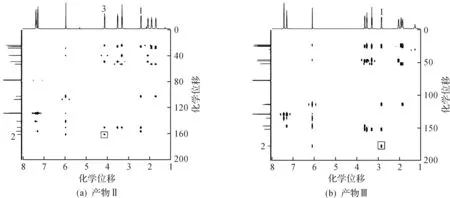
图1 产物Ⅱ和Ⅲ的HMBC图Fig.1 HMBC spectrums of product Ⅱ and Ⅲ
产物Ⅱ的形成如机理图中的路线b所示,DBU共振式碳负部分先进攻苯丙炔酸乙酯三键,形成季铵盐中间体;然后烯碳负离子夺取氮上氢,生成含氮负离子的中间体b1;氮负离子进攻分子内羰基碳,得到b2中间体;羰基碳上的乙氧基片段以氧负离子的形式夺取Hx,形成乙醇小分子,最终异构形成产物Ⅱ.在这个过程中,DBU首先表现出来碳负亲核性,然后又表现出氮负亲核性.苯丙炔酸乙酯与DBU的反应机理为
2.5 产物鉴定
产物2-1(产物I和II),淡黄色液体,1H NMR(500 MHz, CDCl3)δ1.66~1.71(m,2H),1.87~1.92 (m,2H),2.04~2.09(m,2H),2.38~2.40(t,J=5.80 Hz,2H),3.28~3.31(t,J=6.70 Hz,2H),3.41~3.51(t,J=5.73 Hz,2H),4.11~4.13(t,J=5.50 Hz,2H),5.95(s,1H),7.27~7.29(d,J=7.26 Hz,2H),7.34~7.39(m,3H);13C NMR(125 MHz, CDCl3)δ23.5,25.0,25.3,27.7,31.1,48.6,52.5,102.0,106.9,127.7,128.1,128.3,140.6,150.0,155.9,160.8; HRMS-ESI[M+H]+Calcd for C18H21N2O 281.164 8, found 281.163 5.
产物2-2,淡黄色液体,1H NMR (500 MHz, CDCl3)δ1.66~1.71(m,2H),1.86~1.91(m,2H),2.03~2.08(m,2H),2.38(s,3H),2.40~2.42(t,J=6.05 Hz,2H),3.27~3.30(t,J=6.75 Hz,2H),3.49~3.51(t,J=6.01 Hz,2H),4.10~4.12(t,J=5.61 Hz, 2H),5.95(s,1H),7.18(s,4H);13C NMR(125 MHz, CDCl3)δ21.1,23.5,25.0,25.3,27.8,39.1,48.5,52.4,102.3,106.6,128.2,128.8,137.6,150.0,156.0,160.8; HRMS-ESI[M+H]+Calcd for C19H23N2O 295.180 5, found 295.184 4.
产物2-4,淡黄色液体,1H NMR(500 MHz, CDCl3)δ1.62~1.65(m,2H),1.81~1.86(m,2H),1.92~2.02(m,2H),2.30~2.32(t,J=5.85 Hz,2H),3.23~3.25(t,J=6.79 Hz,2H),3.43~3.45(t,J=5.91 Hz,2H),4.04~4.06(t,J=5.44 Hz,2H),5.84(s,1H),7.16~7.17(d,J=8.42 Hz,2H),7.29~7.30(d,J=8.38 Hz,2H);13C NMR(125 MHz, CDCl3)δ23.2,24.8,25.0,27.5,39.0,48.4,52.2,101.5,106.2,128.2,129.5,133.6,138.8,150.0,154.4,160.5; ESI-HRMS[M+H]+Calcd for C18H19ClN2O 315.126 4, found 315.125 1.
产物2-5,棕黄色液体,1H NMR(500 MHz, CDCl3)δ1.63~1.68(m,2H),1.84~1.89(m,2H),2.00~2.05(m,2H),2.33~2.35(t,J=5.91 Hz 2H),3.25~3.28(t,J=6.91 Hz,2H),3.46~3.48(t,J=6.81 Hz,2H),4.06~4.08(t,J=5.55 Hz,2H),5.86(s,1H),7.11~7.14(m,1H),7.23(s,1H),7.28~7.39(m,2H);13C NMR(125 MHz, CDCl3)δ23.2,24.8,25.0,27.5,39.1,48.4,52.2,101.5,106.3,126.4,127.7,128.2,129.4,133.8,142.2,150.1,154.3,160.5; ESI-HRMS[M+H]+Calcd for C18H19ClN2O 315.126 4, found 315.124 5.
产物III,黄色液体,1H NMR(500 MHz, CDCl3)δ1.81~1.86(m,2H),1.89~1.94(m,2H),2.00~2.05(m,2H),2.28~2.85(t,J=5.53 Hz,2H),3.28~3.30(t,J=7.03 Hz,2H),3.51~3.53(t,J=5.86 Hz,2H),3.61~3.63(t,J=5.19 Hz,2H),6.09(s,1H),7.29~7.30(t,J=3.29 Hz,2H),7.43~7.44(m,3H);13C NMR(125 MHz, CDCl3)δ22.7,23.8,24.6,25.0,45.6,47.2,51.6,113.6,114.2,128.6,128.7,129.1,135.0,146.9,152.0,177.7; ESI-HRMS[M+H]+Calcd for C18H21N2O 281.1648, found 281.164 2.
3 结 论
以苯丙炔酰胺类化合物和苯丙炔酸乙酯为底物,与DBU在80 ℃乙腈中反应,获得两种DBU骨架结构的含氮杂环并环化合物.比较分析了两种化合物的HMBC谱,确定了含羰基碳环的位置,并讨论了该反应的可能反应机理.DBU与苯丙炔酰胺类化合物反应时,DBU共振式碳负部分先进攻苯丙炔酰胺的三键,然后DBU环上氮负离子进攻羰基,在整个反应过程中DBU首先表现出碳负亲核性,接着表现出氮负亲核性;而DBU与苯丙炔酸乙酯反应时体现出了另一反应性能,DBU共振式氮负部分先进攻苯丙炔酸乙酯的三键,然后DBU环上碳负离子进攻羰基,所以DBU在反应中先表现出氮负亲核性,再表现出碳负亲核性.该研究为一步合成含DBU骨架的化合物提供了新的思路,后续将在提高产率,反应机理方面继续深入研究.
[1] LIU R, LI J H.光化学法合成2-羟基咔唑[J].浙江工业大学学报,2012,40(4):405-407.
[2] QI J, CAI P, LAI H Q, LIN F Y, MIAO L.杀菌剂嘧菌环胺的合成[J].浙江工业大学学报,2012,40(1):17-20.
[3] LIN C M, ZHENG X Q, YU Y,YANG X.四种三唑类杀菌剂的超临界色谱手性分离[J].浙江工业大学学报,2013,41(5):473-477.
[4] CHEN G C, WANG Z J, GAO Z X. DBU——一种多功能的碱性试剂[J].化学试剂,1999,21(6):339-346.
[5] NI Z G.强有机碱试剂DBU和DBN在有机合成中的应用[J].中国医药工业杂志,1991,22(4):180-186.
[6] LI M R,YUAN H Y, ZHAO B Z. Alkyne aminohalogenation enabled by DBU-activated N-haloimides: direct synthesis of halogenated enamines[J]. Chemical communications,2014,18
(18):2360-2363.
[7] NIKSERESHT A, BAYRAQ M S. DBU: an efficient base catalyst for synthesis of the new oxazolo[5,4-d]pyrimidine derivatives[J]. Synthetic communications,2014,44(18):2662-2668.
[8] WANG L Q, ZHANG D M, LI J, XU G Y, SUN J T. A highly efficient DBU-catalyzed green synthesis of spiro-oxindoles[J]. RSC advances,2014,4:44193-44196.
[9] GRYKO D T , PIECHOWSKA J, TASIOR M. From bifunctional nucleophilic behavior of DBU to a new heterocyclic fluorescent platform[J]. Organic letters,2006,8(21):4747-4750.
[10] PORONIK Y M, GRYKO D T. Pentacyclic coumarin-based blue emitters-the case of bifunctional nucleophilic behavior of amidines[J]. Chemical communications,2014,50:5688-5690.
[11] CHEN J B, NATTE K, WU X F. Convenient palladium-catalyzed cardonylative synthesis of caprolactam and butyrolactam derived phthalimides and amides by using DBU and DBN as the nitrogen source[J]. Tetrahedron letters,2015,56:243-245.
[12] ZHAO W, LIU W. Progresses of weinreb amides in organic synthesis[J].Chinese journal of organic chemistry,2015,35:55-69.
[13] NIE Q L, SHI Z J, CAO W G. DBU与全氟炔酸酯的迈克尔型加成及其产物的NMR谱学研究[J].波谱学杂志,2002,19(4):377-384.
[14] ZHI Z J, NENG Q L, CAO W G. DBU及DBN与丙炔酸甲酯的迈克尔型加成及其产物的核磁共振谱学研究[J].分析科学学报,2004,20(6):586-588.
[15] MA L, DOLPHIN D. Michael-type addition of 1,8-diazabicyclo[5.4.0]undec-7-ene to dimethyl acetylenedicarboxylate[J]. Journal of the chemical society chemical communications,1995,22:2251-2252.

