团簇Ni3 B2热力学稳定性及其催化性质
程子轩,方志刚,崔远东,李历红,徐诗浩
(辽宁科技大学 化学工程学院,辽宁 鞍山 114051)
非晶态合金作为新兴材料相较于普通的晶态材料具有多方面的优异性能。近年来,Ni-B体系作为该领域的核心热点在催化电极材料[1-6],超级电容器材料[7-9],耐磨材料[10],还原氢材料[11]等方面有着广阔的应用前景,并且在包括物质结构[12-13],制备方法[14-15]等诸多方面有不同层次的研究,但缺少微观尺度下的理论支撑。为了解释Ni-B材料的某些特性,需要对Ni-B体系进行理论上的研究。同时根据文献[16]的配比,本文设计了Ni3B2的团簇模型,并引用前线轨道理论对其稳定构型的HOMO、LUMO轨道进行分析,以期为Ni-B体系研究提供有价值的信息。
1 计算方法
根据拓扑学原理[17]设计出团簇Ni3B2所有可能的构型,在B3LYP/Lan12dz水平[18]下对其进行全参数优化和频率计算,获得八种稳定构型。对于过渡金属Ni采用Hay P J等人[19]的含相对论校正的有效核电势价电子从头计算基组,即采用18-eECP的双ξ基组(3s,3p,3d/2s,2p,2d),对类金属B原子采用 Dunning/Huzinaga双ξ基组(9s,5p/3s,2p)。全部计算在启天M4390上由Gaussian09程序完成。
2 结果与讨论
2.1 团簇Ni3B2构型
图1列出了能够稳定存在的八种团簇构型。其中,单重态4种,三重态4种。用自然数1,2,3,...表示构型能量从低到高的排序,右上角括号里的数字表示构型的多重度。团簇Ni3B2稳定构型按照能量从低到高依次为:三角双锥1(3)<四棱锥2(3)<三角双锥3(3)<五边形 4(3)<五边形 1(1)<三角双锥 2(1)<三角双锥 3(1)<戴帽三角锥4(1)。
2.2 团簇Ni3B2稳定性分析
从能量角度分析比较各构型的稳定性,图2给出了各构型的吉布斯自由能变(ΔG)和结合能(EBE)随构型的变化趋势。其中,ΔG=GNi3B2-3 GNi-2GB,EBE=3ENi+2EB-ENi3B2。从图2中可以看出,除了构型4(3)的结合能 EBE=0.4086 a.u,略大于3(3)的结合能 EBE=0.408 4 a.u,其余构型的结合能均随能量增加而降低,三重态的能量整体低于单重态的能量,三重态的结合能高于单重态的结合能,因而三重态稳定性好于单重态稳定性,所占比例也应较高。三重态中ΔG和EBE数值整体波动较小,2(3),3(3),4(3)吉布斯自由能变和结合能趋于一致;单重态相应的数值波动较大,特别是3(1)和4(1),由于其对称度较低,能量较高,是结合能最低的两个,说明这两个构型原子间引力作用较小,较不稳定,可能不会大量存在;而1(3)的结合能最高,吉布斯自由能变的绝对值最大,说明构型1(3)最容易生成,且稳定性最好。
值得一提的是,平面构型4(3)(EBE=0.420 2 a.u)和 2(1)( EBE=0.410 8 a.u)的结合能均大于平均值(EA=0.408 4 a.u),在其他类型的非晶态合金微观团簇中,平面不对称构型通常稳定性较差,结合能较低,该性质可能与Ni复杂的内部电子结构有关。
2.3 关于构型内部结构的讨论
构型相似的 1(3)和 2(1),3(3)和 3(1)各方面的差值都很大。为了分析内在的成因,表1列出了各构型的原子间距,表2列出了各构型的键级。

图1 团簇Ni3B2各优化稳定构型图Fig.1 Optimized configurations of cluster Ni3B2

图2 团簇Ni3B2的吉布斯自由能变和结合能Fig.2 ΔGandEBEof cluster Ni3B2

表1 Ni3B2构型原子间距,nmTab.1 Atomic distance of cluster Ni3B2,nm

表2 Ni3B2构型键级Tab.2 Mullikenbond order for cluster Ni3B2
从表1和表2可以看出,在考虑电子环境的条件下,表中Ni-B键级均为正值,即Ni-B为主要键级贡献;Ni原子间距对键级贡献有很明显的差异,在Ni-Ni间距小于0.240 nm时表现为成键作用,而在0.240 nm到0.345 nm之间表现为反键作用。例如 4(1)中 Ni1-Ni2 原子间距为 0.228 9 nm,键级为0.148 7;而1(3)中Ni1-Ni2原子间距为0.325 8 nm,键级为-0.2392,2(3)中 Ni2-Ni3 原子间距为 0.348 5 nm,键级为0.005 4,可以初步推断在团簇Ni3B2中,Ni-Ni原子间距在0.240 nm到0.345 nm之间形成的键与Ni-Ni间距在小于0.240 nm之间形成的键不是同一类型的键,前者有反键作用,后者有成键作用,原子间距数值上越接近0.240 nm(/0.345 nm),对键级影响越弱。例如4(1)Ni1-Ni3间距为0.242 9 nm,键级为-0.020 3。同样地,当B-B间距大于0.170 nm时与小于0.170n m时形成的键不是同一个类型,前者有反键作用,后者有成键作用,原子间距数值越接近0.170 nm时,对键级影响越弱。例如4(3)中B1-B2间距为0.169 6 nm,键级为0.005 2。这一结果与方志刚等人的研究相符[20]。并可以据此推测,在其他类型的非晶态合金微观团簇中,也存在类似的规律。
4(1)和 3(3)构型相似,但二者原子间距相去甚远,因此各方面性质差异较大。不完全符合这一规律的构型 4(3)和 1(1)均为平面构型,4(3)中 Ni1-Ni3间距为0.285 8 nm,键级为-0.003 3,1(1)中Ni1-Ni3原子间距为0.367 0 nm,键级为-0.045 9,可以推测两者内部电子运动有更强的相互作用,存在更复杂的电子结构,即前文提及的电子环境的影响。
2.4HOMO和LUMO轨道贡献
为探究分析团簇中催化活性的规律,表3提供了团簇中不同原子最高占据轨道能(EHOMO)和最低空轨道的能级(ELUMO)、能隙差(EGAP)、以及不同Ni的贡献率;图3给出了各构型的能隙差。
Ni原子HOMO的总贡献率和LUMO的总贡献率均大于50%,说明前线轨道的主要贡献者是Ni原子。EGAP在某种程度上可以反映出分子参加反应的能力。能隙差越低,表明团簇越容易发生反应。团簇参与反应的强弱顺序为:三重态:4(3)>1(3)>2(3)>3(3);单重态:3(1)>4(1)>2(1)>1(1)。相较而言,三重态的能隙差要高于单重态,波动幅度较大,而单重态的能隙差较低,保持在一个很小的区间内;单重态参与反应的能力要高于三重态。平面构型4(3)能隙差要远低于其他三重态的构型;1(1)能隙差(EGAP=0.078 0 a.u)要高于其他单重态的构型,并与4(3)能隙差接近(EGAP=0.078 0 a.u),这是因为平面构型中由于原子间距相对较小,电子运动状态受到其他电子影响更强,因而表现出与其他构型不同的性质,能隙差就是一个很好的例子。
综上所述,构型4(3),1(1),2(1)兼具较高的结合能和较低的能隙差,即在保证可以稳定存在的同时具有较强参与反应的能力,并且平面结构有更广阔的应用前景,是催化材料的理想构型,也为Ni-B非晶态薄膜提高催化电极催化性能的研究[14]提供了理论上的依据。
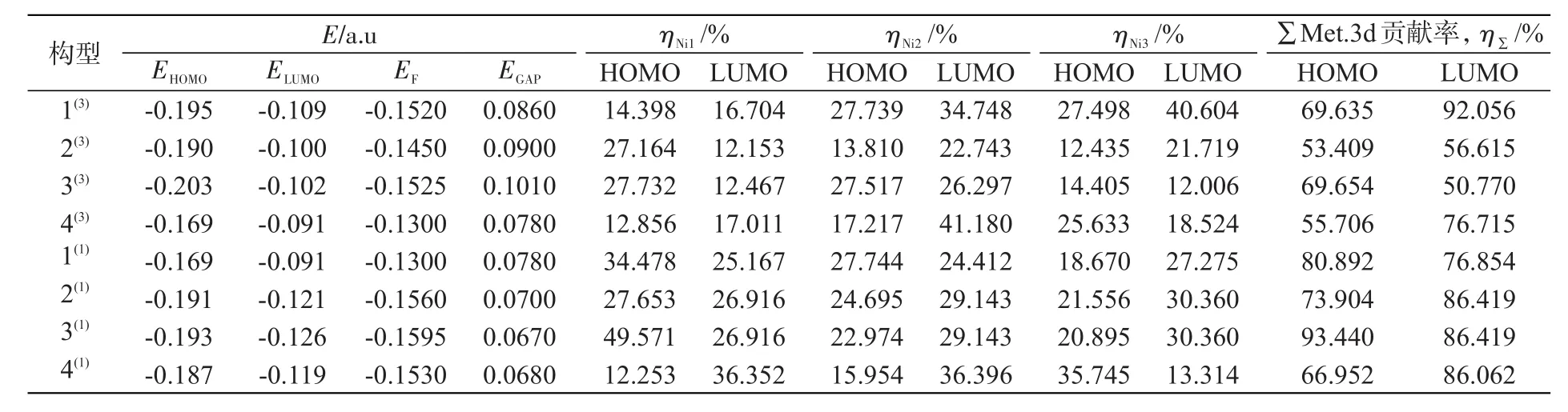
表3 团簇Ni3B2的能级参数、Ni原子的3d轨道前线轨道贡献Tab.3 Parameters of energy level,contribution of Ni atoms to 3d orbitals frontier molecular orbitsof cluster Ni3B2

图3 团簇Ni3B2各优化构型能隙差Fig.3 EGAPin stable structures of cluster Ni3B2
3 结论
在非晶态合金Ni3B2团簇中,三重态构型的稳定性比单重态好,三重态的能隙差整体高于单重态,即三重态构型稳定存在的可能性大于单重态,但参与反应的能力弱于单重态。在考虑电子环境的情况下,Ni-Ni间距小于0.240 nm时有利于构型的稳定,在0.240 nm到0.345 nm时不利于构型的稳定,两者形成的键不是同一种类型;同样,B-B间距小于0.170 nm时有利于构型的稳定,大于0.170 nm时不利于构型的稳定,两者形成的键不是同一种类型。平面构型 4(3)和 2(1)具有更复杂的内部电子结构,并且兼具较高的结合能和较低的能隙差,可以稳定存在的同时具有较强参与反应的能力,是催化材料的理想构型。
[1]LI H,LI H,DAI W L,et al.XPS studies on surface electronic characteristics of Ni-B and Ni-P amorphous alloy and its correlation to their catalytic properties[J].Applied Surface Science,1999,152(1):25-34.
[2]QIU S J,HUANG J L,SHEN F H,et al.Ternary Co-Ni-B amorphous alloy with a superiorelectrochemical performance in a widetemperature range[J].International Journal of Hydrogen Energy,2016,41(6):3955-3960.
[3]RHEN F M F,RICHARDSON D,et al.Investigation of magnetic properties of Ni-B nanotubes at low temperatures[J].IEEE Transaction on Magnetic,2015 52(5):1-4.
[4]GENG Y X,LIN X,WANG Y X,et al.Mechanical and magnetic properties of new(Fe,Co,Ni)-B-Si-Ta bulk glassy alloys[J].ActaMetallurgicaSinica-English Letters,2017,30(7):1-6.
[5]DENG Y,YANG Y,GE L,et al.Preparation of magnetic Ni-P amorphous alloy microspheres and their catalytic performance towards thermal decomposition of ammonium perchlorate[J].Applied Surface Science,2017,425:261-271.
[6]WEI W,ZHAO Y,PENG S C,et al.Hollow Ni-Co-B amorphous alloy nanospheres:facile fabrication via vesicle-assisted chemical reduction and their enhanced catalytic performances[J].Journal of Materials Chemistry A,2014,2(45):19253-19259.
[7]LI Z,GAO Y,WU J,et al.Synthesis and electrochemical characterization of Ni-B/ZIF-8 as electrode materials for supercapacitors[J].Electronic Materials Letters,2016,12(5):645-650.
[8]LI W B,LIL,REN Q L,et al.Ni-B-doped NaAlH 4 hydrogen storage materials prepared bya facile two-step synthesis method[J].Rare Metals,2015 34(9):679-682.
[9]TAN Y,ZHANG W,GAO Y,et al.Synthesis of ordered mesoporous carbon nanofiber arrays/nickel-boron amorphous alloy with high electrochemical performance for supercapacitor[J].Journal of Materials Science,2015,50(13):4622-4628.
[10]WANG Y,TAKEUCHI A,MAKINO A,et al.Nanocrystallization and magnetic mechanisms of Fe85Si2B8-P4Cu1 amorphous alloy by ab initio molecular dynamics simulation[J].Journal of Applied Physics,2014,115(17):3024-3027.
[11]CHEN J S,CAI T T Z W,JING X H,et al.Surface chemistry and catalytic performance of amorphous NiB/HβCatalystfor n-hexane isomerization[J].Applied Surface Science,2016,390:157-166.
[12]ZHANG J,SONG W,et al.Corrosion behavior of electroless Ni-P/Ni-B coating on magnesium alloy AZ91D in NaCl environment[J].International Journal of Electrochemical Science,2016,11:10053-10066.
[13]PERMYAKOVA I E,GLEZER A M,IVANOV A A,et al.Application of laser design of amorphous fecobased alloys for the formation of amorphous-crystalline composites[J].Russian Physics,2016,58(9):1331-1338.
[14]GUO J,HOU Y J,et al.Morphology-controlled synthesis of Ni-B nanoparticles by addition of hydrogen peroxide[J].Materials Letters.2017,200:90-93.
[15]LIU Z L,LI Y N,et al.Preparation and characterization of Ni-B/SiO2sol amorphous catalyst andits catalytic activity for hydrogenation of nitrobenzene[J].Catalysis Communications,2016,85:17-21.
[16]ZHANG J,LI C,LI L,et al.Multi-shaped amorphous alloy Ni-B:ultrasonically aided complexing-reduction preparation, catalytic ability for NaBH4, hydrolysis yielding H2,gas[J].ZeitschriftFürAnorganische Und AllgemeineChemie,2013,640(2):456-461.
[17]LICHT S,HETTIGE C,LAU J,et al.Nano-VB2 synthesis from elemental vanadium and boron:nano-VB2 anode/air batteries[J].Electrochemical Solid-State Letters,2011,15(1):A12-A14.
[18]ORIO M,PANTAZIS D A,NEESE F.Density functional theory[J].Photosynthesis Research,2009,102(2-3):443-453.
[19]HAY P J,WADT W R.Ab initio effective core potentials for molecular calculations.Potentials for K to Au including the outermost core orbitals[J].Journal of Chemical Physics.,1985,82(1):299-310.
[20]方志刚,沈百荣,陆靖,等.Ni-B非晶态合金中电子转移问题的 DFT 研究[J].化学学报,1999,57(8):894-900.

