β-环糊精及其衍生物对薄荷醇的增溶作用及热力学研究
雷华平,姚 杰,张 辉,冯纪南
(1.湘南学院 药学院,湖南 郴州 423043;2.湘南学院 化学生物与环境工程学院,湖南 郴州 423043)
薄荷醇为薄荷挥发油的主要药用成分,具有消炎、止痒、镇痛、防腐、调味等用途[2],其特殊风味能使食用者口气清新。因此,薄荷醇被广泛用于饮料、糖果、糕点及牙膏、香皂、卷烟、化妆品中。此外,在多种非处方药中添加薄荷醇,除有润肤、利尿、健胃还可缓解身体各种肌肉痉挛及疼痛,同时可通过促透作用而影响配伍药物的疗效[1-2],薄荷醇的特性使得它可广泛作用于口腔、鼻腔、消化系统、呼吸系统、中枢神经系统等人体多个部位。由于薄荷醇易挥发性,低水溶性导致稳定性较低,大大增加了其在各领域应用的困难,因此最大化地发挥薄荷醇的使用效率是当前迫切需要解决的问题和研究重点。
本实验采用相溶解度法研究不同环糊精对薄荷醇的包合作用、增溶作用及包合过程中热力学参数的变化,旨在为研制薄荷醇的环糊精包合物制剂提供参考。
1 仪器和材料
紫外分光光度计(UV-6100PC,上海美普达仪器有限公司);电子天平(YP2002,上海越平科学仪器有限公司);数显恒温水浴锅(HH-4,国华电器有限公司);高低温振荡培养箱(HZQ-X500C,上海一恒科学仪器有限公司);分析天平(AUY220,日本岛津公司)。
β-CD和HP-β-CD(均购自山东滨州智源生物科技有限公司);薄荷醇(购自吉安市天源药用油厂);对二甲氨基苯甲醛、硫酸和95%乙醇均为分析纯。
2 方法与结果
2.1 薄荷醇分析方法的建立
2.1.1 标准曲线的绘制
薄荷醇标准液的配制:精密称定100.0 mg经五氧化二磷干燥至恒重的薄荷醇,以乙醇为溶剂定容于100 mL量瓶中,得到1.0 mg/mL的母液,备用。
精密吸取母液0.10,0.20,0.40,0.60,0.80,1.00 mL,分别置于10 mL量瓶中,以1∶1体积比的乙醇/水溶液稀释至刻度,摇匀;分别取1mL各浓度溶液,加入10 mL试管中,加5 mL比色剂5 mg/mL对-二甲氨基苯甲醛的硫酸溶液(1.6体积浓酸/1体积水)[3],摇匀后置于沸水中准确加热2 min,于自来水中冷却2 min,以比色剂+醇水混合物为参比,采用紫外分光光度法,于550 nm处测定吸光度A值;以薄荷醇浓度(C)对 A回归,得薄荷醇溶液的标准曲线方程为C=151.515A-4.197,r=0.994 9,线性范围为20~100 μg/mL。
2.1.2 加样回收率实验
精密称取薄荷醇0.0005,0.0012,0.0022 g,置100mL容量瓶,以水为溶剂定容,得到浓度为0.0050 mg/mL,0.0125 mg/mL,0.0225 mg/mL的薄荷醇100 mL母液,备用;分别向母液中加入HP-β-CD 0.004 5,0.010 8,0.019 7 g,超声5 min使之溶解并以水为溶剂定容至刻度,用0.45 μm微孔滤膜过滤,取滤液于550 nm处测定吸光度值;配制母液,向母液中加入β-CD 0.003 6,0.008 7,0.016 0 g,以相同方法测定吸光度A。测得在β-CD和HP-β-CD中薄荷醇的加样回收率分别为(99.24±2.17)%和(99.23±1.79)%。
2.2 薄荷醇相溶解度的测定
精密称取β-CD和HP-β-CD,配制成不同浓度的水溶液;取上述水溶液各10 mL,置于25 mL容量瓶中,加入过饱和量的薄荷醇,再将不同浓度的混合液置于37 ℃的恒温条件下振荡包合3天;取上清液,0.45 μm孔径的微孔滤膜过滤,经适当稀释后,在波长550 nm处测吸光度A,根据标准曲线线性回归方程分别得出不同浓度的环糊精溶液下对应的薄荷醇的浓度;以β-CD及HP-β-CD浓度(mmol/L)为横坐标,混合液中薄荷醇浓度为纵坐标,得出该温度下薄荷醇/HP-β-CD和薄荷醇/β-CD的相溶解度图;改变测定温度,同法操作,再分别求出温度为37 ℃和45 ℃时不同浓度的CD溶液下对应的薄荷醇的浓度。
薄荷醇在不同浓度β-CD和HP-β-CD中的溶解度及增溶倍数如表1和表2所示。

表1 薄荷醇在β-CD中的溶解度及增溶倍数表

表2 薄荷醇在HP-β-CD中的溶解度及增溶倍数表
表1和表2增溶结果表明,在3种不同温度下,β-CD及HP-β-CD的浓度的增加,薄荷醇的溶解度也随之增加。在相同浓度的环糊精溶液中薄荷醇的溶解度均随温度的升高而增大。衍生物HP-β-CD与母体β-CD相比,显著增加了薄荷醇在水中的溶解度,这是因为HP-β-CD在水中的溶解度(750 g/L)远远大于β-CD在水中的溶解度(18 g/L)。
薄荷醇与β-CD和HP-β-CD形成包合物的相溶解度见图1和图2。

图1 薄荷醇与β-CD形成包合物的相溶解度图

图2 薄荷醇与HP-β-CD形成包合物的相溶解度图
从图1和图2可以看出,在各种温度条件下,薄荷醇的溶解度随β-CD及HP-β-CD浓度的增加而呈直线上升,表明有形成可溶性的包合物。根据相溶解度图求出每条曲线的线性回归方程,根据公式,其中是薄荷醇在水溶液中的固有饱和浓度,相当于相溶解度曲线上的截距,可得到不同温度下薄荷醇与β-环糊精包合物的稳定常数,结果如表3,4所示。
由上可知,随着温度的升高,薄荷醇-β-CD和薄荷醇-HP-β-CD包合物的稳定常数降低,形成薄荷醇-环糊精包合物的趋势减弱,包合平衡向解离方向进行。而且HP-β-CD对薄荷醇的增溶作用明显强于β-CD,稳定常数也高于薄荷醇-β-CD包合物。

表3 不同温度下薄荷醇与β-CD包合物的相溶解度回归方程和稳定常数

表4 不同温度下薄荷醇与HP-β-CD包合物的相溶解度回归方程和稳定常数
2.3 包合过程热力学参数的计算
依据稳定常数K与温度T的关系,即Vant’t Hoff方程lnK=-ΔH/RT+ΔS/R,作出不同温度下薄荷醇与β-CD及HP-β-CD包合反应的lnK-1/T图,并求出其线性回归方程。在实验温度范围内(25~45 ℃),可以认为ΔH和ΔS是与温度无关的常数[4-5]。由回归方程的斜率(-ΔH/R)和截距(ΔS/R)分别求出反应的标准焓变和熵变ΔS。其中R为摩尔气体常数,R=8.314 J·mol-1·K-1。由Gibss-Helmholtz公式ΔG=ΔH-TΔS,求得包合过程的吉布斯自由能变ΔG。所得数据详见表5、6。

表5 薄荷醇与β-CD包合反应的热力学参数
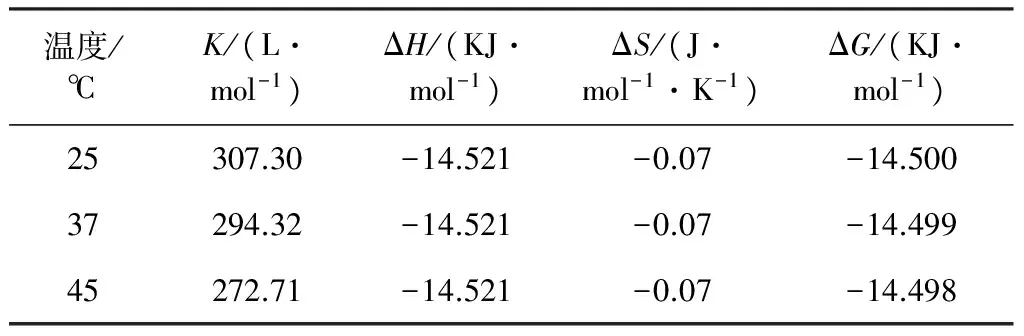
表6 薄荷醇与HP-β-CD包合反应的热力学参数
由表中可得出,薄荷醇与β-CD及HP-β-CD的包合反应中焓变(ΔH)、熵变(ΔS)、吉布斯自由能变化(ΔG)均为负值,表明包合过程为放热反应。
3 讨 论
从表1和表2可以看出,β-CD和HP-β-CD对薄荷醇都具有一定的增溶作用。在不同温度下,薄荷醇的溶解度均随β-CD和HP-β-CD的浓度的增加而呈线性增加。随着温度的升高,在CD浓度相同的情况下,薄荷醇的溶解度也相应增大。β-CD由于受自身溶解度的影响,虽然在一定程度上增加了薄荷醇的溶解度,同时也限制了其增溶作用。
薄荷醇对β-CD和HP-β-CD的相溶解度研究结果表明,在不同温度下,薄荷醇的溶解度均随β-CD和HP-β-CD的浓度的增加而呈不同程度的增加,β-CD 和HP-β-CD与薄荷醇形成的可溶性包合物的摩尔比均为 1∶1。随着温度的升高,薄荷醇与β-CD和HP-β-CD形成包合物的稳定常数K值均降低,表明混合液中形成包合物的趋势会随着温度升高而降低,包合物中的客分子可能越来越多的离开主分子的空囊而进入水相。实验测得的稳定常数都不太大,薄荷醇-HP-β-CD包合物为272~307 L/mol,而薄荷醇-β-CD包合物仅为228~235 L/mol,说明环糊精分子与薄荷醇分子之间的作用力较弱,衍生物 HP-β-CD的包合能力比母体β-CD强。但是,如果K值太大,将导致药物很难从包合物中解离出来发挥作用,因此K值并不是越大越好,必须根据制剂目的确定适宜的K值。
薄荷醇与β-CD和薄荷醇与HP-β-CD在水溶液中的包合过程热力学参数变化是ΔG和ΔH为绝对值较大的负值,ΔS为绝对值很小的负值。这表明包合过程为放热反应,常温常压下可自发形成包合物,降低温度使反应向包合物生成的方向进行,因此在实际操作中应综合考虑选择适宜的反应温度及制备工艺。在包合物中,β-CD和HP-β-CD将薄荷醇限制在分子囊中,使其自由度降低,从而包合体系的混乱度减小,熵值减小。根据热力学第二定律,熵值减小不利于反应的正向进行,但较大的负焓极大的补偿了熵变值小的不利,因此在 3种实验温度下,包合过程的ΔG都小于零。虽然热焓的变化为负值,但比一般的化学反应热小,表明主分子和客分子在进行包合作用时,相互之间没有发生化学反应,故没有形成共价键、离子键等化学键,因此β-环糊精与薄荷醇的包合主要是一种物理过程。从经典的疏水性相互作用的模型中可以得出,体系的焓只稍有增加,而体系的熵则会大量增加,显然整个过程是由熵驱动的。由此可见,包合物的形成并不是一种经典的疏水性作用。因此,分子间氢键和范德华力可能是环糊精与薄荷醇形成包合物的主要作用力,环糊精分子的疏水性作用导致其空腔中的水分子之间不能充分形成氢键而具有非常巨大的焓值。所以如果体系的焓有大幅度的下降则可能是因为极性比水小的薄荷醇分子替代了疏水空腔中富焓的水分子。从能量的角度来看,包合作用可以看成是之前存在于环糊精空囊中的水分子被薄荷醇分子取代的过程,β-CD 和HP-β-CD 分子空腔中的富焓水的释放是包合反应的主要驱动力。
5 结 论
薄荷醇能分别与β-CD和HP-β-CD在常温常压下自发形成包合物,包合过程为放热反应,较低温有利于包合物的形成和稳定。包合物的生成是一种焓驱动的物理过程,主要是分子间氢键和范德华
力作用的结果。薄荷醇与2种环糊精形成的包合物能够增加药物的溶解性,特别是HP-β-CD能够显著提高薄荷醇在水中的溶解度,得到的包合物的稳定性也优于薄荷醇-β-CD,说明衍生物HP-β-CD比母体β-CD对薄荷醇有更强的包合能力。
参考文献:
[1] 陈光亮,佘玉宝,李冬梅.薄荷油及其有效成分药理作用的研究概况[J].中国中医药信息杂志,2000,7(2):33-34.
[2] 李祥,刑文峰.薄荷的化学成分及临床应用研究进展[J].中南药学, 2011, 9(5):362-365.
[3] 彭姣凤,李建成,李庆廷,等.高效装载的水溶性薄荷醇微胶囊的制备研究[J].中国食品添加剂,2007(5):94-98.
[4] 王建华,冯静.超分子材料环糊精与布洛芬包合的热力学测定[J].重庆大学学报,2009,32(6):654-657.
[5] KIM H S, KIM J H. A two-step circle detection algorithm from the intersection chords [J]. Pattern Recognition Letters, 2001(22):787-798.

