厚朴化学成分研究进展△
荆文光,杜杰,王继永,孙晓波,兰青山*
(1.中国医学科学院&北京协和医学院 药用植物研究所,北京 100193;2.中国中药有限公司,北京 102600)
厚朴Magnoliae Officinalis Cortex,始载于《神农本草经》,列为中品,为木兰科植物厚朴MagnoliaofficinalisRehd.et Wils.或凹叶厚朴M.offcinalisRehd.et Wils.var.bilobaRehd.etWils.的干燥干皮、根皮及枝皮[1]。本品性温,味苦、辛,具有燥湿消痰、下气除满的功效,用于湿滞伤中、脘痞吐泻、食积气滞、腹胀便秘、痰饮喘满,为临床常见理气药。现代药理研究表明厚朴具有抗菌、抗炎、抗肿瘤、抗氧化等作用;其中促进胃肠动力、缓解胃肠动力障碍是厚朴主要的药效作用,临床上用于慢性腹泻、便秘、肠梗阻、急慢性胃炎、胃轻瘫、胃十二指肠溃疡等疾病[2]。由于厚朴酚、和厚朴酚等脂溶性成分在药材中含量较高,国内外对厚朴化学成分的研究也主要集中在此类成分,但厚朴作为传统中药多入水煎剂,近年来其水溶性成分研究逐渐兴起,并发现了一些苯乙醇苷类化合物。为了更好的开发厚朴植物资源,本研究对文献报道的厚朴化学成分进行整理和综述,以便后来研究人员查询利用。
1 厚朴化学成分
厚朴中化学成分主要有苯丙素和木脂素类共计65个(1~65);小分子酚醛酯类12个(66~77);苷类化合物共计47个(78~124),其中苯乙醇苷类17个(78~94),酚苷类30个(95~124);生物碱类22个(125~146),黄酮类6个(147~152),但仅在厚朴叶中有发现;萜类和甾体类化合物13个(154~165),另外,厚朴中还有β-桉叶醇(153)、胡萝卜苷(170)和尿苷(171)和无机元素等成分。
1.1木脂素类
木脂素类成分是厚朴中最丰富的一类化学成分,以厚朴酚(magnolol,1)、和厚朴酚(honokiol,2)为代表的联苯型新木脂素是厚朴中发现最早的一类成分,也是主要的药效成分。进入21世纪,随着厚朴中化学成分研究的深入,一些降木脂素、萜类木脂素和二聚木脂素陆续被发现,现分类总结如下。
1.1.1新木脂素 厚朴酚(magnolol,1)[3-7]与和厚朴酚(honokiol,2)[3-8]作为厚朴的代表性成分,其结构主要为两个苯丙素分子以非8-8′相连接成的二聚体,而后报道的化合物也多以两者为基本母核,部分结构在厚朴酚的羟基或者母核上存在甲氧基取代5,5′-二-2-丙烯基-2-羟基-3,2′,3′-三甲氧基-1,1′-联苯(5,5′-di-2-propenyl-2-hydroxy-3,2′,3′-trimethoxy-1,1′-biphenyl,5)[9]、醛基取代厚朴脂素E(houpulin E,6)和羟基取代4,4′,5-三羟基-1,1′-二-2-丙烯基联苯(4,4′,5-trihydroxy-1,1′-di-2-propenylbiphenyl,7)[10];而和厚朴酚的羟基被甲氧基取代构成6′-甲氧基和厚朴酚(6′-O-methylhonokiol,3)[3]和4-甲氧基和厚朴酚(4-methoxyhonokiol,4)[6,11]。2008年Yahara[3]从中国厚朴中陆续分离得到母核侧链的末端烯烃被氧化的结构,并命名为厚朴木脂素A~D(magnolignans A-D,8~11),类似结构还有桧木醇(honokitriol,12)[3-6]、8′,9′-二羟基和厚朴酚(8′,9′-dihydroxyhonokiol,13)[8]、赤式-7-O-甲基桧木醇(erythro-7-O-methylhonokitriol,14)[5,8]、苏式-7-O-甲基桧木醇(threo-7-O-methylhonokitriol,15)[5,8]和7-O-乙基桧木醇(7-O-ethylhonokitriol,16)[8]。而木兰醛C(magnaldehyde C,17)[3]、4′-甲氧基木兰醛(4′-methoxymagndialdehyde,18)[6]、台湾檫木醛(randainal,19)[3-4]、木兰醛B(magnaldehyde B,20)[3,6,8,12]、4′-甲氧基木兰醛B(4′-methoxymagnaldehyde B,21)[6]则是单侧或双侧丙烯基上取代有醛基的联苯木脂素。此外,还有一些其他类的木脂素母核结构不似厚朴酚,如(E)-5-烯丙基-3′-(丙-l-烯基)联苯-2,4′-二醇[(E)-5-烯丙基-3′-(丙-l-烯基)联苯-2,4′-二醇,22][4]、或在侧链上增加羟基取代如5-allyl-5′-(1″-hydroxyallyloxy)biphenyl-2,2′-diol[5-allyl-5′-(1″-hydroxyallyloxy)biphenyl-2,2′-diol,23][4]、或侧链对位羟基被烯丙基和异戊烯基取代例如5,5′-二烯丙基-2′-(烯丙氧基)联苯-2-二醇[5,5′-diallyl-2′-(allyloxy)biphenyl-2-ol,24][4]和5,5′-二烯丙基-2′-(3-甲基丁-2-丁氧基)联苯-2-二醇[5,5′-diallyl-2′-(3-methylbut-2-enyloxy)biphenyl-2-ol,25][4]。
1.1.2萜类木脂素 目前为止,厚朴中发现的萜类木脂素有16个,其结构类型主要是在厚朴酚或和厚朴酚的5位或5′位单侧或者双侧取代单萜,或者在酚羟基上取代倍半萜。1989年,Fukuyama[13]从日本厚朴(MagnoliaobovateThunb.)中分离得到了两个倍半萜木脂素eudesobovatol A(26)和eudesobovatol B(27)[13-14]。1991年该学者又首次报道一个具有神经营养作用的倍半萜类木脂素丁香三环烷厚朴酚(clovanemagnolol,28)[14-16],次年又分离得到了其他4个倍半萜类木脂素,分别为桉醇厚朴酚(eudesmagnolol,29)[14]、桉醇和厚朴酚A(eudeshonokiol A,30)[14],桉醇和厚朴酚B(eudeshonokiol B,31)[14]和丁香烷厚朴酚(caryolanemagnolol,32)[14,16]。2011年Khaing Zina[16]也报道了28和32,并对这两个化合物的神经营养作用进行了验证。单萜木脂素主要是在(和)厚朴酚母核的5位和5′位单侧或双侧取代辣薄荷基(piperityl)或龙脑基(bomyl),包括辣薄荷基厚朴酚(piperitylmagnolol,33)[3-4]、辣薄荷基和厚朴酚(piperitylhonokiol,34)[4]、双辣薄荷基厚朴酚(dipiperitylmagnolol,35)[3,17]和龙脑基厚朴酚(bornylmagnolol,36)[3]。2016年韩国学者从厚朴根皮中分离2个在厚朴酚母核的5位上取代有松油醇基(terpineol)的单萜木脂素,并命名为厚朴脂素F(houpulin F,37)和厚朴脂素G(houpulin G,38),以及在松油醇基上多一个羟基的厚朴脂素H(houpulin H,39),和松油醇基上羟基与厚朴酚的4位羟基脱水成环的厚朴脂素I(houpulin I,40)和厚朴脂素J(houpulin J,41)[7]。
1.1.3氧新木脂素 氧新木脂素又称为二芳基醚类木脂素,即两个C6-C3单元之间以氧原子连接。从厚朴中分离的氧新木脂素有日本厚朴酚(obovatol,42)[3,5]和4,4′-二-2-丙烯基-3,2′,6′-三甲氧基-1,1′-联苯醚[4,4′-di-2-propenyl-3,2′,6′-trimethoxy-1,1′-diphenyl ether,43][9],而萜类木脂素41、26和27也属于氧新木脂素。
1.1.4 二聚木脂素 厚朴中的二聚木脂素多为两个联苯木脂素通过直链或环合的方式连接,其中Yahara[3]报道了以两个厚朴酚为单位的二聚体木兰木脂素G(magnolignan G,44)和一个非常罕见的以两个氧新木脂素为单位的二聚体木兰木脂素F(magnolignan F,45)。厚朴脂素A[18](houpulin A,46)与厚朴脂素B(houpulin B,47)[18]则是以两个和厚朴酚为单位构成的二聚体。厚朴脂素(houpulin) C(48)[18]、D(49)[18]、K(50)[7]和L(51)[7]都是两分子木脂素以吡喃环的形式结合。木兰木脂素(magnolignan)H(52)[3]和I(53)[3]则是以呋喃环的方式连接。
1.1.5其他类型木脂素 其他类型木脂素主要包括二芳基丁烷类,有1-(4-羟基-3-甲氧基苯基-2-[4-ω-羟丙基]-2-甲氧基苯氧基]丙烷-l,3-二醇{1-(4-hydroxy-3-methoxyphenyl-2-[4-ω-hydroxypropyl]-2-methoxyphenoxy]propane-l,3-diol,54}[3];苯骈呋喃类有木兰木脂素E(magnolignan E,55)[3]、4-烯丙基-2-(2′-甲基苯并呋喃-5′-基)苯酚[4-allyl-2-(2′-methylbenzofuran-5′-yl)phenol,56][4]和从厚朴叶中分离得到的落叶松脂素(lariciresinol,57)[10]。杨竹雅[10]从厚朴叶中分离出双四氢呋喃类木脂素丁香脂素(syringaresinol,58)[3,5,17];吴锦玉从凹叶厚朴中分离出鹅掌楸树脂醇A(lirioresinol A,59)[19]。此外还有一些联苯型的降木脂素,包括台湾檫木酚(randaiol,60)[3-5]、厚朴三醇B(magnatriol B,61)[3]、木兰醛D(magnaldehyde D,62)[3-5]、木兰醛E(magnaldehyde E,63)[3,6,8]、4′-甲氧基木兰醛E(4′-methoxymagnaldehyde E,64)[3,6]和厚朴脂素M(houpulin M,65)[7],所有木脂素类化学成分结构见图1。

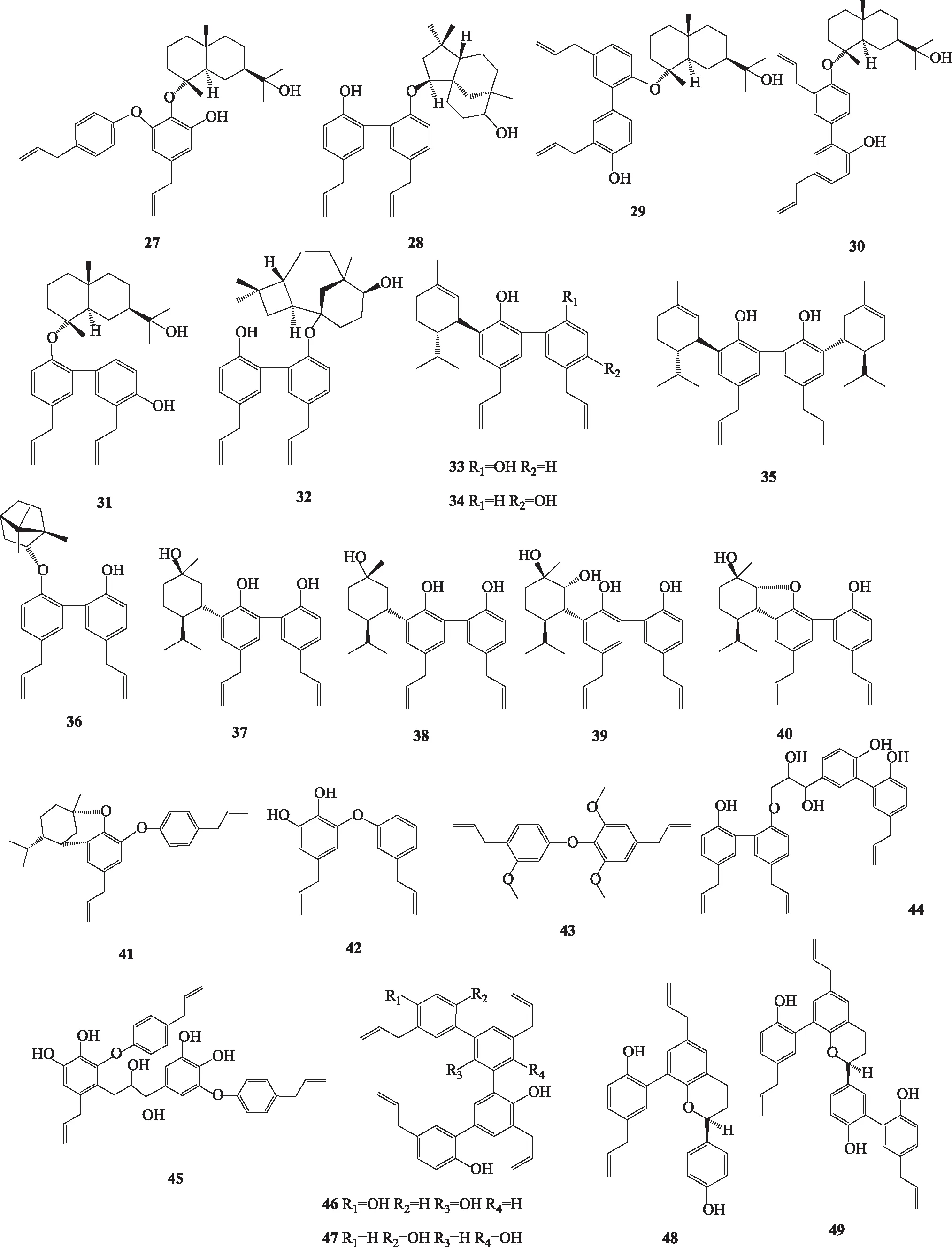
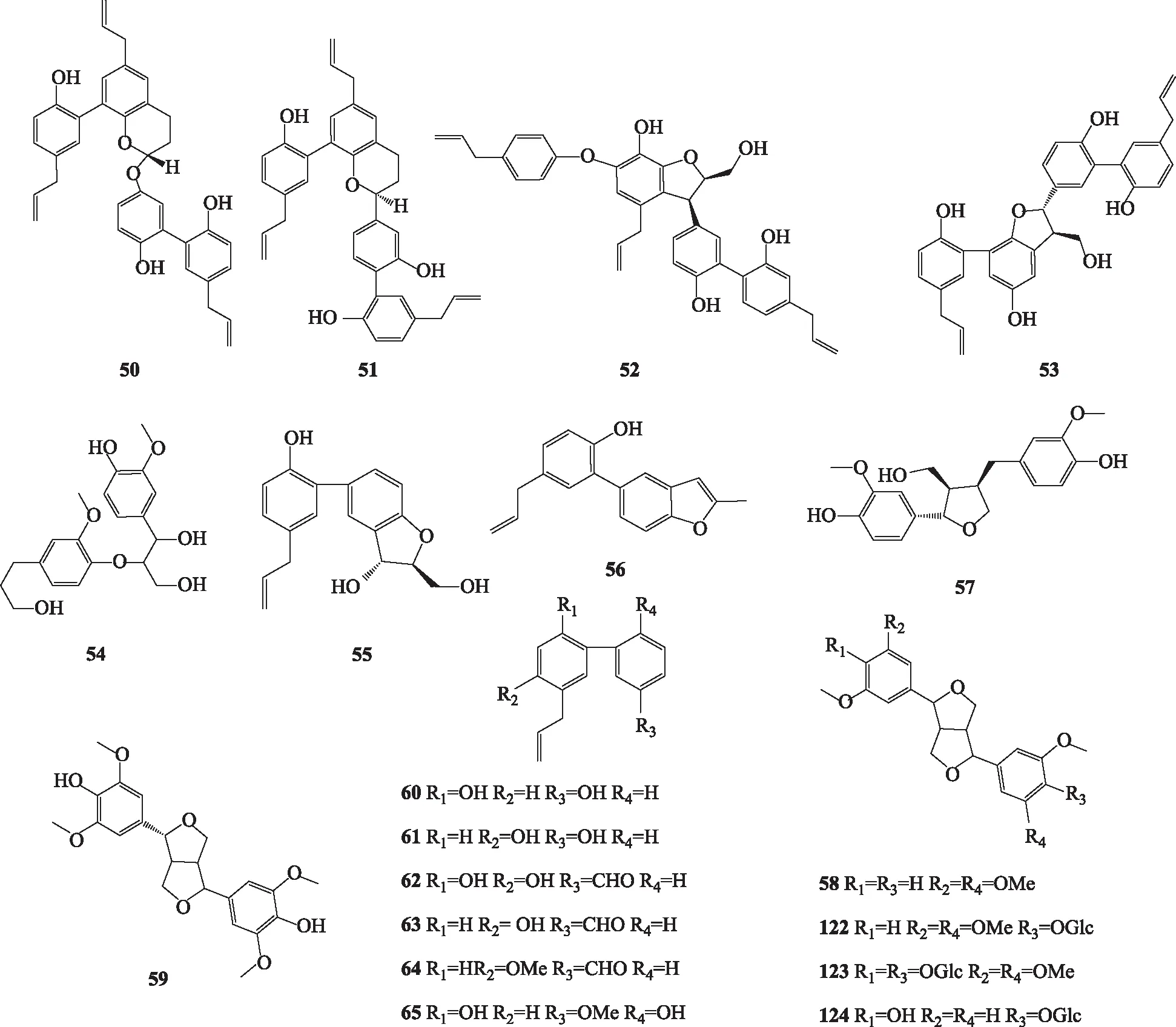
图1 厚朴中的木脂素类化合物
1.2 酚、醛和酯类
小分子的酚酸、醛类化合物在自然界普遍,具有广泛的生理活性。从厚朴中分离报道的醛类化合物有丁香醛(syringaldehyde,66)[5]、对羟基苯甲醛(p-hydroxylbenzaldehyde,67)[5]、芥子醛(sinapic aldehyde,68)[6,17]、松柏醛(coniferaldehyde,69)[5]和吲哚-3-甲醛(indole-3-aldehyde,70)[19];酚酸类主要有咖啡酸(caffeic acid,71)[6,17]、香草酸(vanilic acid,72)[20]、丁香酸(syringic acid,73)[20]、咖啡酸甲酯(methyl caffeate,74)[21]、松柏醇(coniferolalcohol,75)[5]、O-甲基丁香酚(O-methyleugenol,76)[9]和木兰酮(magnolianone,77)[5],其结构见图2。
1.3 苷类化合物
2012年Yu从厚朴水溶性部位分离得到苯乙醇苷类化合物木兰苷(magnoloside)A(78)[21-22]、D(79)[21-22]、E(80)[21-22]和B(81)[21-23]后,苷类化合物研究成为了厚朴化学成分研究的热点。薛珍珍[23]在此基础上从厚朴的水溶性部位又发现了大量的苯乙醇苷类和酚苷类化合物,且苯乙醇苷相比于酚苷类有显著的α-葡萄糖苷酶抑制活性及肿瘤细胞毒活性。由于传统中医临床上厚朴多以水煎入药,水溶性苷类成分的研究为厚朴药效物质基础的阐述奠定了基础。
1.3.1苯乙醇苷 厚朴中的苯乙醇苷类化合物在糖基部分除含有葡萄糖(Glc)、鼠李糖(Rha)、和芹糖(Api)外,还含有自然界非常少见的阿洛糖(Allose),且糖上还存在香豆酰基(coumaroyl)、咖啡酰基(caffeoyl)、丁香酰基(syringoyl)、阿魏酰基(feruloyl)和香草酰基(vanilloyl)等取代基。薛珍珍在前人基础上,从厚朴的水溶性部位又分离到了11个新的苯乙醇苷,分别为木兰苷F~P(magnoloside F-P,82~92)[23-24]和一个已知的苯乙醇苷2-(3,4-二羟基苯基)乙醇-1-O-[4-O-咖啡酰基-2-O-α-L-吡喃鼠李糖基-3-O-α-L-吡喃鼠李糖基-6-O-β-D-吡喃葡萄糖基]-β-D-吡喃葡萄糖苷{2-(3,4-dihydroxyphenyl)ethanol-1-O-[4-O-caffeoyl-2-O-α-L-rhamnopyranosyl-3-O-α-L-rhamnopyranosyl-6-O-β-D-glucopyranosyl]-β-D-glucopyranoside,93}[23-25]。韩国学者从厚朴中分离出了毛蕊花糖苷(acteoside,94)[5]。而阿洛糖上存在咖啡酰基取代的苯乙醇苷类化合物在不同溶媒和温度下,咖啡酰基的取代位置会发生转移,如木兰苷(magnoloside)A(78)、D(79)和M(89)三者之间会相互转化[26]。迄今为止,从厚朴中共发现17个苯乙醇苷,其结构见图3。
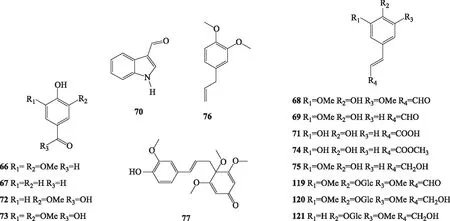
图2 厚朴中小分子酚酸、醛和酯类化合物

图3 厚朴中苯乙醇苷类化合物
1.3.2 酚苷 酚苷类苷元多以咖啡酸、芥子酸、香草酸和肉桂酸为主,糖部分主要以葡萄糖(Glc)和鼠李糖(Rha)为主,少数连接有芹糖(Api)和木糖(Xyl)。晏仁义等[20]从厚朴中分离得到一个苷元为丁香酸的新酚苷类化合物丁香酸-4-O-β-D-吡喃葡萄糖基-(1→5)-α-L-吡喃鼠李糖苷[syringic acid-4-O-β-D-glucopyranosyl-(1→5)-α-L-rhamnopyranoside,95]和6个已知的酚苷丁香酸-4-O-α-L-吡喃鼠李糖苷(syringic acid-4-O-α-L-rhamnopyranoside,96)、香草酸-4-O-α-L-鼠李糖苷(vannilic acid-4-O-α-L-rhamnoside,97)、3,4-二甲氧基苯酚-β-D-呋喃芹糖基-(1→6)-β-D-吡喃葡糖糖苷[3,4-dimethoxyphenol-β-D-apiofuranosyl-(1→6)-β-D-glucopyranoside,98]、3,4,5-三甲氧基苯酚-β-D-呋喃芹糖基-(1→6)-β-D-吡喃葡糖糖苷[3,4,5-trimethoxyphenol-β-D-apiofuranosyl-(1→6)-β-D-glucopyranoside,99]、1-(α-L-鼠李糖基-(1→6)-β-D-吡喃葡糖糖氧基)-3,4,5-三甲氧基苯[1-(α-L-rhamnosyl-(1→6)-β-D-glucopyranosyloxy)-3,4,5-trimethoxybenzene,100]、3,4,5-三甲氧基苯基-1-O-β-D-吡喃木糖基-(1→6)-β-D-吡喃葡糖糖苷[3,4,5-trimethoxyphenyl-1-O-β-D-xylopyranosyl-(1→6)-β-D-glucopyranoside,101]。薛珍珍[23-24]从厚朴中共分离得到10种新的酚苷命名为木兰苷(magnoloside) Q~Z(102~111)以及已知酚苷1,1′-二苯基-6′,8′,9′-三羟基-3-烯丙基-4-O-β-D-吡喃葡糖糖苷(1,1′-dibenzene-6′,8′,9′-trihydroxy-3-allyl-4-O-β-D-glucopyranoside,112)和淫羊藿次苷E5(icariside E5,113)。余盛贤[22]从厚朴甲醇超声提取物中分离得到木莲苷D(manglieside D,114)和柴胡木脂素苷A(saikolignanoside A,115)。卓越等[11]首次从厚朴中分离得到3,4,5-三甲氧基苯基-β-D-吡喃葡糖糖苷(3,4,5-trimethoxyphenylβ-D-glucopyranoside,116),同时分离得到其他3种酚苷:3,4-二羟基-烯丙基苯-3-O-α-L-吡喃鼠李糖基-(1→6)-β-D-吡喃葡糖糖苷[3,4-dihydroxy-allylbenzene-3-O-α-L-rhamnopyranosyl-(1→6)-β-D-glucopyranoside,117]、3,4-二羟基-烯丙基苯-3-O-α-L-吡喃鼠李糖基-(1→2)-β-D-吡喃葡糖糖苷[3,4-dihydroxy-allylbenzene-3-O-α-L-rhamnopyranosyl-(1→2)-β-D-glucopyranoside,118]和芥子醛-4-O-β-D-吡喃葡糖糖苷(sinapaldehyde-4-O-β-D-glucopyranoside,119)。杨竹雅[10]为明确厚朴叶血管活性作用物质基础,从厚朴叶中分离得到了紫丁香苷(syringin,120)、松柏苷(coniferin,121)以及3个木脂素苷丁香树脂酚-4′-O-β-D-吡喃葡糖糖苷(syringaresinol-4′-O-β-D-glucopyranoside,122)[10,27]、丁香树脂酚-4,4′-二-O-β-D-吡喃葡糖糖苷(syringaresinol-4,4′-bis-O-β-D-glucopyranoside,123)[10,20]和松脂素-4-β-D-吡喃葡萄糖苷(pinoresionol-4-O-β-D-glucopyranoside,124)[28],化合物结构见图4。
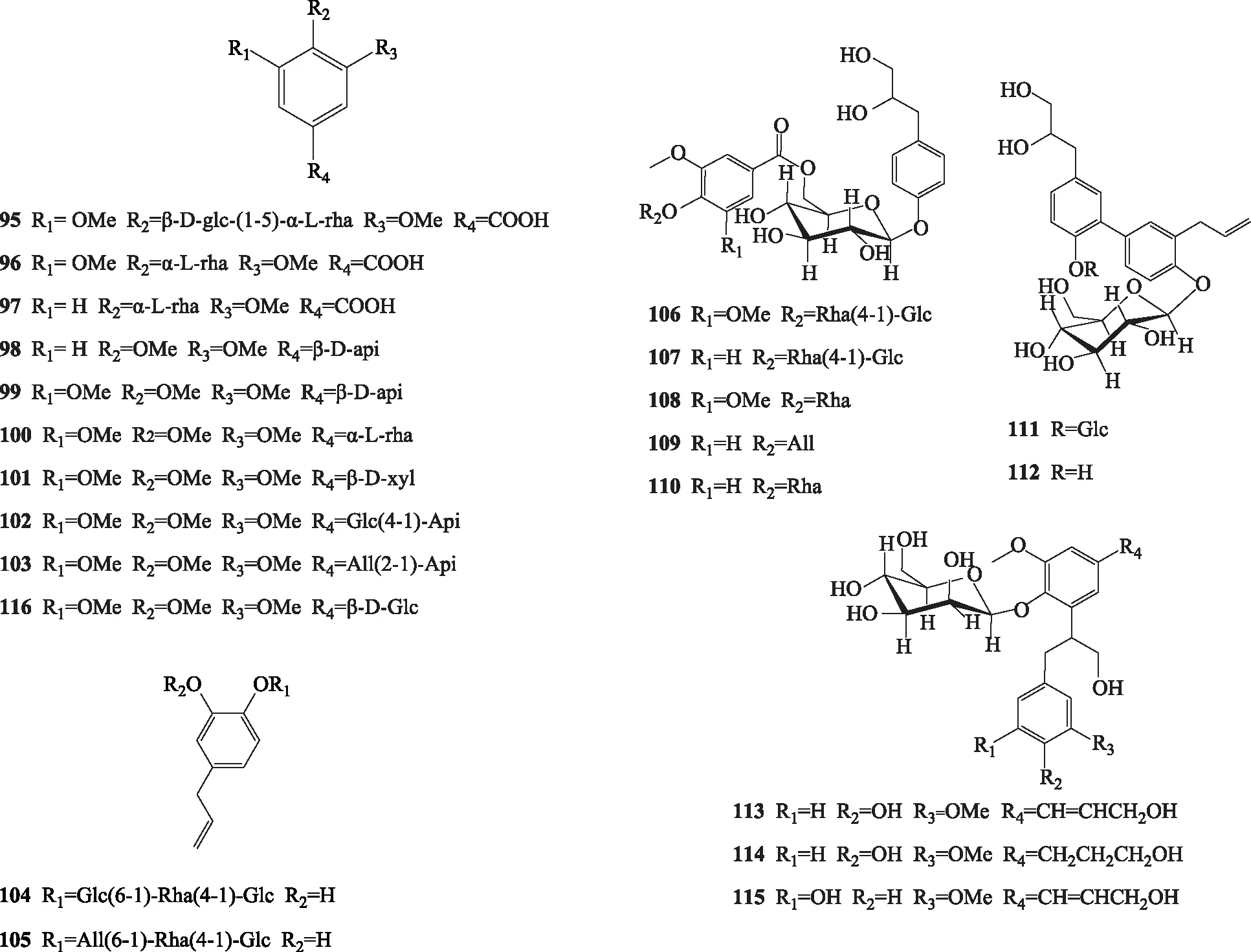
图4 厚朴中酚苷类化合物
1.4 生物碱类
厚朴中的生物碱以木兰花碱(magnoflorine,125)[29-30]和木兰箭毒碱(magnocurarine,128)[29-30]为代表,郭健[30]从厚朴干皮中分离得到10个生物碱成分,其中6个季铵型生物碱,包括3个阿朴啡类生物碱:木兰花碱(magnoflorine,125)、4-酮基木兰花碱(4-keto-magnoflorine,126)和巴婆碱(asimilobine,127),4个苄基异喹啉类生物碱:木兰箭毒碱(magnocurarine,128)、oblongine(129)、N-甲基网叶番荔枝碱(tembetarine,130)、3,4-去氢木兰箭毒碱(3,4-dehydromagnocurarine,131)以及3个有机胺类生物碱反式-N-阿魏酰腐胺(trans-N-feruloylputrescine,132)、顺式-N-阿魏酰腐胺(cis-N-feruloylputrescine,133)和甜菜碱(betaine,146),而131和126为新的生物碱结构。Guo等[31]从厚朴根皮中分离得到一个新阿朴啡类生物碱厚朴新碱(magnofficine,134) 和6个已知的生物碱:番荔枝碱(anonaine,135)、10-羟基番荔枝碱(anolobine,136)、anaxagoreine(137)、瑞枯灵(reticuline,138)、鹅掌楸碱(liriodenine,139)、7-酮基去氢巴婆碱(7-oxodehydroasimilobine,140)。黄洪燕[32]首次从凹叶厚朴中得到5个已知的异喹啉生物碱:罗默碱(roemerine,141)、鹅掌楸尼定(lirinidine,142)、观音莲明碱(lysicamine,143)、异萨苏林(isosalsoline,144)、N-甲基异萨苏林(N-methylisosalsoline,145),所有生物碱的结构见图5。木兰花碱和木兰箭毒碱作为厚朴中生物碱含量较大的成分,龙飞[33]对厚朴中的木兰箭毒碱含量进行了测定,薛珍珍等[34]对木兰花碱含量进行了测定,综合结果表明不同产地、不同等级的厚朴药材和饮片中两者含量差异较大。

图5 厚朴中生物碱类化合物
1.5 黄酮类
杨竹雅[10]从厚朴叶的正丁醇溶性部位分离出槲皮苷(quercitrin,147)、阿福豆苷(afzelin,148)、异鼠李素-3-O-β-D-葡萄糖苷(isorhamnetin-3-O-β-D-glucoside,149)、南酸枣苷(choerospondin,150)和5,7-二羟基色原酮-7-O-β-D-葡萄糖苷(5,7-dihydroxychromone-7-O-β-D-glucoside,151)等5个黄酮苷类化合物,经验证槲皮苷和阿福豆苷具有较好的舒张血管活性,可将槲皮苷作为厚朴叶舒张血管的主要活性物质用于质量控制研究。此外,龙飞等[33]也从厚朴叶中分离得到槲皮苷(quercitrin,147)和芦丁(rutin,152),其结构见图6。

图6 厚朴中黄酮类化合物
1.6 挥发油
厚朴中挥发油的含量约为1%,其化学成分复杂,其中主要成分为桉叶醇类及其同分异构体。陈张金等[35]采用毛细管气相色谱法测定厚朴中β-桉叶醇的含量在0.06%~0.35%之间,且厚朴药材中的含量明显高于饮片。李玲玲[36]采用GC-MS比较了厚朴不同部位挥发油成分,从中共鉴定了48个化合物,其中β-桉叶醇(β-eudesmol,153,结构见图7)及其同分异构体分别占干皮、根皮、枝皮挥发油总量的40.51%,38.48%,49.34%。由于厚朴中的挥发油成分以枝皮中含量较高,树龄不同,挥发油含量也不尽相同,而传统用药认为篼朴(靠近根部树皮)和根朴质量优于枝朴,故厚朴中的挥发油成分与厚朴的药效有何关联值得深入研究。
1.7 其他化合物
厚朴中含存在一些萜类化合物,晏仁义从厚朴中分离两个萜类化合物布卢门醇A(blumenol A,154)和布卢门醇B(blumenol B,155)[20]。李平等[37]从厚朴超临界提取物中首次分离出倍半萜化合物柳杉双醇(crytomeridiol,156)。吴锦玉等[19]报道了凹叶厚朴中的萜类化合物S-(+)-去氢吐叶醇(S-(+)-dehydrovomifoliol,157)、蚱蜢酮(grasshopper ketone,158)和黑麦草内酯(loliolide,159)。同时谷甾醇(β-sitosterol,160)、β-谷甾烯酮(β-sitostenone,161)、豆甾-4,22-二烯-3-酮(stigmasta-4,22-dien-3-one,162)、豆甾醇(stigmasterol,163)、3β-羟基豆甾-5-烯-7-酮(3β-hydroxystigmast-5-en-7-one,164)和3β-羟基豆甾-5,22-二烯-7-酮(3β-hydroxystigmast-5,22-dien-7-one,165)等甾体类化合物也有报道[4]。此外,厚朴叶中还报道含有棕榈酮(palmitone,166)[33]、正二十九烷酸(nonacosanoic acid,167)[19]、花生酸(arachidic acid,168)[33]、二十六烷醇(hexacosanol,169)[33]、胡萝卜苷(daucosterol,170)[33]和尿苷(uridine,171)[28],部分化合物结构见图7。厚朴中的无机成分包括铁、铜、锌、锰、钙、镁等微量元素[38]。
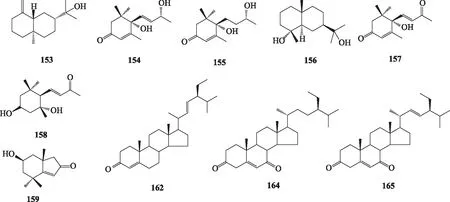
图7 厚朴中其他化合物
2 结语
目前厚朴的化学成分研究多集中在厚朴酚与和厚朴酚的分离、分析以及药理作用阐述等方面,随着厚朴中水溶性成分报道的增多,为厚朴的开发利用带来了新的方向。此外,由于临床中厚朴多入水煎剂,而厚朴酚与和厚朴酚为脂溶性成分,在水煎剂中转移率较低,因此水溶性成分的深入研究,将为厚朴药效物质基础的阐述带来新的思路和基础。厚朴中的挥发油成分以β-桉叶醇为主要成分,而根据文献报道[39],β-桉叶醇可以作为苍术健脾燥湿作用的有效活性成分之一,具有明显促进正常小鼠的胃肠运动,而厚朴常与苍术配伍使用,用于湿滞脾胃证,如方剂平胃散,因此β-桉叶醇是否也是厚朴“下气除满”的活性成分,值得药理实验研究和验证。厚朴叶与传统皮类入药部位化学成分有所不同,叶中含有丰富的黄酮类化合物,这为厚朴叶资源利用开辟了重要的新途径。伴随新的分离分析技术的创新发展,厚朴中微量的化学成分逐渐被发现,这为进一步合理开发厚朴资源提供了新的物质基础,为其临床研究提供了有效的参考价值。
[1] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2015:251-252.
[2] 张林,王洪.厚朴的现代药理研究进展[J].内蒙古中医药,2010,29(8):105-107.
[3] Yahara S,Nishiyori T,Kohda A,et al.Isolation and characterization of phenolic compounds from Magnoliae Cortex produced in China[J].Chem Pharm Bull,2008,39(8):2024-2036.
[4] Kuo W L,Chung C Y,Hwang T L,et al.Biphenyl-type neolignans fromMagnoliaofficinalisand their anti-inflammatory activities[J].Phytochemistry,2013,85(2):153-160.
[5] Shen C C,Ni C L,Shen Y C,et al.Phenolic constituents from the stem bark ofMagnoliaofficinalis[J].J Nat Prod,2009,72(1):168-171.
[6] Youn U J,Chen Q C,Jin W Y,et al.Cytotoxic lignans from the stem bark ofMagnoliaofficinalis[J].J Nat Prod,2007,70(10):1687-1689.
[7] Shih H C,Kuo P C,Wu S J,et al.Anti-inflammatory neolignans from the roots ofMagnoliaofficinalis[J].Bioorg Med Chem,2016,24(7):1439-1445.
[8] Zhang B B,Wang H,Chen S Z.Quantification and structural identification of related phenolic compounds in the raw medicinal material honokiol[J].J Chin Pharm Sci,2013,22(5):420-426.
[9] Baek N I,Kim H,Lee Y H,et al.A new dehydrodieugenol fromMagnoliaofficinalis.[J].Planta med,1992,58(6):566-568.
[10] 杨竹雅.厚朴叶药用价值研究[D].成都:成都中医药大学,2012.
[11] 卓越,王建农,邹本良,等.厚朴水溶性成分分离[J].中国实验方剂学杂志,2015,21(9):39-41.
[12] Youn U J,Fatima N,Chen Q C,et al.Apoptosis-inducing and antitumor activity of neolignans isolated fromMagnoliaofficinalisin HeLa cancer cells[J].Phytother Res,2013,27(9):1419-22.
[13] Fukuyama Y,Otoshi Y,Kodama M,et al.Novel neurotrophic sesquiterpene-neolignans frommagnoliaobovata[J].Tetrahedron Lett,1989,30(43):5907-5910.
[14] Fukuyama Y,Otoshi Y,Miyoshi K,et al.Neurotrophic sesquiterpene-neolignans frommagnoliaobovata:structure and neurotrophic activity[J].Tetrahedron,1992,48(3):377-392.
[15] Fukuyama Y,Otoshi Y,Kodama M,et al.Structure of clovanemagnolol,a novel neurotrophic sesquiterpene-neolignan frommagnoliaobovata[J].Tetrahedron Lett,1990,31(31):4477-4480.
[16] Khaing Z,Kang D,Camelio A M,et al.Hippocampal and cortical neuronal growth mediated by the small molecule natural product clovanemagnolol[J].Bioorg Med Chem Lett,2011,21(16):4808-4812.
[17] Youn U J,Lee I S,Chen Q C,et al.A cytotoxic monoterpene-neolignan from the stem bark ofMagnoliaofficinalis[J].Nat Prod Sci,2011,17(2):95-99.
[18] Shih H C,Hwang T L,Chen H C,et al.Honokiol dimers and magnolol derivatives with new carbon skeletons from the roots ofMagnoliaofficinalisand their inhibitory effects on superoxide anion generation and elastase release[J].Plos One,2013,8(5):8750-8750.
[19] 吴锦玉,吴岩斌,易骏,等.凹叶厚朴叶的化学成分研究[J].中草药,2013,44(21):2965-2968.
[20] Yan R Y,Liu H L,Zhang J Y,et al.Phenolic glycosides and other constituents from the bark ofMagnoliaofficinalis[J].J Asian Nat Prod Res,2014,16(4):400.
[21] Yu S X,Yan R Y,Liang R X,et al.Bioactive polar compounds from stem bark ofMagnoliaofficinalis[J].Fitoterapia,2012,83(2):356-361.
[22] 余盛贤.基于水溶性成分分析的厚朴质量评价[D].北京:中国中医科学院,2011.
[23] 薛珍珍.厚朴水溶性化学成分及其活性筛选[D].北京:中国中医科学院,2015.
[24] Xue Z Z,Yan R Y,Yang B.Phenylethanoid glycosides and phenolic glycosides from stem bark ofMagnoliaofficinalis[J].Phytochemistry,2016,127:50.
[25] Porter E A,Kite G C,Veitch N C,et al.Phenylethanoid glycosides in tepals ofMagnoliasalicifoliaand their occurrence in flowers of Magnoliaceae[J].Phytochemistry,2015,117:185-193.
[26] Xue Z Z,Li H,Yang B.Positional isomerization of phenylethanoid glycosides fromMagnoliaofficinalis[J].Nat Prod Commun,2016,11(12):1861-1863.
[27] 杨竹雅,卫莹芳,周志宏,等.厚朴叶中具血管活性作用部位的化学成分研究[J].中草药,2013,44(3):260-264.
[28] 杨竹雅,卫莹芳,周志宏,等.厚朴叶中具血管舒张作用的化学成分研究[J].天然产物研究与开发,2012,24(3):298-302.
[29] Yan R,Wang W,Guo J,et al.Studies on the alkaloids of the bark ofMagnoliaofficinalis:isolation and on-line analysis by HPLC-ESI-MS(n)[J].Molecules,2013,18(7):7739-50.
[30] 郭健.厚朴中生物碱成分及炮制地厚朴化学成分影响的研究[D].成都:西南交通大学,2012.
[31] Guo Z F,Wang X B,Luo J G,et al.A novel aporphine alkaloid fromMagnoliaofficinalis[J].Fitoterapia,2011,82(4):637.
[32] 王洪燕,周先礼,黄帅,等.凹叶厚朴中生物碱成分的研究[J].华西药学杂志,2007,22(1):30-33.
[33] 龙飞.厚朴资源综合利用研究—厚朴叶药用价值的初步研究[D].成都:成都中医药大学,2006.
[34] 薛珍珍,晏仁义,余盛贤,等.HPLC-DAD测定厚朴中6种活性成分的含量[J].中国实验方剂学杂志,2014,20(22):45-49.
[35] 陈张金,余华丽,毛菊华,等.毛细管气相色谱法测定厚朴中β-桉叶醇的含量[J].中国药师,2016,19(3):602-604.
[36] 李玲玲.厚朴挥发油化学成分研究[J].中草药,2001,8(32):686-687.
[37] 李平,何文妮,孙博航,等.厚朴超临界提取物的化学成分研究[J].中国现代中药,2008,10(2):26-27.
[38] 周利兵,陈伟,张红雨.不同地区厚朴中6种微量元素的主成分分析和聚类分析[J].安徽农业科学,2010,38(20):10674-10675.
[39] 王金华,薛宝云,梁爱华,等.苍术有效成分β-桉叶醇对小鼠小肠推进功能的影响[J].中国药学杂志,2002,37(4):266-268.

