白鲜皮中脂肪酸类成分的分离与结构鉴定*
杨圣财,王剑丽,李 正,郑 畅,王 涛,张 祎
(天津中医药大学,天津市中药化学与分析重点实验室,天津 300193)
白鲜皮是白鲜(Dictamnus dasycarpus Turcz.)的干燥根皮,其主要成分为萜、柠檬苦素、生物碱、脂肪酸等化学成分,首录于《神农本草经》中品系列,性苦、寒,归脾、胃、膀胱经,具有清热燥湿、祛风解毒之功效[1]。现代药理研究表明,白鲜皮具有抗菌、抗肿瘤、抗炎、抗变态反应、抗溃疡、抗冠状动脉粥样硬化及保护肝脏、神经等多种生理活性[2]。作者采用多种色谱法相结合,对白鲜皮70%乙醇提取物的化学成分进行分离制备,并利用与文献[3-4]类似的方法,鉴定了5个脂肪酸类化合物,分别为亚油酸(1)、1-O-linoleoyl-glycerol(2)、油酸(3)、棕榈酸(4)、α-棕榈酸单甘油酯(5)。其中2为首次从白鲜属中分离得到,5为首次从该植物中分离得到的化合物。图1。
1 仪器与材料
Bruker 500MR超导核磁共振波谱仪(德国Bruker公司,AvanceⅢ 500 MR),安捷伦 6520系列四级杆-飞行时间质谱仪(美国Aglient公司,6520 Accurate-Mass Q-TOF LC/MS)。正相柱色谱用硅胶(48~75 μm),高效液相色谱法用分析柱以及制备柱型号分别为 [Cosmosil 5C18-MS-II(250 mm×4.6 mm,5 μm)及(250 mm × 20 mm,5 μm),Cosmosil PBr(250 mm×4.6 mm,5 μm)及(250 mm×20 mm,5 μm),日本 Nacalai Tesque公司],氘代试剂(北京崇熙科技孵化器公司)。分析/色谱纯氯仿、乙酸乙酯、石油醚、正己烷、甲醇、乙腈、冰醋酸等试剂购自天津康科德科技有限公司。白鲜皮购自于河北安国,由天津中医药大学李天祥教授鉴定为白鲜属植物白鲜(Dictamnus dasycarpus Turcz.)的干燥根皮。标本保存于天津中医药大学中医药研究中心。
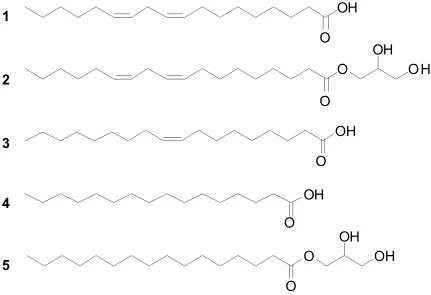
图1 化合物1-5的结构
2 提取与分离
取干燥白鲜皮(9.0 kg),用70%乙醇溶液加热回流提取,减压回收溶剂,得浸膏1 910.1 g。取浸膏1 725.3 g溶于水,用EtOAc-H2O萃取,得到EtOAc和H2O层萃取物分别为267.3 g和1454.9 g。EtOAc层萃取物(175.0 g)经硅胶柱层析 [正己烷-乙酸乙酯(100∶1 → 20∶1 → 10∶1 → 5∶1 → 3∶1 → 1∶1 → 0∶1,v/v)→ MeOH],得到 10 个组分(Fr.E1~Fr.E10)。FractionE5(3.9g)经制备型高效液相色谱法(PHPLC)分离制备[MeOH-H2O(90∶10,v/v)5C18-MS-II柱],得到 10个组分(Fr.E5-1~5-10)。Fraction E5-8(190.0 mg)经 PHPLC 分离制备 [MeOH-H2O(88∶12,v/v)+1%HAc,PBr柱],得到棕榈酸(4,57.2 mg)和油酸(3,32.3 mg)。Fraction E6(13.0 g)经硅胶柱层析[石油醚-氯仿(1∶1 → 1∶5,V/V)→ 氯仿-丙酮(100∶0→ 100∶1 → 100∶2 →0∶100,V/V)],得到 5 个组分(Fr.E6-1~Fr.E6-5)。Fraction E6-3(3.4 g)经 PHPLC 分离制备 [MeOH-H2O(85∶15,v/v),PBr柱],得到 8 个组分(Fr.E6-3-1~Fr.E6-3-8)。Fraction E6-3-6(107.3 mg)经 PHPLC 分离制备 [MeOH-H2O(90∶10,V/V),PBr柱],得亚油酸(1,34.5 mg)。Fraction E8(37.0 g)经正己烷溶解后离心,将上清液(35.1 g)经硅胶柱层析[石油醚-乙酸乙酯(5∶1 → 3∶1 → 2∶1 →1∶1 → 0∶1,V/V)],得到 9 个组分(Fr.E8-2-1~Fr.E8-2-9)。Fraction E8-2-6(7.1 g)经硅胶柱层析 [石油醚-乙酸乙酯(5∶1 → 4∶1 → 3∶1 → 2∶1 → 1∶1 → 0∶1,V/V)→ 甲醇],得 8 个组分(Fr.E8-2-6-1~Fr.E8-2-6-8)。Fraction E8-2-6-4(3.5 g)经 PHPLC 分离制备[MeOH-H2O(85∶15,V/V),5C18-MS-II柱],得到 10个组分(Fr.E8-2-6-4-1~Fr.E8-2-6-4-10)。Fraction E8-2-6-4-6(50.1 mg)与 E8-2-6-4-7(66.7 mg)分别经 PHPLC 分离制备 [MeOH-H2O(90∶10,V/V),5C18-MS-II 柱],得到 1-O-linoleoyl-glycerol(2,33.5 mg)和 α-棕榈酸单甘油酯(5,29.5 mg)。
3 结构鉴定
化合物1:黄色油状固体。高分辨Q-TOF-ESIMS给出其准分子离子峰m/z 279.2324[M-H]-(calcd for C18H31O2,279.2330),确定其分子式为 C18H32O2。1H NMR(CDCl3,500 MHz)谱数据:δ 2.33(2H,t,J=7.5 Hz,H2-2),1.63(2H,m,H2-3),1.32(10H,m,H2-4~7 and 15),2.05(4H,m,H2-8 and 14),5.37(2H,m,H-9 and 13),5.34(1H,m,overlapped,H-10),2.77(2H,t,J=7.0 Hz,H2-11),5.34(1H,m,overlapped,H-12),1.28(2H,m,H2-16),1.27(2H,m,H2-17),0.89 (3H,t,J=6.5 Hz,H3-18)。13C NMR(CDCl3,125 MHz)谱数据:δ 180.0(C-1),34.2(C-2),24.8(C-3),29.1~29.6(C-4~7 and 15),27.2(C-8 and 14),130.2(C-9 and 13),128.1(C-10),25.7(C-11),127.9(C-12),31.6(C-16),22.6(C-17),14.1(C-18)。C-8和C-14的化学位移为27.2,确定其构型为9Z,12Z[5-6]。其1H、13C NMR谱数据与文献[14]中报道的亚油酸基本一致,故鉴定化合物1为亚油酸(linoleic acid)。
化合物2:黄色油状固体。高分辨Q-TOF-ESIMS给出其准分子离子峰m/z 433.1956[M+Br]-(calcd for C21H38O4Br,433.1959),确定其分子式为C21H38O4。1H NMR(C5D5N,500 MHz)谱数据:δ 2.34(2H,t,J=7.5 Hz,H2-2),1.63 (2H,m,H2-3),1.14~1.28(6H,m,H2-4~6),1.34(2H,m,H2-7),2.08(2H,m,H2-8),5.47(2H,m,H-9 and 13),5.48(2H,m,H-10 and 12),2.91(2H,t,J=5.5 Hz,H2-11),2.11(2H,m,H2-14),1.36(2H,m,H2-15),1.26(2H,m,overlapped,H-16 and 17),0.86(3H,t,J=7.5 Hz,H3-18),[4.63 (1H,dd,J=6.5、11.0 Hz),4.70(1H,dd,J=4.5、11.0 Hz),H2-1'],4.44(1H,m,H-2'),4.11(2H,d,J=5.5 Hz,H2-3')。13C NMR(C5D5N,125 MHz)谱数据:δ 173.7(C-1),34.4(C-2),25.3(C-3),29.4(C-4 and 6),29.5(C-5),29.9(C-7),27.5(C-8 and 14),130.4(C-9 and 13),128.4(C-10 and 12),26.0(C-11),29.6(C-15),31.7(C-16),22.8(C-17),14.2(C-18),66.8(C-1'),70.9(C-2'),64.3(C-3')。C-8和C-14的化学位移为27.5,确定其构型为9Z,12Z[12-13]。其1H、13C NMR 谱数据与文献[17]相对照,鉴定该化合物为1-O-linoleoyl-glycerol。
化合物3:黄色油状固体。高分辨Q-TOF-ESIMS给出其准分子离子峰m/z 281.2475[M-H]-(calcd for C18H33O2,281.2486),确定其分子式为 C18H34O2。1H NMR(C5D5N,500 MHz)谱数据:δ 2.51(2H,t,J=7.5 Hz,H2-2),1.79 (2H,m,H2-3),1.24~1.40(16H,m,H2-4~7 and 12~15),2.09(4H,m,H2-8 and 11),5.47(2H,m,H-9 and 10),1.24(2H,m,overlapped,H2-16),1.24(2H,m,overlapped,H2-17),0.87(3H,t,J=6.5 Hz,H3-18)。13C NMR(C5D5N,125 MHz)谱数据:δ 176.1(C-1),34.9(C-2),25.7(C-3),29.5~30.1(C-4~7 and 12~15),27.5(C-8 and 11),130.2(C-9 and 10),32.1(C-16),22.9(C-17),14.3(C-18)。C-8和C-11的化学位移为27.5,确定其构型为9Z[5-6]。其1H、13C NMR谱数据与文献[6]相对照,鉴定该化合物为油酸(oleic acid)。
化合物4:白色固体。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 255.2325[M-H]-(calcd for C16H31O2,255.2330),确定其分子式为 C16H32O2。1H NMR(C5D5N,500 MHz)谱数据:δ 2.51(2H,t,J=7.0 Hz,H2-2),1.79(2H,m,H2-3),1.20~1.41(20H,m,overlapped,H2-4~13),1.25 (2H,m,H2-14),1.24(2H,m,H2-15),0.87 (3H,t,J=7.0 Hz,H3-16)。13C NMR(C5D3N,125 MHz)谱数据:δ 176.0(C-1),34.9(C-2),25.7(C-3),29.6~30.0(C-4~13),32.2(C-14),23.0(C-15),14.3(C-16)。该化合物的结构经1D NMR及包括1H1H COSY、HSQC及HMBC在内的2D NMR谱的解析,鉴定为棕榈酸(palmitic acid)[9]。
化合物5:白色固体。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 365.2474[M+Cl]-calcd for C19H38O4Cl,365.2464),确定其分子式为 C19H38O4。1H NMR(C5D5N,500 MHz)谱数据:δ 2.37(2H,t,J=7.5 Hz,H2-2),1.66(2H,m,H2-3),1.21~1.26(24H,m,overlapped,H2-4~H2-15),0.89(3H,t,J=7.0 Hz,H3-16),[4.66 (1H,dd,J=5.5、11.0 Hz),4.73(1H,dd,J=4.5、11.0 Hz),H2-1'],4.47(1H,m,H-2'),4.13 (2H,d,J=5.5 Hz,H2-3')。13C NMR(C5D5N,125 MHz)谱数据:δ 173.7(C-1),34.4(C-2),25.3(C-3),29.4~30.0(C-4~C-13),32.2(C-14),22.9(C-15),14.3(C-16),66.8(C-1'),70.9(C-2'),64.3(C-3')。其1H、13C NMR谱数据与文献[10]相对照,并结合2D NMR的解析,鉴定该化合物为α-棕榈酸单甘油酯(glyceryl α-mono-palmitate)。
4 总结与讨论
由于传统中药多采取水煎的服药方法,脂肪酸的药理作用长期以来未得到足够的重视。近年来,随着对脂肪酸成分研究的不断深入,其抑菌、抗炎、抗肿瘤、抗动脉粥样硬化、抗氧化以及调节中枢神经系统的活性陆续被挖掘出来。本课题以白鲜皮为例,对其中的脂肪酸类化合物进行了初步化学成分研究,以期为后续药理学研究奠定了物质基础。

