熔盐法合成Na2/3Ni1/3Mn2/3O2@C钠离子电池正极材料及其电化学性能
,, ,,
(合肥工业大学材料科学与工程学院,安徽 合肥 230009)
1 前 言
随着环境污染和能源短缺问题日益加剧,可再生清洁能源的开发利用成为当前研究热点,其中储能技术是清洁能源大规模应用的关键[1-2]。在各种能量存储方式中,锂离子电池因其能量密度高,循环寿命长,工作电压高等特点在移动设备和电动汽车中被广泛应用[3]。但地壳中锂元素有限的储量和不断增长的市场需求之间的矛盾导致含锂化合物的价格不断上涨,这严重制约了锂离子电池的大规模开发。与此同时,与锂同族的钠元素因其与锂元素相似的化学性质和非常丰富的储量受到广泛关注,因而,钠离子电池有望替代锂离子电池成为下一代可充电电池体系[4]。然而,钠的离子半径(0.102nm)比锂离子半径(0.076nm)大将近35%,钠离子在电极材料中扩散困难,容易引起电极材料的结构破坏导致循环性能下降。因此,寻找理想的电极材料是钠离子电池发展的关键。
目前,在研究中发现的钠离子电池负极材料有硬碳,合金材料及其化合物(如Sn,SnSb,CuSb,Sb/C等[5-6]),氧化物及其合金(如Na2Ti3O7[7])还有某些有机物(如Na2C8H4O4[8])等。在正极材料中,研究较多的有聚阴离子化合物(如NaMPO4(M=Fe, Mn等)[9]),钠超离子导体材料(如NaxM2(PO4)3(M=V, Ti等[10-11])),普鲁士蓝[12]及P2型过渡金属氧化物(如 NayMn1-xMxO2(x,y≤1, M=Ni, Mg, Li等))。本课题组也在钠离子电池电极材料方面进行了大量研究,其中有Na3V2(PO4)3[10,13]、NaV6O15[14-15]、MoSe2[16-18]等。曹殿学等[19]分别采用共沉淀法和固相法均合成了纯相的Na2/3Ni1/3Mn2/3O2,首次放电容量为157mA·h·g-1,但在0.2C倍率下循环80次后,容量仅有42mA·h·g-1,循环性能有待提高。周崇武等[20]制备了Al2O3包覆的NNM,改善了其循环性能。Shinichi·Komaba课题组[21]合成了Na2/3Ni1/3Mn2/3-xTixO2,研究了Ti原子取代部分Mn原子后引起的结构变化及对容量和循环性能的影响。马紫峰等[22]制备了还原氧化石墨烯(RGO)/NNM复合材料,提高了电极材料的导电性,改善了其循环性能。但是,通过Hummer’s法[23]制备RGO工艺复杂,限制了其大批量生产,还存在一定的危险性。之前报道的对锂离子电池电极材料与碳进行复合后可改善其电化学性能的研究[24,6]为探究改善钠离子电池电极材料性能的新方法提供了思路。
本文以葡萄糖为碳源,通过绿色安全的熔盐法制得了三维碳网负载Na2/3Ni1/3Mn2/3O2颗粒的复合材料(NNM@C)用作钠离子电池的正极材料,考察了这种材料的合成条件和在钠离子电池体系中的电化学性能。
2 实 验
2.1 实验原料
实验中所有药品如NaCO3、MnO2、LiCl、KCl、葡萄糖、无水乙醇及NiO,均为分析纯。
2.2 材料合成
图1为熔盐法合成NNM/C材料的工艺流程,葡萄糖在高温下分解成碳后均匀地分散在熔融盐中,并形成C-C键。当熔盐冷却结晶时,碳原子向晶面处移动,最终形成三维网状结构[27],同时,NNM颗粒附着在碳网表面,改善颗粒之间的导电性。

图1 熔盐法合成NNM@C示意图Fig.1 Schematic of the synthesized NNM@C by molten-salt growth method
按化学计量比称取一定量的NaCO3(由于高温下Na易挥发,过量5%)、NiO、MnO2,采用400r/min球磨混合12h后干燥。在空气中900℃煅烧12h制得纯相的p2-Na2/3Ni1/3Mn2/3O2电极材料。将制得的NNM粉末与葡萄糖按一定比例混合后加入LiCl/KCl(2∶3)混合盐(熔点350℃)[25],研磨使之均匀混合,在氩气保护下以不同温度煅烧12h,冷却后用去离子水洗涤,将混合盐去除,干燥后得到产品。
2.3 材料表征
使用D/MAX2500V型X射线衍射仪对合成的材料进行结构表征。采用SU8020型场发射扫描电子显微镜对材料形貌和成分进行分析。
2.4 电化学测试
材料的电化学性能通过在手套箱组装的CR2032扣式电池进行测试。正极是由质量分数分别为75%的活性物质,15%乙炔黑,10%聚偏氟乙烯(PVDF)及适量的粘接剂N-甲基吡咯烷酮(NMP)均匀混合成浆料涂覆在铝箔上,真空干燥后冲压而成;负极为金属钠片;以1mol·L-1NaClO4碳酸乙烯酯/碳酸丙烯酯(体积比为1∶1)溶液为电解液;隔膜采用Whatman GF/D。充放电测试通过NEWWARE BST-5V10mA电池测试系统在室温2~3.9V电压范围内以不同电流进行。循环伏安(CV)测试和交流阻抗(EIS)测试均使用CHI600D型电化学工作站,循环伏安测试扫描电压范围为2~3.9V,扫描速率为0.8mV/s;交流阻抗测试电位振幅为8mV,频率范围为0.01Hz~100KHz。
3 结果与讨论
图2(a)为合成的NNM样品的XRD精修图谱,其中Rp=7.08%,Rwp=8.20%,其晶胞参数a=2.887133Å,c=11.146814Å,V=80.466Å3。图中所有的衍射峰的位置及强度与计算结果高度吻合,属于六方晶系P63/mmc空间群,说明通过固相烧结法可以制得纯度高、结晶性优良的NNM样品,其中各种原子的坐标参数见表1。图2(b)中为其晶体结构,MO2(M=Ni,Mn)构成的八面体以共边形式连接组成层状结构,钠离子处于层间,并与O原子构成三棱柱结构,宽阔的矩形通道非常有利于钠离子在层间迁移,这为电池获得更高的容量和优异的循环性能提供了保障[26]。
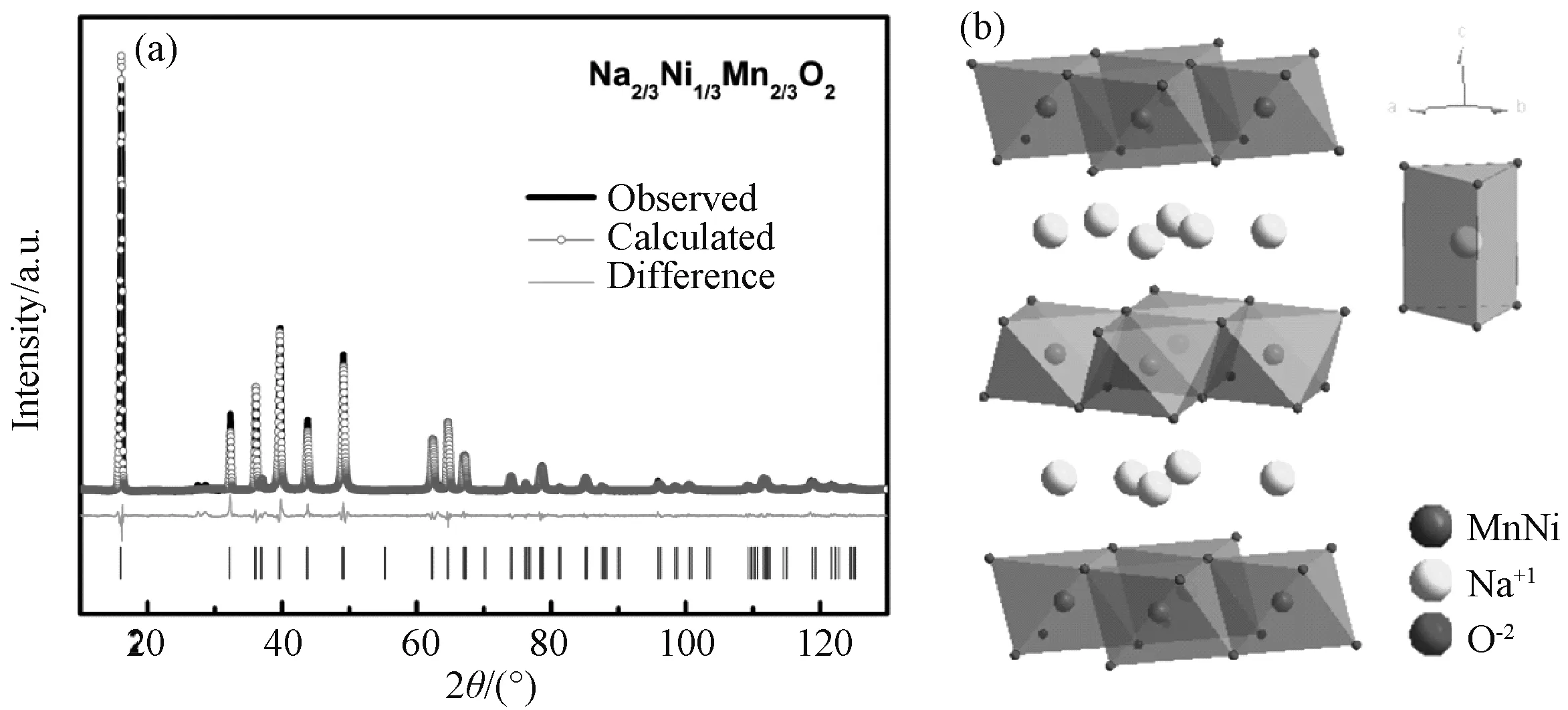
图2 NNM样品的(a)XRD精修图谱;(b)晶体结构Fig.2 (a) Rietveld refinement pattern of XRD; (b) crystal structure of the as-prepared NNM

Atomx/ay/bz/cS.O.F.Na10.00000.00000.25000.3333Na20.33330.66670.75000.3333Ni0.00000.00000.00000.3333Mn0.00000.00000.00000.6667O0.66670.33330.09491
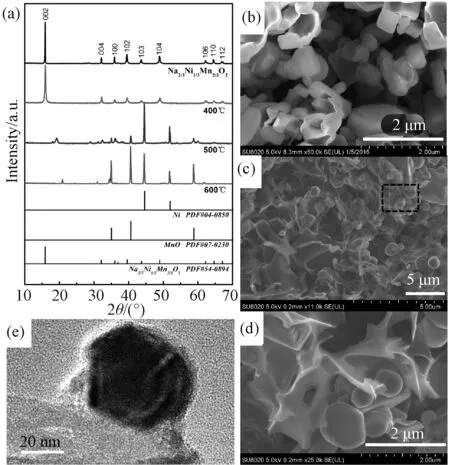
图3 (a)不同温度下合成的NNM@C的XRD图谱;(b)固相法合成NNM颗粒和(c、d)400℃熔盐法合成NNM@C的扫描电镜图;(e)NNM@C的透射电镜图Fig.3 (a)XRD pattern of NNM@C prepared in different temperatures; SEM images of (b)NNM particles by solid phase method and (c, d) NNM@C synthesized at 400℃ by molten-salt growth method;(e) TEM images of NNM@C
图3(a)所示为纯相NNM和不同温度下制备的NNM/C复合材料的XRD图谱。400℃时样品的衍射峰相较于NNM没有其他多余的杂峰出现,这说明在反应过程中NNM未发生相变,且从对比图3(b)和图3(d)可以看到NNM晶粒尺寸几乎没有变化,只是复合材料中的非晶态的无定型碳对X射线的散射角产生了影响,导致所有的衍射峰变宽;500℃时的衍射图谱中NNM相已经消失,而出现Ni单质的衍射峰,这说明在500℃时NNM已与葡萄糖分解产生的碳在氩气中反应;600℃时,NNM发生反应生成Ni和MnO。图3(b)为固相法制备的NNM样品的扫描电镜图,从图可见,样品颗粒尺寸约为0.5~1μm,无固定形貌。图3(c, d)为在400℃盐浴中保温12h制得的NNM/C复合材料的形貌,NNM颗粒与反应前一致,并且均匀地附着在三维碳网的表面。从图3(e)中可以看到,NNM颗粒与碳网物理结合,使电极材料具有了好的导电性。说明NNM颗粒与葡萄糖均匀混合后,在氩气气氛保护的LiCl/KCl(2∶3)混合盐中,400℃反应12h后可制得三维碳网负载NNM颗粒的复合材料。
NNM/C复合材料的Mapping图谱及EDS能谱见图4。所有元素在样品中都有分布,含量与合成材料的大致相当,并且没有其他杂质元素出现(Si元素来自于放置样品的硅片),但C元素的分布与其他几种元素(Na、Ni、Mn、O)的分布明显不同,结合扫描电镜图进一步证实通过熔盐法可以制得NNM/C复合材料。
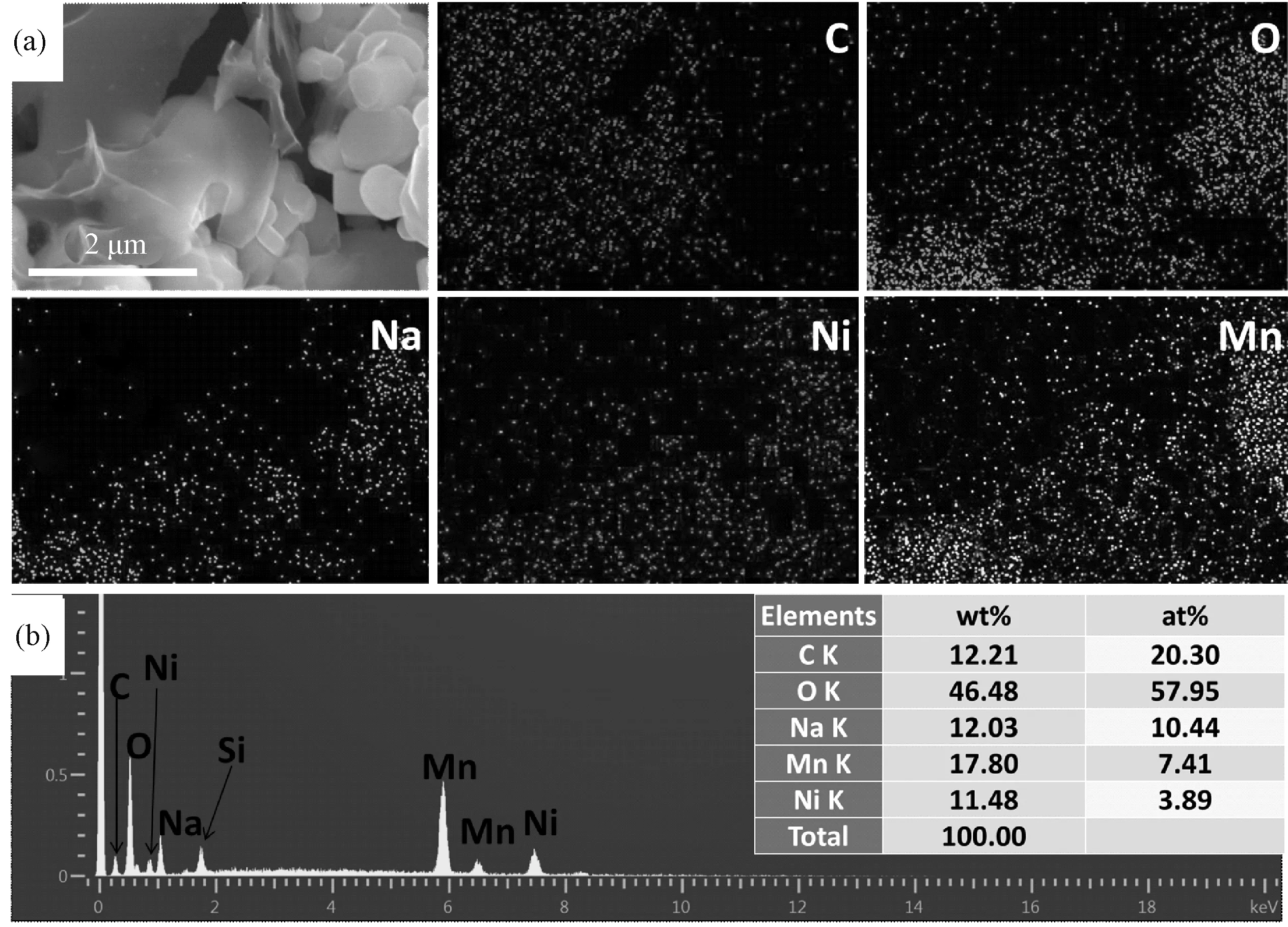
图4 NNM@C样品的(a)Mapping图谱和(b)EDS能谱图Fig.4 (a) Elemental mapping images; (b) Energy dispersive X-ray spectroscopy of NNM@C
图5 NNM和NNM@C的电化学性能 (a) 首次充放电曲线; (b) 倍率性能; (c) 循环性能
Fig.5 Electrochemical performance of NNM and NNM@C (a) the first charge/discharge curve ; (b) rate capability ;(c) cycle performance
图5(a)所示为NNM和NNM@C的首次充放电曲线,NNM的放电比容量(94.85mA·h·g-1)略大于NNM@C(93.18mA·h·g-1),这是因为NNM@C中由于的C的加入降低了电极材料中活性材料的相对含量,而两组材料的充放电曲线形状高度一致,说明三维碳网没有影响活性材料的电极反应。在图5(b)所示的不同倍率的充放电过程中,NNM的容量均小于NNM@C,并且循环倍率越大容量衰减越明显,在2C倍率下,NNM@C的放电比容量为79.56mA·h·g-1,远大于NNM的放电比容量46.72mA·h·g-1,这是由于电极材料在高倍率充放电过程中,碳网的作用增加了电极材料的导电率,减弱了电极极化现象,大力地改善了电池的倍率性能。图5(c)中,循环100次后,NNM@C的比容量(85.83mA·h·g-1)比NNM(48.16mA·h·g-1)高出很多,电池的容量保持率得到大幅度提高,这是因为C具有很高的电导率,NNM颗粒均匀地负载在三维网状C表面,C作为电子传输的高速通道,大大提高了电子传输的效率,减弱了电极极化现象,使电极材料的循环性能得到显著改善[13]。
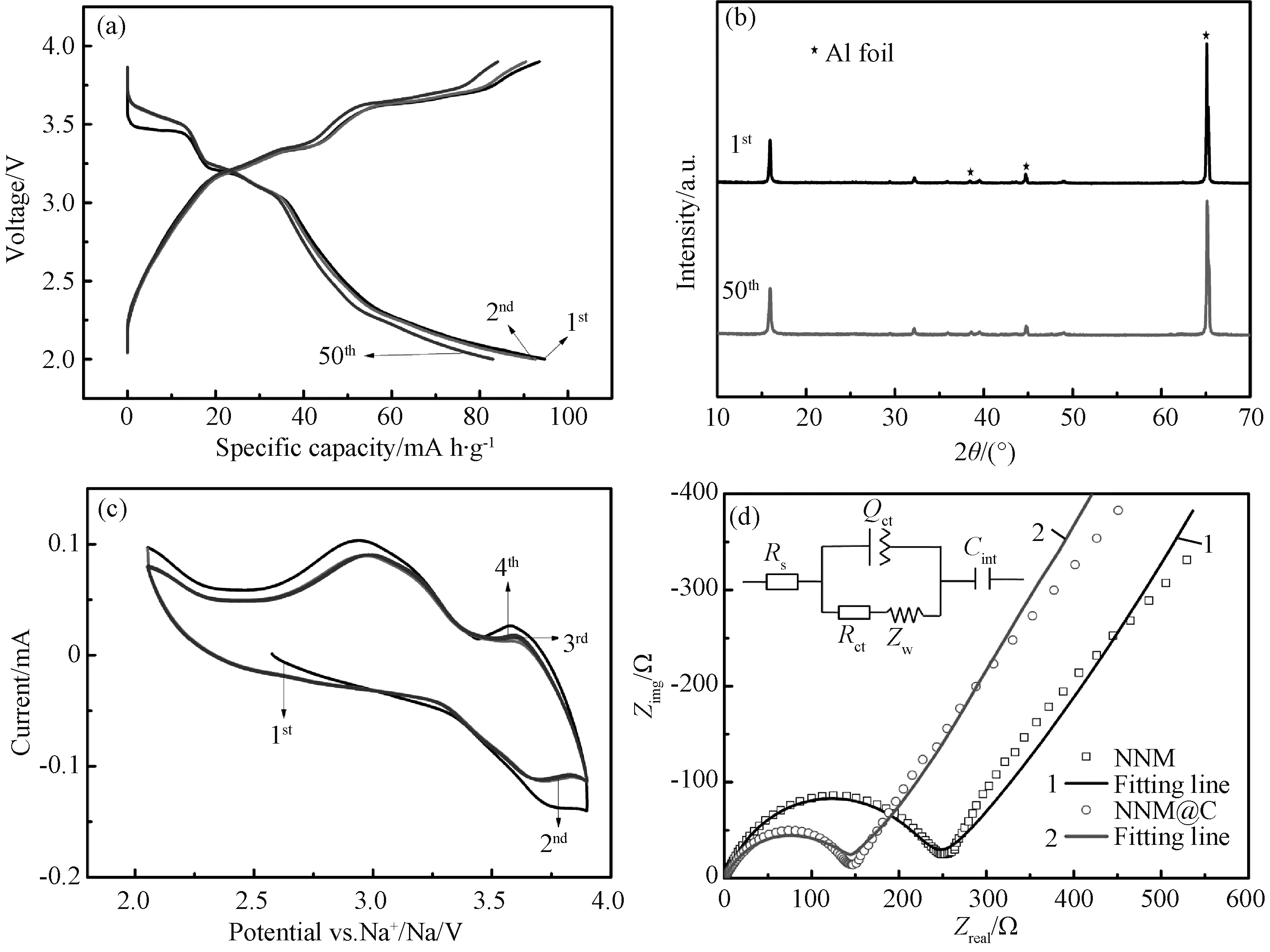
图6 NNM@C经循环50次的(a)充放电曲线和(b)XRD图谱; (c)NNM@C电极的循环伏安曲线; (d)NNM@C和NNM的交流阻抗图谱Fig.6 (a) charge/discharge curves and (b) XRD patterns of NNM@C from 1st to 50th cycle; (c) CV curves of NNM@C; (d) Nyquist plots of NNM and NNM@C
图6(a)为NNM@C电池经50次循环后的充放电曲线。如图所示,该电池具有非常好的循环性能,50次循环后,放电比容量仍达82.35mA·h·g-1。图6(b)为NNM@C电极第一次充放电之前和进行50次循环之后的XRD图谱,图中38.5°、44.8°和65.2°的三个峰为铝箔的衍射峰。两条曲线几乎完全一致,说明该电极材料在充放电过程中结构非常稳定,从而使得电池具有优异的循环性能。图6(c)为前四次循环伏安曲线图,四条曲线极其相似,几乎完全重合,这说明NNM@C具有很好的循环性能,与b图结果相吻合,图中的氧化峰和还原峰与充放电曲线相对应。图6(d)为NNM@C和NNM分别组装电池后的交流阻抗图谱,图中两条曲线均由中高频区的的小截距(表示电池的内阻Re,包括电极,隔膜和电解质的电阻)、中频区的半圆(表示固液界面的电荷转移电阻)和低频区的直线(表示与材料内部Na+扩散相关的Warburg内阻)组成。插图为等效电路图,图中,Re表示溶液电阻,Rct表示电荷转移电阻,Zw表示与扩散过程相关的阻抗,Qct与电极的表面性质有关,Cint表示电荷转移产生的电容。等效电路的模拟参数见表2,所有值都在误差范围内。由表可知,NNM@C复合材料由于三维碳网的加入,降低了电池内阻,改善了电池的电化学性能。且本研究采用的处理工艺简单易操作,具有较好的工业应用价值。

表2 等效电路拟合参数Table 2 Impedance parameters obtained by fitting the experimental data using the equivalent circuit
4 结 论
采用熔盐法成功地合成了三维碳网负载Na2/3Ni1/3Mn2/3O2复合材料(NNM@C)钠离子电池正极材料。熔盐法的独特体系,不仅使葡萄糖分解成的碳在混合盐冷却结晶时形成三维网状,同时使Na2/3Ni1/3Mn2/3O2(NNM)颗粒均匀地附着在碳网表面,由于碳的作用,改善了电子在NNM颗粒之间的传输性能,增强了电极材料的电导率。碳负载后的NNM@C电极材料在2~3.9V电压范围内以0.2C倍率进行充放电,获得93.18mA·h·g-1的可逆容量,并在100次循环后容量保持率高达87%,2C放电倍率下放电比容量仍能达到79.56mA·h·g-1。结果表明三维碳网负载的NNM电极材料具有优异的循环和倍率性能。

