还原氧化石墨烯/硫堇复合物修饰的手性表面对色氨酸的选择性识别
朱宇萍, 倪 萍
(内江师范学院 化学化工学院, 四川 内江 641112)
色氨酸(tryptophan, Trp)是一种手性氨基酸, 是人体必需的氨基酸之一[1], 在生命体内Trp可缓慢旋光异构[2]. Trp的手性对映异构体(D/L-Trp)具有不同药理作用, 对其选择性识别具有重要意义. 电化学手性识别是基于手性选择剂与目标手性分子作用后, 电极表面性质发生变化, 使电子在电极表面的传递性能及速率发生改变, 利用电化学信号的差异进行识别的过程[3]. 寻求优良的修饰材料固载手性选择剂是目前电化学手性传感器研究的热点.
还原氧化石墨烯(RGO)是将氧化石墨烯(GO)还原得到的产物. 在还原过程中, GO表面的环氧基和部分羧基、 羟基等被去掉, 使得RGO的亲水性、 分散性较石墨烯(graphene)更强[4], 利于制备RGO复合物, 且RGO比GO的导电性强[5]. 硫堇(thionin, Thi)分子含有两个苯环、 一个杂环和两个氨基, 是一种氧化还原染料. 由于Thi为二维平面芳环结构, 因此易通过堆积和非共价电荷转移协同效应与RGO结合, 有助于提高比电容[6], 且RGO特殊的空间结构可为手性选择剂提供更多空间. 牛血清蛋白(bovine albumin, BSA)是由单一氨基酸构成的球形疏水蛋白[3], 常作为手性选择剂, 尤其适于分离氨基酸[7]. BSA分子中有两个Trp, 分别位于134和212位, 同时这两处也是手性识别位点[8]. 本文制备RGO/Thi复合物, 将其固载手性选择剂BSA, 考察其对D/L-Trp的选择性识别及其条件.
1 实 验
1.1 仪器与试剂
CHI660E型电化学工作站, 金电极, 铂电极, Ag-AgCl电极(上海辰华仪器公司); BRANSONIC 200型超声清洗仪(德国Branson Ultrashall公司); AB204-S型电子天平(上海天美天平仪器有限公司); DF-101S型集热式恒温加热磁力搅拌器(上海兴创科学仪器有限公司); pH计(上海仪电科学仪器股份有限公司).
牛血清白蛋白(上海博奥生物科技有限公司); 硫堇(英国BICF公司); 氧化石墨烯(GO, 南京先丰纳米材料科技有限公司);D/L-Trytophan(上海源叶生物科技有限公司); NaAc·3H2O,NaCl,K3[Fe(CN)6](成都金山化学试剂有限公司); K4[Fe(CN)6],FeCl3,Na2HPO4,KH2PO4,KCl,NaOH,无水乙醇,冰乙酸(成都科龙化工试剂厂). 所用试剂均为分析纯(AR级), 实验用水均为超纯水.
1.2 RGO/Thi的制备
称取0.015 g GO, 用超纯水超声溶解, 制得15 mg/mL的GO分散液, 先向其中加入0.8 mol/L的NaOH 2 mL, 超声15 min, 制备RGO[9], 再用超纯水制得1 mg/L的RGO黑褐色分散液15 mL. 将上述分散液和1 mg/mL的Thi溶液各15 mL超声混合均匀, 水浴锅内搅拌12 h, 离心, 多次洗涤除去未反应的Thi, 收集沉淀即得RGO/Thi纳米复合材料. 将该纳米复合材料用超纯水分散制得1 mg/mL的RGO/Thi紫色分散液[6], 于4 ℃保存备用.
1.3 手性传感器的制备
依次用0.3,0.05 μm的Al2O3糊将玻碳电极(GCE, 直径4 mm)抛光打磨成镜面, 用超纯水冲洗干净. 再分别用超纯水、 无水乙醇、 超纯水超声清洗5 min, 在室温下自然晾干. 将所得RGO/Thi溶液滴涂于已预处理的电极表面, 待其晾干后, 再在其表面滴加BSA(ω=0.25%), 晾干, 于4 ℃保存备用. 制备过程如图1所示.

图1 手性传感器制备过程示意图Fig.1 Schematic diagram of preparation process of chiral sensors
1.4 检测方法
利用循环伏安法(cyclic voltammetry, CV)对电极的制备及优化实验条件过程进行表征. 检测方法采用三电极体系: 参比电极为Ag-AgCl电极, 对电极为Pt电极, 被修饰的GCE为工作电极. 在pH=6的NaAc-HAc测试底液中进行电极表征, 电压扫描范围为-0.6~0.2 V, 扫描速度为0.05 V/s. 在开路电位下, 电化学阻抗谱(EIS)测试的频率范围为0.01~106Hz, 振幅为0.22 V. 若无特殊说明, 实验均在室温下进行.
2 结果与讨论
2.1 电极修饰过程的CV表征
图2为电极在修饰过程中的CV表征. 由图2可见: 曲线a无明显的氧化还原峰, 这是由于电极和测试底液中均没有电活性物质所致; 曲线b有一对可逆的氧化还原峰, 这是由于RGO/Thi复合材料中的Thi可作氧化还原探针[10], 加快了电子转移速率; 曲线c的还原峰电流值减小, 这是由于BSA吸附到电极表面后, 阻碍了电极表面的电子传输[11]; 曲线d和e的还原峰电流值均减小, 这是由于D/L-Trp为蛋白质分子, 阻碍了电子传递[12]. 在相同条件下, 曲线e的峰电流值下降更多, 表明手性表面吸附L-Trp的量比吸附D-Trp的量更多, 即该手性表面对L-Trp的作用更强.
2.2 电极修饰过程的EIS表征

a. GCE电极; b. (RGO/Thi)/GCE; c. BSA/(RGO/Thi)/GCE; d. D-Trp/BSA/(RGO/Thi)/GCE;e. L-Trp/BSA/(RGO/Thi)/GCE.图2 电极修饰过程的CV表征Fig.2 Cyclic voltammetry characterization of modified electrode process

a. GCE电极; b. (RGO/Thi)/GCE;c. BSA/(RGO/Thi)/GCE; d. D-Trp/BSA/(RGO/Thi)/GCE;e. L-Trp/BSA/(RGO/Thi)/GCE.图3 电极修饰过程的EIS表征Fig.3 Electrochemical impedance spectroscopy characterization of modified electrode process
在pH=6的NaAc-HAc缓冲溶液中, 对扫描速度分别为0.01,0.05,0.08,0.1,0.15,0.2,0.3,0.4,0.5,0.6,0.7,0.8 V/s的修饰电极进行CV表征, 结果如图4所示. 由图4可见, 随着扫描速度的增加, 氧化峰和还原峰的电流值均增加. 由图4(B)可见, 氧化/还原峰的电流值均与扫描速度呈良好的线性关系, 表明电极表面的电化学过程受表面吸附控制[16].

图4 修饰电极在不同扫描速度下的循环伏安曲线(A)及峰电流与扫描速度的关系(B)Fig.4 Cyclic voltammograms of modified electrodes at different scanning speeds (A) and relationship between peak current and scanning speeds (B)
2.3 实验条件的优化
2.3.1 测试底液pH值对修饰电极的影响 缓冲溶液pH值的变化通常会导致氨基酸离子化程度和蛋白质结构发生变化, 从而影响其相互作用力[17]. 图5为修饰电极在不同pH值缓冲溶液中分别对D-Trp(A)和L-Trp(B)的循环伏安曲线. 由图5可见, pH值从3增加到9, 氧化还原峰电位发生了负位移, 表明较高的酸度会使Thi的氧化还原过程中电子快速转移[18]. 但酸度过高会破坏电极表面的绝缘膜, 导致电极出现裸露的针孔, 从而影响电流大小; 而碱度过高(pH>8)会使氧化峰变形并出现杂峰.

图5 修饰电极D/L-Trp在不同pH值下的循环伏安曲线Fig.5 Cyclic voltammograms of modified electrodes of D/L-Trp at different pH values
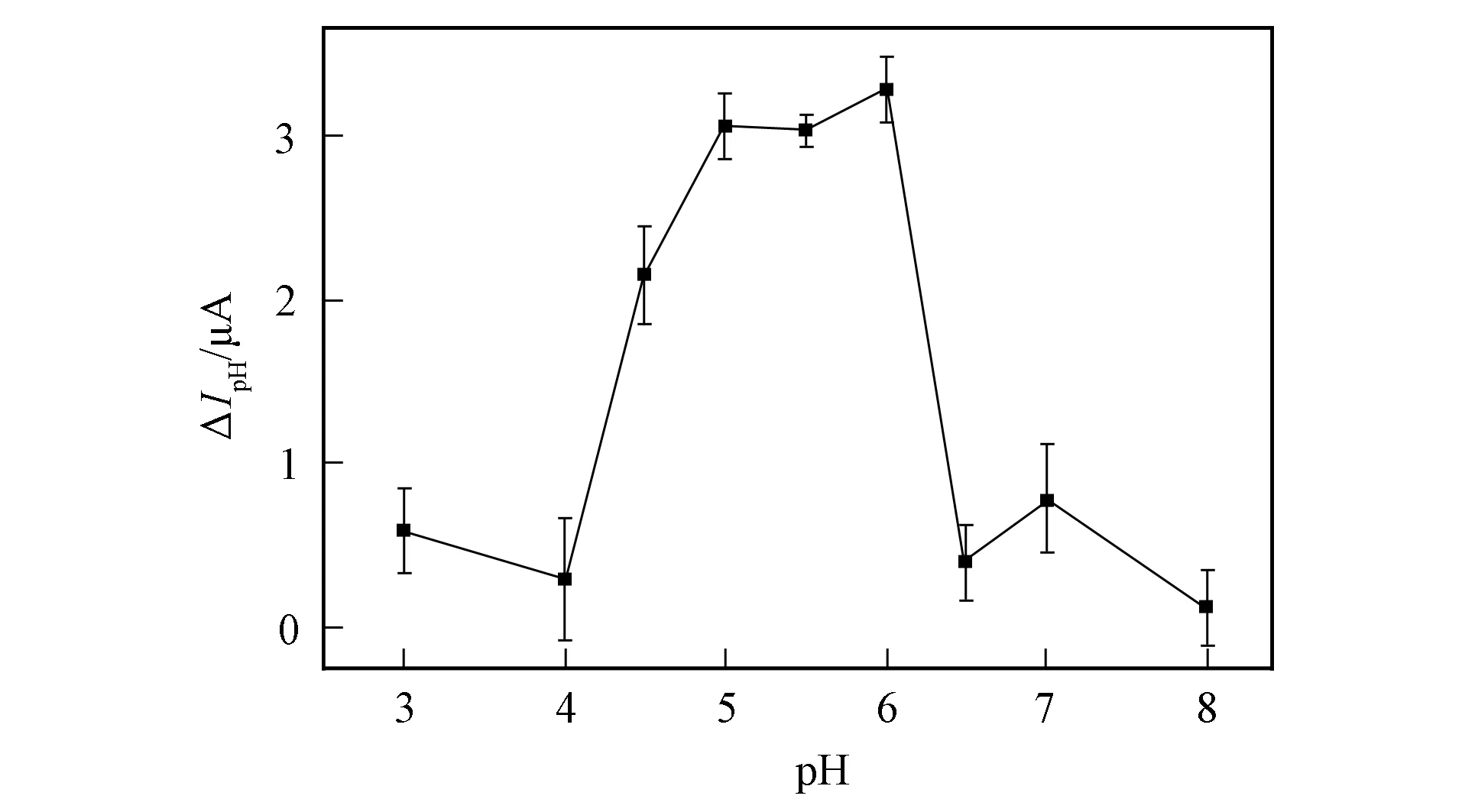
图6 pH值对D/L-Trp选择性识别的影响Fig.6 Effects of pH values on selective recognition of D/L-Trp
图6为pH值对D/L-Trp选择性识别的影响, 其中纵坐标ΔIpH为修饰电极与L-Trp反应前后的还原峰电流差值减去修饰电极与D-Trp反应前后的还原峰电流差值. 由图6可见, 当pH=4~6时, 立体选择性随pH值的增大而增强, 即当pH=6时, ΔIpH值最大. 当pH值进一步增大时, 立体选择性减小. 因此, 实验选择pH=6.
2.3.2 反应时间与对映体选择性识别的关系 将修饰电极分别放入D-Trp和L-Trp对映体溶液中, 反应时间依次为2,15,20,25,30,35 min, 结果如图7所示, 其中纵坐标ΔIt为修饰电极分别与D/L-Trp反应不同时间的还原峰电流差值. 由图7可见, 当反应时间为20 min时, 电极吸附的D/L-Trp量最多, 响应峰电流差值最大, 因此, 实验选择反应时间为20 min.
2.4 手性传感器的电化学响应性能
当修饰电极分别浸入浓度为1,2,3,4,5,6,7 mmol/L的D/L-Trp溶液中反应20 min时, 结果如图8所示, 其中纵坐标ΔIc为修饰电极(GCE/(RGO/Thi)/BSA)分别与不同浓度D/L-Trp反应前后的峰电流差值. 由图8可见, ΔIc与D/L-Trp浓度呈良好的线性关系, 其线性方程分别为
ΔIc=0.415 3c+2.865(L-Trp),
ΔIc=0.441 4c+1.126(D-Trp).
检测限为0.33 mmol/L(S/N=3). ΔIc(L-Trp)>ΔIc(D-Trp), 进一步说明BSA修饰表面更易吸附L-Trp.

图7 修饰电极与D/L-Trp反应时间的关系Fig.7 Relationship between modified electrode and reaction time of D/L-Trp

图8 修饰电极与D/L-Trp浓度的关系Fig.8 Relationship between modified electrode and concentration of D/L-Trp
2.5 手性传感器的应用
分别配制不同质量分数的D/L-Trp混合溶液. 图9为峰电流和w(L-Trp)的关系, 其中纵坐标ΔI为(RGO/Thi)/BSA与不同质量分数(w)的D/L-Trp混合溶液反应后的峰电流差值. 由图9可见, 随着L-Trp质量分数的增加, ΔI不断增大, 且ΔI与w(L-Trp)呈良好的线性关系:
ΔIa=0.037 69w+1.667,
ΔIb=0.013 17w+0.648 1.
可见D-Trp和L-Trp引起的电流变化存在明显差异, 由于ΔIL-Trp>ΔID-Trp, 因此该手性表面更易与L-Trp结合.
将GCE/(RGO/Thi)/BSA手性表面置于溶液中以0.05 V/s的扫描速度连续扫描50圈, 结果如图10所示. 由图10可见, 其氧化还原峰电流仅发生微小变化, 还原峰的相对标准偏差RSD=0.875%, 表明该GCE/(RGO/Thi)/BSA表面具有较好的稳定性.

图9 峰电流和w(L-Trp)的关系Fig.9 Relationship between peak current and w(L-Trp)
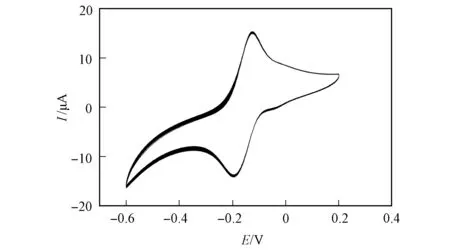
图10 传感器的稳定性Fig.10 Stability of sensor
为检验该手性传感器的抗干扰能力, 将其置于含有D-Trp、 苯丙氨酸对映体(D/L-Phenylalanine)、 半胱氨酸对映体(D/L-Lys)的混合溶液中测试其电流响应值. 实验结果表明, GCE/RGO/BSA和混合溶液反应前后的电流差值与不含干扰物时无明显变化, 因此该手性传感器对L-Trp的对映选择抗干扰能力较强.
2.6 性能对比
实验测试不含Thi的GCE/RGO/BSA与D/L-Trp反应. 经多次CV表征, 结果表明, 其氧化还原峰不稳定, 远小于GCE/RGO+Thi/BSA的电流增加值, 且其图形成峰性较差. 最终确定以GCE/(RGO/Thi)/BSA为手性传感器的构建方式. 将该手性传感器与其他电化学方法识别色氨酸的手性传感器性能进行比较, 结果列于表1. 由表1可见, 本文方法制得了一种识别色氨酸对映体的新方法, 且检测范围更大, 检测限较低.

表1 不同手性传感器的性能对比
综上可见, 本文实验合成了RGO/Thi复合材料修饰GCE, 由于形成了比表面积较大的表面, 因此构建了具有高灵敏的电流型手性传感器. 通过CV和EIS考察了电极表面的电化学特性. 以BSA作为手性物质模型, 实现了对D/L-Trp对映体的选择性识别. 实验结果表明, 在相同条件下, 该手性表面对L-Trp的识别能力优于D-Trp, 从而实现了BSA大分子与氨基酸小分子间的手性识别作用.

